2.3.1物质的量的单位---摩尔 课件(共24张PPT)2023-2024学年高一上学期人教版(2019)必修第一册
文档属性
| 名称 | 2.3.1物质的量的单位---摩尔 课件(共24张PPT)2023-2024学年高一上学期人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-07 00:00:00 | ||
图片预览







文档简介
(共24张PPT)
第二章 海水中的重要元素
——钠和氯
第三节 物质的量
第1课时 物质的量的单位——摩尔
学习目标
1、宏观辨识与微观探析:通过对物质的量及其单位摩尔的学习,从微观上理解物质由不同粒子构成,进而从宏观上明确物质的量的应用。
2、证据推理与模型认知:通过完成物质的量的学习,使学生体会物理量建立的推理过程,并形成物理概念的认知模型。
3、科学态度与社会责任:通过物质的量概念的建立过程,理解化学家从微观研究到宏观概念的哲学思想和科学态度,进而培养学生学习化学的兴趣,树立良好的社会责任感。
教学重点:物质的量及其单位
教学难点:物质的量的概念建立及理解、应用
比一比:大家一口气能喝多少的水?
小明:我一口气能喝18g的水
夸父:我追赶太阳,口渴极了,我跑到了黄河边,一口气把黄河水喝完了,还是渴,我又跑到渭河边,一口气把渭河水也喝完了。
化学老师:小样,我一口气能喝下约600万亿亿个水分子
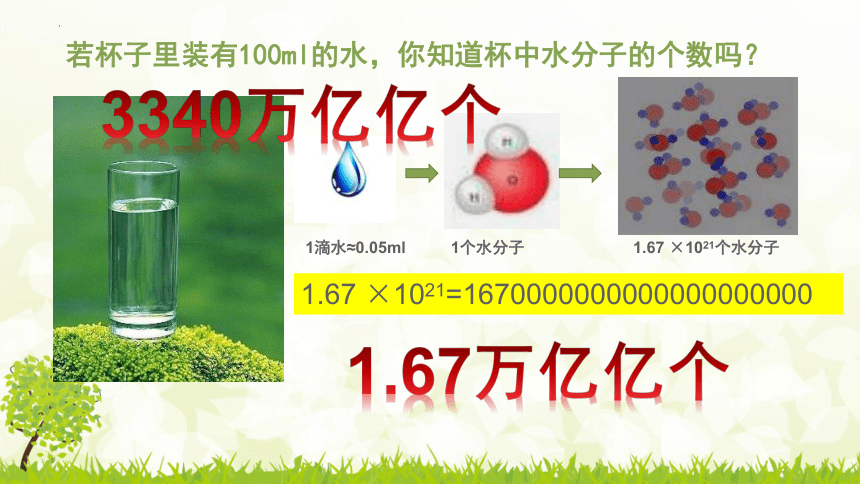
若杯子里装有100ml的水,你知道杯中水分子的个数吗?
1.67 ×1021=1670000000000000000000
1滴水≈0.05ml
1个水分子
1.67 ×1021个水分子
1.67万亿亿个
3340万亿亿个
想办法在水分子数和水的质量之间找到一个桥梁
——集体单位。
这个桥梁就是本节课标题:化学中常用的物理量
——物质的量
化学反应是原子、离子或分子之间按一定的数目关系进行的。对于原子、离子和分子等我们不仅直接用肉眼看不到,而且难以称量。用什么方法来计量原子、离子或分子(外观很小)呢?
集体单位
物 理 量 单位名称 单位符号
√长 度 米 m
√质 量 千克(公斤) kg
√时 间 秒 s
√电 流 安[培] A
热力学温度 开[尔文] K
发光强度 坎[德拉] cd
物质的量 摩[尔] mol
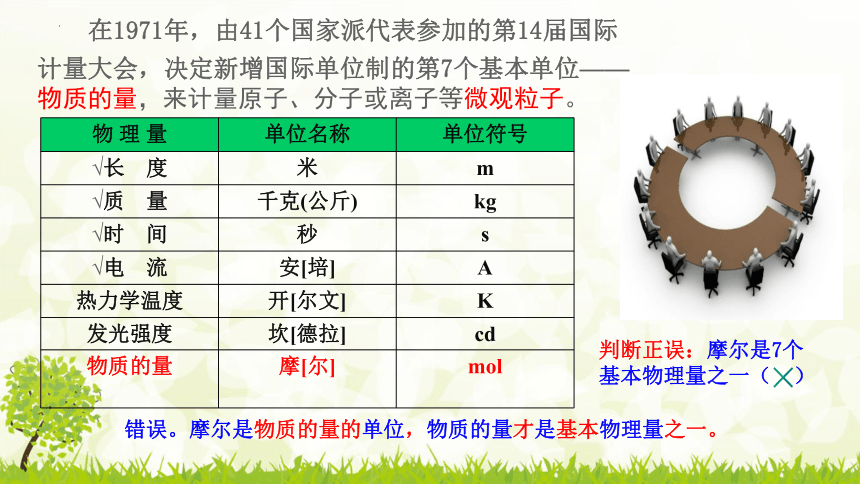
在1971年,由41个国家派代表参加的第14届国际
计量大会,决定新增国际单位制的第7个基本单位——物质的量,来计量原子、分子或离子等微观粒子。
判断正误:摩尔是7个基本物理量之一( )
错误。摩尔是物质的量的单位,物质的量才是基本物理量之一。
×
一、物质的量
1.概念:表示含有一定数目粒子的集合体的物理量。
3.单位:“摩尔”,简称“摩”,符号为mol
4.对象:微观粒子
【注意】①专业化:“物质的量”是一个专有名词,由四个字组成,是一个统一的整体,不能分割,也不可加字、减字。
判断正误1:物质的量将一定数目微观粒子与可称量的宏观物质之间联系起来了,以后我们就可以让“质量”这一个物理量“下岗”了( )
×
物质的质量( )
物质量( )
物质的数量( )
×
×
×
2.符号:n
判断正误2:1mol H( )0.5mol大米( )1mol苹果( )
√
×
×
【注意】②微观化:“物质的量”是只用来描述微观粒子,如原子、分子、离子、中子、质子、电子等;不能表示宏观物质。
判断正误3:1 mol H2O( )0.5 mol SO42-( )2 mol NaCl( )
√
√
√
【注意】③集体化:“物质的量”可以表示多个微粒的特定组合或集合体
思考
1 mol H、1 mol H+、1 mol H2的含义一样吗?为什么?
提示:含义不一样,尽管都是1摩尔微粒,但微粒种类不同,他们分别表示1摩尔氢原子、1摩尔氢离子、1摩尔氢分子
判断正误4:1 mol 氧( )1 mol 氧分子( )
×
必须指明微粒的种类,是氧原子、氧分子还是氧离子
【注意】④具体化:使用“物质的量”时一般用化学式表示,既规范又显得简洁准确;若用中文,则必须指明微粒的种类。如:1摩尔H、1摩尔CO2 、 1mol钠离子等。
√
说出下列语句的含义。
(1)1mol H
(2)3mol H2
(3)1mol CO2
【及时巩固】
表示氢原子的物质的量是1mol
表示氢气分子的物质的量是3mol
表示二氧化碳分子的物质的量是1mol
物质的量的表示方法:
物质的量的多少(mol)+能表示微观粒子的符号
一打铅笔是12支,
每12个为1打
一盒香烟是20支
每20支为1盒
吸烟有害健康!
【问题探究】
1mol
个
【提示】国际上规定,1mol粒子集合体所含的粒子数与0.012 kg 12C中所含的碳原子数相同。
(1)质量的单位是千克,1千克=1000克,物质的量的单位是摩尔,1mol含有多少个微粒?
【想一想】
(2)0.012 kg12C中所含的碳原子数到
底有多少个?已知一个碳原子的质量为 1.993 × 10-23g
阿伏加德罗
解:
≈ 6.02×1023
12g
1.993 × 10-23g
碳原子数=
指质子数为6,中子数为6的碳原子
二、阿伏伽德罗常数
1、国际规定:1mol任何粒子所含的粒子数与0.012kg 12C中所含的碳原子数相同。
(1) 准确量:是一个物理量,等于0.012kg 12C所含的碳原子数
(2) 近似值:约为6.02×1023 mol-1
2、含义:1mol 任何粒子的粒子数,叫阿伏加德罗常数。
3、符号及单位:符号用NA表示,单位是mol-1
①1mol是6.02×1023个微粒的粒子集合体。
概念辨析:
错误。6.02×1023是阿伏加德罗常数的近似值,二者不能简单等同。
②1mol任何物质均含有6.02×1023个原子。
错误。构成物质的微粒不同,1mol任何物质不一定含有6.02×1023个原子
③1molCO2和H2的混合气体所含的分子数约为6.02×1023
正确,1mol任何粒子集合体所含的粒子数约为6.02×1023,
这里的粒子集合体可以是纯净物,也可以是混合物。
1、喜欢下国际象棋的同学可能听说过舍罕王重赏国际象棋发现者达依尔的故事:
“陛下,请您在这张棋盘的第一个小格内,赏给我一粒麦粒;在第二个小格内给两粒;第三格内给四粒,照这样下去,后一小格都比前一小格加一倍,然后把摆在棋盘上所有64格的麦粒都赏给您的仆人吧!”
感受阿伏加德罗常数
麦粒的总数= 1 + 2 + 4 + 8 + … + 263
= 264 – 1
=1.845 × 1019
这竟是全世界在2000年内所生产的全部小麦!
感受阿伏加德罗常数
如果把 6.02×1023 粒米给全球60亿人吃,
每人每天吃一斤,要吃14万年。
如果把6.02×1023个直径为2.5cm的硬币排
成一行,可以来回于地球与太阳之间240.8亿次。
注意:摩尔只用来计量分子、原子、离子等微观粒子。
探究物质的量(n)与粒子数(N)的关系:
n(物质的量)
N(粒子总数)
1mol H
NA个H
2mol H
2×NA个H
…
…
n mol H
n×NA个H
N=
n×NA
n=
N
NA
1molH2O
【练一练】
个H2O
个H
个O
mol H
mol O
6.02×1023
2
1
1.204×1024
6.02×1023
N(H)=n(H)*NA
N(H2O)=n(H2O)*NA
n(O)=N(O)/NA
mol电子
10
在0.5 mol O2中含有的氧原子数目是多少?
解:每个O2分子中含有两个氧原子,氧原子数为
N(O)= n(O2)×2×NA
=0.5 mol×2×6.02×1023 mol-1
= 6.02×1023
答:O2中含有的氧原子数为6.02×1023个。
【练一练】
课堂小结
一、物质的量
1、概念:国际单位制中七个基本物理量之一,它表示含有一定数目粒子的集合体。
2、符号及单位:符号为n,单位为 mol。
3、单位——摩尔
符号
标准
对象
mol
1mol粒子的集合体所含的粒子数约为6.02×1023
微观粒子及其特定组合
二、阿伏伽德罗常数
阿伏伽德罗常数
含义
1mol任何粒子集合体所含的粒子数
符号是NA,单位是mol-1
符号单位
数值
约6.02×1023 mol-1
关系
n=
N/NA
(基础)1.课堂上同学们学习了“物质的量”这一物理量,以下是几位同学的谈话记录,你认为错误的是( )
A.1mol任何物质都含有阿伏伽德罗常数个微粒数
B.使用物质的量时要指明所量化的微观粒子是谁,最好用化学式表示,既规范,又显得简洁准确
C.物质的量是一个专用名词,是一个完整的名称,在读、写时不能添加或删减
D.学习了物质的量后,我们就能大致知道一杯水中大约有多少个水分子了
√
配餐作业
题点一:“物质的量”概念的理解
(提升)2、(2019 云南玉溪)现有NO、NO2、O3三种气体,它们含有的氧原子数目相同,则三种气体的物质的量之比为( )
A、1:2:3 B、3:2:1 C、6:3:2 D、1:1:1
√
解析:设NO、NO2、O3三种气体都含有3mol氧原子,则NO、NO2、O3三种气体的物质的量分别为3mol、1.5mol、1mol,则三种气体的物质的量之比为6:3:2
(提升)3、下列物质所含的原子数与0.2molH3PO4所含有的原子数相等( ) A、0.2mol H2SO4 B、0.4mol H2O2
C、0.8mol NaCl D、0.3mol HNO3
√
解析:0.2molH3PO4所含有的原子数为0.2×8=1.6mol,0.2mol H2SO4中含有的原子数为0.2×7=1.4mol,0.4mol H2O2中含有的原子数为0.4×4=1.6mol,NaCl中不含有原子,只有Na+和Cl-,0.3mol HNO3中含有的原子数为0.3×5=1.5mol,故选B
4.(基础)1mol的H2O和6.02 ×1022个CO2
题点二:以n=N/NA为中心的计算
CO2的物质的量为 ;
物质的量之比 分子数之比 ;
原子数之比 氧原子数之比 。
0.1mol
10:1
10:1
10:1
5:1
5.(提升)对于1.204×1024个H2,下列说法不正确的是( )
A、它可与1molO2完全反应(点燃)
B、它是4molH
C、它与6.02×1023个CH4所含的H的数目相同
D、它与2NA个H2SO4所含的H的数目相同
√
解析:它是2molH2,不是4molH
谢谢聆听
第二章 海水中的重要元素
——钠和氯
第三节 物质的量
第1课时 物质的量的单位——摩尔
学习目标
1、宏观辨识与微观探析:通过对物质的量及其单位摩尔的学习,从微观上理解物质由不同粒子构成,进而从宏观上明确物质的量的应用。
2、证据推理与模型认知:通过完成物质的量的学习,使学生体会物理量建立的推理过程,并形成物理概念的认知模型。
3、科学态度与社会责任:通过物质的量概念的建立过程,理解化学家从微观研究到宏观概念的哲学思想和科学态度,进而培养学生学习化学的兴趣,树立良好的社会责任感。
教学重点:物质的量及其单位
教学难点:物质的量的概念建立及理解、应用
比一比:大家一口气能喝多少的水?
小明:我一口气能喝18g的水
夸父:我追赶太阳,口渴极了,我跑到了黄河边,一口气把黄河水喝完了,还是渴,我又跑到渭河边,一口气把渭河水也喝完了。
化学老师:小样,我一口气能喝下约600万亿亿个水分子
若杯子里装有100ml的水,你知道杯中水分子的个数吗?
1.67 ×1021=1670000000000000000000
1滴水≈0.05ml
1个水分子
1.67 ×1021个水分子
1.67万亿亿个
3340万亿亿个
想办法在水分子数和水的质量之间找到一个桥梁
——集体单位。
这个桥梁就是本节课标题:化学中常用的物理量
——物质的量
化学反应是原子、离子或分子之间按一定的数目关系进行的。对于原子、离子和分子等我们不仅直接用肉眼看不到,而且难以称量。用什么方法来计量原子、离子或分子(外观很小)呢?
集体单位
物 理 量 单位名称 单位符号
√长 度 米 m
√质 量 千克(公斤) kg
√时 间 秒 s
√电 流 安[培] A
热力学温度 开[尔文] K
发光强度 坎[德拉] cd
物质的量 摩[尔] mol
在1971年,由41个国家派代表参加的第14届国际
计量大会,决定新增国际单位制的第7个基本单位——物质的量,来计量原子、分子或离子等微观粒子。
判断正误:摩尔是7个基本物理量之一( )
错误。摩尔是物质的量的单位,物质的量才是基本物理量之一。
×
一、物质的量
1.概念:表示含有一定数目粒子的集合体的物理量。
3.单位:“摩尔”,简称“摩”,符号为mol
4.对象:微观粒子
【注意】①专业化:“物质的量”是一个专有名词,由四个字组成,是一个统一的整体,不能分割,也不可加字、减字。
判断正误1:物质的量将一定数目微观粒子与可称量的宏观物质之间联系起来了,以后我们就可以让“质量”这一个物理量“下岗”了( )
×
物质的质量( )
物质量( )
物质的数量( )
×
×
×
2.符号:n
判断正误2:1mol H( )0.5mol大米( )1mol苹果( )
√
×
×
【注意】②微观化:“物质的量”是只用来描述微观粒子,如原子、分子、离子、中子、质子、电子等;不能表示宏观物质。
判断正误3:1 mol H2O( )0.5 mol SO42-( )2 mol NaCl( )
√
√
√
【注意】③集体化:“物质的量”可以表示多个微粒的特定组合或集合体
思考
1 mol H、1 mol H+、1 mol H2的含义一样吗?为什么?
提示:含义不一样,尽管都是1摩尔微粒,但微粒种类不同,他们分别表示1摩尔氢原子、1摩尔氢离子、1摩尔氢分子
判断正误4:1 mol 氧( )1 mol 氧分子( )
×
必须指明微粒的种类,是氧原子、氧分子还是氧离子
【注意】④具体化:使用“物质的量”时一般用化学式表示,既规范又显得简洁准确;若用中文,则必须指明微粒的种类。如:1摩尔H、1摩尔CO2 、 1mol钠离子等。
√
说出下列语句的含义。
(1)1mol H
(2)3mol H2
(3)1mol CO2
【及时巩固】
表示氢原子的物质的量是1mol
表示氢气分子的物质的量是3mol
表示二氧化碳分子的物质的量是1mol
物质的量的表示方法:
物质的量的多少(mol)+能表示微观粒子的符号
一打铅笔是12支,
每12个为1打
一盒香烟是20支
每20支为1盒
吸烟有害健康!
【问题探究】
1mol
个
【提示】国际上规定,1mol粒子集合体所含的粒子数与0.012 kg 12C中所含的碳原子数相同。
(1)质量的单位是千克,1千克=1000克,物质的量的单位是摩尔,1mol含有多少个微粒?
【想一想】
(2)0.012 kg12C中所含的碳原子数到
底有多少个?已知一个碳原子的质量为 1.993 × 10-23g
阿伏加德罗
解:
≈ 6.02×1023
12g
1.993 × 10-23g
碳原子数=
指质子数为6,中子数为6的碳原子
二、阿伏伽德罗常数
1、国际规定:1mol任何粒子所含的粒子数与0.012kg 12C中所含的碳原子数相同。
(1) 准确量:是一个物理量,等于0.012kg 12C所含的碳原子数
(2) 近似值:约为6.02×1023 mol-1
2、含义:1mol 任何粒子的粒子数,叫阿伏加德罗常数。
3、符号及单位:符号用NA表示,单位是mol-1
①1mol是6.02×1023个微粒的粒子集合体。
概念辨析:
错误。6.02×1023是阿伏加德罗常数的近似值,二者不能简单等同。
②1mol任何物质均含有6.02×1023个原子。
错误。构成物质的微粒不同,1mol任何物质不一定含有6.02×1023个原子
③1molCO2和H2的混合气体所含的分子数约为6.02×1023
正确,1mol任何粒子集合体所含的粒子数约为6.02×1023,
这里的粒子集合体可以是纯净物,也可以是混合物。
1、喜欢下国际象棋的同学可能听说过舍罕王重赏国际象棋发现者达依尔的故事:
“陛下,请您在这张棋盘的第一个小格内,赏给我一粒麦粒;在第二个小格内给两粒;第三格内给四粒,照这样下去,后一小格都比前一小格加一倍,然后把摆在棋盘上所有64格的麦粒都赏给您的仆人吧!”
感受阿伏加德罗常数
麦粒的总数= 1 + 2 + 4 + 8 + … + 263
= 264 – 1
=1.845 × 1019
这竟是全世界在2000年内所生产的全部小麦!
感受阿伏加德罗常数
如果把 6.02×1023 粒米给全球60亿人吃,
每人每天吃一斤,要吃14万年。
如果把6.02×1023个直径为2.5cm的硬币排
成一行,可以来回于地球与太阳之间240.8亿次。
注意:摩尔只用来计量分子、原子、离子等微观粒子。
探究物质的量(n)与粒子数(N)的关系:
n(物质的量)
N(粒子总数)
1mol H
NA个H
2mol H
2×NA个H
…
…
n mol H
n×NA个H
N=
n×NA
n=
N
NA
1molH2O
【练一练】
个H2O
个H
个O
mol H
mol O
6.02×1023
2
1
1.204×1024
6.02×1023
N(H)=n(H)*NA
N(H2O)=n(H2O)*NA
n(O)=N(O)/NA
mol电子
10
在0.5 mol O2中含有的氧原子数目是多少?
解:每个O2分子中含有两个氧原子,氧原子数为
N(O)= n(O2)×2×NA
=0.5 mol×2×6.02×1023 mol-1
= 6.02×1023
答:O2中含有的氧原子数为6.02×1023个。
【练一练】
课堂小结
一、物质的量
1、概念:国际单位制中七个基本物理量之一,它表示含有一定数目粒子的集合体。
2、符号及单位:符号为n,单位为 mol。
3、单位——摩尔
符号
标准
对象
mol
1mol粒子的集合体所含的粒子数约为6.02×1023
微观粒子及其特定组合
二、阿伏伽德罗常数
阿伏伽德罗常数
含义
1mol任何粒子集合体所含的粒子数
符号是NA,单位是mol-1
符号单位
数值
约6.02×1023 mol-1
关系
n=
N/NA
(基础)1.课堂上同学们学习了“物质的量”这一物理量,以下是几位同学的谈话记录,你认为错误的是( )
A.1mol任何物质都含有阿伏伽德罗常数个微粒数
B.使用物质的量时要指明所量化的微观粒子是谁,最好用化学式表示,既规范,又显得简洁准确
C.物质的量是一个专用名词,是一个完整的名称,在读、写时不能添加或删减
D.学习了物质的量后,我们就能大致知道一杯水中大约有多少个水分子了
√
配餐作业
题点一:“物质的量”概念的理解
(提升)2、(2019 云南玉溪)现有NO、NO2、O3三种气体,它们含有的氧原子数目相同,则三种气体的物质的量之比为( )
A、1:2:3 B、3:2:1 C、6:3:2 D、1:1:1
√
解析:设NO、NO2、O3三种气体都含有3mol氧原子,则NO、NO2、O3三种气体的物质的量分别为3mol、1.5mol、1mol,则三种气体的物质的量之比为6:3:2
(提升)3、下列物质所含的原子数与0.2molH3PO4所含有的原子数相等( ) A、0.2mol H2SO4 B、0.4mol H2O2
C、0.8mol NaCl D、0.3mol HNO3
√
解析:0.2molH3PO4所含有的原子数为0.2×8=1.6mol,0.2mol H2SO4中含有的原子数为0.2×7=1.4mol,0.4mol H2O2中含有的原子数为0.4×4=1.6mol,NaCl中不含有原子,只有Na+和Cl-,0.3mol HNO3中含有的原子数为0.3×5=1.5mol,故选B
4.(基础)1mol的H2O和6.02 ×1022个CO2
题点二:以n=N/NA为中心的计算
CO2的物质的量为 ;
物质的量之比 分子数之比 ;
原子数之比 氧原子数之比 。
0.1mol
10:1
10:1
10:1
5:1
5.(提升)对于1.204×1024个H2,下列说法不正确的是( )
A、它可与1molO2完全反应(点燃)
B、它是4molH
C、它与6.02×1023个CH4所含的H的数目相同
D、它与2NA个H2SO4所含的H的数目相同
√
解析:它是2molH2,不是4molH
谢谢聆听
