1.2 物质的转化 课件(共30张PPT)2023-2024学年高一化学苏教版必修一
文档属性
| 名称 | 1.2 物质的转化 课件(共30张PPT)2023-2024学年高一化学苏教版必修一 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-07 16:44:26 | ||
图片预览











文档简介
(共30张PPT)
高中同步学案优化设计
GAO ZHONG TONG BU XUE AN YOU HUA SHE JI
专题1
第一单元 第2课时 物质的转化
素养 目标
1.了解常见单质、氧化物、酸、碱、盐之间的相互转化关系,掌握一类物质可能与哪些类别的物质发生反应,体现宏观辨识与微观探析的核心素养。
2.体验并了解研究一类物质与其他类别物质之间反应关系的过程与方法,体现科学态度与社会责任的核心素养。
基础落实·必备知识全过关
重难探究·能力素养全提升
学以致用·随堂检测全达标
目录索引
基础落实·必备知识全过关
自主梳理
一、酸、碱、盐、氧化物的通性
物质 化学通性 举例
酸 使紫色石蕊试液变红色 —
酸能与活泼金属反应放出氢气
酸能与碱发生中和反应
酸能与碱性氧化物反应
酸能与某些盐反应
由溶液中的H+体现(微观角度)
Fe+H2SO4===FeSO4+H2↑
HCl+NaOH===NaCl+H2O
CaO+2HCl===CaCl2+H2O
HCl+AgNO3===AgCl↓+HNO3
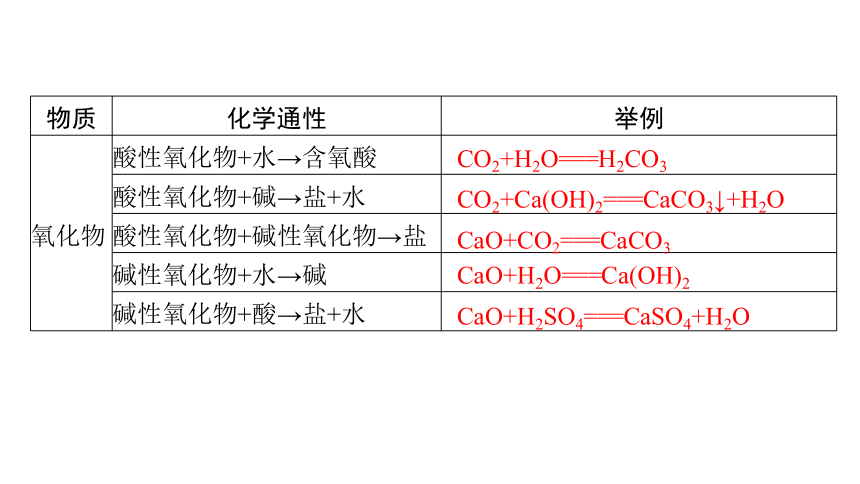
物质 化学通性 举例
氧化物 酸性氧化物+水→含氧酸
酸性氧化物+碱→盐+水
酸性氧化物+碱性氧化物→盐
碱性氧化物+水→碱
碱性氧化物+酸→盐+水
CO2+H2O===H2CO3
CO2+Ca(OH)2===CaCO3↓+H2O
CaO+CO2===CaCO3
CaO+H2O===Ca(OH)2
CaO+H2SO4===CaSO4+H2O
物质 化学通性 举例
碱 由溶液中的OH-体现(微 观角度) 使紫色石蕊试液变蓝色 —
使无色酚酞溶液变红色 —
碱+酸性氧化物→盐+水
碱+酸→盐+水
碱+盐→新碱+新盐
盐 盐+酸→新酸+新盐
盐+碱→新碱+新盐
盐+盐→新盐+新盐
由溶液中的阴、阳离子决定(微观角度)
CO2+2NaOH===Na2CO3+H2O
HCl+NaOH===NaCl+H2O
CuSO4+2NaOH===Cu(OH)2↓+Na2SO4
CaCO3+2HCl===CaCl2+CO2↑+H2O
MgCl2+2NaOH===Mg(OH)2↓+2NaCl
AgNO3+NaCl===AgCl↓+NaNO3
【微思考】能使紫色石蕊试液变红的一定是酸吗
提示 不一定,如NaHSO4溶液也能使紫色石蕊试液变红。
二、物质的转化
1.判断物质发生化学变化的基本依据:原子发生重新组合生成新物质;化学变化中 种类不发生改变。
遵循质量守恒定律
元素
2.根据物质的组成和性质,通过化学变化可实现物质间的转化。
化学方程式分别为
① 。
② 。
③ 。
④ 。
⑤ 。
⑥ 。
2Ca+O2===2CaO
CaO+H2O===Ca(OH)2
Ca(OH)2+H2SO4===CaSO4↓+2H2O
C+O2 CO2
CO2+H2O===H2CO3
Ca(OH)2+H2CO3===CaCO3↓+2H2O
3.从单质到盐的转化关系可表示为
并非都能与水反应
碱
碱
酸
酸
酸
酸
碱
碱
自我检测
判断下列说法是否正确,正确的画“√”,错误的画“×”。
(1)红热的铁丝在空气中剧烈燃烧、火星四射,生成黑色固体Fe3O4。( )
(2)把CO2气体通入澄清石灰水中,溶液变浑浊。( )
(3)所有的碱性氧化物与水反应都能得到对应的碱。( )
(4)碱与所有的盐都可以发生反应。( )
(5)酸与所有的盐都能发生反应。( )
(6)酸与碱反应都能生成水。( )
×
√
×
×
×
√
重难探究·能力素养全提升
探究 单质、氧化物、酸、碱、盐的转化关系
情境探究
(1)铁属于常见金属,可与哪些类别的物质反应
(2)硫酸属于常见的酸,可与哪些类别的物质反应
提示 铁可与某些非金属单质、酸、某些盐反应。
提示 硫酸可与活泼金属单质、碱性氧化物、碱、某些盐反应。
知识归纳
一般情况下,单质、氧化物、酸、碱、盐的转化关系
(1)金属的化学通性。
(2)氧化物的通性。
(3)酸的通性。
(4)碱的通性。
(5)盐的通性。
应用体验
1.X、Y、Z、W各代表一种物质,若X+Y===Z+W,则X和Y之间不可能是
( )
A.盐和盐的反应
B.碱性氧化物和水的反应
C.酸与碱的反应
D.酸性氧化物和碱的反应
B
解析 盐和盐反应能生成两种新盐,A可能;碱性氧化物和水反应只生成碱一种物质,B不可能;酸和碱反应生成盐和水,C可能;碱和酸性氧化物反应生成盐和水,D可能。
2.已知X和Y能发生如下反应:X+Y===H2O+盐。下列有关物质X和Y所属种类的判断中一定不正确的是( )
A.X为酸、Y为碱
B.X为碱性氧化物、Y为酸
C.X为盐、Y为碱
D.X为碱性氧化物、Y为酸性氧化物
D
解析 X和Y可能为酸和碱、碱性氧化物和酸、酸式盐和碱(如NaHCO3+NaOH===Na2CO3+H2O)。不可能是碱性氧化物和酸性氧化物,因为二者反应只生成盐,无水生成,D项符合题目要求。
3.下列物质可以与其他物质直接反应生成盐的是( )
①金属 ②碱性氧化物 ③碱 ④酸性氧化物 ⑤酸
A.①②③
B.①④
C.②⑤
D.①②③④⑤
D
解析 金属与酸反应可以生成盐,①正确;碱性氧化物与酸性氧化物或酸反应可以生成盐,②④正确;碱与酸或酸性氧化物反应可以生成盐,③⑤正确;故选D。
4.推理是化学学习中常用的思维方法,下列推理中正确的是( )
A.酸中都含有氢元素,所以含有氢元素的化合物一定是酸
B.碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性
C.酸与碱反应有盐和水生成,所以有盐和水生成的反应一定是酸与碱反应
D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
B
解析 电离产生的阳离子只有氢离子的化合物为酸,所以酸中都含有氢元素,但含有氢元素的化合物不一定是酸,如碱和酸式盐,故A错误;石蕊试液遇碱性溶液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性,故B正确;中和反应生成盐和水,但是生成盐和水的反应不一定是中和反应,如氧化铜与酸反应生成盐和水,但不是中和反应,故C错误;碳酸盐与盐酸反应放出CO2气体,锌与盐酸反应放出H2,则与盐酸反应放出气体的物质不一定是碳酸盐,故D错误。
学以致用·随堂检测全达标
1
2
3
4
5
1.科技助力北京2022年冬奥会。下列变化不属于化学变化的是( )
A.火炬“飞扬”中的氢燃料燃烧
B.二氧化碳跨临界直接制冰
C.剪切增稠流体智能分子材料的合成
D.电动汽车的全气候电池充电
B
解析 氢气燃烧有新物质生成,属于化学变化,故A不符合题意;二氧化碳跨临界直接制冰,只存在状态变化,属于物理变化,故B符合题意;合成智能分子材料有新物质生成,属于化学变化,故C不符合题意;充电过程中有新物质生成,属于化学变化,故D不符合题意。
1
2
3
4
5
2.我国科学家在国际上首次实现了从二氧化碳到淀粉的全合成。通常条件下,下列物质中不能与CO2发生反应的是( )
A.H2SO4 B.CaO
C.H2O D.NaOH
A
解析 H2SO4是酸,不能与酸性氧化物CO2发生反应,A符合题意;CaO是碱性氧化物,能够与酸性氧化物CO2反应产生CaCO3,B不符合题意;CO2能够溶于水,与水反应产生H2CO3,C不符合题意;酸性氧化物CO2能与碱NaOH发生反应,D不符合题意。
1
2
3
4
5
3.要验证Mg、Fe、Cu三种金属的活动性顺序,可选用下列哪组物质进行实验( )
A.Cu、FeCl2溶液、MgCl2溶液
B.Fe、Cu、MgCl2溶液
C.Mg、CuO、FeSO4溶液
D.Fe、CuSO4溶液、MgCl2溶液
D
解析 铜与FeCl2溶液、MgCl2溶液都不反应,没法证明,A错误;Fe、Cu和MgCl2溶液都不反应,没法证明,B错误;Mg与FeSO4溶液能反应,说明镁的活动性比铁强,但没法证明铁与铜的活动性强弱,C错误;Fe与CuSO4溶液反应置换出铜,证明铁比铜活泼,Fe不能与MgCl2溶液反应,证明镁比铁活泼,D正确。
1
2
3
4
5
4.下面为一些常见物质的pH。食醋pH=4;牙膏pH=9;食盐水pH=7;肥皂水pH=10;火碱液pH=13。蚊子、蜂、蚂蚁等昆虫叮咬人时,会向人体分泌蚁酸(具有酸性的物质),使皮肤红肿、瘙痒甚至疼痛。要消除这种症状,可在叮咬处涂抹下列物质中的( )
A.牙膏或肥皂水 B.食盐水
C.火碱液 D.食醋
A
解析 使皮肤红肿、瘙痒甚至疼痛的原因是这些昆虫向人体内射入了酸性物质,消除症状应该选用碱性物质进行中和,但火碱液碱性太强,对皮肤本身具有很强的腐蚀性,故选用碱性较弱的牙膏或肥皂水比较合适。
1
2
3
4
5
5.请写出下列转化的化学方程式。
(1)P→P2O5→H3PO4→Ca3(PO4)2;
(2)C→CO2→CaCO3。
本 课 结 束
高中同步学案优化设计
GAO ZHONG TONG BU XUE AN YOU HUA SHE JI
专题1
第一单元 第2课时 物质的转化
素养 目标
1.了解常见单质、氧化物、酸、碱、盐之间的相互转化关系,掌握一类物质可能与哪些类别的物质发生反应,体现宏观辨识与微观探析的核心素养。
2.体验并了解研究一类物质与其他类别物质之间反应关系的过程与方法,体现科学态度与社会责任的核心素养。
基础落实·必备知识全过关
重难探究·能力素养全提升
学以致用·随堂检测全达标
目录索引
基础落实·必备知识全过关
自主梳理
一、酸、碱、盐、氧化物的通性
物质 化学通性 举例
酸 使紫色石蕊试液变红色 —
酸能与活泼金属反应放出氢气
酸能与碱发生中和反应
酸能与碱性氧化物反应
酸能与某些盐反应
由溶液中的H+体现(微观角度)
Fe+H2SO4===FeSO4+H2↑
HCl+NaOH===NaCl+H2O
CaO+2HCl===CaCl2+H2O
HCl+AgNO3===AgCl↓+HNO3
物质 化学通性 举例
氧化物 酸性氧化物+水→含氧酸
酸性氧化物+碱→盐+水
酸性氧化物+碱性氧化物→盐
碱性氧化物+水→碱
碱性氧化物+酸→盐+水
CO2+H2O===H2CO3
CO2+Ca(OH)2===CaCO3↓+H2O
CaO+CO2===CaCO3
CaO+H2O===Ca(OH)2
CaO+H2SO4===CaSO4+H2O
物质 化学通性 举例
碱 由溶液中的OH-体现(微 观角度) 使紫色石蕊试液变蓝色 —
使无色酚酞溶液变红色 —
碱+酸性氧化物→盐+水
碱+酸→盐+水
碱+盐→新碱+新盐
盐 盐+酸→新酸+新盐
盐+碱→新碱+新盐
盐+盐→新盐+新盐
由溶液中的阴、阳离子决定(微观角度)
CO2+2NaOH===Na2CO3+H2O
HCl+NaOH===NaCl+H2O
CuSO4+2NaOH===Cu(OH)2↓+Na2SO4
CaCO3+2HCl===CaCl2+CO2↑+H2O
MgCl2+2NaOH===Mg(OH)2↓+2NaCl
AgNO3+NaCl===AgCl↓+NaNO3
【微思考】能使紫色石蕊试液变红的一定是酸吗
提示 不一定,如NaHSO4溶液也能使紫色石蕊试液变红。
二、物质的转化
1.判断物质发生化学变化的基本依据:原子发生重新组合生成新物质;化学变化中 种类不发生改变。
遵循质量守恒定律
元素
2.根据物质的组成和性质,通过化学变化可实现物质间的转化。
化学方程式分别为
① 。
② 。
③ 。
④ 。
⑤ 。
⑥ 。
2Ca+O2===2CaO
CaO+H2O===Ca(OH)2
Ca(OH)2+H2SO4===CaSO4↓+2H2O
C+O2 CO2
CO2+H2O===H2CO3
Ca(OH)2+H2CO3===CaCO3↓+2H2O
3.从单质到盐的转化关系可表示为
并非都能与水反应
碱
碱
酸
酸
酸
酸
碱
碱
自我检测
判断下列说法是否正确,正确的画“√”,错误的画“×”。
(1)红热的铁丝在空气中剧烈燃烧、火星四射,生成黑色固体Fe3O4。( )
(2)把CO2气体通入澄清石灰水中,溶液变浑浊。( )
(3)所有的碱性氧化物与水反应都能得到对应的碱。( )
(4)碱与所有的盐都可以发生反应。( )
(5)酸与所有的盐都能发生反应。( )
(6)酸与碱反应都能生成水。( )
×
√
×
×
×
√
重难探究·能力素养全提升
探究 单质、氧化物、酸、碱、盐的转化关系
情境探究
(1)铁属于常见金属,可与哪些类别的物质反应
(2)硫酸属于常见的酸,可与哪些类别的物质反应
提示 铁可与某些非金属单质、酸、某些盐反应。
提示 硫酸可与活泼金属单质、碱性氧化物、碱、某些盐反应。
知识归纳
一般情况下,单质、氧化物、酸、碱、盐的转化关系
(1)金属的化学通性。
(2)氧化物的通性。
(3)酸的通性。
(4)碱的通性。
(5)盐的通性。
应用体验
1.X、Y、Z、W各代表一种物质,若X+Y===Z+W,则X和Y之间不可能是
( )
A.盐和盐的反应
B.碱性氧化物和水的反应
C.酸与碱的反应
D.酸性氧化物和碱的反应
B
解析 盐和盐反应能生成两种新盐,A可能;碱性氧化物和水反应只生成碱一种物质,B不可能;酸和碱反应生成盐和水,C可能;碱和酸性氧化物反应生成盐和水,D可能。
2.已知X和Y能发生如下反应:X+Y===H2O+盐。下列有关物质X和Y所属种类的判断中一定不正确的是( )
A.X为酸、Y为碱
B.X为碱性氧化物、Y为酸
C.X为盐、Y为碱
D.X为碱性氧化物、Y为酸性氧化物
D
解析 X和Y可能为酸和碱、碱性氧化物和酸、酸式盐和碱(如NaHCO3+NaOH===Na2CO3+H2O)。不可能是碱性氧化物和酸性氧化物,因为二者反应只生成盐,无水生成,D项符合题目要求。
3.下列物质可以与其他物质直接反应生成盐的是( )
①金属 ②碱性氧化物 ③碱 ④酸性氧化物 ⑤酸
A.①②③
B.①④
C.②⑤
D.①②③④⑤
D
解析 金属与酸反应可以生成盐,①正确;碱性氧化物与酸性氧化物或酸反应可以生成盐,②④正确;碱与酸或酸性氧化物反应可以生成盐,③⑤正确;故选D。
4.推理是化学学习中常用的思维方法,下列推理中正确的是( )
A.酸中都含有氢元素,所以含有氢元素的化合物一定是酸
B.碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性
C.酸与碱反应有盐和水生成,所以有盐和水生成的反应一定是酸与碱反应
D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
B
解析 电离产生的阳离子只有氢离子的化合物为酸,所以酸中都含有氢元素,但含有氢元素的化合物不一定是酸,如碱和酸式盐,故A错误;石蕊试液遇碱性溶液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性,故B正确;中和反应生成盐和水,但是生成盐和水的反应不一定是中和反应,如氧化铜与酸反应生成盐和水,但不是中和反应,故C错误;碳酸盐与盐酸反应放出CO2气体,锌与盐酸反应放出H2,则与盐酸反应放出气体的物质不一定是碳酸盐,故D错误。
学以致用·随堂检测全达标
1
2
3
4
5
1.科技助力北京2022年冬奥会。下列变化不属于化学变化的是( )
A.火炬“飞扬”中的氢燃料燃烧
B.二氧化碳跨临界直接制冰
C.剪切增稠流体智能分子材料的合成
D.电动汽车的全气候电池充电
B
解析 氢气燃烧有新物质生成,属于化学变化,故A不符合题意;二氧化碳跨临界直接制冰,只存在状态变化,属于物理变化,故B符合题意;合成智能分子材料有新物质生成,属于化学变化,故C不符合题意;充电过程中有新物质生成,属于化学变化,故D不符合题意。
1
2
3
4
5
2.我国科学家在国际上首次实现了从二氧化碳到淀粉的全合成。通常条件下,下列物质中不能与CO2发生反应的是( )
A.H2SO4 B.CaO
C.H2O D.NaOH
A
解析 H2SO4是酸,不能与酸性氧化物CO2发生反应,A符合题意;CaO是碱性氧化物,能够与酸性氧化物CO2反应产生CaCO3,B不符合题意;CO2能够溶于水,与水反应产生H2CO3,C不符合题意;酸性氧化物CO2能与碱NaOH发生反应,D不符合题意。
1
2
3
4
5
3.要验证Mg、Fe、Cu三种金属的活动性顺序,可选用下列哪组物质进行实验( )
A.Cu、FeCl2溶液、MgCl2溶液
B.Fe、Cu、MgCl2溶液
C.Mg、CuO、FeSO4溶液
D.Fe、CuSO4溶液、MgCl2溶液
D
解析 铜与FeCl2溶液、MgCl2溶液都不反应,没法证明,A错误;Fe、Cu和MgCl2溶液都不反应,没法证明,B错误;Mg与FeSO4溶液能反应,说明镁的活动性比铁强,但没法证明铁与铜的活动性强弱,C错误;Fe与CuSO4溶液反应置换出铜,证明铁比铜活泼,Fe不能与MgCl2溶液反应,证明镁比铁活泼,D正确。
1
2
3
4
5
4.下面为一些常见物质的pH。食醋pH=4;牙膏pH=9;食盐水pH=7;肥皂水pH=10;火碱液pH=13。蚊子、蜂、蚂蚁等昆虫叮咬人时,会向人体分泌蚁酸(具有酸性的物质),使皮肤红肿、瘙痒甚至疼痛。要消除这种症状,可在叮咬处涂抹下列物质中的( )
A.牙膏或肥皂水 B.食盐水
C.火碱液 D.食醋
A
解析 使皮肤红肿、瘙痒甚至疼痛的原因是这些昆虫向人体内射入了酸性物质,消除症状应该选用碱性物质进行中和,但火碱液碱性太强,对皮肤本身具有很强的腐蚀性,故选用碱性较弱的牙膏或肥皂水比较合适。
1
2
3
4
5
5.请写出下列转化的化学方程式。
(1)P→P2O5→H3PO4→Ca3(PO4)2;
(2)C→CO2→CaCO3。
本 课 结 束
