7.2.1乙烯的性质课件(共47张PPT)2023-2024学年高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 7.2.1乙烯的性质课件(共47张PPT)2023-2024学年高一下学期化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 18.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-07 00:00:00 | ||
图片预览










文档简介
(共47张PPT)
第七章 有机化合物
第2节 乙烯与有机高分子材料
第1课时 乙烯的性质
素养目标 1.以乙烯为例,认识有机化合物中的碳碳双键的结构,培养宏观辨识与微观探析的能力。
2.通过实验探究,掌握乙烯的氧化反应、加成反应及加聚反应,培养科学探究与创新意识。
3.了解乙烯的用途,培养科学态度与社会责任等学科素养。
【问题情境】:为了促进香蕉成熟,可在密封袋子中放一些成熟的苹果,这是为什么?
认识乙烯
石油最初的用途是燃料,后来偶然发现石油可
以生产出聚乙烯(即日常使用的塑料)这种新材料,
就有了石油化工行业。塑料以飞快的速度成为20世
纪人类手里最重要的一种材料,乙烯也是产量最大的石油化工产品。
由于聚乙烯说是最初被发现的聚合材料,所以最初的石油化工业可以说是乙烯工业。
乙烯
1.乙烯的来源
2.乙烯的用途
石油 乙烯。
分馏、裂化、裂解
乙烯的产量可以用来衡量一个国家的石油化工水平。
(1)重要的化工原料,用于生产有机高分子材料、药物等。
(2)植物生长的调节剂和果蔬的催熟剂。
乙烯
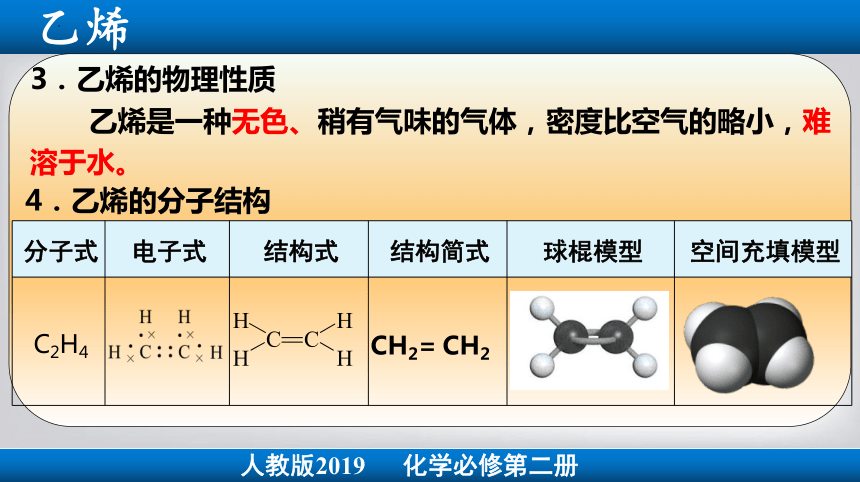
3.乙烯的物理性质
乙烯是一种无色、稍有气味的气体,密度比空气的略小,难溶于水。
4.乙烯的分子结构
分子式 电子式 结构式 结构简式 球棍模型 空间充填模型
C2H4
CH2= CH2
乙烯
【归纳】:乙烯分子6个原子共平面,键角120°,平面型分子,分子中有碳碳双键,碳原子的价键没有全部被氢原子“饱和”。
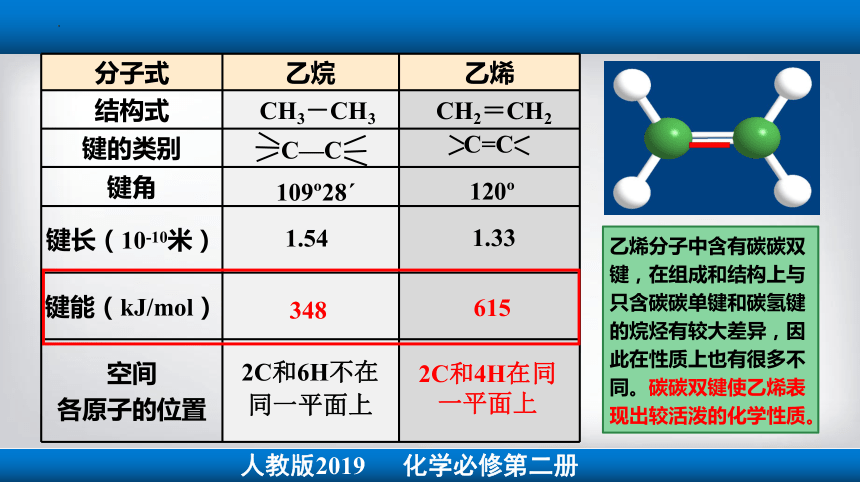
分子式 乙烷 乙烯
结构式
键的类别
键角
键长(10-10米)
键能(kJ/mol)
空间 各原子的位置
2C和4H在同一平面上
109 28ˊ
1.54
348
2C和6H不在同一平面上
120
1.33
615
CH2=CH2
CH3-CH3
C—C
C=C
乙烯分子中含有碳碳双键,在组成和结构上与只含碳碳单键和碳氢键的烷烃有较大差异,因此在性质上也有很多不同。碳碳双键使乙烯表现出较活泼的化学性质。
1.氧化反应
CH2=CH2
+
3O2
点燃
2CO2 + 2H2O
(1)燃烧
现象:火焰明亮,并伴有黑烟,同时放出大量的热。
二、乙烯的化学性质
【实验7-2】(1)点燃纯净的乙烯,观察燃烧时的现象。
【问题探究】
1、乙烯与乙烷燃烧有何不同?为什么?
火焰明亮,伴有黑烟。乙烯的含碳量高,在空气中燃烧不充分,有黑色的炭粒。
【实验7-2】将乙烯通入盛有酸性高锰酸钾溶液的试管中,观察现象。
二、乙烯的化学性质
1.氧化反应
现象:溶液的紫色褪去
应用:鉴别乙烯(与烷烃比)
(2)被酸性KMnO4溶液氧化
CH2=CH2 (C2H4)
CO2
KMnO4(H+)
【问题探究】
1、酸性高锰酸钾具有什么性质?
2、乙烯通入酸性高锰酸钾现象是什么?发生了什么反应?
3、烷烃能使酸性高锰酸钾褪色吗?为什么?
4、如何鉴别乙烷和乙烯?
5、能否用酸性高锰酸钾除去乙烷中的乙烯?
酸性高锰酸钾溶液褪色,乙烯被氧化为二氧化碳。
能使酸性高锰酸钾褪色的是乙烯。
不能,只用酸性高锰酸钾,会引入杂质气体二氧化碳。
强氧化性,高锰酸钾是常见的强氧化剂。
烷烃不能被高锰酸钾氧化;能被高锰酸钾氧化是不饱和烃的一种性质
信息提示:烷烃性质比较稳定,常温下不能与酸、碱和氧化剂反应,
【实验7-3】
将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
【问题探究】
1 、乙烯通入溴的四氯化碳溶液有何现象?
2、根据给出的产物结构,你认为断键位置和成键位置是什么?
3、这个反应是取代反应吗?与取代反应有何不同?你认为乙烷为什么不能发生该反应?
溶液褪色。
碳碳双键中的一个碳碳键断裂,单质溴中的溴溴单键断裂,断了的碳与溴形成新键。
不是,原子加入到断裂的碳碳键两端。乙烷中没有碳碳双键,不能发生此反应。
345 kJ mol—1
265 kJ mol—1
2、加成反应
乙烯碳碳双键中的一个键断裂,两个溴原子分别加在两个价键不饱和的碳原子上,生成无色的1,2-二溴乙烷液体,使得溴的四氯化碳溶液/溴水褪色:
H — C=C — H+Br—Br H — C — C — H
H
H
Br
Br
H
H
碳碳双键中有一个键易断
1,2-二溴乙烷
二、乙烯的化学性质
加成反应
有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应叫加成反应。(形式上类似于化合反应)
1、原理分析(以CH2=CH2和Br2加成为例)
我是
溴分子
加成反应机理
加成反应
在一定条件下,乙烯还可以与H2、Cl2、H2O、HCl等物质
发生加成反应:
①与 H2 加成:CH2 = CH2 + H2 ______________
②与 H2O 加成: CH2 = CH2 + H2O _____________
③与 Cl2 加成: CH2 = CH2 + Cl2 _____________
④与 HCl 加成: CH2 = CH2 + HCl _____________
CH3CH3
CH3CH2OH
CH2ClCH2Cl
CH3CH2Cl
工业制
备乙醇
取 代 反 应 加 成 反 应
意 义
归 属
断键规律
产物特点
小结:取代反应与加成反应的比较
取而代之,有进有出
加而成之,有进无出
烷烃的特征反应
烯烃的特征反应
C-H 断裂
C-C断裂
一种产物
产物较纯净
两种产物
产物复杂,为混合物
问题10:制取氯乙烷,是采取CH3-CH3与Cl2取代反应好,还是采用CH2==CH2与HCl加成反应好?
课堂巩固
1.判断正误(正确的打“√”,错误的打“×”)
(1)乙烯分子中含有,为不饱和化合物。 ( )
(2)乙烯与甲烷的燃烧现象相同,均有黑烟生成。 ( )
(3)乙烯使溴水、酸性KMnO4溶液褪色的反应原理相同。( )
(4)CH2=CH2与 相差一个CH2,互为同系物。( )
(5)酸性KMnO4 既可以验证乙烷和乙烯,还可以除去乙烷中混有的乙烯。 ( )
√
×
×
×
×
2、下列各反应属于加成反应的是( )
课堂巩固
B
3、甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶 ( )
A. 澄清石灰水,浓硫酸
B. 溴水,浓硫酸
C. 酸性高锰酸钾溶液,浓硫酸
D. 浓硫酸,酸性高锰酸钾溶液
课堂巩固
B
课堂巩固
4、长途运输水果时,常常将浸泡有高锰酸钾溶液的硅土放置在盛放水果的容器中,其目的是( )
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
C
课堂巩固
5、(多选)由乙烯性质推测丙烯(CH2= CHCH3)性质,那么丙烯与HCl反应的产物可能是( )
A.CH3— CH2—CH2Cl
B.CH3— CH— CH2Cl
C.CH2Cl— CH2— CH3
D.CH3— CHCl— CH3
ACD
水果包装
趣味活动
探究活动 请三组同学,两两充当乙烯分子,没有其他分子的参与下,
如何使更多的乙烯分子相连在一起?
任务:探究乙烯如何转化为聚乙烯,写出该反应的化学方程式。
二、乙烯的化学性质
在适当的温度、压强和催化剂存在的条件下,乙烯分子中碳碳双键中的一个键断裂,分子间通过碳原子相互结合形成很长的碳链,生成相对分子质量很大的聚合物聚乙烯。
n CH2=CH2
[ CH2—CH2 ]n
催化剂
(聚乙烯)
链节
聚合度
单体
3.加聚反应
像这样,由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应叫做聚合反应。聚合反应在有机高分子材料的生产中有着广泛的应用。乙烯的聚合反应同时也是加成反应,这样的反应又被称为加成聚合反应,简称加聚反应。
加聚反应高聚物的写法
(1)含一个碳碳双键的单体聚合物的写法:断开双键,键分两端,添上括号,n在后面。
(2)含“C=C—C=C”的单体聚合物的写法:双变单,单变双,括住两头,n在后面。
(3)含有一个碳碳双键的两个单体聚合物的写法:双键打开,彼此相连,括住两头,n在后面。
加聚反应生成高聚物的单体的判断
[ CH2— CH ]n
Cl
CH2=CH
Cl
[ CH—CH ]n
CH3
CH3
CH—CH
CH3
CH3
[CH2-CH2-CH-CH2]n
CH3
CH2=CH2 CH=CH2
CH3
CH2CH3
[ CH2-CH=C-CH2 ]n
CH2CH3
CH2=CH—C=CH2
科学合理使用,
化学让生活更美好!
(1)有机化工原料
(2)植物生长调节剂,催熟剂
三、乙烯的用途
→聚乙烯塑料→食品袋、餐具、地膜等
→聚乙烯纤维→无纺布
→乙醇→燃料、化工原料
→涤纶→纺织材料等
→洗涤剂、乳化剂、防冻液
→醋酸纤维、酯类
→增塑剂
→杀虫剂、植物生长调节剂
→聚氯乙烯塑料→包装袋、管材等
→合成润滑油、高级醇、聚乙二醇
乙 烯
衡量一个国家石油化工发展水平的标志是什么?
乙烯的产量
课堂小结
乙烯的性质
稍有气味水难溶,
高锰酸钾溴反应。
现象相同理不同,
前因氧化后加成。
加氧燃烧黑烟冒,
聚合分子碳链增。
课堂巩固
1、有机化学中的反应类型较多,将下列反应归类(填序号)。
①乙烷在空气中燃烧 ②乙烯使溴的四氯化碳溶液褪色
③乙烯使酸性高锰酸钾溶液褪色 ④由乙烯制聚乙烯
⑤甲烷与氯气在光照的条件下反应
其中属于取代反应的是__________;属于氧化反应的是__________;属于加成反应的是__________;④的反应类型是_______________。
⑤
①③
②
加聚反应
课堂巩固
2、由乙烯推测丙烯(CH2=CH—CH3)的结构或性质正确的是
A.不能使酸性高锰酸钾溶液褪色
B.不能发生加聚反应
C.能使溴的四氯化碳溶液褪色
D.与HCl在一定条件下能加成并只得到一种产物
C
3.长途运输水果时,常常将浸泡有高锰酸钾溶液的硅土放置在盛放水果的容器中,其目的是( )
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
C
课堂巩固
4.能证明乙烯分子中含有一个碳碳双键的事实是( )
A.乙烯分子中碳、氢原子的个数比为1∶2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯易与溴水发生加成反应,且1 mol乙烯完全加成需消耗1 mol溴单质
D.乙烯能使酸性KMnO4溶液褪色
C
5.1molCH2=CH2与氯气完全加成后再与氯气取代,整个过程最多需Cl2的物质的量为( )
A.1mol B.4mol C.5mol D.6mol
C
课堂巩固
课堂巩固
6、含有碳碳双键的有机物很多,其性质和乙烯相似,写出下列要求的方程式。
(1)丙烯与溴水反应: 。
(2)丙烯在一定条件下加聚生成聚丙烯:
。
CH3—CH=CH2+Br2
n CH3—CH=CH2
本课结束!
第七章 有机化合物
第2节 乙烯与有机高分子材料
第1课时 乙烯的性质
素养目标 1.以乙烯为例,认识有机化合物中的碳碳双键的结构,培养宏观辨识与微观探析的能力。
2.通过实验探究,掌握乙烯的氧化反应、加成反应及加聚反应,培养科学探究与创新意识。
3.了解乙烯的用途,培养科学态度与社会责任等学科素养。
【问题情境】:为了促进香蕉成熟,可在密封袋子中放一些成熟的苹果,这是为什么?
认识乙烯
石油最初的用途是燃料,后来偶然发现石油可
以生产出聚乙烯(即日常使用的塑料)这种新材料,
就有了石油化工行业。塑料以飞快的速度成为20世
纪人类手里最重要的一种材料,乙烯也是产量最大的石油化工产品。
由于聚乙烯说是最初被发现的聚合材料,所以最初的石油化工业可以说是乙烯工业。
乙烯
1.乙烯的来源
2.乙烯的用途
石油 乙烯。
分馏、裂化、裂解
乙烯的产量可以用来衡量一个国家的石油化工水平。
(1)重要的化工原料,用于生产有机高分子材料、药物等。
(2)植物生长的调节剂和果蔬的催熟剂。
乙烯
3.乙烯的物理性质
乙烯是一种无色、稍有气味的气体,密度比空气的略小,难溶于水。
4.乙烯的分子结构
分子式 电子式 结构式 结构简式 球棍模型 空间充填模型
C2H4
CH2= CH2
乙烯
【归纳】:乙烯分子6个原子共平面,键角120°,平面型分子,分子中有碳碳双键,碳原子的价键没有全部被氢原子“饱和”。
分子式 乙烷 乙烯
结构式
键的类别
键角
键长(10-10米)
键能(kJ/mol)
空间 各原子的位置
2C和4H在同一平面上
109 28ˊ
1.54
348
2C和6H不在同一平面上
120
1.33
615
CH2=CH2
CH3-CH3
C—C
C=C
乙烯分子中含有碳碳双键,在组成和结构上与只含碳碳单键和碳氢键的烷烃有较大差异,因此在性质上也有很多不同。碳碳双键使乙烯表现出较活泼的化学性质。
1.氧化反应
CH2=CH2
+
3O2
点燃
2CO2 + 2H2O
(1)燃烧
现象:火焰明亮,并伴有黑烟,同时放出大量的热。
二、乙烯的化学性质
【实验7-2】(1)点燃纯净的乙烯,观察燃烧时的现象。
【问题探究】
1、乙烯与乙烷燃烧有何不同?为什么?
火焰明亮,伴有黑烟。乙烯的含碳量高,在空气中燃烧不充分,有黑色的炭粒。
【实验7-2】将乙烯通入盛有酸性高锰酸钾溶液的试管中,观察现象。
二、乙烯的化学性质
1.氧化反应
现象:溶液的紫色褪去
应用:鉴别乙烯(与烷烃比)
(2)被酸性KMnO4溶液氧化
CH2=CH2 (C2H4)
CO2
KMnO4(H+)
【问题探究】
1、酸性高锰酸钾具有什么性质?
2、乙烯通入酸性高锰酸钾现象是什么?发生了什么反应?
3、烷烃能使酸性高锰酸钾褪色吗?为什么?
4、如何鉴别乙烷和乙烯?
5、能否用酸性高锰酸钾除去乙烷中的乙烯?
酸性高锰酸钾溶液褪色,乙烯被氧化为二氧化碳。
能使酸性高锰酸钾褪色的是乙烯。
不能,只用酸性高锰酸钾,会引入杂质气体二氧化碳。
强氧化性,高锰酸钾是常见的强氧化剂。
烷烃不能被高锰酸钾氧化;能被高锰酸钾氧化是不饱和烃的一种性质
信息提示:烷烃性质比较稳定,常温下不能与酸、碱和氧化剂反应,
【实验7-3】
将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
【问题探究】
1 、乙烯通入溴的四氯化碳溶液有何现象?
2、根据给出的产物结构,你认为断键位置和成键位置是什么?
3、这个反应是取代反应吗?与取代反应有何不同?你认为乙烷为什么不能发生该反应?
溶液褪色。
碳碳双键中的一个碳碳键断裂,单质溴中的溴溴单键断裂,断了的碳与溴形成新键。
不是,原子加入到断裂的碳碳键两端。乙烷中没有碳碳双键,不能发生此反应。
345 kJ mol—1
265 kJ mol—1
2、加成反应
乙烯碳碳双键中的一个键断裂,两个溴原子分别加在两个价键不饱和的碳原子上,生成无色的1,2-二溴乙烷液体,使得溴的四氯化碳溶液/溴水褪色:
H — C=C — H+Br—Br H — C — C — H
H
H
Br
Br
H
H
碳碳双键中有一个键易断
1,2-二溴乙烷
二、乙烯的化学性质
加成反应
有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应叫加成反应。(形式上类似于化合反应)
1、原理分析(以CH2=CH2和Br2加成为例)
我是
溴分子
加成反应机理
加成反应
在一定条件下,乙烯还可以与H2、Cl2、H2O、HCl等物质
发生加成反应:
①与 H2 加成:CH2 = CH2 + H2 ______________
②与 H2O 加成: CH2 = CH2 + H2O _____________
③与 Cl2 加成: CH2 = CH2 + Cl2 _____________
④与 HCl 加成: CH2 = CH2 + HCl _____________
CH3CH3
CH3CH2OH
CH2ClCH2Cl
CH3CH2Cl
工业制
备乙醇
取 代 反 应 加 成 反 应
意 义
归 属
断键规律
产物特点
小结:取代反应与加成反应的比较
取而代之,有进有出
加而成之,有进无出
烷烃的特征反应
烯烃的特征反应
C-H 断裂
C-C断裂
一种产物
产物较纯净
两种产物
产物复杂,为混合物
问题10:制取氯乙烷,是采取CH3-CH3与Cl2取代反应好,还是采用CH2==CH2与HCl加成反应好?
课堂巩固
1.判断正误(正确的打“√”,错误的打“×”)
(1)乙烯分子中含有,为不饱和化合物。 ( )
(2)乙烯与甲烷的燃烧现象相同,均有黑烟生成。 ( )
(3)乙烯使溴水、酸性KMnO4溶液褪色的反应原理相同。( )
(4)CH2=CH2与 相差一个CH2,互为同系物。( )
(5)酸性KMnO4 既可以验证乙烷和乙烯,还可以除去乙烷中混有的乙烯。 ( )
√
×
×
×
×
2、下列各反应属于加成反应的是( )
课堂巩固
B
3、甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶 ( )
A. 澄清石灰水,浓硫酸
B. 溴水,浓硫酸
C. 酸性高锰酸钾溶液,浓硫酸
D. 浓硫酸,酸性高锰酸钾溶液
课堂巩固
B
课堂巩固
4、长途运输水果时,常常将浸泡有高锰酸钾溶液的硅土放置在盛放水果的容器中,其目的是( )
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
C
课堂巩固
5、(多选)由乙烯性质推测丙烯(CH2= CHCH3)性质,那么丙烯与HCl反应的产物可能是( )
A.CH3— CH2—CH2Cl
B.CH3— CH— CH2Cl
C.CH2Cl— CH2— CH3
D.CH3— CHCl— CH3
ACD
水果包装
趣味活动
探究活动 请三组同学,两两充当乙烯分子,没有其他分子的参与下,
如何使更多的乙烯分子相连在一起?
任务:探究乙烯如何转化为聚乙烯,写出该反应的化学方程式。
二、乙烯的化学性质
在适当的温度、压强和催化剂存在的条件下,乙烯分子中碳碳双键中的一个键断裂,分子间通过碳原子相互结合形成很长的碳链,生成相对分子质量很大的聚合物聚乙烯。
n CH2=CH2
[ CH2—CH2 ]n
催化剂
(聚乙烯)
链节
聚合度
单体
3.加聚反应
像这样,由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应叫做聚合反应。聚合反应在有机高分子材料的生产中有着广泛的应用。乙烯的聚合反应同时也是加成反应,这样的反应又被称为加成聚合反应,简称加聚反应。
加聚反应高聚物的写法
(1)含一个碳碳双键的单体聚合物的写法:断开双键,键分两端,添上括号,n在后面。
(2)含“C=C—C=C”的单体聚合物的写法:双变单,单变双,括住两头,n在后面。
(3)含有一个碳碳双键的两个单体聚合物的写法:双键打开,彼此相连,括住两头,n在后面。
加聚反应生成高聚物的单体的判断
[ CH2— CH ]n
Cl
CH2=CH
Cl
[ CH—CH ]n
CH3
CH3
CH—CH
CH3
CH3
[CH2-CH2-CH-CH2]n
CH3
CH2=CH2 CH=CH2
CH3
CH2CH3
[ CH2-CH=C-CH2 ]n
CH2CH3
CH2=CH—C=CH2
科学合理使用,
化学让生活更美好!
(1)有机化工原料
(2)植物生长调节剂,催熟剂
三、乙烯的用途
→聚乙烯塑料→食品袋、餐具、地膜等
→聚乙烯纤维→无纺布
→乙醇→燃料、化工原料
→涤纶→纺织材料等
→洗涤剂、乳化剂、防冻液
→醋酸纤维、酯类
→增塑剂
→杀虫剂、植物生长调节剂
→聚氯乙烯塑料→包装袋、管材等
→合成润滑油、高级醇、聚乙二醇
乙 烯
衡量一个国家石油化工发展水平的标志是什么?
乙烯的产量
课堂小结
乙烯的性质
稍有气味水难溶,
高锰酸钾溴反应。
现象相同理不同,
前因氧化后加成。
加氧燃烧黑烟冒,
聚合分子碳链增。
课堂巩固
1、有机化学中的反应类型较多,将下列反应归类(填序号)。
①乙烷在空气中燃烧 ②乙烯使溴的四氯化碳溶液褪色
③乙烯使酸性高锰酸钾溶液褪色 ④由乙烯制聚乙烯
⑤甲烷与氯气在光照的条件下反应
其中属于取代反应的是__________;属于氧化反应的是__________;属于加成反应的是__________;④的反应类型是_______________。
⑤
①③
②
加聚反应
课堂巩固
2、由乙烯推测丙烯(CH2=CH—CH3)的结构或性质正确的是
A.不能使酸性高锰酸钾溶液褪色
B.不能发生加聚反应
C.能使溴的四氯化碳溶液褪色
D.与HCl在一定条件下能加成并只得到一种产物
C
3.长途运输水果时,常常将浸泡有高锰酸钾溶液的硅土放置在盛放水果的容器中,其目的是( )
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
C
课堂巩固
4.能证明乙烯分子中含有一个碳碳双键的事实是( )
A.乙烯分子中碳、氢原子的个数比为1∶2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯易与溴水发生加成反应,且1 mol乙烯完全加成需消耗1 mol溴单质
D.乙烯能使酸性KMnO4溶液褪色
C
5.1molCH2=CH2与氯气完全加成后再与氯气取代,整个过程最多需Cl2的物质的量为( )
A.1mol B.4mol C.5mol D.6mol
C
课堂巩固
课堂巩固
6、含有碳碳双键的有机物很多,其性质和乙烯相似,写出下列要求的方程式。
(1)丙烯与溴水反应: 。
(2)丙烯在一定条件下加聚生成聚丙烯:
。
CH3—CH=CH2+Br2
n CH3—CH=CH2
本课结束!
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
