1.2 物质结构研究的范式与方法 课件 (共49张PPT)2023-2024学年高二化学苏教版选择性必修2
文档属性
| 名称 | 1.2 物质结构研究的范式与方法 课件 (共49张PPT)2023-2024学年高二化学苏教版选择性必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-09 00:00:00 | ||
图片预览











文档简介
(共49张PPT)
专题1 揭示物质结构的奥秘
第二单元 物质结构研究的范式与方法
素 养 目 标
1.认识物质结构研究的两种范式及其相互关系,培养证据推理与模型认知的化学核心素养。
2.能举例说明科学假设和论证、实验方法、模型方法等在物质结构研究中起的重要作用,培养宏观辨识与微观探析、证据推理与模型认知的化学核心素养。
3.能描述现代仪器和手段为测定物质结构、建立相关理论作出的重要贡献,培养科学探究与创新意识的化学核心素养。
基础落实·必备知识全过关
重难探究·能力素养全提升
目 录 索 引
基础落实·必备知识全过关
一、物质结构研究的范式
1.归纳范式
从个别到一般
(1)含义:根据事实进行 ,抽象出 ,上升为
。
概括归纳
共同点
本质规律
(2)例证
个别性质 一般规律
通过甲烷(CH4)、乙烷(C2H6)、丙烷(C3H8)、丁烷(C4H10)等的分子式 归纳出饱和烷烃的通式为
通过1~20号元素的 认识前20号元素对应 归纳出元素核外 规律,并从结构上解释同族元素
相似的原因
通过研究含有双键和三键的不饱和烃,发现这类物质容易发生 反应和 反应,不饱和键具有 的性质 根据结构与性质的关系归纳出这类有机物的
原子核外电子排布
原子结构的不同
电子排布
性质
加成
氧化
不稳定
通性
2.演绎范式
从一般到个别
(1)含义:是从某个 出发,向从属于这一结论的
的过程。
一般结论
多个要素进行推理
(2)例证
一般规律 个别性质
门捷列夫建立了 人们发现了“类铝” ,“类硼” ,
“类硅”
根据钠原子最外电子层上1个电子 的特点 推出同族半径更大的 元素具有更强的还原性的结论
水是 性较强的分子,水分子之间存在较强的 ,水分子既可为生成氢键 ,又有孤电子对 CH3CH2OH、CH3COOH极性与水相似,
均可通过 和水结合,在水中的
较大;碳氢化合物 性较小,也难以和水形成 ,在水中溶解度很 ,这就是著名的
“ ”
元素周期表
(镓)
(铊)
(锗)
极易失去表现出强还原性
钾、铷、铯
极
氢键
提供H
接受H
氢键
溶解度
极
氢键
小
相似相溶规则
3.归纳与演绎的关系
(1)化学研究的途径一般为先 、后 。
(2)演绎是从一般到个别,从理论到新的事实;演绎需要归纳提供前提,归纳需要演绎作为指导。
(3)在演绎的指导下归纳,在归纳的基础上演绎。
归纳
演绎
教材阅读 想一想阅读教材“物质结构研究的范式”。
思考:全国科技名词委联合国家语言文字工作委员会召开113号、115号、117号、118号元素中文定名会,形成了《113号、115号、117号、118号元素中文定名方案》,如表所示。由元素周期表推断元素运用了物质结构研究的什么范式
提示 由一般到个别,是演绎范式。
易错辨析 判一判
(1)由元素周期表发现新的元素属于归纳范式。( )
提示 从一般到个别是演绎范式。
(2)由硅是半导体材料推断锡也是半导体材料。( )
提示 硅在金属与非金属分界线上,而锡是典型的金属材料。
(3)归纳范式和演绎范式均为独立的研究方法,不能融合。( )
提示 研究物质结构需要各种范式结合。
(4)从CH3OH、CH3CH2OH、CH3CH2CH2OH等分子中归纳出饱和一元醇的通式为CnH2n+2O,为归纳范式。( )
×
×
×
√
二、物质结构研究的方法
1.科学假设和论证
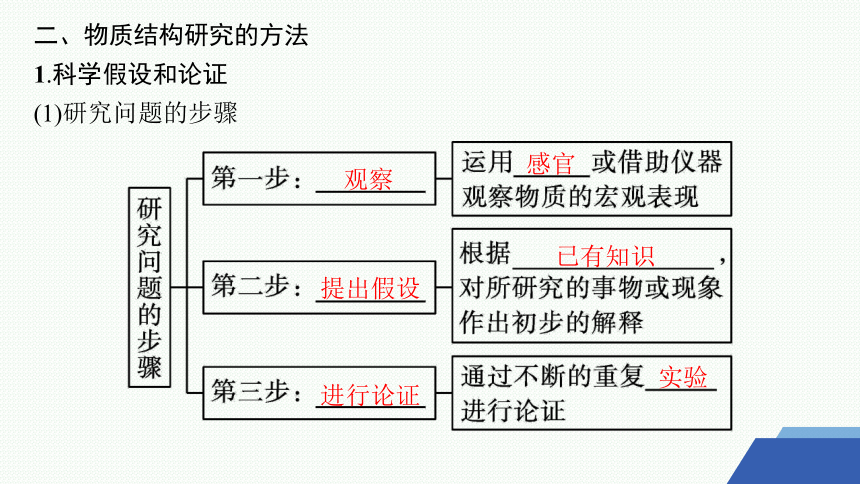
(1)研究问题的步骤
观察
感官
提出假设
已有知识
进行论证
实验
(2)建立理论
①理论: 。
②建立原则:建立在科学家一次又一次的 的基础之上。
建立在大量的观察基础之上并为实验所证实的解释
观察和实验
2.实验方法
(1)含义:化学是一门以实验为基础的学科,人们往往需要借助实验观测的事实对假设的正确与否进行检验。
(2)例证
实验方法 意义
卢瑟福的 实验 启迪人们用粒子轰击和对撞的实验来研究物质的 ,提供了一种研究物质 的思想方法
光学显微镜、扫描隧道显微镜、原子力显微镜等仪器出现,各种光谱和晶体X射线衍射实验方法应用于研究原子、分子和晶体结构 使原子和分子的微观世界不断被揭示
α粒子散射
内部结构
微观结构
3.模型方法
(1)含义:科学家运用一定 对实验结果进行处理。
(2)方法:模型既可以是对原型的 ,也可以是结合某种理论形态下建立的 。
逻辑推理与模型思维
简化和纯化、抽象和近似
思维模型
(3)分类
分类 实物模型 微观结构模型
含 义 可观察到的物体的宏观模型 物质微观层次结构,难以直接观察到,需要通过思维加工使 的微观世界以 的形式展现出来
实 例 如____________________ 如原子结构模型、离子键模型、共价键模型和氢键模型,有机化合物的分子结构模型等
抽象
可视化
汽车模型、飞机模型
和建筑模型
(4)作用
①对沟通科学现象与其本质的认识过程,起到重要的桥梁作用。
②利用模型深刻地认识物质的微观结构特点,揭示结构与性质的关系,是模型研究的重要功能。
教材阅读 想一想自学教材“模型方法”。
思考:乙烯的空间填充模型为 ,该空间填充模型属于哪类模型
提示 属于微观结构模型。
易错辨析 判一判
(1)理论都是正确的,不需要修改。( )
提示 当反常现象大量出现,而原有理论又不能很好地做出解释时,就需要对原有理论加以修改。
(2)模型就是对物质真实形状的加工。( )
提示 微观结构模型是通过思维加工使抽象的微观世界以可视化的形式展现出来,不能说是对物质真实形状的加工。
(3)实验法只能通过化学实验才能实现。( )
提示 物理实验、通过仪器研究也是实验法。
(4)锗是优良的半导体,锗元素属于金属元素,但也具有一定的非金属性。
( )
×
×
×
√
重难探究·能力素养全提升
探究一 归纳范式与演绎范式的关系
情境探究
在研究元素周期律的过程中,门捷列夫仔细分析了当时已知的63种元素的物理性质和化学性质,他准备了许多扑克牌一样的卡片,将63种化学元素的名称及其原子量(即相对原子质量)、氧化物、物理性质、化学性质等分别写在卡片上面。1869年3月1日,门捷列夫仍然在对着这些卡片苦苦思索,他惊喜地发现,所有的已知元素都已经按照原子量递增的顺序排列起来,并且相似元素以一定的间隔出现。第二天门捷列夫将所得出的结果制成一张表,这是人类历史上第一张化学元素周期表。在门捷列夫的元素周期表中,他大胆地为尚待发现的元素留出了位置,并且在其关于元素周期表的发现的论文中指出:按着原子量由小到大的顺序排列各种元素,在原子量跳跃
过大的地方会有新元素被发现,因此元素周期律可以预言尚待发现的元素。
1871年,门捷列夫预言一定存在一种元素,在元素周期表中它紧排在锌的后面,处于铝和铟之间,他将其称为“类铝”,并预测了它的性质。1875年,法国化学家布瓦博德朗在分析闪锌矿时发现一种新元素,将它命名为镓,并将他测得的主要性质公之于众,不久便收到了门捷列夫的来信,信中说镓的比重不是4.7而是5.9,当时布瓦博德朗很疑惑,门捷列夫是怎样知道镓的比重的呢 经重新测定,镓的比重是5.9,结果使他大为惊奇,他认真阅读了门捷列夫的元素周期律论文后,感慨地说:“我没有可说的了,事实证明门捷列夫这一理论的巨大意义。”
1.门捷列夫根据当时已知的63种元素,排布出第一个元素周期表,这是运用了物质结构研究的什么范式
2.门捷列夫运用元素周期表预测了“类铝”,这是运用了物质结构研究的什么范式
提示 由个别到一般,属于归纳范式。
提示 由一般到个别,属于演绎范式。
3.学习元素周期律后,有同学根据原子结构判断碱金属最外层只有一个电子,易失电子呈还原性,进而该同学推断出ⅡA族的原子也易失电子具有还原性,这是运用了物质结构研究的什么范式
4.根据结论:ⅡA族的原子易失电子具有还原性,有同学总结出原子核外最外层电子数是两个的原子都具有强还原性。这是运用了物质结构研究的什么范式 这种结论是否正确
提示 由一般到一般,属于演绎范式。
提示 由个别到一般,属于归纳范式。这种结论不正确,如氦元素原子最外层电子数是两个,不易得也不易失,不具有强还原性。
方法突破
1.归纳与演绎的不同点
2.归纳与演绎的联系
(1)从科学研究的途径来看归纳和演绎的使用,一般为先归纳、后演绎。“实验—假说—理论—新实验”的过程,本质上就是从个别到一般,再到个别的过程。
(2)归纳需要演绎作指导,以解决研究的目的性、方向性和结果的正确性问题;而演绎需要归纳提供前提。在演绎的指导下归纳,在归纳的基础上演绎,两者互相联系、互为前提。
应用体验
视角 物质结构研究的范式
1.门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第4周期的三种元素留下了空位,并对它们的一些性质作了预测,X是其中的一种“类硅”元素,后来被德国化学家温克勒发现,并证实门捷列夫当时的预测相当准确。下列有关描述中错误的是( )
A.根据一般规律的预测结果都是正确的
B.由周期表推断元素是利用了演绎范式
C.由硅的结构可以通过科学假设和论证方法研究“类硅”的结构
D.可以通过实验方法研究硅及“类硅”结构的区别
A
解析 预测可能是正确的,也可能是错误的,要经过不断地重复实验进行论证。
考题点睛
易错提醒 根据一般规律的预测结果可能是正确的,也可能是错误的。预测结果是否正确常可通过实验验证。在解决化学问题时,我们不但要掌握一般规律,也要注意特殊规律,全面掌握物质的性质。
2.[2023河北廊坊第一中学期末]根据元素周期律,由下列事实进行归纳推测,推测不合理的是( )
选项 事实 推测
A 12Mg与水反应缓慢,20Ca与水反应较快 56Ba(ⅡA族)与水反应会更快
B Si与H2高温时反应,S与H2加热能反应 P与H2在高温时能反应
C HCl在1 500 ℃时分解,HI在230 ℃时分解 HBr的分解温度介于二者之间
D Si是半导体材料,同族的Ge也是半导体材料 ⅣA族的元素单质都是半导体材料
D
解析 Be、Mg、Ca、Sr、Ba位于同一主族,其金属性逐渐增强,根据Mg与水反应缓慢、Ca与水反应较快,可以推测Ba与水反应更快,A合理;Si、P、S、Cl位于同一周期,其非金属性逐渐增强,则非金属单质与氢气反应由难到易,根据Si与H2高温时反应,S与H2加热能反应可以推测出P与H2在高温时能反应,B合理;Cl、Br、I位于同一主族,其非金属性逐渐减弱,氢化物的稳定性由强到弱,根据HCl在1 500 ℃时分解、HI在230 ℃时分解,可以推测出HBr的分解温度介于二者之间,C合理;硅和锗位于金属与非金属的分界线附近,这样的元素既有一定的非金属性又有一定的金属性,可在这附近找到半导体材料,而ⅣA族的其他元素距分界线较远,其单质不是半导体材料,如金刚石几乎不导电,锡和铅是金属导体,D不合理。
3.“大爆炸”理论指出:约150亿年以前,宇宙所有物质都包含在一个密度无限大、温度无限高的原始核中,由于某种原因它发生了爆炸,首先产生了中子、质子和电子,随后产生了元素。根据演绎范式,你认为最先产生的第一种元素应该是( )
A.H B.O
C.Fe D.C
A
解析 由于氢原子只含有一个质子和电子,最容易形成,所以最先产生的第一种元素应该是氢元素。
探究二 物质结构研究的方法
情境探究
1911年,卢瑟福用α粒子轰击一张极薄的金箔(散射实验),并据此提出了原子结构的“行星模型”,否定了他的老师汤姆生提出的“葡萄干面包式”的原子结构模型,使人类对原子结构的认识迈出了坚实的一步。卢瑟福的学生玻尔将量子论引入“行星模型”中,解决了经典电磁力学无法解释的难题,使人类对原子结构的认识跨入了一个崭新的时代。
α粒子散射实验
1.根据以上实验现象能得出关于金箔中金原子结构的一些结论,试写出其中的三点:
(1)原子中存在 ,且只占原子体积的很小一部分。
(2)金原子核带 电荷,且电荷数远大于α粒子的电荷数,两者产生静电 作用。
(3)金原子的质量远 (填“大于”“小于”或“等于”)α粒子的质量。
2.这是利用了物质结构研究的什么方法
提示 实验法。
原子核
正
排斥
大于
3.道尔顿的原子论曾经起了很大的作用,其中有两个论点:①原子是不能再分的粒子;②同种元素原子的各种性质和质量都相同。从现在的观点看,你认为这两个论点中,哪个不确切
4.实验现象与当时的原子模型发生了矛盾,你能从卢瑟福的α粒子散射实验中得到哪些启示
提示 ①②均不确切。从现在的观点看:原子由原子核和核外电子构成;大多数元素存在同位素,同位素的质量不同。
提示 卢瑟福的α粒子散射实验给我们很多启示:对待学习要有严谨认真、一丝不苟的态度,绝不放过任何一个疑点,努力使自己成为敢于质疑、敢于向权威挑战、具有创新意识和创新精神的现代中学生(合理即可)。
方法突破
1.物质结构研究方法的分类
2.物质结构研究方法
(1)科学假设和论证
①研究过程流程图
②注意事项
a.为了验证假设是否正确,必须通过不断的重复实验进行论证。正确的假设要接受,如果实验不支持假设,就要对假设进行修改并设计新的实验进行验证。
b.正确的假设还要建立理论将知识组织起来使之成为体系理论。
(2)实验方法
①X射线衍射实验鉴别晶体和非晶体。
②扫描隧道显微镜、原子力显微镜用于研究分子结构。
(3)模型方法
①模型方法是以研究模型来揭示原型的形态、特征和本质的方法,是逻辑方法的一种特有形式。模型舍去了原型的一些次要的细节、非本质的联系,以简化和理想化的形式去再现原型的各种复杂结构、功能和联系,是连接理论和应用的桥梁。
②模型实际上是假设的一种特殊形式,也可以说是科学性和假定性的辩证统一。它不仅要在时间中接受检验,而且还要在实践中扩展、补充和修正。
应用体验
视角1 物质结构研究的方法
1.下列关于化学学习和研究的说法错误的是( )
A.化学模型有助于解释一些化学现象
B.质量守恒定律是大量实验事实的总结
C.化学家提出的假设都能被实验证实
D.化学基本原理的应用是有一定条件的
C
解析 化学家提出的假设并不一定完全正确,有的甚至是错误的,如凯库勒提出的苯分子结构曾经被认为能够解释苯分子的性质及其不饱和度问题,但是随后通过实验发现关于苯分子中存在碳碳双键的说法是错误的。
2.化学实验模型有助于我们形成化学学科的思想和方法,其中属于微观结构模型的是( )
A
解析 难以直接观察到原型的模型为微观结构模型。
3.下列说法不正确的是( )
A.假说经过反复验证和修正,才能发展成为科学的理论
B.模型一般可分为实物模型和思维模型
C.研究物质的性质常用观察、实验、分类、比较等方法
D.科学实验能解决化学学科的所有问题
D
解析 假说只有经过反复验证和修正,才能发展为科学的理论,故A正确;模型一般分为实物模型和思维模型,B正确;研究物质的性质常用观察、实验、分类、比较等方法,C正确;科学实验是化学学科的基础,不能解决化学学科中的所有问题,D错误。
4.下列关于分子结构模型的说法正确的是( )
A.分子结构模型只能表示有机化合物的分子结构
B.分子结构模型可直观展现分子的空间结构
C.分子结构模型中的球体大小相等
D.分子结构模型展现的是分子的二维空间的结构特点
B
解析 分子结构模型可以表示有机化合物和无机化合物的分子结构,A项错误;分子结构模型展现的是分子的三维空间的结构特点,可直观展现分子的空间结构,B项正确,D项错误;分子结构模型中代表不同原子的球体大小不相等,C项错误。
视角2 物质结构研究方法的应用
5.医学界通过放射性14C标记C60,发现一种C60的羧酸衍生物在特定条件下通过断裂DNA而杀死细胞,从而抑制艾滋病,则有关的叙述正确的是( )
A.由14C的化学性质可以归纳12C的化学性质
B.可以通过模型方法了解C60的微观结构
C.用扫描隧道显微镜可以测定二者的相对原子质量
D.可由C60、C70、C80等系列物质演绎一类物质的性质
B
解析 由一般到个别是演绎,A错误;扫描隧道显微镜测的是物质的结构,C错误;由个别到一般是归纳,D错误。
归纳总结 化学上常用的微观结构模型有晶体结构模型、分子结构模型、原子结构模型等,有机物分子结构模型又可分为球棍模型和空间填充模型,如乙醇分子的模型如图所示:
球棍模型
空间填充模型
A.Sr位于元素周期表中第6周期ⅡA族
B.可用质谱法区分87Sr和86Sr
C.87Sr和86Sr含有的中子数分别为49和48
A
解析 Sr位于元素周期表中第5周期ⅡA族,故A错误;质谱法可以测定原子的相对原子质量,87Sr和86Sr的相对原子质量不同,可以用质谱法区分,故B正确;87Sr的中子数为87-38=49,86Sr的中子数为86-38=48,故C正确;由题意可知,38Sr(锶)的87Sr、86Sr稳定同位素在同一地域土壤中 值不变,故D正确。
7.门捷列夫在19世纪中叶曾根据他所发现的元素周期律,预言过第4周期ⅣA族锗元素(当时称为类硅)的性质。当时已知:
密度(g·cm-3):Si 4.8,Sn 5.8;
比热[J/(kg·K)]:Sn 218,Pb 130。
(1)估计锗的密度(g·cm-3)和比热[J/(kg·K)]分别为 、 。
(2)判断锗的金属性和非金属性强弱,它能否与酸或碱反应
答案 (1)5.3 306
(2)锗的金属性比锡弱,非金属性比硅弱;既能与强酸反应又能与强碱反应
解析 单质的密度有一定的变化规律,锗在硅和锡之间,密度大约是它们的平均值5.3;锗、锡、铅比热的变化由已知后两者的数据可知是变小的,那么锗的比热最大,锗与锡间比热的差值应和锡与铅之间比热的差值相当,故得锗的比热约为218+88=306。锗处于金属与非金属的分界线附近,推测有两性。
本 课 结 束
专题1 揭示物质结构的奥秘
第二单元 物质结构研究的范式与方法
素 养 目 标
1.认识物质结构研究的两种范式及其相互关系,培养证据推理与模型认知的化学核心素养。
2.能举例说明科学假设和论证、实验方法、模型方法等在物质结构研究中起的重要作用,培养宏观辨识与微观探析、证据推理与模型认知的化学核心素养。
3.能描述现代仪器和手段为测定物质结构、建立相关理论作出的重要贡献,培养科学探究与创新意识的化学核心素养。
基础落实·必备知识全过关
重难探究·能力素养全提升
目 录 索 引
基础落实·必备知识全过关
一、物质结构研究的范式
1.归纳范式
从个别到一般
(1)含义:根据事实进行 ,抽象出 ,上升为
。
概括归纳
共同点
本质规律
(2)例证
个别性质 一般规律
通过甲烷(CH4)、乙烷(C2H6)、丙烷(C3H8)、丁烷(C4H10)等的分子式 归纳出饱和烷烃的通式为
通过1~20号元素的 认识前20号元素对应 归纳出元素核外 规律,并从结构上解释同族元素
相似的原因
通过研究含有双键和三键的不饱和烃,发现这类物质容易发生 反应和 反应,不饱和键具有 的性质 根据结构与性质的关系归纳出这类有机物的
原子核外电子排布
原子结构的不同
电子排布
性质
加成
氧化
不稳定
通性
2.演绎范式
从一般到个别
(1)含义:是从某个 出发,向从属于这一结论的
的过程。
一般结论
多个要素进行推理
(2)例证
一般规律 个别性质
门捷列夫建立了 人们发现了“类铝” ,“类硼” ,
“类硅”
根据钠原子最外电子层上1个电子 的特点 推出同族半径更大的 元素具有更强的还原性的结论
水是 性较强的分子,水分子之间存在较强的 ,水分子既可为生成氢键 ,又有孤电子对 CH3CH2OH、CH3COOH极性与水相似,
均可通过 和水结合,在水中的
较大;碳氢化合物 性较小,也难以和水形成 ,在水中溶解度很 ,这就是著名的
“ ”
元素周期表
(镓)
(铊)
(锗)
极易失去表现出强还原性
钾、铷、铯
极
氢键
提供H
接受H
氢键
溶解度
极
氢键
小
相似相溶规则
3.归纳与演绎的关系
(1)化学研究的途径一般为先 、后 。
(2)演绎是从一般到个别,从理论到新的事实;演绎需要归纳提供前提,归纳需要演绎作为指导。
(3)在演绎的指导下归纳,在归纳的基础上演绎。
归纳
演绎
教材阅读 想一想阅读教材“物质结构研究的范式”。
思考:全国科技名词委联合国家语言文字工作委员会召开113号、115号、117号、118号元素中文定名会,形成了《113号、115号、117号、118号元素中文定名方案》,如表所示。由元素周期表推断元素运用了物质结构研究的什么范式
提示 由一般到个别,是演绎范式。
易错辨析 判一判
(1)由元素周期表发现新的元素属于归纳范式。( )
提示 从一般到个别是演绎范式。
(2)由硅是半导体材料推断锡也是半导体材料。( )
提示 硅在金属与非金属分界线上,而锡是典型的金属材料。
(3)归纳范式和演绎范式均为独立的研究方法,不能融合。( )
提示 研究物质结构需要各种范式结合。
(4)从CH3OH、CH3CH2OH、CH3CH2CH2OH等分子中归纳出饱和一元醇的通式为CnH2n+2O,为归纳范式。( )
×
×
×
√
二、物质结构研究的方法
1.科学假设和论证
(1)研究问题的步骤
观察
感官
提出假设
已有知识
进行论证
实验
(2)建立理论
①理论: 。
②建立原则:建立在科学家一次又一次的 的基础之上。
建立在大量的观察基础之上并为实验所证实的解释
观察和实验
2.实验方法
(1)含义:化学是一门以实验为基础的学科,人们往往需要借助实验观测的事实对假设的正确与否进行检验。
(2)例证
实验方法 意义
卢瑟福的 实验 启迪人们用粒子轰击和对撞的实验来研究物质的 ,提供了一种研究物质 的思想方法
光学显微镜、扫描隧道显微镜、原子力显微镜等仪器出现,各种光谱和晶体X射线衍射实验方法应用于研究原子、分子和晶体结构 使原子和分子的微观世界不断被揭示
α粒子散射
内部结构
微观结构
3.模型方法
(1)含义:科学家运用一定 对实验结果进行处理。
(2)方法:模型既可以是对原型的 ,也可以是结合某种理论形态下建立的 。
逻辑推理与模型思维
简化和纯化、抽象和近似
思维模型
(3)分类
分类 实物模型 微观结构模型
含 义 可观察到的物体的宏观模型 物质微观层次结构,难以直接观察到,需要通过思维加工使 的微观世界以 的形式展现出来
实 例 如____________________ 如原子结构模型、离子键模型、共价键模型和氢键模型,有机化合物的分子结构模型等
抽象
可视化
汽车模型、飞机模型
和建筑模型
(4)作用
①对沟通科学现象与其本质的认识过程,起到重要的桥梁作用。
②利用模型深刻地认识物质的微观结构特点,揭示结构与性质的关系,是模型研究的重要功能。
教材阅读 想一想自学教材“模型方法”。
思考:乙烯的空间填充模型为 ,该空间填充模型属于哪类模型
提示 属于微观结构模型。
易错辨析 判一判
(1)理论都是正确的,不需要修改。( )
提示 当反常现象大量出现,而原有理论又不能很好地做出解释时,就需要对原有理论加以修改。
(2)模型就是对物质真实形状的加工。( )
提示 微观结构模型是通过思维加工使抽象的微观世界以可视化的形式展现出来,不能说是对物质真实形状的加工。
(3)实验法只能通过化学实验才能实现。( )
提示 物理实验、通过仪器研究也是实验法。
(4)锗是优良的半导体,锗元素属于金属元素,但也具有一定的非金属性。
( )
×
×
×
√
重难探究·能力素养全提升
探究一 归纳范式与演绎范式的关系
情境探究
在研究元素周期律的过程中,门捷列夫仔细分析了当时已知的63种元素的物理性质和化学性质,他准备了许多扑克牌一样的卡片,将63种化学元素的名称及其原子量(即相对原子质量)、氧化物、物理性质、化学性质等分别写在卡片上面。1869年3月1日,门捷列夫仍然在对着这些卡片苦苦思索,他惊喜地发现,所有的已知元素都已经按照原子量递增的顺序排列起来,并且相似元素以一定的间隔出现。第二天门捷列夫将所得出的结果制成一张表,这是人类历史上第一张化学元素周期表。在门捷列夫的元素周期表中,他大胆地为尚待发现的元素留出了位置,并且在其关于元素周期表的发现的论文中指出:按着原子量由小到大的顺序排列各种元素,在原子量跳跃
过大的地方会有新元素被发现,因此元素周期律可以预言尚待发现的元素。
1871年,门捷列夫预言一定存在一种元素,在元素周期表中它紧排在锌的后面,处于铝和铟之间,他将其称为“类铝”,并预测了它的性质。1875年,法国化学家布瓦博德朗在分析闪锌矿时发现一种新元素,将它命名为镓,并将他测得的主要性质公之于众,不久便收到了门捷列夫的来信,信中说镓的比重不是4.7而是5.9,当时布瓦博德朗很疑惑,门捷列夫是怎样知道镓的比重的呢 经重新测定,镓的比重是5.9,结果使他大为惊奇,他认真阅读了门捷列夫的元素周期律论文后,感慨地说:“我没有可说的了,事实证明门捷列夫这一理论的巨大意义。”
1.门捷列夫根据当时已知的63种元素,排布出第一个元素周期表,这是运用了物质结构研究的什么范式
2.门捷列夫运用元素周期表预测了“类铝”,这是运用了物质结构研究的什么范式
提示 由个别到一般,属于归纳范式。
提示 由一般到个别,属于演绎范式。
3.学习元素周期律后,有同学根据原子结构判断碱金属最外层只有一个电子,易失电子呈还原性,进而该同学推断出ⅡA族的原子也易失电子具有还原性,这是运用了物质结构研究的什么范式
4.根据结论:ⅡA族的原子易失电子具有还原性,有同学总结出原子核外最外层电子数是两个的原子都具有强还原性。这是运用了物质结构研究的什么范式 这种结论是否正确
提示 由一般到一般,属于演绎范式。
提示 由个别到一般,属于归纳范式。这种结论不正确,如氦元素原子最外层电子数是两个,不易得也不易失,不具有强还原性。
方法突破
1.归纳与演绎的不同点
2.归纳与演绎的联系
(1)从科学研究的途径来看归纳和演绎的使用,一般为先归纳、后演绎。“实验—假说—理论—新实验”的过程,本质上就是从个别到一般,再到个别的过程。
(2)归纳需要演绎作指导,以解决研究的目的性、方向性和结果的正确性问题;而演绎需要归纳提供前提。在演绎的指导下归纳,在归纳的基础上演绎,两者互相联系、互为前提。
应用体验
视角 物质结构研究的范式
1.门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第4周期的三种元素留下了空位,并对它们的一些性质作了预测,X是其中的一种“类硅”元素,后来被德国化学家温克勒发现,并证实门捷列夫当时的预测相当准确。下列有关描述中错误的是( )
A.根据一般规律的预测结果都是正确的
B.由周期表推断元素是利用了演绎范式
C.由硅的结构可以通过科学假设和论证方法研究“类硅”的结构
D.可以通过实验方法研究硅及“类硅”结构的区别
A
解析 预测可能是正确的,也可能是错误的,要经过不断地重复实验进行论证。
考题点睛
易错提醒 根据一般规律的预测结果可能是正确的,也可能是错误的。预测结果是否正确常可通过实验验证。在解决化学问题时,我们不但要掌握一般规律,也要注意特殊规律,全面掌握物质的性质。
2.[2023河北廊坊第一中学期末]根据元素周期律,由下列事实进行归纳推测,推测不合理的是( )
选项 事实 推测
A 12Mg与水反应缓慢,20Ca与水反应较快 56Ba(ⅡA族)与水反应会更快
B Si与H2高温时反应,S与H2加热能反应 P与H2在高温时能反应
C HCl在1 500 ℃时分解,HI在230 ℃时分解 HBr的分解温度介于二者之间
D Si是半导体材料,同族的Ge也是半导体材料 ⅣA族的元素单质都是半导体材料
D
解析 Be、Mg、Ca、Sr、Ba位于同一主族,其金属性逐渐增强,根据Mg与水反应缓慢、Ca与水反应较快,可以推测Ba与水反应更快,A合理;Si、P、S、Cl位于同一周期,其非金属性逐渐增强,则非金属单质与氢气反应由难到易,根据Si与H2高温时反应,S与H2加热能反应可以推测出P与H2在高温时能反应,B合理;Cl、Br、I位于同一主族,其非金属性逐渐减弱,氢化物的稳定性由强到弱,根据HCl在1 500 ℃时分解、HI在230 ℃时分解,可以推测出HBr的分解温度介于二者之间,C合理;硅和锗位于金属与非金属的分界线附近,这样的元素既有一定的非金属性又有一定的金属性,可在这附近找到半导体材料,而ⅣA族的其他元素距分界线较远,其单质不是半导体材料,如金刚石几乎不导电,锡和铅是金属导体,D不合理。
3.“大爆炸”理论指出:约150亿年以前,宇宙所有物质都包含在一个密度无限大、温度无限高的原始核中,由于某种原因它发生了爆炸,首先产生了中子、质子和电子,随后产生了元素。根据演绎范式,你认为最先产生的第一种元素应该是( )
A.H B.O
C.Fe D.C
A
解析 由于氢原子只含有一个质子和电子,最容易形成,所以最先产生的第一种元素应该是氢元素。
探究二 物质结构研究的方法
情境探究
1911年,卢瑟福用α粒子轰击一张极薄的金箔(散射实验),并据此提出了原子结构的“行星模型”,否定了他的老师汤姆生提出的“葡萄干面包式”的原子结构模型,使人类对原子结构的认识迈出了坚实的一步。卢瑟福的学生玻尔将量子论引入“行星模型”中,解决了经典电磁力学无法解释的难题,使人类对原子结构的认识跨入了一个崭新的时代。
α粒子散射实验
1.根据以上实验现象能得出关于金箔中金原子结构的一些结论,试写出其中的三点:
(1)原子中存在 ,且只占原子体积的很小一部分。
(2)金原子核带 电荷,且电荷数远大于α粒子的电荷数,两者产生静电 作用。
(3)金原子的质量远 (填“大于”“小于”或“等于”)α粒子的质量。
2.这是利用了物质结构研究的什么方法
提示 实验法。
原子核
正
排斥
大于
3.道尔顿的原子论曾经起了很大的作用,其中有两个论点:①原子是不能再分的粒子;②同种元素原子的各种性质和质量都相同。从现在的观点看,你认为这两个论点中,哪个不确切
4.实验现象与当时的原子模型发生了矛盾,你能从卢瑟福的α粒子散射实验中得到哪些启示
提示 ①②均不确切。从现在的观点看:原子由原子核和核外电子构成;大多数元素存在同位素,同位素的质量不同。
提示 卢瑟福的α粒子散射实验给我们很多启示:对待学习要有严谨认真、一丝不苟的态度,绝不放过任何一个疑点,努力使自己成为敢于质疑、敢于向权威挑战、具有创新意识和创新精神的现代中学生(合理即可)。
方法突破
1.物质结构研究方法的分类
2.物质结构研究方法
(1)科学假设和论证
①研究过程流程图
②注意事项
a.为了验证假设是否正确,必须通过不断的重复实验进行论证。正确的假设要接受,如果实验不支持假设,就要对假设进行修改并设计新的实验进行验证。
b.正确的假设还要建立理论将知识组织起来使之成为体系理论。
(2)实验方法
①X射线衍射实验鉴别晶体和非晶体。
②扫描隧道显微镜、原子力显微镜用于研究分子结构。
(3)模型方法
①模型方法是以研究模型来揭示原型的形态、特征和本质的方法,是逻辑方法的一种特有形式。模型舍去了原型的一些次要的细节、非本质的联系,以简化和理想化的形式去再现原型的各种复杂结构、功能和联系,是连接理论和应用的桥梁。
②模型实际上是假设的一种特殊形式,也可以说是科学性和假定性的辩证统一。它不仅要在时间中接受检验,而且还要在实践中扩展、补充和修正。
应用体验
视角1 物质结构研究的方法
1.下列关于化学学习和研究的说法错误的是( )
A.化学模型有助于解释一些化学现象
B.质量守恒定律是大量实验事实的总结
C.化学家提出的假设都能被实验证实
D.化学基本原理的应用是有一定条件的
C
解析 化学家提出的假设并不一定完全正确,有的甚至是错误的,如凯库勒提出的苯分子结构曾经被认为能够解释苯分子的性质及其不饱和度问题,但是随后通过实验发现关于苯分子中存在碳碳双键的说法是错误的。
2.化学实验模型有助于我们形成化学学科的思想和方法,其中属于微观结构模型的是( )
A
解析 难以直接观察到原型的模型为微观结构模型。
3.下列说法不正确的是( )
A.假说经过反复验证和修正,才能发展成为科学的理论
B.模型一般可分为实物模型和思维模型
C.研究物质的性质常用观察、实验、分类、比较等方法
D.科学实验能解决化学学科的所有问题
D
解析 假说只有经过反复验证和修正,才能发展为科学的理论,故A正确;模型一般分为实物模型和思维模型,B正确;研究物质的性质常用观察、实验、分类、比较等方法,C正确;科学实验是化学学科的基础,不能解决化学学科中的所有问题,D错误。
4.下列关于分子结构模型的说法正确的是( )
A.分子结构模型只能表示有机化合物的分子结构
B.分子结构模型可直观展现分子的空间结构
C.分子结构模型中的球体大小相等
D.分子结构模型展现的是分子的二维空间的结构特点
B
解析 分子结构模型可以表示有机化合物和无机化合物的分子结构,A项错误;分子结构模型展现的是分子的三维空间的结构特点,可直观展现分子的空间结构,B项正确,D项错误;分子结构模型中代表不同原子的球体大小不相等,C项错误。
视角2 物质结构研究方法的应用
5.医学界通过放射性14C标记C60,发现一种C60的羧酸衍生物在特定条件下通过断裂DNA而杀死细胞,从而抑制艾滋病,则有关的叙述正确的是( )
A.由14C的化学性质可以归纳12C的化学性质
B.可以通过模型方法了解C60的微观结构
C.用扫描隧道显微镜可以测定二者的相对原子质量
D.可由C60、C70、C80等系列物质演绎一类物质的性质
B
解析 由一般到个别是演绎,A错误;扫描隧道显微镜测的是物质的结构,C错误;由个别到一般是归纳,D错误。
归纳总结 化学上常用的微观结构模型有晶体结构模型、分子结构模型、原子结构模型等,有机物分子结构模型又可分为球棍模型和空间填充模型,如乙醇分子的模型如图所示:
球棍模型
空间填充模型
A.Sr位于元素周期表中第6周期ⅡA族
B.可用质谱法区分87Sr和86Sr
C.87Sr和86Sr含有的中子数分别为49和48
A
解析 Sr位于元素周期表中第5周期ⅡA族,故A错误;质谱法可以测定原子的相对原子质量,87Sr和86Sr的相对原子质量不同,可以用质谱法区分,故B正确;87Sr的中子数为87-38=49,86Sr的中子数为86-38=48,故C正确;由题意可知,38Sr(锶)的87Sr、86Sr稳定同位素在同一地域土壤中 值不变,故D正确。
7.门捷列夫在19世纪中叶曾根据他所发现的元素周期律,预言过第4周期ⅣA族锗元素(当时称为类硅)的性质。当时已知:
密度(g·cm-3):Si 4.8,Sn 5.8;
比热[J/(kg·K)]:Sn 218,Pb 130。
(1)估计锗的密度(g·cm-3)和比热[J/(kg·K)]分别为 、 。
(2)判断锗的金属性和非金属性强弱,它能否与酸或碱反应
答案 (1)5.3 306
(2)锗的金属性比锡弱,非金属性比硅弱;既能与强酸反应又能与强碱反应
解析 单质的密度有一定的变化规律,锗在硅和锡之间,密度大约是它们的平均值5.3;锗、锡、铅比热的变化由已知后两者的数据可知是变小的,那么锗的比热最大,锗与锡间比热的差值应和锡与铅之间比热的差值相当,故得锗的比热约为218+88=306。锗处于金属与非金属的分界线附近,推测有两性。
本 课 结 束
