3.1.2 金属晶体 课件 (共42张PPT)2023-2024学年高二化学苏教版选择性必修2
文档属性
| 名称 | 3.1.2 金属晶体 课件 (共42张PPT)2023-2024学年高二化学苏教版选择性必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 8.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-09 00:00:00 | ||
图片预览










文档简介
(共42张PPT)
专题3 微粒间作用力与物质性质
第一单元 第2课时 金属晶体
素 养 目 标
1.能借助模型说明常见晶体中晶胞的构成。理解金属晶体的堆积模型,并能用切割法分析晶胞组成,培养证据推理与模型认知的化学核心素养。
2.了解合金的性质,会举例说明合金的优越性能,培养科学态度与社会责任的化学核心素养。
基础落实·必备知识全过关
重难探究·能力素养全提升
目 录 索 引
基础落实·必备知识全过关
金属晶体
1.相关概念
(1)晶体:内部微粒(原子、离子或分子)在空间按一定规律做周期性重复排列构成的固体物质称为晶体。通常条件下,大多数金属单质属于晶体。
(2)晶胞:能够反映晶体结构特征的 。金属晶体是金属晶胞在空间连续重复延伸而形成的。
(3)金属晶体:通过 与 之间的强烈的相互作用而形成的晶体。
基本重复单位
金属阳离子
自由电子
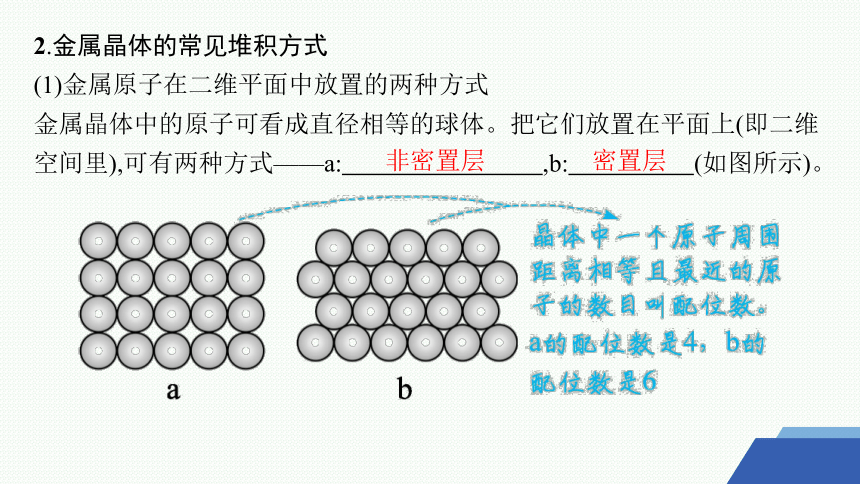
2.金属晶体的常见堆积方式
(1)金属原子在二维平面中放置的两种方式
金属晶体中的原子可看成直径相等的球体。把它们放置在平面上(即二维空间里),可有两种方式——a: ,b: (如图所示)。
非密置层
密置层
(2)金属晶体的原子在三维空间里的4种堆积方式
金属原子在三维空间按一定的规律堆积,有4种基本堆积方式。
简单立方
体心立方
面心立方
六方
3.立方体晶胞中微粒数目的计算
(1)晶胞顶点的原子是 个晶胞共用;
(2)晶胞棱上的原子是 个晶胞共用;
(3)晶胞面上的原子是 个晶胞共用;
(4)晶胞体心的原子是 个晶胞共用。
4.合金
(1)定义:由 或 混合形成具有金属性质的物质称为合金。
(2)合金的性质
①合金的熔、沸点一般比组成它的各成分金属的熔、沸点 。
②形成合金后硬度、强度 (一般情况下)。
8
4
2
1
金属与金属
金属与非金属
低
增大
教材阅读 想一想阅读教材“在金属晶体中,金属原子如同半径相等的小球一样”等连续三段。
思考:晶胞是能够反映晶体结构特征的基本重复单位,不同的金属晶体中,晶胞的大小和形状是否相同
提示 相同晶体中晶胞的大小和形状完全相同,不同晶体中,晶胞的大小和形状不一定相同。
易错辨析 判一判
(1)晶胞是晶体的最小重复单元。( )
(2)不同的晶体中晶胞的大小和形状都相同。( )
提示 不同晶体的结构不同,所以其晶胞大小和形状不一定都相同。
(3)晶胞中的任何一个粒子都只属于该晶胞。( )
提示 晶胞顶点、棱及面上的粒子都和其他晶胞共用,所以并非任何一个粒子都只属于该晶胞。
(4)钋的晶胞为简单立方堆积,则一个晶胞中含有1个钋原子。( )
√
×
×
√
重难探究·能力素养全提升
探究一 晶胞结构和晶胞中微粒数的计算
情境探究
人们最初对晶体的认识完全是理性思考的结果。法国的结晶学家阿羽衣依据晶体具有沿一定晶面碎裂的性质,对晶体的微观结构做了合理而大胆的设想,于1784年提出晶体是由具有多面体形状的晶胞平行而无间隙地堆积而成的。阿羽衣的思想被法国物理学家布拉维发展为空间点阵学说,即构成晶体的粒子按一定规则排列为空间点阵结构。
俄国的费多罗夫、德国的熊富利斯和英国的巴洛三位科学家分别于1890年、1891年和1894年以晶体结构周期性重复单位为基础,推导出描述晶体空间排列的对称性理论——230种空间群。这些思考完全是在不能测定晶体内部结构的情况下产生的,科学和技术的发展后来完全证实了上述理性思考的正确性。
空间点阵
1.在平行六面体晶胞中顶点上的原子是否都只属于该晶胞
2.晶体与晶胞的关系是怎样的 如何理解晶体结构中“周期性重复单位”
提示 不是。构成晶体的微粒是“无隙并置”的,顶点上的原子都是被几个晶胞共用的。
提示 将一个个晶胞及其包含的微粒上、下、前、后、左、右并置,就构成了整个晶体结构。因此,知道了晶胞的大小和形状以及晶胞中包含的微粒的种类、数目和空间位置,就可以了解整个晶体的结构。晶体与晶胞的关系好比蜂巢与蜂室的关系。
“周期性重复单位”是指晶体中最小的结构单元可以无限重复。
3.计算晶胞中的微粒数目为什么采用切割法
提示 整块晶体可以看作是数量巨大的晶胞堆积而成。位于晶胞顶点、棱上、面上的微粒并不为一个晶胞所独占,因此,需采用切割法。
方法突破
1.晶体和晶胞结构
2.常见晶胞含有微粒数目的计算方法——切割法
(1)长方体形(正方体形)晶胞中不同位置的粒子数的计算:
某个微粒为n个晶胞所共有,则该微粒有 属于这个晶胞。
(2)六棱柱晶胞中不同位置的粒子数的计算:
(3)切割法在计算其他结构晶胞中微粒数的应用:
其他结构晶胞中微粒数目的计算同样可以用切割法,其关键是根据立体结构特点分析某处微粒被几个晶胞共用。如:某晶体的晶胞结构如图所示,该晶胞中,1个A微粒被12个晶胞共用,1个C微粒被1个晶胞所有,而B微粒分两种情况:位于上底面和下底面棱上的B微粒被4个晶胞共用、位于侧面棱上的B微粒被6个晶胞共用,则一个晶胞中包含的A、B、C三种微粒的数目分别是 、2、1,则该晶体的化学式(按A、B、C顺序)为AB4C2。
应用体验
视角1 晶胞结构
1.对图中某金属晶体结构的模型进行分析,判断下列有关说法正确的是
( )
A.该种堆积方式称为六方堆积
B.该种堆积方式称为体心立方堆积
C.该种堆积方式称为面心立方堆积
D.金属Mg就属于此种堆积方式
C
解析 由题图知该堆积方式为面心立方堆积,A、B错误,C正确;Mg是六方堆积,D错误。
2.金属原子在二维空间里的放置有如图所示的两种方式,下列说法中正确的是( )
A.图(a)为非密置层,配位数为6
B.图(b)为密置层,配位数为4
C.图(a)在三维空间里堆积可
得六方堆积和面心立方堆积
D.图(b)在三维空间里堆积仅得简单立方
C
解析 密置层原子的配位数为6,非密置层原子的配位数为4,图(a)为密置层,图(b)为非密置层。密置层在三维空间堆积可得到六方堆积和面心立方堆积,非密置层在三维空间堆积可得简单立方和体心立方两种堆积。
3.下列有关晶胞的说法正确的是( )
A.晶胞中所含粒子数即为晶体的化学式
B.若晶胞为立方体,则棱上的粒子为3个晶胞共用
C.若晶胞为六棱柱( ),则顶点上的粒子为6个晶胞共用
D.晶胞中不可能存在多种粒子
C
解析 A项,晶胞中的粒子数不一定为晶体的化学式,如课本中的金属铜的晶胞中,铜原子的个数为4;B项,立方体棱上的粒子为4个晶胞共用;C项,如题图所示顶点为6个晶胞共用;D项,如合金晶胞中可以存在多种粒子。
视角2 晶胞中微粒数的计算
4.已知某晶体晶胞如图所示,则该晶体的化学式为( )
A.XYZ B.X2Y4Z
C.XY4Z D.X4Y2Z
C
解析 该晶体的晶胞是立方体形晶胞。该晶胞拥有的X原子数为8× =1;Y原子位于该晶胞内,共有4个,因此该晶胞中拥有的Y原子数为4;Z只有1个,位于晶胞的体心上,故该晶体的化学式为XY4Z。
归纳总结 晶胞中含有微粒数目计算的一般步骤
(1)明确微粒在晶胞中的位置关系。
(2)按照位置关系的平均占有数及同一位置的微粒数目进行计算。
5.现有甲、乙、丙(如图)三种晶体的晶胞(甲中x处于晶胞的中心,乙中a处于晶胞的中心),如图所示。
可推知:甲晶胞中x与y的个数比是 ;乙晶胞中a与b的个数比是 ;丙晶胞中有 个c,有 个d。
答案 4∶3 1∶1 4 4
解析 处于晶胞中心的x或a为晶胞单独占有,位于立方体顶点的微粒为8个立方体共有,位于立方体棱上的微粒为4个立方体共有,位于立方体面上的微粒为2个立方体共有,
6.某物质的晶体中,含A、B、C 3种元素,其排列方式如图所示(其中前后两面心上的B原子未画出),晶体中A、B、C的原子个数比为( )
A.1∶3∶1 B.2∶3∶1
C.2∶2∶1 D.1∶3∶3
A
解析 A原子位于晶胞的顶点,故晶胞中A原子个数为8× =1,B原子位于晶胞的面心,故晶胞中B原子个数为6× =3,C原子位于晶胞的体心,故晶胞中C原子个数为1,所以晶胞中A、B、C的原子个数比为1∶3∶1,A项正确。
7.钛在许多领域都有重要用途,因为可以制造人类关节和接骨,被称为“生物金属”。
(1)钛在元素周期表中位于第 周期
族,其基态原子核外电子排布式为 。
(2)某种钛氧化物晶体的晶胞如图,该晶体每个晶胞中的钛、氧原子个数比为
。
答案 (1)4 ⅣB 1s22s22p63s23p63d24s2
(2)1∶2
解析 (1)钛是22号元素,位于元素周期表第4周期ⅣB族,基态原子核外电子排布式为1s22s22p63s23p63d24s2。
因此钛、氧原子个数比为2∶4=1∶2。
探究二 与晶胞有关的计算
情境探究
铜晶体为面心立方晶胞,其晶胞结构与切割示意图如下。
若铜的相对原子质量为M,铜原子的半径为r m,用NA表示阿伏加德罗常数的值。
1.如何确定铜晶胞中铜原子的个数
2.如何计算铜金属晶体中的晶胞长度和晶胞的体积
3.铜晶胞的质量是多少 铜的密度是多少g·cm-3
4.若晶胞的空间利用率= ×100%,试计算铜晶胞的空间利用率。
方法突破
1.晶体密度的有关计算
假设某晶体的晶胞如图:
以M表示该晶体的摩尔质量,NA表示阿伏加德罗常数,N表示一个晶胞中所含的微粒数,a表示晶胞的棱长,ρ 表示晶体的密度,计算如下:
应用体验
视角 与晶胞有关的计算
1.用X射线研究某金属晶体,测得其立方晶胞的边长为
360 pm,此时金属的密度为9.0 g·cm-3。试回答:
(1)此晶胞中含金属原子 个。
(2)每个晶胞的质量是 g。
(3)此金属的相对原子质量为 。
答案 (1)4 (2)4.2×10-22 (3)63
(2)根据晶胞的边长为360 pm,可得晶胞的体积为(3.6×10-8)3 cm3。
根据m=ρV,可得晶胞的质量=9.0 g·cm-3×(3.6×10-8)3 cm3≈4.2×10-22 g。
(3)金属的摩尔质量M=NA×原子的质量
考题点睛
归纳总结 根据晶胞结构计算晶体密度的方法
(1)确定晶胞中微粒个数;
(2)根据阿伏加德罗常数、微粒个数、微粒的摩尔质量确定晶胞质量;
(3)确定晶胞体积;
2.铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图所示(黑球代表Fe,白球代表Mg)。则下列说法错误的是( )
A.铁镁合金的化学式可表示为Mg2Fe
B.晶胞中有14个铁原子
C.晶体中存在的化学键类型为金属键
B
3.[2023河北邯郸高二期末]砷化硼晶体是具有超高热导率的半导体材料,其结构如图所示,若晶胞参数为a nm,下列说法正确的是( )
A.砷化硼的化学式为B7As2
B.与顶点B原子距离最近且等距的B原子有6个
C.晶胞内的4个As原子所围成的空间结构为正四面体形
C
本 课 结 束
专题3 微粒间作用力与物质性质
第一单元 第2课时 金属晶体
素 养 目 标
1.能借助模型说明常见晶体中晶胞的构成。理解金属晶体的堆积模型,并能用切割法分析晶胞组成,培养证据推理与模型认知的化学核心素养。
2.了解合金的性质,会举例说明合金的优越性能,培养科学态度与社会责任的化学核心素养。
基础落实·必备知识全过关
重难探究·能力素养全提升
目 录 索 引
基础落实·必备知识全过关
金属晶体
1.相关概念
(1)晶体:内部微粒(原子、离子或分子)在空间按一定规律做周期性重复排列构成的固体物质称为晶体。通常条件下,大多数金属单质属于晶体。
(2)晶胞:能够反映晶体结构特征的 。金属晶体是金属晶胞在空间连续重复延伸而形成的。
(3)金属晶体:通过 与 之间的强烈的相互作用而形成的晶体。
基本重复单位
金属阳离子
自由电子
2.金属晶体的常见堆积方式
(1)金属原子在二维平面中放置的两种方式
金属晶体中的原子可看成直径相等的球体。把它们放置在平面上(即二维空间里),可有两种方式——a: ,b: (如图所示)。
非密置层
密置层
(2)金属晶体的原子在三维空间里的4种堆积方式
金属原子在三维空间按一定的规律堆积,有4种基本堆积方式。
简单立方
体心立方
面心立方
六方
3.立方体晶胞中微粒数目的计算
(1)晶胞顶点的原子是 个晶胞共用;
(2)晶胞棱上的原子是 个晶胞共用;
(3)晶胞面上的原子是 个晶胞共用;
(4)晶胞体心的原子是 个晶胞共用。
4.合金
(1)定义:由 或 混合形成具有金属性质的物质称为合金。
(2)合金的性质
①合金的熔、沸点一般比组成它的各成分金属的熔、沸点 。
②形成合金后硬度、强度 (一般情况下)。
8
4
2
1
金属与金属
金属与非金属
低
增大
教材阅读 想一想阅读教材“在金属晶体中,金属原子如同半径相等的小球一样”等连续三段。
思考:晶胞是能够反映晶体结构特征的基本重复单位,不同的金属晶体中,晶胞的大小和形状是否相同
提示 相同晶体中晶胞的大小和形状完全相同,不同晶体中,晶胞的大小和形状不一定相同。
易错辨析 判一判
(1)晶胞是晶体的最小重复单元。( )
(2)不同的晶体中晶胞的大小和形状都相同。( )
提示 不同晶体的结构不同,所以其晶胞大小和形状不一定都相同。
(3)晶胞中的任何一个粒子都只属于该晶胞。( )
提示 晶胞顶点、棱及面上的粒子都和其他晶胞共用,所以并非任何一个粒子都只属于该晶胞。
(4)钋的晶胞为简单立方堆积,则一个晶胞中含有1个钋原子。( )
√
×
×
√
重难探究·能力素养全提升
探究一 晶胞结构和晶胞中微粒数的计算
情境探究
人们最初对晶体的认识完全是理性思考的结果。法国的结晶学家阿羽衣依据晶体具有沿一定晶面碎裂的性质,对晶体的微观结构做了合理而大胆的设想,于1784年提出晶体是由具有多面体形状的晶胞平行而无间隙地堆积而成的。阿羽衣的思想被法国物理学家布拉维发展为空间点阵学说,即构成晶体的粒子按一定规则排列为空间点阵结构。
俄国的费多罗夫、德国的熊富利斯和英国的巴洛三位科学家分别于1890年、1891年和1894年以晶体结构周期性重复单位为基础,推导出描述晶体空间排列的对称性理论——230种空间群。这些思考完全是在不能测定晶体内部结构的情况下产生的,科学和技术的发展后来完全证实了上述理性思考的正确性。
空间点阵
1.在平行六面体晶胞中顶点上的原子是否都只属于该晶胞
2.晶体与晶胞的关系是怎样的 如何理解晶体结构中“周期性重复单位”
提示 不是。构成晶体的微粒是“无隙并置”的,顶点上的原子都是被几个晶胞共用的。
提示 将一个个晶胞及其包含的微粒上、下、前、后、左、右并置,就构成了整个晶体结构。因此,知道了晶胞的大小和形状以及晶胞中包含的微粒的种类、数目和空间位置,就可以了解整个晶体的结构。晶体与晶胞的关系好比蜂巢与蜂室的关系。
“周期性重复单位”是指晶体中最小的结构单元可以无限重复。
3.计算晶胞中的微粒数目为什么采用切割法
提示 整块晶体可以看作是数量巨大的晶胞堆积而成。位于晶胞顶点、棱上、面上的微粒并不为一个晶胞所独占,因此,需采用切割法。
方法突破
1.晶体和晶胞结构
2.常见晶胞含有微粒数目的计算方法——切割法
(1)长方体形(正方体形)晶胞中不同位置的粒子数的计算:
某个微粒为n个晶胞所共有,则该微粒有 属于这个晶胞。
(2)六棱柱晶胞中不同位置的粒子数的计算:
(3)切割法在计算其他结构晶胞中微粒数的应用:
其他结构晶胞中微粒数目的计算同样可以用切割法,其关键是根据立体结构特点分析某处微粒被几个晶胞共用。如:某晶体的晶胞结构如图所示,该晶胞中,1个A微粒被12个晶胞共用,1个C微粒被1个晶胞所有,而B微粒分两种情况:位于上底面和下底面棱上的B微粒被4个晶胞共用、位于侧面棱上的B微粒被6个晶胞共用,则一个晶胞中包含的A、B、C三种微粒的数目分别是 、2、1,则该晶体的化学式(按A、B、C顺序)为AB4C2。
应用体验
视角1 晶胞结构
1.对图中某金属晶体结构的模型进行分析,判断下列有关说法正确的是
( )
A.该种堆积方式称为六方堆积
B.该种堆积方式称为体心立方堆积
C.该种堆积方式称为面心立方堆积
D.金属Mg就属于此种堆积方式
C
解析 由题图知该堆积方式为面心立方堆积,A、B错误,C正确;Mg是六方堆积,D错误。
2.金属原子在二维空间里的放置有如图所示的两种方式,下列说法中正确的是( )
A.图(a)为非密置层,配位数为6
B.图(b)为密置层,配位数为4
C.图(a)在三维空间里堆积可
得六方堆积和面心立方堆积
D.图(b)在三维空间里堆积仅得简单立方
C
解析 密置层原子的配位数为6,非密置层原子的配位数为4,图(a)为密置层,图(b)为非密置层。密置层在三维空间堆积可得到六方堆积和面心立方堆积,非密置层在三维空间堆积可得简单立方和体心立方两种堆积。
3.下列有关晶胞的说法正确的是( )
A.晶胞中所含粒子数即为晶体的化学式
B.若晶胞为立方体,则棱上的粒子为3个晶胞共用
C.若晶胞为六棱柱( ),则顶点上的粒子为6个晶胞共用
D.晶胞中不可能存在多种粒子
C
解析 A项,晶胞中的粒子数不一定为晶体的化学式,如课本中的金属铜的晶胞中,铜原子的个数为4;B项,立方体棱上的粒子为4个晶胞共用;C项,如题图所示顶点为6个晶胞共用;D项,如合金晶胞中可以存在多种粒子。
视角2 晶胞中微粒数的计算
4.已知某晶体晶胞如图所示,则该晶体的化学式为( )
A.XYZ B.X2Y4Z
C.XY4Z D.X4Y2Z
C
解析 该晶体的晶胞是立方体形晶胞。该晶胞拥有的X原子数为8× =1;Y原子位于该晶胞内,共有4个,因此该晶胞中拥有的Y原子数为4;Z只有1个,位于晶胞的体心上,故该晶体的化学式为XY4Z。
归纳总结 晶胞中含有微粒数目计算的一般步骤
(1)明确微粒在晶胞中的位置关系。
(2)按照位置关系的平均占有数及同一位置的微粒数目进行计算。
5.现有甲、乙、丙(如图)三种晶体的晶胞(甲中x处于晶胞的中心,乙中a处于晶胞的中心),如图所示。
可推知:甲晶胞中x与y的个数比是 ;乙晶胞中a与b的个数比是 ;丙晶胞中有 个c,有 个d。
答案 4∶3 1∶1 4 4
解析 处于晶胞中心的x或a为晶胞单独占有,位于立方体顶点的微粒为8个立方体共有,位于立方体棱上的微粒为4个立方体共有,位于立方体面上的微粒为2个立方体共有,
6.某物质的晶体中,含A、B、C 3种元素,其排列方式如图所示(其中前后两面心上的B原子未画出),晶体中A、B、C的原子个数比为( )
A.1∶3∶1 B.2∶3∶1
C.2∶2∶1 D.1∶3∶3
A
解析 A原子位于晶胞的顶点,故晶胞中A原子个数为8× =1,B原子位于晶胞的面心,故晶胞中B原子个数为6× =3,C原子位于晶胞的体心,故晶胞中C原子个数为1,所以晶胞中A、B、C的原子个数比为1∶3∶1,A项正确。
7.钛在许多领域都有重要用途,因为可以制造人类关节和接骨,被称为“生物金属”。
(1)钛在元素周期表中位于第 周期
族,其基态原子核外电子排布式为 。
(2)某种钛氧化物晶体的晶胞如图,该晶体每个晶胞中的钛、氧原子个数比为
。
答案 (1)4 ⅣB 1s22s22p63s23p63d24s2
(2)1∶2
解析 (1)钛是22号元素,位于元素周期表第4周期ⅣB族,基态原子核外电子排布式为1s22s22p63s23p63d24s2。
因此钛、氧原子个数比为2∶4=1∶2。
探究二 与晶胞有关的计算
情境探究
铜晶体为面心立方晶胞,其晶胞结构与切割示意图如下。
若铜的相对原子质量为M,铜原子的半径为r m,用NA表示阿伏加德罗常数的值。
1.如何确定铜晶胞中铜原子的个数
2.如何计算铜金属晶体中的晶胞长度和晶胞的体积
3.铜晶胞的质量是多少 铜的密度是多少g·cm-3
4.若晶胞的空间利用率= ×100%,试计算铜晶胞的空间利用率。
方法突破
1.晶体密度的有关计算
假设某晶体的晶胞如图:
以M表示该晶体的摩尔质量,NA表示阿伏加德罗常数,N表示一个晶胞中所含的微粒数,a表示晶胞的棱长,ρ 表示晶体的密度,计算如下:
应用体验
视角 与晶胞有关的计算
1.用X射线研究某金属晶体,测得其立方晶胞的边长为
360 pm,此时金属的密度为9.0 g·cm-3。试回答:
(1)此晶胞中含金属原子 个。
(2)每个晶胞的质量是 g。
(3)此金属的相对原子质量为 。
答案 (1)4 (2)4.2×10-22 (3)63
(2)根据晶胞的边长为360 pm,可得晶胞的体积为(3.6×10-8)3 cm3。
根据m=ρV,可得晶胞的质量=9.0 g·cm-3×(3.6×10-8)3 cm3≈4.2×10-22 g。
(3)金属的摩尔质量M=NA×原子的质量
考题点睛
归纳总结 根据晶胞结构计算晶体密度的方法
(1)确定晶胞中微粒个数;
(2)根据阿伏加德罗常数、微粒个数、微粒的摩尔质量确定晶胞质量;
(3)确定晶胞体积;
2.铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图所示(黑球代表Fe,白球代表Mg)。则下列说法错误的是( )
A.铁镁合金的化学式可表示为Mg2Fe
B.晶胞中有14个铁原子
C.晶体中存在的化学键类型为金属键
B
3.[2023河北邯郸高二期末]砷化硼晶体是具有超高热导率的半导体材料,其结构如图所示,若晶胞参数为a nm,下列说法正确的是( )
A.砷化硼的化学式为B7As2
B.与顶点B原子距离最近且等距的B原子有6个
C.晶胞内的4个As原子所围成的空间结构为正四面体形
C
本 课 结 束
