4.1.1 醇课件(共58张PPT) 2023-2024学年高二化学苏教版选择性必修3
文档属性
| 名称 | 4.1.1 醇课件(共58张PPT) 2023-2024学年高二化学苏教版选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 14.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-09 00:00:00 | ||
图片预览








文档简介
(共58张PPT)
专题4
第一单元 第1课时 醇
素养 目标
1.通过认识羟基的结构,了解醇类的结构特点;从化学键、官能团的角度理解醇类消去反应、催化氧化反应的特征和规律,了解有机反应类型和有机化合物组成结构特点的关系,培养宏观辨识与微观探析的化学核心素养。
2.认识醇的组成和结构特点、性质、转化关系及其在生产、生活的重要应用,培养科学态度与社会责任的化学核心素养。
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
基础落实·必备知识全过关
一、醇的结构与性质
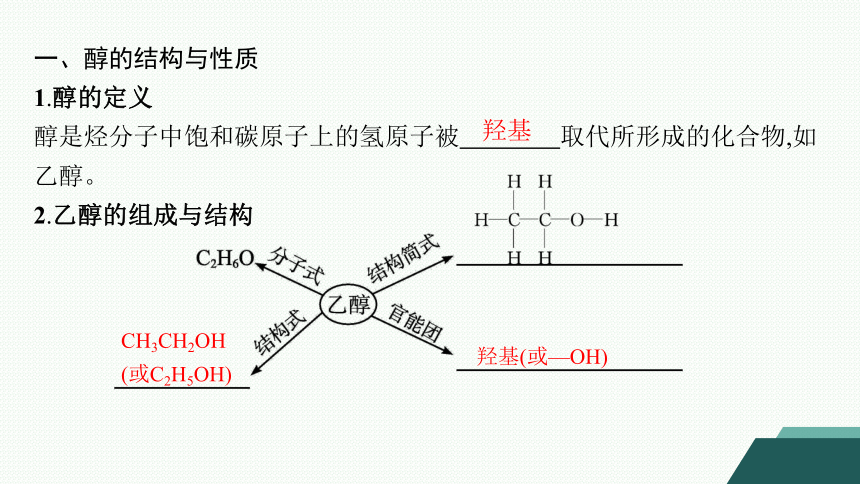
1.醇的定义
醇是烃分子中饱和碳原子上的氢原子被 取代所形成的化合物,如乙醇。
2.乙醇的组成与结构
羟基
CH3CH2OH
(或C2H5OH)
羟基(或—OH)
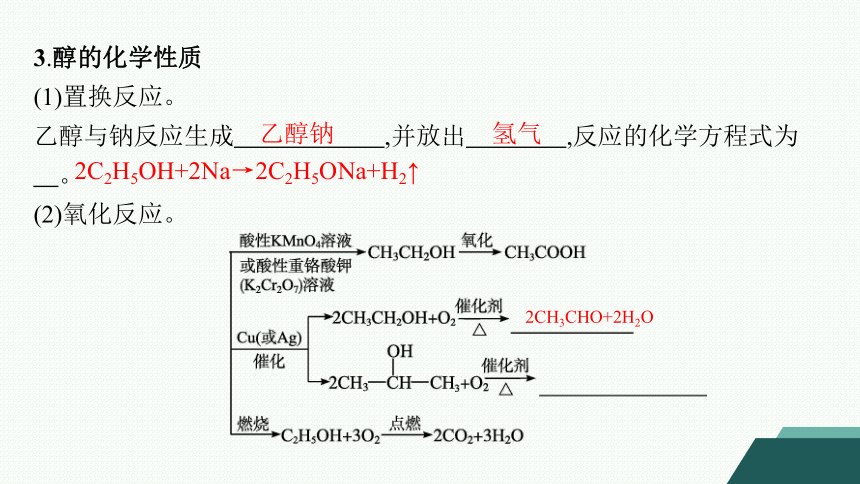
3.醇的化学性质
(1)置换反应。
乙醇与钠反应生成 ,并放出 ,反应的化学方程式为 。
(2)氧化反应。
乙醇钠
氢气
2C2H5OH+2Na→2C2H5ONa+H2↑
2CH3CHO+2H2O
(3)取代反应。
①卤代反应:醇可以与氢卤酸反应,醇分子中的羟基被 取代生成 ,例如乙醇与氢溴酸的反应,化学方程式为 。
②酯化反应:羧酸与醇可发生酯化反应,如制取乙酸乙酯的反应为 。
卤素原子
卤代烃
CH3CH2OH+HBr CH3CH2Br+H2O
CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
(4)脱水反应。
在一定条件下,醇可以发生脱水反应,醇既可以分子内脱水得到烯烃,也可以分子间脱水得到醚。
①乙醇分子内脱水。
乙醇在浓硫酸作用下,加热到170 ℃,发生反应生成乙烯,化学方程式为
。
消去反应:在一定条件下,一个有机物分子内脱去一个或几个 生成
化合物(含双键或三键)的反应,称为消去反应。
化学方程式中注明170 ℃,不能写成“△”
CH3CH2OH CH2==CH2↑+H2O
小分子
不饱和
②分子间脱水。
乙醇在浓硫酸作用下,加热到140 ℃,发生反应生成了乙醚,化学方程式为 。
化学方程式中注明140 ℃,不能写成“△”
2CH3CH2OH CH3CH2OCH2CH3+H2O
易错辨析判一判
(1)从碘水中提取单质碘时,能用无水乙醇代替CCl4。( )
(2)乙醇与HBr、CH3COOH在一定条件下均可发生取代反应,反应中乙醇断键位置相同。( )
(3)乙醇与乙醚互为同分异构体。( )
(4)1-丙醇和2-丙醇发生消去反应的产物相同,但发生催化氧化的产物不同。
( )
×
×
提示 乙醇与HBr、CH3COOH的反应均为取代反应,乙醇与HBr反应时,乙醇分子中碳氧键断裂;乙醇与CH3COOH反应时,乙醇分子中氧氢键断裂,因此两反应中乙醇断键位置不同。
×
提示 乙醇与乙醚的分子式不同,乙醇与甲醚互为同分异构体。
√
二、醇的重要应用
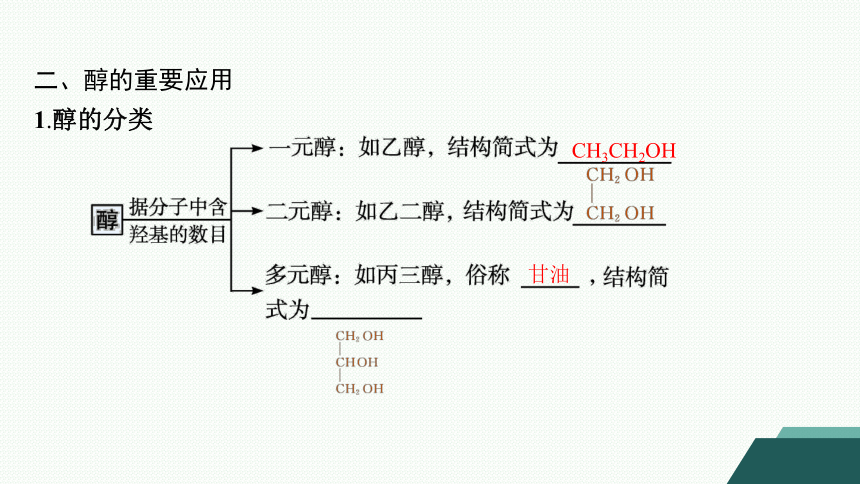
1.醇的分类
CH3CH2OH
甘油
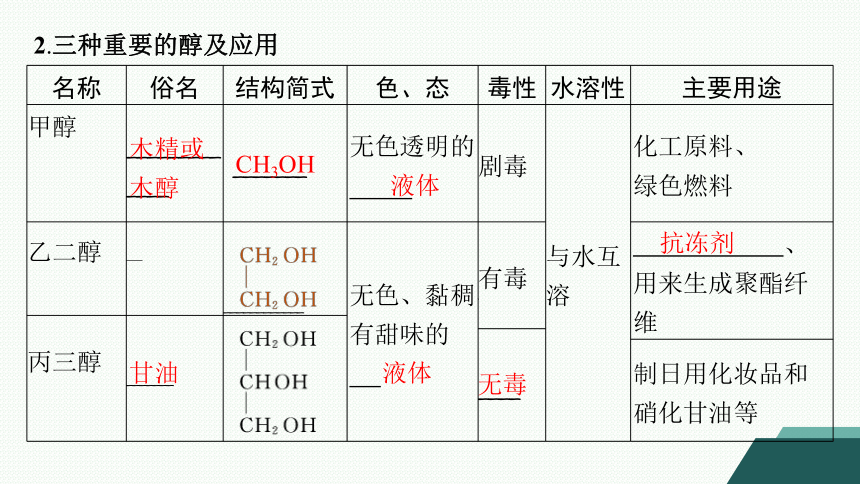
2.三种重要的醇及应用
名称 俗名 结构简式 色、态 毒性 水溶性 主要用途
甲醇 _____________ _______ 无色透明的 剧毒 与水互溶 化工原料、
绿色燃料
乙二醇 — ____________ 无色、黏稠、有甜味的 有毒 、用来生成聚酯纤维
丙三醇 _______
____
制日用化妆品和硝化甘油等
木精或木醇
CH3OH
液体
液体
抗冻剂
甘油
无毒
3.醇的同分异构现象
(1)醇分子内,因羟基的位置不同、碳原子的连接方式不同而存在同分异构现象。例如:
(2)醇和醚之间也存在同分异构现象。例如:
微点拨 醇结构的两个注意点
(1)同一个碳原子上连有两个或两个以上羟基时结构不稳定,容易脱去一分子水,转化为其他类有机化合物,如:
(2)羟基与碳碳双键或碳碳三键相连所形成的醇一般不稳定,如:
CH2==CH—OH→CH3CHO
易错辨析判一判
(1)甲醇、乙二醇、丙三醇不是同系物。( )
(2)质量分数为95%的乙醇溶液常作消毒剂。( )
(3)硝化甘油是一种烈性炸药。( )
(4)乙二醇的水溶液凝固点很高,可用作汽车发动机的抗冻剂。( )
提示 作消毒剂的乙醇溶液体积分数为75%。
提示 乙二醇的水溶液凝固点很低。
√
×
√
×
重难探究·能力素养全提升
探究一 醇的消去反应和取代反应
情境探究
WHO建议的两种醇类洗手液能使流感病毒失活。其中,世卫组织制剂Ⅰ以85%乙醇为基础,高效灭活病毒;世卫组织制剂Ⅱ以75%异丙醇为基础,在低浓度下表现出更好的抗病毒效果,病毒完全失活。
异丙醇与正丙醇互为同分异构体。
1.实验室中用异丙醇制取丙烯时,若异丙醇中混有正丙醇,对得到的丙烯纯度是否有影响
提示 无影响,异丙醇和正丙醇发生消去反应的产物相同。
2.异丙醇和正丙醇的混合物在一定条件下脱水可得到几种醚 试写出它们的结构简式。
3.请写出乙醇与浓硫酸的混合物在170 ℃和140 ℃两种条件下反应的化学方程式,注明反应类型,并分析两反应中乙醇分子中断键位置。
提示 3种。结构简式为CH3CH2CH2OCH2CH2CH3、(CH3)2CHOCH(CH3)2、CH3CH2CH2OCH(CH3)2。
提示 CH3CH2OH CH2==CH2↑+H2O,消去反应;2CH3CH2OH CH3CH2OCH2CH3+H2O,取代反应。
乙醇的消去反应中,乙醇分子断裂碳氧键和相邻碳原子上的碳氢键;乙醇的成醚反应中两分子乙醇一分子断裂碳氧键,另一分子断裂氧氢键。
方法突破
1.醇的消去反应机理
(1)结构特点。
醇分子中,连接—OH的碳原子(α-碳原子)的相邻碳原子上必须连有氢原子时,才能发生消去反应。
与官能团直接相连的碳原子
(2)反应规律。
2.乙醇的消去反应——实验室制取乙烯
(1)实验装置(以浓硫酸为催化剂)。
(2)试剂及其作用。
试剂 作用
浓硫酸 催化剂和脱水剂
氢氧化钠溶液 吸收CO2、SO2和乙醇(SO2和乙醇都与酸性高锰酸钾溶液反应)
溴的CCl4溶液 验证乙烯的不饱和性
酸性高锰酸钾溶液 验证乙烯的还原性
碎瓷片 防止暴沸
(3)实验的关键——严格控制温度。
3.醇的取代反应规律
应用体验
视角1醇的消去反应及规律
1.下列属于消去反应的是( )
A.乙醇与氢溴酸反应
B.乙醇与氧气反应生成乙醛
C.乙醇与乙酸反应生成乙酸乙酯
D.乙醇与浓硫酸共热到170 ℃
D
解析 A项属于取代反应,B项属于氧化反应,C项属于酯化反应(或取代反应),D项属于消去反应,答案选D。
2.下列醇能发生消去反应且只能得到一种单烯烃的是( )
A
视角2乙烯的实验室制取
3.[2023河北保定高二阶段练习]用如下装置制备并收集乙烯,下列说法正确的是( )
A.为防止暴沸,烧瓶中应放入几片碎瓷片
B.为控制反应温度,温度计的量程为0~150 ℃
C.为除去杂质SO2,试剂X可选择酸性KMnO4溶液
D.可用排气法或排水法收集乙烯
A
解析 为防止暴沸,烧瓶中应放入几片碎瓷片,故A正确;该反应为乙醇在浓硫酸的作用下发生消去反应生成乙烯,温度为170 ℃,故B错误;产生SO2说明浓硫酸表现了氧化性,故还应有CO2生成,同时乙醇易挥发,故乙烯中混有乙醇蒸气、SO2、CO2,因此应选择NaOH溶液除杂,酸性KMnO4溶液能与乙烯反应且不能除去CO2,故C错误;乙烯的相对分子质量为28,空气的相对分子质量约为29,乙烯与空气的密度接近,故不可用排气法收集乙烯,故D错误。
4.某化学兴趣小组用如图甲所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到装置Ⅱ试管中溴水褪色,烧瓶中浓硫酸与乙醇的混合液体变为棕黑色。
(1)写出该实验中生成乙烯的化学方程式:
。
(2)甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是 (填字母)。
a.乙烯与溴水易发生取代反应
b.使溴水褪色的反应,未必是加成反应
c.使溴水褪色的物质,未必是乙烯
(3)乙同学经过细致观察装置Ⅱ试管中另一实验现象后,证明反应中有乙烯生成,请简述这一实验现象: 。
(4)丙同学对上述实验装置进行了改进,在装置Ⅰ和装置Ⅱ之间增加如图乙装置以除去乙醇蒸气和SO2,则A中的试剂为 ,B中的试剂为 。
bc
CH3CH2OH CH2==CH2↑+H2O
液体分层,下层为油状液体
NaOH溶液
品红溶液
解析 (1)乙醇与浓硫酸的混合物加热到170 ℃生成乙烯。
(2)由题意知反应中有SO2生成,因SO2具有还原性,也能与溴水发生反应使溴水褪色,所以使溴水褪色的物质,未必是乙烯,SO2同样可以使溴水褪色。
(3)若有乙烯生成,生成的乙烯与溴水发生加成反应生成油状液体1,2-二溴乙烷。即观察到液体分层,下层为油状液体。
(4)A是为了除去SO2和乙醇蒸气,可用NaOH溶液,B是为了检验SO2是否除尽,可用品红溶液。
思维点拨 验证与卤素单质的反应是取代还是加成的方法
有机物与卤素单质反应,若为加成反应则只有有机物生成,若为取代反应则得到有机物和卤化氢,可以通过实验检验是否有卤化氢生成,确定该反应是取代反应还是加成反应。
检验卤化氢可有两种思路,卤化氢溶于水可得氢卤酸,氢卤酸(除HF)均为强酸,可以测定溶液的酸碱性确定;也可用AgNO3溶液检验卤离子。
【变式设问】
(1)若将装置Ⅱ中的溴水改为酸性KMnO4溶液则不能证明生成乙烯,为什么
(2)装置Ⅱ中干燥管的作用是什么
(3)装置Ⅰ中碎瓷片的作用是什么 若实验开始时,忘记添加碎瓷片,应如何操作
提示 反应生成的SO2以及挥发出的乙醇蒸气均可使酸性KMnO4溶液褪色。
提示 防止倒吸。
提示 碎瓷片的作用是防止暴沸。实验开始时,忘记添加碎瓷片,应停止加热,待混合液冷却后再添加。
探究二 醇的催化氧化反应
情境探究
乙酸戊酯是青霉素、丹宁生产中的溶剂和萃取剂。它还广泛用于油漆、香料、木材、纺织、医药等领域。它也可用于牛乳中脂肪的分离,锇与铂族金属的分离等。其中的合成原料之一为戊醇(C5H12O)。
1.戊醇共有多少种
也可根据戊基数目分析:戊醇可表示为C5H11—OH,由于戊基C5H11—有8种,因此戊醇有8种。
2.所有戊醇中能被氧化为醛的有几种 试写出这些醇的结构简式。
提示 4种。能被氧化为醛的戊醇的结构可表示为C4H9—CH2OH,丁基C4H9—有4种,因此可被氧化成醛的戊醇有4种。这4种醇的结构简式为
3.写出戊醇被氧化生成的酮的结构简式。戊醇中有一种不能发生催化氧化的醇,试写出其结构简式和名称。
1.乙醇催化氧化的反应机理
方法突破
2.醇的催化氧化规律
醇能否被氧化以及被氧化的产物的类别,取决于与羟基相连的碳原子上的氢原子的个数,具体分析如下:
应用体验
视角1醇的化学反应机理
1.[2023河北邯郸大名县第一中学高二阶段练习]下列有关乙醇的说法正确的是( )
A.与钠反应,断裂②键
B.发生消去反应生成乙烯,断裂③、④键
C.发生酯化反应,断裂①键
D.发生氧化反应生成乙醛,断裂①、④键
C
解析 与钠反应,断裂①键,A错误;发生消去反应生成乙烯,断裂②、④键,B错误;发生酯化反应,断裂①键,C正确;发生氧化反应生成乙醛,断裂①、③键,D错误。
2.下列关于丙醇的叙述中,不正确的是( )
A.1-丙醇与氧气的混合气体通过赤热的铜,可生成CH3CH2CHO
B.1-丙醇可与HI溶液发生取代反应
C.2-丙醇在NaOH溶液中能发生消去反应,生成一种烯烃
D.1-丙醇、2-丙醇互为同分异构体
C
解析 1-丙醇的结构简式为CH3CH2CH2OH,在铜催化作用下可被O2氧化生成CH3CH2CHO,A正确;醇可与氢卤酸发生取代反应,B正确;2-丙醇在NaOH溶液中不能发生消去反应,C错误;1-丙醇、2-丙醇分子式相同,结构不同,它们互为同分异构体,D正确。
3.下列既能发生消去反应,又能被氧化成含醛基的物质是( )
C
解析 A中与羟基相连的碳原子上只有一个氢原子,被氧化不能生成醛基,A错误;B中与羟基相连的碳原子的邻位碳原子上没有氢原子,不能发生消去反应,B错误;C中与羟基相连的碳原子上有2个氢原子,可以被氧化成醛基,与羟基相连的碳原子的邻位碳原子上有氢原子,可以发生消去反应,C正确;D中与羟基相连的碳原子的邻位碳原子上没有氢原子,不能发生消去反应,D错误。
【变式设问】
(1)写出A项中醇发生消去反应所得产物的结构简式及名称。
(2)写出B项中物质发生催化氧化反应所得产物的结构简式及名称。
提示 CH3CH2CH==CH2,名称为1-丁烯;
CH3CH==CHCH3,名称为2-丁烯。
提示 (CH3)3CCHO,名称为2,2-二甲基丙醛。
技巧规律 醇的化学性质与断键位置
反应类型 反应物 断键位置 反应条件
置换反应 醇、活泼金属 ① —
取代反应 卤代反应 醇、HX ② H+,△
酯化反应 醇、羧酸 ① 浓硫酸,△
成醚反应 醇 一分子断①,另一分子断② 浓硫酸,△
反应类型 反应物 断键位置 反应条件
消去反应 醇 ②④ 浓硫酸,△
氧化反应 催化氧化 醇、氧气 ①③ Cu、Ag,△
燃烧反应 醇、氧气 全部 点燃
视角2符合条件的醇的结构判断
4.[2023河北保定高二期中联考]某饱和一元醇发生消去反应后的产物完全加氢,可以得到2,2,4-三甲基己烷,已知原一元醇能发生催化氧化反应,其可能的结构有( )
A.4种 B.3种
C.2种 D.1种
A
解析 某饱和一元醇发生消去反应的产物是单烯烃,完全加氢生成烷烃2,2,4-三甲基己烷,原一元醇能发生催化氧化反应,其可能的结构有
5.某饱和一元醇35.2 g与足量金属Na反应,生成标准状况下氢气为4.48 L,该醇能被催化氧化生成醛的结构可能有( )
A.1种 B.2种
C.3种 D.4种
D
解析 标准状况下4.48 L氢气物质的量为 =0.2 mol
设饱和一元醇的组成为CnH2n+1OH,则:
2CnH2n+1OH ~ H2
(28n+36)g 1 mol
35.2 g 0.2 mol
得n=5
故该醇的组成为C5H11OH,该醇能被氧化成醛,说明存在—CH2OH,可以看作丁烷中1个氢原子被CH2OH替代,丁烷有CH3CH2CH2CH3、CH(CH3)3,均有2种氢原子,故符合条件的醇共有4种,故选D。
视角3乙醇的催化氧化实验
6.实验小组用下列装置进行乙醇催化氧化的实验。已知:乙醛可被氧化为乙酸。
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式:
、 。
2Cu+O2 2CuO
CH3CH2OH+CuO CH3CHO+Cu+H2O
(2)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是 反应。进一步研究表明,鼓入空气的速率与反应体系的温度关系曲线如图所示。
试解释出现图中现象的原因: 。
放热
流速过快的气体将体系中的热量带走
(3)甲和乙两个水浴作用不相同。甲的作用是 ;
乙的作用是 。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 。要除去该物质,可在混合液中加入 (填字母)。然后,再通过 (填实验操作名称)即可除去。
A.氯化钠溶液
B.苯
C.碳酸氢钠溶液
D.四氯化碳
加热乙醇,便于乙醇的挥发
冷却,便于乙醛的收集
乙酸
C
蒸馏
解析 (1)乙醇的催化氧化反应实质是金属铜被氧气氧化为氧化铜,反应的化学方程式为2Cu+O2 2CuO,氧化铜将乙醇氧化为乙醛,反应的化学方程式为CH3CH2OH+CuO CH3CHO+Cu+H2O。
(2)熄灭酒精灯,反应仍能继续进行,说明该乙醇催化氧化反应是放热反应,根据图示的曲线:反应放出热量的多少和氧气的量有关,开始阶段鼓气增多反应放热增多,温度升高,但是过量的气体会将体系中的热量带走,温度降低。
(3)甲和乙两个水浴作用不相同,甲是热水浴,作用是使乙醇平稳转化成乙醇蒸气;乙是冷水浴,目的是将乙醛冷却下来,便于乙醛的收集。
(4)若试管a中收集到的液体用蓝色石蕊试纸检验,试纸显红色,说明液体中还含有乙酸,四个选择答案中,只有碳酸氢钠可以和乙酸反应,生成乙酸钠、水和二氧化碳,故合理选项是C;实现两种互溶物质的分离用蒸馏法。
本 课 结 束
专题4
第一单元 第1课时 醇
素养 目标
1.通过认识羟基的结构,了解醇类的结构特点;从化学键、官能团的角度理解醇类消去反应、催化氧化反应的特征和规律,了解有机反应类型和有机化合物组成结构特点的关系,培养宏观辨识与微观探析的化学核心素养。
2.认识醇的组成和结构特点、性质、转化关系及其在生产、生活的重要应用,培养科学态度与社会责任的化学核心素养。
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
基础落实·必备知识全过关
一、醇的结构与性质
1.醇的定义
醇是烃分子中饱和碳原子上的氢原子被 取代所形成的化合物,如乙醇。
2.乙醇的组成与结构
羟基
CH3CH2OH
(或C2H5OH)
羟基(或—OH)
3.醇的化学性质
(1)置换反应。
乙醇与钠反应生成 ,并放出 ,反应的化学方程式为 。
(2)氧化反应。
乙醇钠
氢气
2C2H5OH+2Na→2C2H5ONa+H2↑
2CH3CHO+2H2O
(3)取代反应。
①卤代反应:醇可以与氢卤酸反应,醇分子中的羟基被 取代生成 ,例如乙醇与氢溴酸的反应,化学方程式为 。
②酯化反应:羧酸与醇可发生酯化反应,如制取乙酸乙酯的反应为 。
卤素原子
卤代烃
CH3CH2OH+HBr CH3CH2Br+H2O
CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
(4)脱水反应。
在一定条件下,醇可以发生脱水反应,醇既可以分子内脱水得到烯烃,也可以分子间脱水得到醚。
①乙醇分子内脱水。
乙醇在浓硫酸作用下,加热到170 ℃,发生反应生成乙烯,化学方程式为
。
消去反应:在一定条件下,一个有机物分子内脱去一个或几个 生成
化合物(含双键或三键)的反应,称为消去反应。
化学方程式中注明170 ℃,不能写成“△”
CH3CH2OH CH2==CH2↑+H2O
小分子
不饱和
②分子间脱水。
乙醇在浓硫酸作用下,加热到140 ℃,发生反应生成了乙醚,化学方程式为 。
化学方程式中注明140 ℃,不能写成“△”
2CH3CH2OH CH3CH2OCH2CH3+H2O
易错辨析判一判
(1)从碘水中提取单质碘时,能用无水乙醇代替CCl4。( )
(2)乙醇与HBr、CH3COOH在一定条件下均可发生取代反应,反应中乙醇断键位置相同。( )
(3)乙醇与乙醚互为同分异构体。( )
(4)1-丙醇和2-丙醇发生消去反应的产物相同,但发生催化氧化的产物不同。
( )
×
×
提示 乙醇与HBr、CH3COOH的反应均为取代反应,乙醇与HBr反应时,乙醇分子中碳氧键断裂;乙醇与CH3COOH反应时,乙醇分子中氧氢键断裂,因此两反应中乙醇断键位置不同。
×
提示 乙醇与乙醚的分子式不同,乙醇与甲醚互为同分异构体。
√
二、醇的重要应用
1.醇的分类
CH3CH2OH
甘油
2.三种重要的醇及应用
名称 俗名 结构简式 色、态 毒性 水溶性 主要用途
甲醇 _____________ _______ 无色透明的 剧毒 与水互溶 化工原料、
绿色燃料
乙二醇 — ____________ 无色、黏稠、有甜味的 有毒 、用来生成聚酯纤维
丙三醇 _______
____
制日用化妆品和硝化甘油等
木精或木醇
CH3OH
液体
液体
抗冻剂
甘油
无毒
3.醇的同分异构现象
(1)醇分子内,因羟基的位置不同、碳原子的连接方式不同而存在同分异构现象。例如:
(2)醇和醚之间也存在同分异构现象。例如:
微点拨 醇结构的两个注意点
(1)同一个碳原子上连有两个或两个以上羟基时结构不稳定,容易脱去一分子水,转化为其他类有机化合物,如:
(2)羟基与碳碳双键或碳碳三键相连所形成的醇一般不稳定,如:
CH2==CH—OH→CH3CHO
易错辨析判一判
(1)甲醇、乙二醇、丙三醇不是同系物。( )
(2)质量分数为95%的乙醇溶液常作消毒剂。( )
(3)硝化甘油是一种烈性炸药。( )
(4)乙二醇的水溶液凝固点很高,可用作汽车发动机的抗冻剂。( )
提示 作消毒剂的乙醇溶液体积分数为75%。
提示 乙二醇的水溶液凝固点很低。
√
×
√
×
重难探究·能力素养全提升
探究一 醇的消去反应和取代反应
情境探究
WHO建议的两种醇类洗手液能使流感病毒失活。其中,世卫组织制剂Ⅰ以85%乙醇为基础,高效灭活病毒;世卫组织制剂Ⅱ以75%异丙醇为基础,在低浓度下表现出更好的抗病毒效果,病毒完全失活。
异丙醇与正丙醇互为同分异构体。
1.实验室中用异丙醇制取丙烯时,若异丙醇中混有正丙醇,对得到的丙烯纯度是否有影响
提示 无影响,异丙醇和正丙醇发生消去反应的产物相同。
2.异丙醇和正丙醇的混合物在一定条件下脱水可得到几种醚 试写出它们的结构简式。
3.请写出乙醇与浓硫酸的混合物在170 ℃和140 ℃两种条件下反应的化学方程式,注明反应类型,并分析两反应中乙醇分子中断键位置。
提示 3种。结构简式为CH3CH2CH2OCH2CH2CH3、(CH3)2CHOCH(CH3)2、CH3CH2CH2OCH(CH3)2。
提示 CH3CH2OH CH2==CH2↑+H2O,消去反应;2CH3CH2OH CH3CH2OCH2CH3+H2O,取代反应。
乙醇的消去反应中,乙醇分子断裂碳氧键和相邻碳原子上的碳氢键;乙醇的成醚反应中两分子乙醇一分子断裂碳氧键,另一分子断裂氧氢键。
方法突破
1.醇的消去反应机理
(1)结构特点。
醇分子中,连接—OH的碳原子(α-碳原子)的相邻碳原子上必须连有氢原子时,才能发生消去反应。
与官能团直接相连的碳原子
(2)反应规律。
2.乙醇的消去反应——实验室制取乙烯
(1)实验装置(以浓硫酸为催化剂)。
(2)试剂及其作用。
试剂 作用
浓硫酸 催化剂和脱水剂
氢氧化钠溶液 吸收CO2、SO2和乙醇(SO2和乙醇都与酸性高锰酸钾溶液反应)
溴的CCl4溶液 验证乙烯的不饱和性
酸性高锰酸钾溶液 验证乙烯的还原性
碎瓷片 防止暴沸
(3)实验的关键——严格控制温度。
3.醇的取代反应规律
应用体验
视角1醇的消去反应及规律
1.下列属于消去反应的是( )
A.乙醇与氢溴酸反应
B.乙醇与氧气反应生成乙醛
C.乙醇与乙酸反应生成乙酸乙酯
D.乙醇与浓硫酸共热到170 ℃
D
解析 A项属于取代反应,B项属于氧化反应,C项属于酯化反应(或取代反应),D项属于消去反应,答案选D。
2.下列醇能发生消去反应且只能得到一种单烯烃的是( )
A
视角2乙烯的实验室制取
3.[2023河北保定高二阶段练习]用如下装置制备并收集乙烯,下列说法正确的是( )
A.为防止暴沸,烧瓶中应放入几片碎瓷片
B.为控制反应温度,温度计的量程为0~150 ℃
C.为除去杂质SO2,试剂X可选择酸性KMnO4溶液
D.可用排气法或排水法收集乙烯
A
解析 为防止暴沸,烧瓶中应放入几片碎瓷片,故A正确;该反应为乙醇在浓硫酸的作用下发生消去反应生成乙烯,温度为170 ℃,故B错误;产生SO2说明浓硫酸表现了氧化性,故还应有CO2生成,同时乙醇易挥发,故乙烯中混有乙醇蒸气、SO2、CO2,因此应选择NaOH溶液除杂,酸性KMnO4溶液能与乙烯反应且不能除去CO2,故C错误;乙烯的相对分子质量为28,空气的相对分子质量约为29,乙烯与空气的密度接近,故不可用排气法收集乙烯,故D错误。
4.某化学兴趣小组用如图甲所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到装置Ⅱ试管中溴水褪色,烧瓶中浓硫酸与乙醇的混合液体变为棕黑色。
(1)写出该实验中生成乙烯的化学方程式:
。
(2)甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是 (填字母)。
a.乙烯与溴水易发生取代反应
b.使溴水褪色的反应,未必是加成反应
c.使溴水褪色的物质,未必是乙烯
(3)乙同学经过细致观察装置Ⅱ试管中另一实验现象后,证明反应中有乙烯生成,请简述这一实验现象: 。
(4)丙同学对上述实验装置进行了改进,在装置Ⅰ和装置Ⅱ之间增加如图乙装置以除去乙醇蒸气和SO2,则A中的试剂为 ,B中的试剂为 。
bc
CH3CH2OH CH2==CH2↑+H2O
液体分层,下层为油状液体
NaOH溶液
品红溶液
解析 (1)乙醇与浓硫酸的混合物加热到170 ℃生成乙烯。
(2)由题意知反应中有SO2生成,因SO2具有还原性,也能与溴水发生反应使溴水褪色,所以使溴水褪色的物质,未必是乙烯,SO2同样可以使溴水褪色。
(3)若有乙烯生成,生成的乙烯与溴水发生加成反应生成油状液体1,2-二溴乙烷。即观察到液体分层,下层为油状液体。
(4)A是为了除去SO2和乙醇蒸气,可用NaOH溶液,B是为了检验SO2是否除尽,可用品红溶液。
思维点拨 验证与卤素单质的反应是取代还是加成的方法
有机物与卤素单质反应,若为加成反应则只有有机物生成,若为取代反应则得到有机物和卤化氢,可以通过实验检验是否有卤化氢生成,确定该反应是取代反应还是加成反应。
检验卤化氢可有两种思路,卤化氢溶于水可得氢卤酸,氢卤酸(除HF)均为强酸,可以测定溶液的酸碱性确定;也可用AgNO3溶液检验卤离子。
【变式设问】
(1)若将装置Ⅱ中的溴水改为酸性KMnO4溶液则不能证明生成乙烯,为什么
(2)装置Ⅱ中干燥管的作用是什么
(3)装置Ⅰ中碎瓷片的作用是什么 若实验开始时,忘记添加碎瓷片,应如何操作
提示 反应生成的SO2以及挥发出的乙醇蒸气均可使酸性KMnO4溶液褪色。
提示 防止倒吸。
提示 碎瓷片的作用是防止暴沸。实验开始时,忘记添加碎瓷片,应停止加热,待混合液冷却后再添加。
探究二 醇的催化氧化反应
情境探究
乙酸戊酯是青霉素、丹宁生产中的溶剂和萃取剂。它还广泛用于油漆、香料、木材、纺织、医药等领域。它也可用于牛乳中脂肪的分离,锇与铂族金属的分离等。其中的合成原料之一为戊醇(C5H12O)。
1.戊醇共有多少种
也可根据戊基数目分析:戊醇可表示为C5H11—OH,由于戊基C5H11—有8种,因此戊醇有8种。
2.所有戊醇中能被氧化为醛的有几种 试写出这些醇的结构简式。
提示 4种。能被氧化为醛的戊醇的结构可表示为C4H9—CH2OH,丁基C4H9—有4种,因此可被氧化成醛的戊醇有4种。这4种醇的结构简式为
3.写出戊醇被氧化生成的酮的结构简式。戊醇中有一种不能发生催化氧化的醇,试写出其结构简式和名称。
1.乙醇催化氧化的反应机理
方法突破
2.醇的催化氧化规律
醇能否被氧化以及被氧化的产物的类别,取决于与羟基相连的碳原子上的氢原子的个数,具体分析如下:
应用体验
视角1醇的化学反应机理
1.[2023河北邯郸大名县第一中学高二阶段练习]下列有关乙醇的说法正确的是( )
A.与钠反应,断裂②键
B.发生消去反应生成乙烯,断裂③、④键
C.发生酯化反应,断裂①键
D.发生氧化反应生成乙醛,断裂①、④键
C
解析 与钠反应,断裂①键,A错误;发生消去反应生成乙烯,断裂②、④键,B错误;发生酯化反应,断裂①键,C正确;发生氧化反应生成乙醛,断裂①、③键,D错误。
2.下列关于丙醇的叙述中,不正确的是( )
A.1-丙醇与氧气的混合气体通过赤热的铜,可生成CH3CH2CHO
B.1-丙醇可与HI溶液发生取代反应
C.2-丙醇在NaOH溶液中能发生消去反应,生成一种烯烃
D.1-丙醇、2-丙醇互为同分异构体
C
解析 1-丙醇的结构简式为CH3CH2CH2OH,在铜催化作用下可被O2氧化生成CH3CH2CHO,A正确;醇可与氢卤酸发生取代反应,B正确;2-丙醇在NaOH溶液中不能发生消去反应,C错误;1-丙醇、2-丙醇分子式相同,结构不同,它们互为同分异构体,D正确。
3.下列既能发生消去反应,又能被氧化成含醛基的物质是( )
C
解析 A中与羟基相连的碳原子上只有一个氢原子,被氧化不能生成醛基,A错误;B中与羟基相连的碳原子的邻位碳原子上没有氢原子,不能发生消去反应,B错误;C中与羟基相连的碳原子上有2个氢原子,可以被氧化成醛基,与羟基相连的碳原子的邻位碳原子上有氢原子,可以发生消去反应,C正确;D中与羟基相连的碳原子的邻位碳原子上没有氢原子,不能发生消去反应,D错误。
【变式设问】
(1)写出A项中醇发生消去反应所得产物的结构简式及名称。
(2)写出B项中物质发生催化氧化反应所得产物的结构简式及名称。
提示 CH3CH2CH==CH2,名称为1-丁烯;
CH3CH==CHCH3,名称为2-丁烯。
提示 (CH3)3CCHO,名称为2,2-二甲基丙醛。
技巧规律 醇的化学性质与断键位置
反应类型 反应物 断键位置 反应条件
置换反应 醇、活泼金属 ① —
取代反应 卤代反应 醇、HX ② H+,△
酯化反应 醇、羧酸 ① 浓硫酸,△
成醚反应 醇 一分子断①,另一分子断② 浓硫酸,△
反应类型 反应物 断键位置 反应条件
消去反应 醇 ②④ 浓硫酸,△
氧化反应 催化氧化 醇、氧气 ①③ Cu、Ag,△
燃烧反应 醇、氧气 全部 点燃
视角2符合条件的醇的结构判断
4.[2023河北保定高二期中联考]某饱和一元醇发生消去反应后的产物完全加氢,可以得到2,2,4-三甲基己烷,已知原一元醇能发生催化氧化反应,其可能的结构有( )
A.4种 B.3种
C.2种 D.1种
A
解析 某饱和一元醇发生消去反应的产物是单烯烃,完全加氢生成烷烃2,2,4-三甲基己烷,原一元醇能发生催化氧化反应,其可能的结构有
5.某饱和一元醇35.2 g与足量金属Na反应,生成标准状况下氢气为4.48 L,该醇能被催化氧化生成醛的结构可能有( )
A.1种 B.2种
C.3种 D.4种
D
解析 标准状况下4.48 L氢气物质的量为 =0.2 mol
设饱和一元醇的组成为CnH2n+1OH,则:
2CnH2n+1OH ~ H2
(28n+36)g 1 mol
35.2 g 0.2 mol
得n=5
故该醇的组成为C5H11OH,该醇能被氧化成醛,说明存在—CH2OH,可以看作丁烷中1个氢原子被CH2OH替代,丁烷有CH3CH2CH2CH3、CH(CH3)3,均有2种氢原子,故符合条件的醇共有4种,故选D。
视角3乙醇的催化氧化实验
6.实验小组用下列装置进行乙醇催化氧化的实验。已知:乙醛可被氧化为乙酸。
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式:
、 。
2Cu+O2 2CuO
CH3CH2OH+CuO CH3CHO+Cu+H2O
(2)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是 反应。进一步研究表明,鼓入空气的速率与反应体系的温度关系曲线如图所示。
试解释出现图中现象的原因: 。
放热
流速过快的气体将体系中的热量带走
(3)甲和乙两个水浴作用不相同。甲的作用是 ;
乙的作用是 。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 。要除去该物质,可在混合液中加入 (填字母)。然后,再通过 (填实验操作名称)即可除去。
A.氯化钠溶液
B.苯
C.碳酸氢钠溶液
D.四氯化碳
加热乙醇,便于乙醇的挥发
冷却,便于乙醛的收集
乙酸
C
蒸馏
解析 (1)乙醇的催化氧化反应实质是金属铜被氧气氧化为氧化铜,反应的化学方程式为2Cu+O2 2CuO,氧化铜将乙醇氧化为乙醛,反应的化学方程式为CH3CH2OH+CuO CH3CHO+Cu+H2O。
(2)熄灭酒精灯,反应仍能继续进行,说明该乙醇催化氧化反应是放热反应,根据图示的曲线:反应放出热量的多少和氧气的量有关,开始阶段鼓气增多反应放热增多,温度升高,但是过量的气体会将体系中的热量带走,温度降低。
(3)甲和乙两个水浴作用不相同,甲是热水浴,作用是使乙醇平稳转化成乙醇蒸气;乙是冷水浴,目的是将乙醛冷却下来,便于乙醛的收集。
(4)若试管a中收集到的液体用蓝色石蕊试纸检验,试纸显红色,说明液体中还含有乙酸,四个选择答案中,只有碳酸氢钠可以和乙酸反应,生成乙酸钠、水和二氧化碳,故合理选项是C;实现两种互溶物质的分离用蒸馏法。
本 课 结 束
