6.2 蛋白质课件(共56张PPT) 2023-2024学年高二化学苏教版选择性必修3
文档属性
| 名称 | 6.2 蛋白质课件(共56张PPT) 2023-2024学年高二化学苏教版选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 14.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-09 00:00:00 | ||
图片预览









文档简介
(共56张PPT)
专题6
第二单元 蛋白质
素养 目标
1.认识氨基酸的组成、结构特点和主要的化学性质,知道氨基酸和蛋白质的相互转化关系,培养宏观辨识与微观探析的化学核心素养。
2.了解氨基酸、蛋白质与人体健康的关系,认识人工合成多肽、蛋白质等的意义;能初步认识核酸的结构特点和生物功能,体会化学科学在生命科学发展中所起的重要作用,培养科学态度与社会责任的化学核心素养。
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
基础落实·必备知识全过关
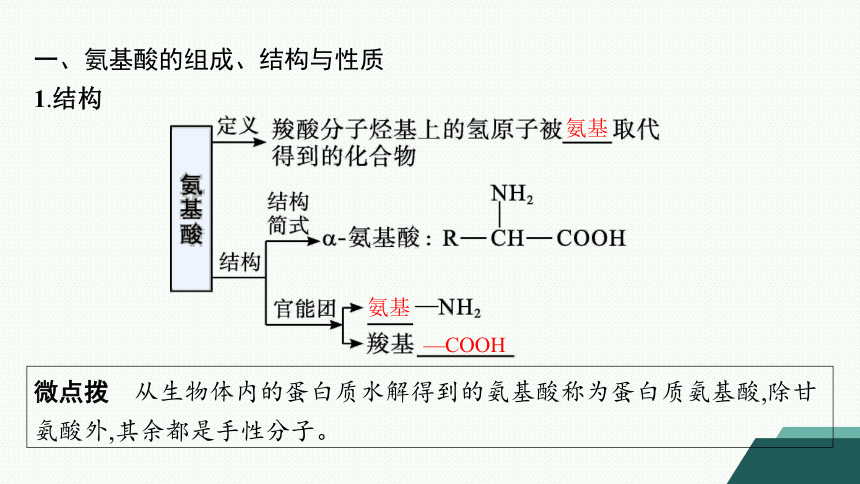
一、氨基酸的组成、结构与性质
1.结构
微点拨 从生物体内的蛋白质水解得到的氨基酸称为蛋白质氨基酸,除甘氨酸外,其余都是手性分子。
氨基
氨基
—COOH
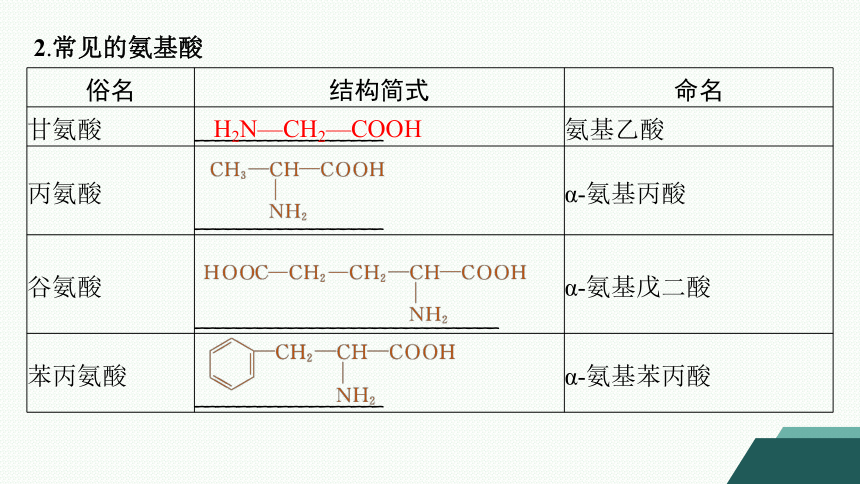
2.常见的氨基酸
俗名 结构简式 命名
甘氨酸 __________________ 氨基乙酸
丙氨酸 __________________ α-氨基丙酸
谷氨酸 _____________________________ α-氨基戊二酸
苯丙氨酸 __________________ α-氨基苯丙酸
H2N—CH2—COOH
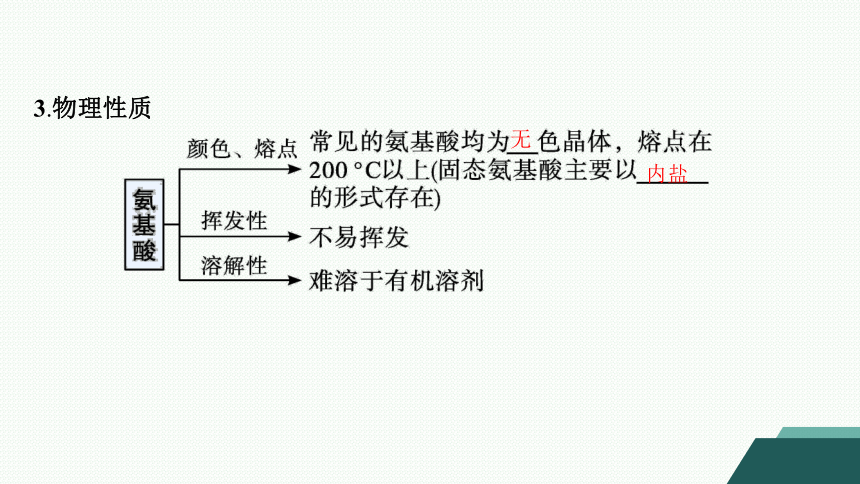
3.物理性质
无
内盐
4.化学性质
(1)两性。
①氨基酸分子中既含有氨基(显 性),又含有羧基(显 性),因此,氨基酸是 化合物,能与酸、碱反应生成盐。如:
碱
酸
两性
②自身反应生成内盐。
氨基酸分子中的氨基和羧基发生相互作用,使氨基酸成为带有正电荷和负电荷的 (称为内盐): 。
两性离子
(2)氨基酸的缩合反应。
一分子α-氨基酸中的 与另一分子α-氨基酸中的 可以发生像酯化反应那样的脱水反应,形成 (酰胺键),称为氨基酸的缩合反应,得到的产物称为肽,组成肽的氨基酸单元称为 。如:
羧基
氨基
肽键
氨基酸残基
(3)茚三酮反应。
含有—NH2的α-氨基酸遇茚三酮均显 反应。该反应非常灵敏,是鉴定 最简便的方法。
紫色
氨基酸
教材阅读想一想阅读教材“方法导引·肽键的形成和肽的水解”。谷氨酸的结构简式为 ,在一定条件下,一分子谷氨酸分子内缩合可形成含有五元环的化合物,试写出该化合物的结构简式。
易错辨析判一判
(1)氨基酸分子中的—COOH能电离出H+显酸性,—NH2能结合H+显碱性。
( )
(2)成肽反应的规律为—COOH脱—OH,—NH2脱—H。( )
(3)氨基酸能发生酯化反应、成肽反应和水解反应。( )
(4)两个氨基酸分子脱水后形成的二肽中含有两个肽键。( )
√
√
提示 氨基酸不能发生水解反应。
提示 两个氨基酸分子脱水后形成的二肽中只含有一个肽键。
×
×
二、蛋白质的结构与性质
1.结构
(1)组成结构。
蛋白质中主要含有 等元素,由氨基酸通过 等相互连接而形成的一类具有特定结构和一定生物学功能的生物大分子。
(2)四级结构。
C、H、O、N、S
肽键
蛋白质
的生物活性
2.化学性质
(1)两性。
在多肽链的两端存在着自由的 和 ,因此蛋白质既能与酸反应,又能与碱反应。
(2)水解。
①水解原理:
氨基
羧基
②水解过程:
多肽
氨基酸
氨基酸
(3)盐析。
①实质:向蛋白质溶液中加入浓的 (如饱和硫酸铵溶液、硫酸钠溶液等),使蛋白质的溶解度 而从溶液中析出。
②特点:盐析是一个 过程,盐析出的蛋白质在水中能 ,并不影响其 。
③应用:多次盐析和溶解可以 蛋白质。
无机盐溶液
降低
可逆
溶解
活性
分离、提纯
(4)变性。
(5)颜色反应。
①蛋白质遇双缩脲试剂会呈现 色。
②含有苯环的蛋白质与浓硝酸作用时会产生 色固态物质。
强酸
强碱
不能
活性
紫玫瑰
黄
3.存在和作用
(1)存在:蛋白质是细胞和组织结构的重要组成部分,存在于一切生物体中。
(2)作用:有些蛋白质负责输送氧气,激素或酶在新陈代谢中起调节或催化作用,抗体能预防疾病的发生,核蛋白与遗传相关。
4.酶的催化特点
绝大多数酶是 ,具有催化作用,其催化反应具有 、 、 等特点。
蛋白质
条件温和
效率高
高度专一
易错辨析判一判
(1)医疗器械高温消毒的原理是蛋白质的变性。( )
(2)蛋白质遇浓硝酸都会显黄色。( )
(3)向蛋白质溶液中加入饱和(NH4)2SO4溶液或CuSO4溶液,会产生沉淀,如再加水,会溶解。( )
(4)酶是一种高效催化剂,对各类化学反应都有良好的催化作用,温度越高,催化效果越好。( )
提示 含有苯环的蛋白质遇浓硝酸显黄色。
提示 CuSO4溶液使蛋白质变性,产生的沉淀再加水时也不会溶解。
提示 酶的催化作用具有专一性、高效性等特点,且催化反应条件温和,温度过高会使酶失去活性。
√
×
×
×
三、核酸的结构及生物功能
1.核酸的种类
2.核酸水解得到的碱基
(1)核糖核苷酸:腺嘌呤(A)、鸟嘌呤(G)、胞嘧啶(C)、尿嘧啶(U)。
(2)脱氧核苷酸:腺嘌呤(A)、鸟嘌呤(G)、胞嘧啶(C)、胸腺嘧啶(T)。
脱氧核糖核酸
3.核酸的水解和生成
4.核酸的结构
(1)核酸的一级结构是指组成核酸的核苷酸的排列顺序。
(2)核酸的二级结构和三级结构是指核酸的空间结构。
5.碱基互补配对原则
DNA的双螺旋结构中,不同的碱基通过氢键两两配对,碱基配对存在着严格的关系,即一条链上的碱基A与另一条链上的碱基T通过两个氢键配对;同样,碱基G和碱基C之间通过三个氢键配对。
6.核酸的生物功能
(1)DNA主要存在于细胞核中,是 的储存和携带者。
(2)RNA主要存在于细胞质中,以DNA为模板形成,将DNA的遗传信息翻译并表达成具有特定功能的蛋白质。
遗传信息
易错辨析判一判
(1)核酸分为DNA和RNA,是一类含磷的生物高分子。( )
(2)蛋白质的N元素主要存在于肽键中,核酸的N元素存在于碱基中。( )
(3)判断核酸种类可依据戊糖或碱基的种类。( )
(4)DNA、RNA均为双螺旋结构。( )
√
√
√
×
提示 RNA不是双螺旋结构。
重难探究·能力素养全提升
探究一 氨基酸的性质
情境探究
氨基酸分子间可以发生像酯化反应那样的脱水缩合反应,形成肽键
1.氨基酸脱水形成二肽的反应,属于取代反应吗
提示 属于。因为从反应过程看,氨基酸的缩合反应可以看成氨基上的H被取代,也可以看成羧基上的羟基被取代。
2.3个甘氨酸分子发生缩合反应最多可以生成几个水分子
提示 3个。氨基酸分子缩合既可形成链状也可以形成环状,其中形成环状时,3个甘氨酸分子可以生成3个水分子。
3.甘氨酸和丙氨酸的混合物在一定条件下能形成几种二肽 写出可能形成二肽的结构简式。
提示 4种。结构简式为
方法突破
1.氨基酸的两性
2.氨基酸的缩合反应
(1)氨基酸的缩合机理——羧脱羟基氨脱氢。
(2)氨基酸的缩合类型。
①两分子间缩合成二肽,两种不同分子发生缩合反应生成的二肽有四种:自身结合有两种,两两互相结合有两种。
②分子间或分子内缩合成环。
应用体验
视角1氨基酸的结构与性质
1.青霉素是医学上常用的一种抗生素,其高效、低毒、临床应用广泛。青霉素在体内酸性条件下水解后,得到青霉氨基酸,其结构简式如图所示(分子中的—SH与—OH具有类似性质)。
下列关于青霉氨基酸的推断合理的是( )
A.青霉氨基酸分子中所有碳原子均在同一直线上
B.青霉氨基酸只有酸性,没有碱性
C.青霉氨基酸分子间能形成多肽
D.1 mol青霉氨基酸与足量的金属钠反应生成0.5 mol H2
C
解析 根据甲烷的分子结构,青霉氨基酸分子中有饱和碳原子,形成的碳链不可能是直线形,A错误;青霉氨基酸分子中含有—NH2,所以具有碱性,B错误;青霉氨基酸分子中的—NH2和—COOH可以缩合,形成多肽,C正确;青霉氨基酸中—COOH和—SH均可与Na反应,所以1 mol青霉氨基酸与足量的金属钠反应生成的H2的物质的量为1 mol,D错误。
2.已知酪氨酸是生命活动不可缺少的一种氨基酸,它的结构简式是
(1)酪氨酸能发生的化学反应类型有 (填字母)。
A.取代反应 B.加成反应
C.酯化反应 D.中和反应
(2)在酪氨酸的同分异构体中,同时满足以下三个条件,除酪氨酸外还有
种。
①属于氨基酸且“碳骨架”与酪氨酸相同;②羟基直接连在苯环上;③氨基(—NH2)不与苯环直接相连。
ABCD
5
解析 (1)酪氨酸含有的—COOH能发生酯化反应、中和反应,其中酯化反应也属于取代反应;含有苯环可发生取代反应和加成反应。(2)酪氨酸的同分异构体符合条件:①碳骨架不变,②—OH仍连在苯环上,③—NH2连在苯环侧链上,即—OH在苯环上发生位置异构,—NH2在侧链上发生位置异构,因
视角2成肽反应的分析
3.科学家发现半胱氨酸能增强艾滋病病毒感染者的免疫力,对控制艾滋病病毒的蔓延有一定效果。已知半胱氨酸的结构简式为
,则下列说法错误的是( )
A.半胱氨酸属于α-氨基酸
B.半胱氨酸既能与强酸反应又能与强碱反应
C.半胱氨酸不能与NaOH溶液反应放出碱性气体
D.两分子半胱氨酸脱水形成的二肽结构简式为
D
解析 半胱氨酸中—NH2和—COOH连在同一碳原子上,属于α-氨基酸,A正确;半胱氨酸既含有羧基又含有氨基,既能与强碱反应又能与强酸反应,B正确;半胱氨酸与NaOH溶液反应只能生成半胱氨酸钠,不能生成氨气,C正确;两分子半胱氨酸脱水形成的二肽结构简式应为
归纳总结 成肽反应两特点
(1)二肽是由2个氨基酸分子形成的,n个氨基酸分子脱去(n-1)个水分子,形成n肽,含有(n-1)个肽键。
(2)无论肽链有多长,在链的两端,一端有游离的氨基(—NH2),另一端有游离的羧基(—COOH),因此,多肽也具有“两性”。
4.有一分子式为C8H14N2O5的二肽,经水解得丙氨酸 和另一种氨基酸X,则X的分子式可能是( )
A.C3H7NO3 B.C5H9NO4
C.C5H11NO5 D.C5H7NO4
B
5.某物质的球棍模型如图所示,下列关于该物质的说法不正确的是( )
A.该物质的结构简式为
B.该物质可以发生加成反应
C.该物质既可以与强酸反应也可以与强碱反应
D.该物质可以聚合成高分子物质
A
解析 题给结构简式中应将六元环改为苯环,A项错误;该氨基酸分子中含有苯环,可与H2发生加成反应,B项正确;氨基可与强酸反应,而羧基可与强碱反应,C项正确;分子中含有羧基和氨基,故该氨基酸可以聚合成有机高分子,D项正确。
探究二 蛋白质的性质
情境探究
蛋白质是生命活动的主要物质基础,是生命活动的主要承担者。蛋白质在机体中发挥着多种功能,能够供给机体营养、提供保护机能、输送氧气、防止病菌侵袭、控制代谢过程等。多肽也是一种在生命活动过程中有着重要作用的物质。蛋白质和多肽都是由氨基酸形成的。
1.可以采用什么方法检验蛋白质
提示 (1)显色反应
①蛋白质遇双缩脲试剂会呈现紫玫瑰色。
②含苯环的蛋白质与浓硝酸作用会产生黄色固态物质。
(2)灼烧法:灼烧蛋白质,可闻到烧焦羽毛气味。
2.如何分离和提纯蛋白质
3.在临床上解救Cu2+、Pb2+、Hg2+等重金属盐中毒的病人时,为什么要求病人服用大量蛋白质含量丰富的生鸡蛋、牛奶或豆浆等
提示 ①常用盐析法来分离和提纯蛋白质,因为盐析是可逆的。②对于蛋白质溶液(属于胶体),可用渗析法除去其中的杂质离子。
提示 生鸡蛋、牛奶、豆浆中含有丰富的蛋白质,重金属离子会使这些食物中的蛋白质变性形成沉淀,可减少对病人本身蛋白质的损伤。
方法突破
1.蛋白质的水解反应
蛋白质的水解:在酸、碱或酶的作用下,肽键断裂,碳原子连接—OH,氮原子连接—H。
肽键水解的原理示意图如下:
2.盐析、变性和渗析的对比
名称 盐析 变性 渗析
原理 加入浓的无机盐溶液使蛋白质从溶液中析出 一定条件下,使蛋白质失去原有的生理活性 利用半透膜分离胶体粒子与普通分子、离子
条件 浓的轻金属盐或铵盐,如(NH4)2SO4、Na2SO4、NaCl溶液等 加热、紫外线、X射线、重金属盐、强酸、强碱、乙醇、甲醛等 胶体、半透膜、水等
特点 可逆,蛋白质仍保持原有活性 不可逆,蛋白质失去原有活性 需多次换水
实例 向蛋白质溶胶中加浓Na2SO4溶液使蛋白质析出 消毒、灭菌、给果树使用波尔多液 除去淀粉溶液(胶体)中的NaNO3杂质
应用体验
视角1蛋白质的水解反应
1.某蛋白质的结构片段如下:
(1)上述蛋白质的结构片段的水解产物中不属于α-氨基酸的结构简式
是 。
解析 根据蛋白质的水解规律,可得该蛋白质的结构片段水解生成的氨基酸如下:
(2)上述蛋白质的结构片段水解后的氨基酸中,某氨基酸的碳、氢原子数比值最大。
①该氨基酸与NaOH反应的化学方程式为
。
②两分子该氨基酸缩合形成环状物质的结构简式为 ,
分子式为 。
C16H14N2O2
解析 分子中碳、氢原子数比值最大,其分子式为C8H9NO2,两分子缩合形成环状物质时应脱去两分子H2O,根据原子个数守恒可知所得缩合物的分子式为C16H14N2O2,结构简式为
。
(3)已知上述蛋白质结构片段的相对分子质量为364,则水解生成的各种氨基酸的相对分子质量之和为 。
436
解析 该蛋白质结构片段水解生成了4种氨基酸,相应地增加了4个H2O分子的相对分子质量,即水解生成的各种氨基酸的相对分子质量之和为364+72=436。
思维点拨 (1)分子式或相对分子质量推断。两个氨基酸分子形成1个肽键,产生1分子H2O;n个氨基酸形成一条肽链时,含有(n-1)个肽键,产生(n-1)分子H2O。据此可根据形成多肽的氨基酸分子式,推断多肽的分子式或相对分子质量;也可根据多肽的分子式或相对分子质量,推断形成多肽的氨基酸分子式之和或相对分子质量之和。
(2)氨基酸数目的计算。利用氮原子守恒即一般一个氨基酸分子含有一个氮原子(氨基)来求解多肽水解后氨基酸的数目。当条件不完整时,可用讨论法;当条件完整但不能直接推导时,可用方程组法。
视角2蛋白质的盐析、变性
2.人类肝脏蛋白质的两谱三图三库已经全面破译完成,它将为肝脏疾病的预警、预防、诊断和治疗提供科学依据。下列关于肝脏蛋白质的说法不正确的是( )
A.属于生物高分子
B.水解的最终产物能与酸或碱反应
C.遇浓硝酸会变性
D.水解时碳氧键断裂
D
解析 蛋白质属于生物高分子,A正确;蛋白质水解的最终产物是氨基酸,能与酸或碱反应,B正确;蛋白质遇强酸会变性,C正确;水解时,肽键( )中的C—N键断裂,D错误。
3.下列说法不正确的是( )
A.组成天然蛋白质的氨基酸都是α-氨基酸
B.利用盐析可以分离和提纯蛋白质
C.DNA是生物体遗传信息的载体,蛋白质合成的模板
D.RNA主要存在于细胞核中,它根据DNA提供的信息控制体内蛋白质的合成
D
解析 组成天然蛋白质的氨基酸都是α-氨基酸,A说法正确;盐析可以使蛋白质因溶解度变小而析出,所以利用盐析可以分离、提纯蛋白质,B说法正确;DNA是生物体遗传信息的载体,蛋白质合成的模板,C说法正确;RNA主要存在于细胞质中,D说法错误。
本 课 结 束
专题6
第二单元 蛋白质
素养 目标
1.认识氨基酸的组成、结构特点和主要的化学性质,知道氨基酸和蛋白质的相互转化关系,培养宏观辨识与微观探析的化学核心素养。
2.了解氨基酸、蛋白质与人体健康的关系,认识人工合成多肽、蛋白质等的意义;能初步认识核酸的结构特点和生物功能,体会化学科学在生命科学发展中所起的重要作用,培养科学态度与社会责任的化学核心素养。
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
基础落实·必备知识全过关
一、氨基酸的组成、结构与性质
1.结构
微点拨 从生物体内的蛋白质水解得到的氨基酸称为蛋白质氨基酸,除甘氨酸外,其余都是手性分子。
氨基
氨基
—COOH
2.常见的氨基酸
俗名 结构简式 命名
甘氨酸 __________________ 氨基乙酸
丙氨酸 __________________ α-氨基丙酸
谷氨酸 _____________________________ α-氨基戊二酸
苯丙氨酸 __________________ α-氨基苯丙酸
H2N—CH2—COOH
3.物理性质
无
内盐
4.化学性质
(1)两性。
①氨基酸分子中既含有氨基(显 性),又含有羧基(显 性),因此,氨基酸是 化合物,能与酸、碱反应生成盐。如:
碱
酸
两性
②自身反应生成内盐。
氨基酸分子中的氨基和羧基发生相互作用,使氨基酸成为带有正电荷和负电荷的 (称为内盐): 。
两性离子
(2)氨基酸的缩合反应。
一分子α-氨基酸中的 与另一分子α-氨基酸中的 可以发生像酯化反应那样的脱水反应,形成 (酰胺键),称为氨基酸的缩合反应,得到的产物称为肽,组成肽的氨基酸单元称为 。如:
羧基
氨基
肽键
氨基酸残基
(3)茚三酮反应。
含有—NH2的α-氨基酸遇茚三酮均显 反应。该反应非常灵敏,是鉴定 最简便的方法。
紫色
氨基酸
教材阅读想一想阅读教材“方法导引·肽键的形成和肽的水解”。谷氨酸的结构简式为 ,在一定条件下,一分子谷氨酸分子内缩合可形成含有五元环的化合物,试写出该化合物的结构简式。
易错辨析判一判
(1)氨基酸分子中的—COOH能电离出H+显酸性,—NH2能结合H+显碱性。
( )
(2)成肽反应的规律为—COOH脱—OH,—NH2脱—H。( )
(3)氨基酸能发生酯化反应、成肽反应和水解反应。( )
(4)两个氨基酸分子脱水后形成的二肽中含有两个肽键。( )
√
√
提示 氨基酸不能发生水解反应。
提示 两个氨基酸分子脱水后形成的二肽中只含有一个肽键。
×
×
二、蛋白质的结构与性质
1.结构
(1)组成结构。
蛋白质中主要含有 等元素,由氨基酸通过 等相互连接而形成的一类具有特定结构和一定生物学功能的生物大分子。
(2)四级结构。
C、H、O、N、S
肽键
蛋白质
的生物活性
2.化学性质
(1)两性。
在多肽链的两端存在着自由的 和 ,因此蛋白质既能与酸反应,又能与碱反应。
(2)水解。
①水解原理:
氨基
羧基
②水解过程:
多肽
氨基酸
氨基酸
(3)盐析。
①实质:向蛋白质溶液中加入浓的 (如饱和硫酸铵溶液、硫酸钠溶液等),使蛋白质的溶解度 而从溶液中析出。
②特点:盐析是一个 过程,盐析出的蛋白质在水中能 ,并不影响其 。
③应用:多次盐析和溶解可以 蛋白质。
无机盐溶液
降低
可逆
溶解
活性
分离、提纯
(4)变性。
(5)颜色反应。
①蛋白质遇双缩脲试剂会呈现 色。
②含有苯环的蛋白质与浓硝酸作用时会产生 色固态物质。
强酸
强碱
不能
活性
紫玫瑰
黄
3.存在和作用
(1)存在:蛋白质是细胞和组织结构的重要组成部分,存在于一切生物体中。
(2)作用:有些蛋白质负责输送氧气,激素或酶在新陈代谢中起调节或催化作用,抗体能预防疾病的发生,核蛋白与遗传相关。
4.酶的催化特点
绝大多数酶是 ,具有催化作用,其催化反应具有 、 、 等特点。
蛋白质
条件温和
效率高
高度专一
易错辨析判一判
(1)医疗器械高温消毒的原理是蛋白质的变性。( )
(2)蛋白质遇浓硝酸都会显黄色。( )
(3)向蛋白质溶液中加入饱和(NH4)2SO4溶液或CuSO4溶液,会产生沉淀,如再加水,会溶解。( )
(4)酶是一种高效催化剂,对各类化学反应都有良好的催化作用,温度越高,催化效果越好。( )
提示 含有苯环的蛋白质遇浓硝酸显黄色。
提示 CuSO4溶液使蛋白质变性,产生的沉淀再加水时也不会溶解。
提示 酶的催化作用具有专一性、高效性等特点,且催化反应条件温和,温度过高会使酶失去活性。
√
×
×
×
三、核酸的结构及生物功能
1.核酸的种类
2.核酸水解得到的碱基
(1)核糖核苷酸:腺嘌呤(A)、鸟嘌呤(G)、胞嘧啶(C)、尿嘧啶(U)。
(2)脱氧核苷酸:腺嘌呤(A)、鸟嘌呤(G)、胞嘧啶(C)、胸腺嘧啶(T)。
脱氧核糖核酸
3.核酸的水解和生成
4.核酸的结构
(1)核酸的一级结构是指组成核酸的核苷酸的排列顺序。
(2)核酸的二级结构和三级结构是指核酸的空间结构。
5.碱基互补配对原则
DNA的双螺旋结构中,不同的碱基通过氢键两两配对,碱基配对存在着严格的关系,即一条链上的碱基A与另一条链上的碱基T通过两个氢键配对;同样,碱基G和碱基C之间通过三个氢键配对。
6.核酸的生物功能
(1)DNA主要存在于细胞核中,是 的储存和携带者。
(2)RNA主要存在于细胞质中,以DNA为模板形成,将DNA的遗传信息翻译并表达成具有特定功能的蛋白质。
遗传信息
易错辨析判一判
(1)核酸分为DNA和RNA,是一类含磷的生物高分子。( )
(2)蛋白质的N元素主要存在于肽键中,核酸的N元素存在于碱基中。( )
(3)判断核酸种类可依据戊糖或碱基的种类。( )
(4)DNA、RNA均为双螺旋结构。( )
√
√
√
×
提示 RNA不是双螺旋结构。
重难探究·能力素养全提升
探究一 氨基酸的性质
情境探究
氨基酸分子间可以发生像酯化反应那样的脱水缩合反应,形成肽键
1.氨基酸脱水形成二肽的反应,属于取代反应吗
提示 属于。因为从反应过程看,氨基酸的缩合反应可以看成氨基上的H被取代,也可以看成羧基上的羟基被取代。
2.3个甘氨酸分子发生缩合反应最多可以生成几个水分子
提示 3个。氨基酸分子缩合既可形成链状也可以形成环状,其中形成环状时,3个甘氨酸分子可以生成3个水分子。
3.甘氨酸和丙氨酸的混合物在一定条件下能形成几种二肽 写出可能形成二肽的结构简式。
提示 4种。结构简式为
方法突破
1.氨基酸的两性
2.氨基酸的缩合反应
(1)氨基酸的缩合机理——羧脱羟基氨脱氢。
(2)氨基酸的缩合类型。
①两分子间缩合成二肽,两种不同分子发生缩合反应生成的二肽有四种:自身结合有两种,两两互相结合有两种。
②分子间或分子内缩合成环。
应用体验
视角1氨基酸的结构与性质
1.青霉素是医学上常用的一种抗生素,其高效、低毒、临床应用广泛。青霉素在体内酸性条件下水解后,得到青霉氨基酸,其结构简式如图所示(分子中的—SH与—OH具有类似性质)。
下列关于青霉氨基酸的推断合理的是( )
A.青霉氨基酸分子中所有碳原子均在同一直线上
B.青霉氨基酸只有酸性,没有碱性
C.青霉氨基酸分子间能形成多肽
D.1 mol青霉氨基酸与足量的金属钠反应生成0.5 mol H2
C
解析 根据甲烷的分子结构,青霉氨基酸分子中有饱和碳原子,形成的碳链不可能是直线形,A错误;青霉氨基酸分子中含有—NH2,所以具有碱性,B错误;青霉氨基酸分子中的—NH2和—COOH可以缩合,形成多肽,C正确;青霉氨基酸中—COOH和—SH均可与Na反应,所以1 mol青霉氨基酸与足量的金属钠反应生成的H2的物质的量为1 mol,D错误。
2.已知酪氨酸是生命活动不可缺少的一种氨基酸,它的结构简式是
(1)酪氨酸能发生的化学反应类型有 (填字母)。
A.取代反应 B.加成反应
C.酯化反应 D.中和反应
(2)在酪氨酸的同分异构体中,同时满足以下三个条件,除酪氨酸外还有
种。
①属于氨基酸且“碳骨架”与酪氨酸相同;②羟基直接连在苯环上;③氨基(—NH2)不与苯环直接相连。
ABCD
5
解析 (1)酪氨酸含有的—COOH能发生酯化反应、中和反应,其中酯化反应也属于取代反应;含有苯环可发生取代反应和加成反应。(2)酪氨酸的同分异构体符合条件:①碳骨架不变,②—OH仍连在苯环上,③—NH2连在苯环侧链上,即—OH在苯环上发生位置异构,—NH2在侧链上发生位置异构,因
视角2成肽反应的分析
3.科学家发现半胱氨酸能增强艾滋病病毒感染者的免疫力,对控制艾滋病病毒的蔓延有一定效果。已知半胱氨酸的结构简式为
,则下列说法错误的是( )
A.半胱氨酸属于α-氨基酸
B.半胱氨酸既能与强酸反应又能与强碱反应
C.半胱氨酸不能与NaOH溶液反应放出碱性气体
D.两分子半胱氨酸脱水形成的二肽结构简式为
D
解析 半胱氨酸中—NH2和—COOH连在同一碳原子上,属于α-氨基酸,A正确;半胱氨酸既含有羧基又含有氨基,既能与强碱反应又能与强酸反应,B正确;半胱氨酸与NaOH溶液反应只能生成半胱氨酸钠,不能生成氨气,C正确;两分子半胱氨酸脱水形成的二肽结构简式应为
归纳总结 成肽反应两特点
(1)二肽是由2个氨基酸分子形成的,n个氨基酸分子脱去(n-1)个水分子,形成n肽,含有(n-1)个肽键。
(2)无论肽链有多长,在链的两端,一端有游离的氨基(—NH2),另一端有游离的羧基(—COOH),因此,多肽也具有“两性”。
4.有一分子式为C8H14N2O5的二肽,经水解得丙氨酸 和另一种氨基酸X,则X的分子式可能是( )
A.C3H7NO3 B.C5H9NO4
C.C5H11NO5 D.C5H7NO4
B
5.某物质的球棍模型如图所示,下列关于该物质的说法不正确的是( )
A.该物质的结构简式为
B.该物质可以发生加成反应
C.该物质既可以与强酸反应也可以与强碱反应
D.该物质可以聚合成高分子物质
A
解析 题给结构简式中应将六元环改为苯环,A项错误;该氨基酸分子中含有苯环,可与H2发生加成反应,B项正确;氨基可与强酸反应,而羧基可与强碱反应,C项正确;分子中含有羧基和氨基,故该氨基酸可以聚合成有机高分子,D项正确。
探究二 蛋白质的性质
情境探究
蛋白质是生命活动的主要物质基础,是生命活动的主要承担者。蛋白质在机体中发挥着多种功能,能够供给机体营养、提供保护机能、输送氧气、防止病菌侵袭、控制代谢过程等。多肽也是一种在生命活动过程中有着重要作用的物质。蛋白质和多肽都是由氨基酸形成的。
1.可以采用什么方法检验蛋白质
提示 (1)显色反应
①蛋白质遇双缩脲试剂会呈现紫玫瑰色。
②含苯环的蛋白质与浓硝酸作用会产生黄色固态物质。
(2)灼烧法:灼烧蛋白质,可闻到烧焦羽毛气味。
2.如何分离和提纯蛋白质
3.在临床上解救Cu2+、Pb2+、Hg2+等重金属盐中毒的病人时,为什么要求病人服用大量蛋白质含量丰富的生鸡蛋、牛奶或豆浆等
提示 ①常用盐析法来分离和提纯蛋白质,因为盐析是可逆的。②对于蛋白质溶液(属于胶体),可用渗析法除去其中的杂质离子。
提示 生鸡蛋、牛奶、豆浆中含有丰富的蛋白质,重金属离子会使这些食物中的蛋白质变性形成沉淀,可减少对病人本身蛋白质的损伤。
方法突破
1.蛋白质的水解反应
蛋白质的水解:在酸、碱或酶的作用下,肽键断裂,碳原子连接—OH,氮原子连接—H。
肽键水解的原理示意图如下:
2.盐析、变性和渗析的对比
名称 盐析 变性 渗析
原理 加入浓的无机盐溶液使蛋白质从溶液中析出 一定条件下,使蛋白质失去原有的生理活性 利用半透膜分离胶体粒子与普通分子、离子
条件 浓的轻金属盐或铵盐,如(NH4)2SO4、Na2SO4、NaCl溶液等 加热、紫外线、X射线、重金属盐、强酸、强碱、乙醇、甲醛等 胶体、半透膜、水等
特点 可逆,蛋白质仍保持原有活性 不可逆,蛋白质失去原有活性 需多次换水
实例 向蛋白质溶胶中加浓Na2SO4溶液使蛋白质析出 消毒、灭菌、给果树使用波尔多液 除去淀粉溶液(胶体)中的NaNO3杂质
应用体验
视角1蛋白质的水解反应
1.某蛋白质的结构片段如下:
(1)上述蛋白质的结构片段的水解产物中不属于α-氨基酸的结构简式
是 。
解析 根据蛋白质的水解规律,可得该蛋白质的结构片段水解生成的氨基酸如下:
(2)上述蛋白质的结构片段水解后的氨基酸中,某氨基酸的碳、氢原子数比值最大。
①该氨基酸与NaOH反应的化学方程式为
。
②两分子该氨基酸缩合形成环状物质的结构简式为 ,
分子式为 。
C16H14N2O2
解析 分子中碳、氢原子数比值最大,其分子式为C8H9NO2,两分子缩合形成环状物质时应脱去两分子H2O,根据原子个数守恒可知所得缩合物的分子式为C16H14N2O2,结构简式为
。
(3)已知上述蛋白质结构片段的相对分子质量为364,则水解生成的各种氨基酸的相对分子质量之和为 。
436
解析 该蛋白质结构片段水解生成了4种氨基酸,相应地增加了4个H2O分子的相对分子质量,即水解生成的各种氨基酸的相对分子质量之和为364+72=436。
思维点拨 (1)分子式或相对分子质量推断。两个氨基酸分子形成1个肽键,产生1分子H2O;n个氨基酸形成一条肽链时,含有(n-1)个肽键,产生(n-1)分子H2O。据此可根据形成多肽的氨基酸分子式,推断多肽的分子式或相对分子质量;也可根据多肽的分子式或相对分子质量,推断形成多肽的氨基酸分子式之和或相对分子质量之和。
(2)氨基酸数目的计算。利用氮原子守恒即一般一个氨基酸分子含有一个氮原子(氨基)来求解多肽水解后氨基酸的数目。当条件不完整时,可用讨论法;当条件完整但不能直接推导时,可用方程组法。
视角2蛋白质的盐析、变性
2.人类肝脏蛋白质的两谱三图三库已经全面破译完成,它将为肝脏疾病的预警、预防、诊断和治疗提供科学依据。下列关于肝脏蛋白质的说法不正确的是( )
A.属于生物高分子
B.水解的最终产物能与酸或碱反应
C.遇浓硝酸会变性
D.水解时碳氧键断裂
D
解析 蛋白质属于生物高分子,A正确;蛋白质水解的最终产物是氨基酸,能与酸或碱反应,B正确;蛋白质遇强酸会变性,C正确;水解时,肽键( )中的C—N键断裂,D错误。
3.下列说法不正确的是( )
A.组成天然蛋白质的氨基酸都是α-氨基酸
B.利用盐析可以分离和提纯蛋白质
C.DNA是生物体遗传信息的载体,蛋白质合成的模板
D.RNA主要存在于细胞核中,它根据DNA提供的信息控制体内蛋白质的合成
D
解析 组成天然蛋白质的氨基酸都是α-氨基酸,A说法正确;盐析可以使蛋白质因溶解度变小而析出,所以利用盐析可以分离、提纯蛋白质,B说法正确;DNA是生物体遗传信息的载体,蛋白质合成的模板,C说法正确;RNA主要存在于细胞质中,D说法错误。
本 课 结 束
