2024届高三化学一轮复习 电化学里的“魔法师”——离子交换膜 课件(共15张PPT)
文档属性
| 名称 | 2024届高三化学一轮复习 电化学里的“魔法师”——离子交换膜 课件(共15张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-09 23:49:15 | ||
图片预览




文档简介
(共15张PPT)
电化学里的“膜法师”——离子交换膜
2024届高三专题复习
2023全国甲卷 2022全国甲卷 2021全国甲卷
2023全国乙卷 2022全国乙卷 2021全国乙卷
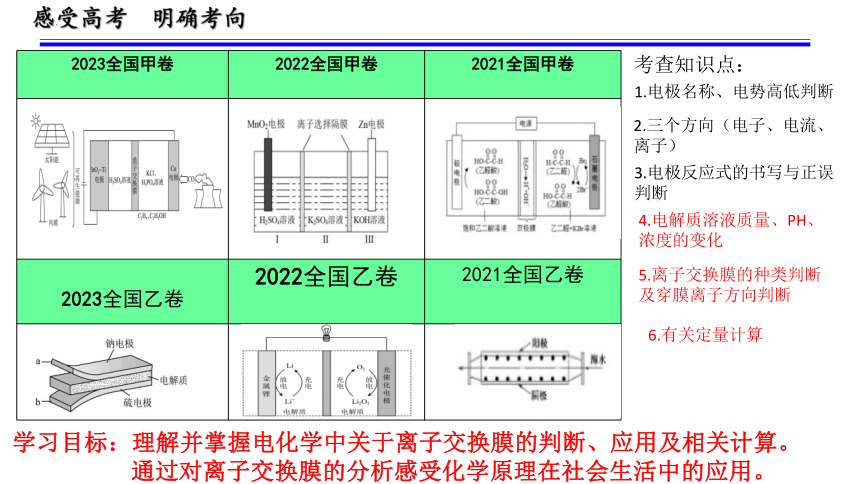
感受高考 明确考向
考查知识点:
1.电极名称、电势高低判断
3.电极反应式的书写与正误判断
2.三个方向(电子、电流、离子)
4.电解质溶液质量、PH、浓度的变化
5.离子交换膜的种类判断及穿膜离子方向判断
6.有关定量计算
学习目标:理解并掌握电化学中关于离子交换膜的判断、应用及相关计算。
通过对离子交换膜的分析感受化学原理在社会生活中的应用。
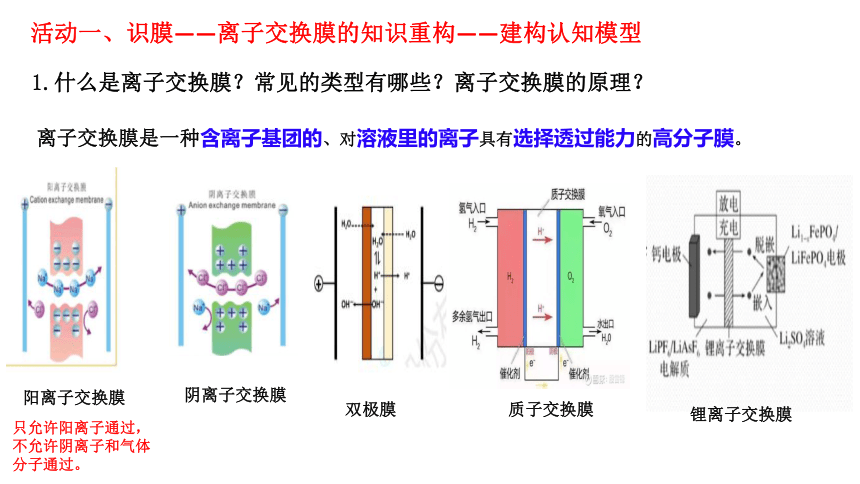
活动一、识膜——离子交换膜的知识重构——建构认知模型
1.什么是离子交换膜?常见的类型有哪些?离子交换膜的原理?
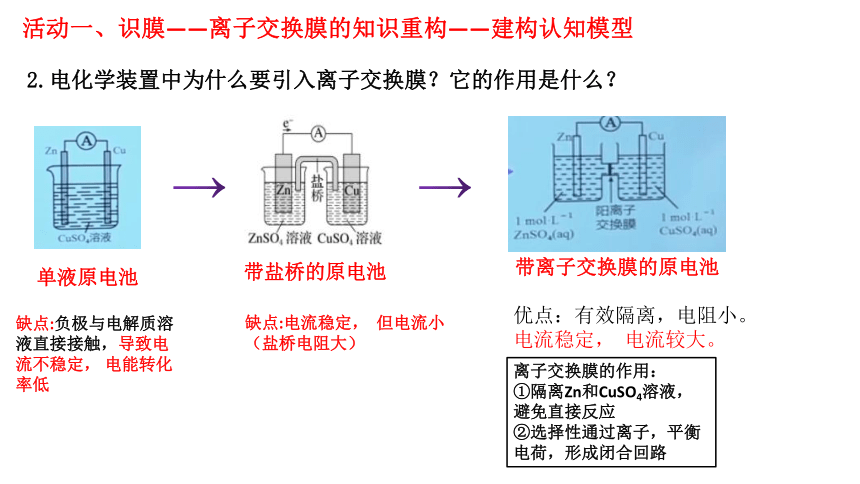
2.电化学装置中为什么要引入离子交换膜?它的作用是什么?
3.离子交换膜在教材中的原理模型
离子交换膜是一种含离子基团的、对溶液里的离子具有选择透过能力的高分子膜。
阳离子交换膜
阴离子交换膜
双极膜
活动一、识膜——离子交换膜的知识重构——建构认知模型
1.什么是离子交换膜?常见的类型有哪些?离子交换膜的原理?
质子交换膜
锂离子交换膜
只允许阳离子通过,不允许阴离子和气体分子通过。
2.电化学装置中为什么要引入离子交换膜?它的作用是什么?
缺点:负极与电解质溶液直接接触,导致电流不稳定, 电能转化率低
单液原电池
→
带盐桥的原电池
→
缺点:电流稳定, 但电流小 (盐桥电阻大)
优点:有效隔离,电阻小。
电流稳定, 电流较大。
带离子交换膜的原电池
离子交换膜的作用:
①隔离Zn和CuSO4溶液,避免直接反应
②选择性通过离子,平衡电荷,形成闭合回路
活动一、识膜——离子交换膜的知识重构——建构认知模型
[回归教材1]选修4教材P80 画出氯碱工业电解装置图
3.离子交换膜在教材中的经典原理模型
活动一、识膜——离子交换膜的知识重构——建构认知模型
写出电极反应式和总化学方程式
[回归教材1]选修4教材P80 画出氯碱工业离子交换膜电解装置图(一膜二进四出)
3.离子交换膜在教材中的经典原理模型
活动一、识膜——离子交换膜的知识重构——建构认知模型
写出电极反应式和总化学方程式
思考:根据阳极室电解质溶液浓度的变化和工作原理,再提出氯碱工业的一个化工用途?
[回归教材2] 必修2教材P90 海水淡化的方法有蒸馏法、电渗析法、离子交换法等。
已知海水中含有大量的Na+和Cl- 及少量Ca2+、Mg2+、SO42-
活动一、识膜——离子交换膜的知识重构——建构认知模型
模拟氯碱工业装置图自主设计“三室式电渗析法”海水淡化装置图,写出电极反应式
3.离子交换膜在教材中的经典原理模型
两膜三进三出
化学电源
物质制备
物质分离提纯
活动二、析膜——题型例析——建构思维模型
例1:(2018浙江高考改编)以K2CrO4为原料,利用电解法制备K2Cr2O7的实验装置如下图
(1)K2CrO4 为什么能在阳极区转化为K2Cr2O7,用离子方程式和简单的语言文字说明 。
(2)电解的总化学方程式为 。
(3)若电解前K2CrO4 1mol,通电一段时间后阳极室中K和Cr的物质的量之比为3:2,则K+通过阳离子交换膜向阴极室移动 mol,
左侧KOH溶液增重 g。
2.离子交换膜的计算注意点:
①.迁移离子所带的电荷数=外电路上转移的电子数
②溶液质量变化=电极反应引起的变化和离子迁移引起的变化之和
角度一、单膜
Ⅰ、物质制备型
1.思维建模——“隔膜”电化学装置的解题步骤:
一判池
二判极
三写电极反应
四判膜类型和穿膜离子方向
五计算
例2:我国科学家最近发明了一种Zn - PbO2电池,电解质为K2SO4、H2SO4和KOH,由a和b两离子交换膜隔开,形成I、II、III三个电解质溶液区域,结构示意图如图,回答下列问题:
(1)电池中,Zn为 极,II区域的电解质为 (填K2SO4、H2SO4或KOH)
(2)电池反应的离子方程式为 。
(3)阳离子交换膜为图中的 (填“a”或“b”)膜。
活动二、析膜——题型例析——建构思维模型
角度二、双膜
Ⅱ、新型化学电源
负
K2SO4
a
链接高考:(2022全国甲卷)一种水性电解液Zn-MnO2离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH)42-存在)。电池放电时,下列叙述错误的是
D.电池总反应:Zn+4OH-+MnO2+4H+=Zn(OH)42-+Mn2++2H2O
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO42-通过隔膜向Ⅱ区迁移
C. MnO2电极反应:MnO2+2e-+4H+=Mn2++2H2O
角度三、多膜
活动二、析膜——题型例析——建构思维模型
例3、(2023重庆模考)双极膜(BP) 是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH﹣,作为H+和OH﹣离子源。利用双极膜电渗析法电解食盐水可获得淡水、NaOH和HCl,其工作原理如图所示,M、N为离子交换膜,下列说法错误的是
A.Y电极与电源正极相连,发生的反应为4OH﹣﹣4e﹣═O2↑+2H2OB.M为阳离子交换膜,N为阴离子交换膜C.“双极膜组”电渗析法也可应用于从盐溶液(MX)制备相应的酸(HX)和碱(MOH)D.若去掉双极膜(BP),电路中每转移1mol电子,两极共得到0.5mol气体
Ⅲ、电渗析法分离提纯、物质制备
角度四、特殊膜
活动二、析膜——题型例析——建构思维模型
例4.(2023山东)在直流电源作用下,双极膜中间的H2O解离为H+和OH-,利用电解池产生强氧化性的羟基自由基.OH,,处理含苯酚废水和含SO2的烟气的工作原理如图所示。下列说法正确的是
A.M电极为阳极,反应式为:
B.含SO2的烟气被吸收的反应为
C.双极膜中间的H2O解离出的H+向N极迁移
D.每处理9.4g苯酚,理论上有2.8molH+透过膜a
课堂小结
活动三、认膜、析膜、建模——课堂小结
离子交换膜的含义、类型、原理、 作用
知识上:
解题技巧上:
2.判断交换膜种类的方法
3.穿膜离子的判断和膜两边溶液的相关计算:
1.带隔膜的电化学装置的解题步骤
离子迁移量、溶液质量变化、PH变化
电化学里的“膜法师”——离子交换膜
2024届高三专题复习
2023全国甲卷 2022全国甲卷 2021全国甲卷
2023全国乙卷 2022全国乙卷 2021全国乙卷
感受高考 明确考向
考查知识点:
1.电极名称、电势高低判断
3.电极反应式的书写与正误判断
2.三个方向(电子、电流、离子)
4.电解质溶液质量、PH、浓度的变化
5.离子交换膜的种类判断及穿膜离子方向判断
6.有关定量计算
学习目标:理解并掌握电化学中关于离子交换膜的判断、应用及相关计算。
通过对离子交换膜的分析感受化学原理在社会生活中的应用。
活动一、识膜——离子交换膜的知识重构——建构认知模型
1.什么是离子交换膜?常见的类型有哪些?离子交换膜的原理?
2.电化学装置中为什么要引入离子交换膜?它的作用是什么?
3.离子交换膜在教材中的原理模型
离子交换膜是一种含离子基团的、对溶液里的离子具有选择透过能力的高分子膜。
阳离子交换膜
阴离子交换膜
双极膜
活动一、识膜——离子交换膜的知识重构——建构认知模型
1.什么是离子交换膜?常见的类型有哪些?离子交换膜的原理?
质子交换膜
锂离子交换膜
只允许阳离子通过,不允许阴离子和气体分子通过。
2.电化学装置中为什么要引入离子交换膜?它的作用是什么?
缺点:负极与电解质溶液直接接触,导致电流不稳定, 电能转化率低
单液原电池
→
带盐桥的原电池
→
缺点:电流稳定, 但电流小 (盐桥电阻大)
优点:有效隔离,电阻小。
电流稳定, 电流较大。
带离子交换膜的原电池
离子交换膜的作用:
①隔离Zn和CuSO4溶液,避免直接反应
②选择性通过离子,平衡电荷,形成闭合回路
活动一、识膜——离子交换膜的知识重构——建构认知模型
[回归教材1]选修4教材P80 画出氯碱工业电解装置图
3.离子交换膜在教材中的经典原理模型
活动一、识膜——离子交换膜的知识重构——建构认知模型
写出电极反应式和总化学方程式
[回归教材1]选修4教材P80 画出氯碱工业离子交换膜电解装置图(一膜二进四出)
3.离子交换膜在教材中的经典原理模型
活动一、识膜——离子交换膜的知识重构——建构认知模型
写出电极反应式和总化学方程式
思考:根据阳极室电解质溶液浓度的变化和工作原理,再提出氯碱工业的一个化工用途?
[回归教材2] 必修2教材P90 海水淡化的方法有蒸馏法、电渗析法、离子交换法等。
已知海水中含有大量的Na+和Cl- 及少量Ca2+、Mg2+、SO42-
活动一、识膜——离子交换膜的知识重构——建构认知模型
模拟氯碱工业装置图自主设计“三室式电渗析法”海水淡化装置图,写出电极反应式
3.离子交换膜在教材中的经典原理模型
两膜三进三出
化学电源
物质制备
物质分离提纯
活动二、析膜——题型例析——建构思维模型
例1:(2018浙江高考改编)以K2CrO4为原料,利用电解法制备K2Cr2O7的实验装置如下图
(1)K2CrO4 为什么能在阳极区转化为K2Cr2O7,用离子方程式和简单的语言文字说明 。
(2)电解的总化学方程式为 。
(3)若电解前K2CrO4 1mol,通电一段时间后阳极室中K和Cr的物质的量之比为3:2,则K+通过阳离子交换膜向阴极室移动 mol,
左侧KOH溶液增重 g。
2.离子交换膜的计算注意点:
①.迁移离子所带的电荷数=外电路上转移的电子数
②溶液质量变化=电极反应引起的变化和离子迁移引起的变化之和
角度一、单膜
Ⅰ、物质制备型
1.思维建模——“隔膜”电化学装置的解题步骤:
一判池
二判极
三写电极反应
四判膜类型和穿膜离子方向
五计算
例2:我国科学家最近发明了一种Zn - PbO2电池,电解质为K2SO4、H2SO4和KOH,由a和b两离子交换膜隔开,形成I、II、III三个电解质溶液区域,结构示意图如图,回答下列问题:
(1)电池中,Zn为 极,II区域的电解质为 (填K2SO4、H2SO4或KOH)
(2)电池反应的离子方程式为 。
(3)阳离子交换膜为图中的 (填“a”或“b”)膜。
活动二、析膜——题型例析——建构思维模型
角度二、双膜
Ⅱ、新型化学电源
负
K2SO4
a
链接高考:(2022全国甲卷)一种水性电解液Zn-MnO2离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH)42-存在)。电池放电时,下列叙述错误的是
D.电池总反应:Zn+4OH-+MnO2+4H+=Zn(OH)42-+Mn2++2H2O
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO42-通过隔膜向Ⅱ区迁移
C. MnO2电极反应:MnO2+2e-+4H+=Mn2++2H2O
角度三、多膜
活动二、析膜——题型例析——建构思维模型
例3、(2023重庆模考)双极膜(BP) 是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH﹣,作为H+和OH﹣离子源。利用双极膜电渗析法电解食盐水可获得淡水、NaOH和HCl,其工作原理如图所示,M、N为离子交换膜,下列说法错误的是
A.Y电极与电源正极相连,发生的反应为4OH﹣﹣4e﹣═O2↑+2H2OB.M为阳离子交换膜,N为阴离子交换膜C.“双极膜组”电渗析法也可应用于从盐溶液(MX)制备相应的酸(HX)和碱(MOH)D.若去掉双极膜(BP),电路中每转移1mol电子,两极共得到0.5mol气体
Ⅲ、电渗析法分离提纯、物质制备
角度四、特殊膜
活动二、析膜——题型例析——建构思维模型
例4.(2023山东)在直流电源作用下,双极膜中间的H2O解离为H+和OH-,利用电解池产生强氧化性的羟基自由基.OH,,处理含苯酚废水和含SO2的烟气的工作原理如图所示。下列说法正确的是
A.M电极为阳极,反应式为:
B.含SO2的烟气被吸收的反应为
C.双极膜中间的H2O解离出的H+向N极迁移
D.每处理9.4g苯酚,理论上有2.8molH+透过膜a
课堂小结
活动三、认膜、析膜、建模——课堂小结
离子交换膜的含义、类型、原理、 作用
知识上:
解题技巧上:
2.判断交换膜种类的方法
3.穿膜离子的判断和膜两边溶液的相关计算:
1.带隔膜的电化学装置的解题步骤
离子迁移量、溶液质量变化、PH变化
同课章节目录
