第4章 认识化学变化 复习课件(共45张PPT)-2023-2024学年九年级化学上册同步精品课堂(沪教版)
文档属性
| 名称 | 第4章 认识化学变化 复习课件(共45张PPT)-2023-2024学年九年级化学上册同步精品课堂(沪教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-11 00:00:00 | ||
图片预览











文档简介
(共45张PPT)
复习
第4章 认识化学变化
目录
CONTENTS
一
二
常见的化学反应——燃烧
化学反应中的质量关系
三
五
化学方程式的书写与应用
知 识 网 络
认识化
学变化
常见的化学反应——燃烧
燃烧的条件
灭火的原理
促进燃烧的方法
化学反应中的质量关系
化学方程式的书写与应用
定义
书写
简单计算
新课讲解
知识点:
◎认识燃烧发生的条件;
◎燃烧探究的探究;
◎了解防火灭火的措施。
◎认识燃料完全燃烧的重要性;
◎易燃易爆安全常识。
新课讲解
常见的化学反应——燃烧
1. 燃烧
定义 一种________、________的剧烈的________反应 燃烧的条件 a.具有________;b.与________接触; c.达到燃烧所需要的____________(即可燃物的________) 三者缺
一不可
特别提醒:a.有发光、发热现象的不一定是燃烧,如灯泡发光; b.并不是所有的燃烧都有氧气参加,如镁在氮气中燃烧、氢气在氯气中燃烧; c.燃烧既可以造福人类,如提供热量;也可能带来灾难,如引起火灾 发光
发热
化学
可燃性
氧气
最低温度
着火点
新课讲解
燃 烧
完全燃烧与不完全燃烧
完全燃烧 不完全燃烧
条件 _____充足 _____不充足
特点 燃烧速率______, 放出的热量____ 燃烧速率______,放出的热量______
氧气
氧气
快
多
慢
少
新课讲解
燃 烧
原理 破坏______的条件之一即可 常见灭火原理及方法 隔绝氧气 熄灭酒精灯—— ;
油锅着火—— ;
1.清除可燃物;2._________ 3.________ 液化气着火——先关闭液化气阀门,再灭火;
森林着火——将火灾周围的树木砍伐,形成________
木材、衣物着火——喷水;
建筑物着火——用高压水枪灭火
燃烧
用灯帽盖灭
用锅盖盖灭
隔离带
降低温度至着
火点以下
2. 灭火
新课讲解
灭 火
a. 着火点是物质固有的属性, 一般不随外界条件的改变而改变;
b. 在描述灭火原理时不能把“降低温度至可燃物着火点以下”,描述成“降低可燃物的着火点”
新课讲解
特别提醒:
灭 火
3.燃烧条件的探究
1. 探究方法:控制变量法
2. 实验方案的设计
实验装置 现象 实验结论
小石块不燃烧, 小木块燃烧 燃烧需要_________
可燃物
新课讲解
燃烧探究的探究
实验装置 现象 实验结论
薄铜片上的白磷燃烧,薄铜片上红磷不燃烧 燃烧需要温度达到可燃物的_______
薄铜片上的白磷燃烧,热水中的白磷不燃烧 燃烧需要可燃物与______接触
3. 实验结论:物质燃烧的三个条件为 、 、________________。
着火点
氧气
可燃物
与氧气接触
温度达到着火点
新课讲解
灭 火
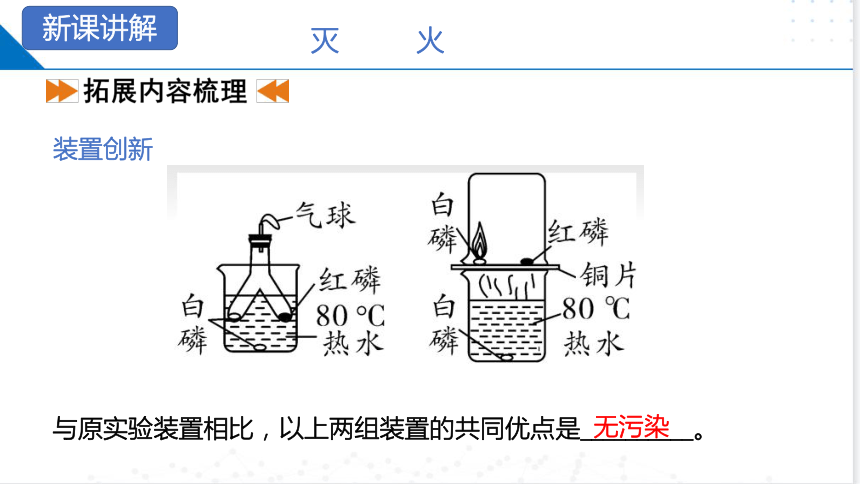
装置创新
与原实验装置相比,以上两组装置的共同优点是__________。
无污染
新课讲解
灭 火
爆炸 可燃物在____________内急剧地燃烧,就会在短时间内聚积__________,使气体的体积_________而引起爆炸
日常生活中的安全常识 a.家用天然气、煤气或液化石油气等泄漏,切不可打开排气扇,应迅速关闭阀门并开窗通风;
b.启用闲置的沼气池前,切不可进行灯火试验;
c.加油站、面粉加工厂和煤矿的矿井内,应通风透气,严禁烟火,同时备有消防器材,要有明显的安全标志;(2019.5B)
d.室内着火,不能立即开窗通风;
有限的空间
大量的热
迅速膨胀
新课讲解
爆 炸
4.爆炸
日常生 活中的 安全常识 e.使用燃煤的炉子取暖时,一定要注意通风,防止煤气(CO)中毒;
f.在生产、运输、使用和储存易燃易爆物时,绝对禁止违章操作(2020.1)
遭遇火灾的自救方法 a.如果火势很小,根据起火原因,可以用适当的灭火器材和方法灭火;如果火势较大,有蔓延的可能,应沿疏散通道,迅速离开现场,并立即拨打火警电话________求救;
b.当被困在火灾区时,应视具体情况,采取相应的措施自救,如:用湿毛巾或口罩捂住口鼻,低下身子沿墙壁或贴近地面跑出火灾区等;
c.山林着火,应向______(填“顺风”或“逆风”)方向跑离火灾区
119
逆风
新课讲解
爆 炸
几种消防安全标志
禁止带火种
禁止烟火
禁止放鞭炮
禁止吸烟
当心火灾
当心爆炸
新课讲解
爆 炸
◎认识质量守恒定律,能说明化学反应中的质量关系。
◎形成“化学变化过程中元素不变”的观念。
◎初步形成“在一定条件下物质可以转化”的观点。
新课讲解
化学反应中的质量关系
知识点:
内容 参加化学反应的各物质的_________等于反应后生
成的各物质的_________
理解 a.前提:一切化学反应;
b.核心:质量守恒。质量守恒定律是指“质量”守恒,
不包括其他方面的守恒,如体积、密度、分子数等;
c.条件:参加反应。没有参加反应的物质的质量和非反应
生成的物质质量______(填“能”或“不能”)计入“总和”中,如杂质;
d.质量总和:“总和”要把各种状态的反应物和生成物都计算在内,如气体或沉淀也应考虑
质量总和
质量总和
不能
新课讲解
质量守恒定律
实质 参加反应的各物质(反应物)的原子重新组合生成新物质(生成物)的过程 宏观与微观解释 六个“不变” 宏观 反应物、生成物的总质量不变
________种类不变
元素质量不变
微观 原子种类不变
原子________不变
原子________不变
两个“一定改变” 宏观 物质的______一定改变
微观 分子的种类一定改变
两个“可能改变” 分子的数目可能改变;元素的化合价可能改变 元素
数目
质量
种类
新课讲解
质量守恒定律
5.质量守恒定律的验证
药品选择 质量守恒定律只适用于化学变化,所以选择的药品必须能发生化学反应且反应现象明显
装置选择 如果所选的化学反应中有气体参加或生成,则反应必须在密闭容器中进行
新课讲解
质量守恒定律
方案设计
实验原理 实验A: (用化学方程式表示);
实验B: 。
实验现象 实验A:___________________________________________
实验B:___________________________________________
实验结论 参加反应的各物质的质量总和等于反应后生成的各物质的质量总和
2NaOH+CuSO4===Cu(OH)2↓+Na2SO4
CaCO3+2HCl=== CaCl2+H2O+CO2↑
锥形瓶中生成蓝色沉淀,指针指向正中间
锥形瓶内有气泡生成,指针指向正中间
新课讲解
质量守恒定律
装置创新
教材中碳酸钙与稀盐酸反应生成气体后,锥形瓶内压强________(填“增大”或“减少”),容易冲开瓶塞,可进行如图改进:装置中气球的作用是________________________________________________。
增大
防止气体逸散和防止容器中压强太大,冲开橡胶塞
新课讲解
质量守恒定律
◎能正确书写简单的化学方程式;
◎初步认识常见的化合反应、分解反应、置换反应和
复分解反应,能用于解释日常生活中的一些化学象;
◎能根据化学方程式进行计算。
◎认识定量研究对于化学科学发展的重大作用。
新课讲解
化学方程式的书写与应用
知识点:
6. 化学方程式的意义及书写
定义 用________来表示__________的式子叫化学方程式 意义 质的方面 表明化学反应的反应物、生成物和反应条件
量的方面 ①微观上:反应物和生成物各物质之间微粒数之比;
②宏观上:反应物和生成物各物质的质量比
书写原则 以客观事实为依据,遵循__________定律 化学式
化学反应
质量守恒
新课讲解
化学方程式的书写与应用
化学方程式的书写 以P与O2反应为例
化学式
配平
条件
等号
状态
新课讲解
化学方程式的书写与应用
a.“↑”的标注:当反应物中没有气体时,生成物中的气体标“↑”;
当反应物中有气体时,生成物中的气体不标“↑”;
b.“↓”的标注:当反应物中没有固体时,生成物中的固体(或沉淀)标“↓”;
当反应物中有固体时,生成物中的固体(或沉淀)不标“↓”
新课讲解
化学方程式的书写与应用
特别提醒:
7. 配平化学方程式的方法
(1)定1法(适用于化合反应、分解反应及有机物的燃烧)
步骤 举例(磷燃烧)
找出组成最复杂物质的化学式 P+O2 P2O5
令找出化学式的系数为1 P+O2 1P2O5
配平其他物质的化学式,“——”变“==” 2P+ O2 1P2O5
通分,将分数化整 4P+5O2 2P2O5
新课讲解
化学方程式的书写与应用
(2)最小公倍数法
步骤 举例(氢气还原氧化铁)
第1步:找出短线两边各出现一次且原子个数变化较大的元素 H2+Fe2O3 Fe+H2O(________元素)
第2步:求出该元素原子个数的最小公倍数 H2+Fe2O3 Fe+H2O(________原子的最小公倍数为______)
第3步:在该元素所在化学式前配上化学计量数 H2+____Fe2O3 Fe+______H2O
第4步:根据质量守恒定律,配平其余各元素的原子数目,“——”变“===” __________________________________
O(或氧)
O(或氧)
3
1
3
3H2+Fe2O3 2Fe+3H2O
新课讲解
化学方程式的书写与应用
8. 基本反应类型
反应类型 概念 表达式 特征
__________ 由两种或两种以上物质生成另一种物质的反应 A+B+……→C 多变一
__________ 由一种反应物生成两种或两种以上其他物质的反应 C→A+B+…… 一变多
__________ 由一种单质与一种化合物反应生成另一种单质和另一种化合物的反应 A+BC→AC+B 单换单
___________ 由两种化合物互相交换成分,生成另外两种化合物的反应 AB+CD→AD+CB 双交换,价不变
化合反应
分解反应
置换反应
复分解反应
新课讲解
化学方程式的书写与应用
依据 __________定律,即各物质间有确定的质量比 计算步骤 以求6.8 g H2O2分解可以得到氧气的质量为例 设:根据题意设未知数 解:设6.8 g H2O2分解可以得到O2的质量为x
写:正确书写化学方程式 2H2O2 2H2O+O2↑
找:找出已知量、未知量的关系 68 32
6.8 g x
列:列出比例式
求:求出未知数 x=3.2 g
答:简明地写出答案 答:6.8 g H2O2分解可以得到氧气的质量为3.2 g。
质量守恒
化学方程式的书写与应用
新课讲解
典例精讲
例1. (2023年山东省滨州市中考)下列关于燃烧与灭火的说法不正确的是( )
A.森林失火时,可将大火蔓延路线前一片树木砍掉,形成隔离带
B.煤炉生火时,利用木材引燃煤炭,是为了降低煤炭的着火点
C.燃着的酒精灯不慎碰倒,若洒出的酒精燃烧起来,应立刻用湿抹布扑灭
D.木柴架空有利于促进燃烧,是因为增大了木柴与氧气的接触面积
【答案】B
典例精讲
例2.(2023年湖北省荆州市中考)作为中学生应该具备应对火灾的安全知识。下列说法错误的是
A. 遇到室内起火,迅速打开门窗通风
B. 遭遇火灾时,可用湿毛巾捂住口鼻跑离着火区域
C. 扑灭电器失火不可用水基型灭火器
D. 扑灭森林火灾时,可砍伐出隔离带,将树木与燃烧区隔离
【答案】A
例3. (2023年江苏省苏州市中考)安全离不开化学知识。下列有关做法不符合安全要求的是( )
A.油锅着火后立即用锅盖盖灭
B.向燃着的酒精炉中直接添加酒精
C.面粉加工厂等场所严禁烟火
D.煤气泄漏立即关闭阀门并开窗通风
【答案】B
典例精讲
4. (2023年山东省枣庄市中考)学习科学知识,树立安全意识。下列做法不符合安全要求的是( )
A.油锅着火,迅速用水浇灭
B.室内发生火灾时,可用湿毛巾捂住口鼻,尽量贴近地面逃离
C.加油站、面粉加工厂严禁烟火
D.电线着火,先断电再灭火
【答案】A
典例精讲
例5.(2023年重庆市中考A卷)有关重庆缙云山山火扑救事件的说法错误的是( )
A.湿毛巾捂口鼻可减少浓烟的吸入
B.挖掘隔离带是为了清除可燃物
C.直升机洒水降低了可燃物的着火点
D.CO2灭火利用其密度大于空气,不助燃不可燃
【答案】C
典例精讲
例6.(2023年山东省滨州市中考)密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是( )
A.物质甲是生成物
B.反应后乙物质的质量分数是18%
C.该化学反应中甲、乙两物质的质量比是14:3
D.物质丁一定是该反应的催化剂
典例精讲
【答案】C
例7.(2023年湖南省怀化市中考)一定条件下,下列物质在密闭容器内反应一段时间,测得反应前后各物质的质量关系如下表:
【答案】B
典例精讲
根据上表信息判断,下列说法中不正确的是( )
A.a=10 B.该反应属于置换反应
C.Z为化合物 D.反应中Y、W两种物质发生改变的质量比为22:9
物质 X Y Z W
反应前质量/g 5 2.2 16.2 0.9
反应后质量/g a 4.4 8.1 1.8
例8.(2023·黑龙江绥化·中考真题)在化学反应A+2B=C+2D中:已知C和D的相对分子质量之比是22:9,当6.4gB与足量A完全反应后,生成3.6gD。则在此反应中,B和C的质量比是( )
A.8:11 B.2:11
C.16:11 D.16:9
【答案】C
典例精讲
典例精讲
例9. (2023·广东·中考真题)梦天舱燃烧科学柜采用a作燃料成功实施首次在轨点火实验。a完全燃烧的反应微观示意图如图所示。下列说法错误的是( )
A.反应前后元素种类不变
B.反应前后分子个数不变
C.a分子中C、H原子个数比为1:4
D.反应生成c、d的质量比为 22:9
【答案】D
典例精讲
例10 .(2023·湖北武汉·中考真题)以CO2和H2为原料合成C2H4是综合利用二氧化碳、实现“碳中和”的研究热点。相关反应的微观示意图如下所示。
关于该反应,下列说法正滩的是( )
A.参加反成的甲和乙的质量比为11:1
B.生成丙和丁的分子个数比为1:2
C.反应物和生成物共涉及两种氧化物
D.反应前后元素的化合价都不变
【答案】C
例11.(2023云南昆明一模)自来水厂净化水的过程为:取水→沉降→过滤→吸附→消毒,高铁酸钾(K2FeO4)能用作絮凝剂。制备K2FeO4的化学方程式为:2Fe(OH)3+3Cl2+10KOH 2K2FeO4+6X+8H2O,则X的化学式为________。
KCl
典例精讲
例12. (2023陕西咸阳二模)关于以下三个反应的相关说法正确的是( )
① CaCO3 CaO+CO2↑
② 2NaHCO3 Na2CO3+H2O+CO2↑
③ NH4HCO3 NH3↑+H2O+CO2↑
A. 三种反应物均可在食品加工中用作膨松剂
B. 用加热的方法无法区分NaHCO3和NH4HCO3
C. 充分加热等质量的三种反应物生成CO2的质量相等
D. 三个反应均属于分解反应
【答案】D
典例精讲
典例精讲
例13. (2023·新疆·中考真题)《天工开物》中有“煤饼烧石成灰”的记载,“烧石成灰”发生的反应为: 。请根据此化学方程式计算,实验室中10g碳酸钙充分反应后。可制得氧化钙的质量是多少?
答案:5.6g
例14.(2023·山西·中考真题)“侯氏制碱法”是我国著名制碱专家侯德榜经过多年研究做出的杰出贡献,其最大的优点是降低了成本,大大提高了NaCl的利用率。
(1)“侯氏制碱法”的原理可表示为: ,X的化学式是_______,X中一种元素的质量分数为__________(精确到0.1%)。
(2)用58.5tNaCl(其利用率在96%以上)制碱,至少能生成Na2CO3的质量是多少?
【答案】(1)NH3 ; 氮元素的质量分数为82.4%或氢元素的质量分数为17.6%;(2)101.76t
典例精讲
例15.有资料表明,氧化铜对氯酸钾(KClO3)的分解有催化作用,现将2.4 g CuO与W g氯酸钾的混合物充分加热,使其不再产生气体后,残留固体经冷却、称量质量为W g。
(1)写出该反应的化学方程式;
(2)求生成O2的质量;
(3)求W的值。
典例精讲
【答案】(1)2KClO3 2KCl + 3O2↑
(2)2.4g;(3)6.125。
CuO
△
====
1.完成配套练习册;
2.完成单元检测卷 。
典例精讲
复习
第4章 认识化学变化
目录
CONTENTS
一
二
常见的化学反应——燃烧
化学反应中的质量关系
三
五
化学方程式的书写与应用
知 识 网 络
认识化
学变化
常见的化学反应——燃烧
燃烧的条件
灭火的原理
促进燃烧的方法
化学反应中的质量关系
化学方程式的书写与应用
定义
书写
简单计算
新课讲解
知识点:
◎认识燃烧发生的条件;
◎燃烧探究的探究;
◎了解防火灭火的措施。
◎认识燃料完全燃烧的重要性;
◎易燃易爆安全常识。
新课讲解
常见的化学反应——燃烧
1. 燃烧
定义 一种________、________的剧烈的________反应 燃烧的条件 a.具有________;b.与________接触; c.达到燃烧所需要的____________(即可燃物的________) 三者缺
一不可
特别提醒:a.有发光、发热现象的不一定是燃烧,如灯泡发光; b.并不是所有的燃烧都有氧气参加,如镁在氮气中燃烧、氢气在氯气中燃烧; c.燃烧既可以造福人类,如提供热量;也可能带来灾难,如引起火灾 发光
发热
化学
可燃性
氧气
最低温度
着火点
新课讲解
燃 烧
完全燃烧与不完全燃烧
完全燃烧 不完全燃烧
条件 _____充足 _____不充足
特点 燃烧速率______, 放出的热量____ 燃烧速率______,放出的热量______
氧气
氧气
快
多
慢
少
新课讲解
燃 烧
原理 破坏______的条件之一即可 常见灭火原理及方法 隔绝氧气 熄灭酒精灯—— ;
油锅着火—— ;
1.清除可燃物;2._________ 3.________ 液化气着火——先关闭液化气阀门,再灭火;
森林着火——将火灾周围的树木砍伐,形成________
木材、衣物着火——喷水;
建筑物着火——用高压水枪灭火
燃烧
用灯帽盖灭
用锅盖盖灭
隔离带
降低温度至着
火点以下
2. 灭火
新课讲解
灭 火
a. 着火点是物质固有的属性, 一般不随外界条件的改变而改变;
b. 在描述灭火原理时不能把“降低温度至可燃物着火点以下”,描述成“降低可燃物的着火点”
新课讲解
特别提醒:
灭 火
3.燃烧条件的探究
1. 探究方法:控制变量法
2. 实验方案的设计
实验装置 现象 实验结论
小石块不燃烧, 小木块燃烧 燃烧需要_________
可燃物
新课讲解
燃烧探究的探究
实验装置 现象 实验结论
薄铜片上的白磷燃烧,薄铜片上红磷不燃烧 燃烧需要温度达到可燃物的_______
薄铜片上的白磷燃烧,热水中的白磷不燃烧 燃烧需要可燃物与______接触
3. 实验结论:物质燃烧的三个条件为 、 、________________。
着火点
氧气
可燃物
与氧气接触
温度达到着火点
新课讲解
灭 火
装置创新
与原实验装置相比,以上两组装置的共同优点是__________。
无污染
新课讲解
灭 火
爆炸 可燃物在____________内急剧地燃烧,就会在短时间内聚积__________,使气体的体积_________而引起爆炸
日常生活中的安全常识 a.家用天然气、煤气或液化石油气等泄漏,切不可打开排气扇,应迅速关闭阀门并开窗通风;
b.启用闲置的沼气池前,切不可进行灯火试验;
c.加油站、面粉加工厂和煤矿的矿井内,应通风透气,严禁烟火,同时备有消防器材,要有明显的安全标志;(2019.5B)
d.室内着火,不能立即开窗通风;
有限的空间
大量的热
迅速膨胀
新课讲解
爆 炸
4.爆炸
日常生 活中的 安全常识 e.使用燃煤的炉子取暖时,一定要注意通风,防止煤气(CO)中毒;
f.在生产、运输、使用和储存易燃易爆物时,绝对禁止违章操作(2020.1)
遭遇火灾的自救方法 a.如果火势很小,根据起火原因,可以用适当的灭火器材和方法灭火;如果火势较大,有蔓延的可能,应沿疏散通道,迅速离开现场,并立即拨打火警电话________求救;
b.当被困在火灾区时,应视具体情况,采取相应的措施自救,如:用湿毛巾或口罩捂住口鼻,低下身子沿墙壁或贴近地面跑出火灾区等;
c.山林着火,应向______(填“顺风”或“逆风”)方向跑离火灾区
119
逆风
新课讲解
爆 炸
几种消防安全标志
禁止带火种
禁止烟火
禁止放鞭炮
禁止吸烟
当心火灾
当心爆炸
新课讲解
爆 炸
◎认识质量守恒定律,能说明化学反应中的质量关系。
◎形成“化学变化过程中元素不变”的观念。
◎初步形成“在一定条件下物质可以转化”的观点。
新课讲解
化学反应中的质量关系
知识点:
内容 参加化学反应的各物质的_________等于反应后生
成的各物质的_________
理解 a.前提:一切化学反应;
b.核心:质量守恒。质量守恒定律是指“质量”守恒,
不包括其他方面的守恒,如体积、密度、分子数等;
c.条件:参加反应。没有参加反应的物质的质量和非反应
生成的物质质量______(填“能”或“不能”)计入“总和”中,如杂质;
d.质量总和:“总和”要把各种状态的反应物和生成物都计算在内,如气体或沉淀也应考虑
质量总和
质量总和
不能
新课讲解
质量守恒定律
实质 参加反应的各物质(反应物)的原子重新组合生成新物质(生成物)的过程 宏观与微观解释 六个“不变” 宏观 反应物、生成物的总质量不变
________种类不变
元素质量不变
微观 原子种类不变
原子________不变
原子________不变
两个“一定改变” 宏观 物质的______一定改变
微观 分子的种类一定改变
两个“可能改变” 分子的数目可能改变;元素的化合价可能改变 元素
数目
质量
种类
新课讲解
质量守恒定律
5.质量守恒定律的验证
药品选择 质量守恒定律只适用于化学变化,所以选择的药品必须能发生化学反应且反应现象明显
装置选择 如果所选的化学反应中有气体参加或生成,则反应必须在密闭容器中进行
新课讲解
质量守恒定律
方案设计
实验原理 实验A: (用化学方程式表示);
实验B: 。
实验现象 实验A:___________________________________________
实验B:___________________________________________
实验结论 参加反应的各物质的质量总和等于反应后生成的各物质的质量总和
2NaOH+CuSO4===Cu(OH)2↓+Na2SO4
CaCO3+2HCl=== CaCl2+H2O+CO2↑
锥形瓶中生成蓝色沉淀,指针指向正中间
锥形瓶内有气泡生成,指针指向正中间
新课讲解
质量守恒定律
装置创新
教材中碳酸钙与稀盐酸反应生成气体后,锥形瓶内压强________(填“增大”或“减少”),容易冲开瓶塞,可进行如图改进:装置中气球的作用是________________________________________________。
增大
防止气体逸散和防止容器中压强太大,冲开橡胶塞
新课讲解
质量守恒定律
◎能正确书写简单的化学方程式;
◎初步认识常见的化合反应、分解反应、置换反应和
复分解反应,能用于解释日常生活中的一些化学象;
◎能根据化学方程式进行计算。
◎认识定量研究对于化学科学发展的重大作用。
新课讲解
化学方程式的书写与应用
知识点:
6. 化学方程式的意义及书写
定义 用________来表示__________的式子叫化学方程式 意义 质的方面 表明化学反应的反应物、生成物和反应条件
量的方面 ①微观上:反应物和生成物各物质之间微粒数之比;
②宏观上:反应物和生成物各物质的质量比
书写原则 以客观事实为依据,遵循__________定律 化学式
化学反应
质量守恒
新课讲解
化学方程式的书写与应用
化学方程式的书写 以P与O2反应为例
化学式
配平
条件
等号
状态
新课讲解
化学方程式的书写与应用
a.“↑”的标注:当反应物中没有气体时,生成物中的气体标“↑”;
当反应物中有气体时,生成物中的气体不标“↑”;
b.“↓”的标注:当反应物中没有固体时,生成物中的固体(或沉淀)标“↓”;
当反应物中有固体时,生成物中的固体(或沉淀)不标“↓”
新课讲解
化学方程式的书写与应用
特别提醒:
7. 配平化学方程式的方法
(1)定1法(适用于化合反应、分解反应及有机物的燃烧)
步骤 举例(磷燃烧)
找出组成最复杂物质的化学式 P+O2 P2O5
令找出化学式的系数为1 P+O2 1P2O5
配平其他物质的化学式,“——”变“==” 2P+ O2 1P2O5
通分,将分数化整 4P+5O2 2P2O5
新课讲解
化学方程式的书写与应用
(2)最小公倍数法
步骤 举例(氢气还原氧化铁)
第1步:找出短线两边各出现一次且原子个数变化较大的元素 H2+Fe2O3 Fe+H2O(________元素)
第2步:求出该元素原子个数的最小公倍数 H2+Fe2O3 Fe+H2O(________原子的最小公倍数为______)
第3步:在该元素所在化学式前配上化学计量数 H2+____Fe2O3 Fe+______H2O
第4步:根据质量守恒定律,配平其余各元素的原子数目,“——”变“===” __________________________________
O(或氧)
O(或氧)
3
1
3
3H2+Fe2O3 2Fe+3H2O
新课讲解
化学方程式的书写与应用
8. 基本反应类型
反应类型 概念 表达式 特征
__________ 由两种或两种以上物质生成另一种物质的反应 A+B+……→C 多变一
__________ 由一种反应物生成两种或两种以上其他物质的反应 C→A+B+…… 一变多
__________ 由一种单质与一种化合物反应生成另一种单质和另一种化合物的反应 A+BC→AC+B 单换单
___________ 由两种化合物互相交换成分,生成另外两种化合物的反应 AB+CD→AD+CB 双交换,价不变
化合反应
分解反应
置换反应
复分解反应
新课讲解
化学方程式的书写与应用
依据 __________定律,即各物质间有确定的质量比 计算步骤 以求6.8 g H2O2分解可以得到氧气的质量为例 设:根据题意设未知数 解:设6.8 g H2O2分解可以得到O2的质量为x
写:正确书写化学方程式 2H2O2 2H2O+O2↑
找:找出已知量、未知量的关系 68 32
6.8 g x
列:列出比例式
求:求出未知数 x=3.2 g
答:简明地写出答案 答:6.8 g H2O2分解可以得到氧气的质量为3.2 g。
质量守恒
化学方程式的书写与应用
新课讲解
典例精讲
例1. (2023年山东省滨州市中考)下列关于燃烧与灭火的说法不正确的是( )
A.森林失火时,可将大火蔓延路线前一片树木砍掉,形成隔离带
B.煤炉生火时,利用木材引燃煤炭,是为了降低煤炭的着火点
C.燃着的酒精灯不慎碰倒,若洒出的酒精燃烧起来,应立刻用湿抹布扑灭
D.木柴架空有利于促进燃烧,是因为增大了木柴与氧气的接触面积
【答案】B
典例精讲
例2.(2023年湖北省荆州市中考)作为中学生应该具备应对火灾的安全知识。下列说法错误的是
A. 遇到室内起火,迅速打开门窗通风
B. 遭遇火灾时,可用湿毛巾捂住口鼻跑离着火区域
C. 扑灭电器失火不可用水基型灭火器
D. 扑灭森林火灾时,可砍伐出隔离带,将树木与燃烧区隔离
【答案】A
例3. (2023年江苏省苏州市中考)安全离不开化学知识。下列有关做法不符合安全要求的是( )
A.油锅着火后立即用锅盖盖灭
B.向燃着的酒精炉中直接添加酒精
C.面粉加工厂等场所严禁烟火
D.煤气泄漏立即关闭阀门并开窗通风
【答案】B
典例精讲
4. (2023年山东省枣庄市中考)学习科学知识,树立安全意识。下列做法不符合安全要求的是( )
A.油锅着火,迅速用水浇灭
B.室内发生火灾时,可用湿毛巾捂住口鼻,尽量贴近地面逃离
C.加油站、面粉加工厂严禁烟火
D.电线着火,先断电再灭火
【答案】A
典例精讲
例5.(2023年重庆市中考A卷)有关重庆缙云山山火扑救事件的说法错误的是( )
A.湿毛巾捂口鼻可减少浓烟的吸入
B.挖掘隔离带是为了清除可燃物
C.直升机洒水降低了可燃物的着火点
D.CO2灭火利用其密度大于空气,不助燃不可燃
【答案】C
典例精讲
例6.(2023年山东省滨州市中考)密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是( )
A.物质甲是生成物
B.反应后乙物质的质量分数是18%
C.该化学反应中甲、乙两物质的质量比是14:3
D.物质丁一定是该反应的催化剂
典例精讲
【答案】C
例7.(2023年湖南省怀化市中考)一定条件下,下列物质在密闭容器内反应一段时间,测得反应前后各物质的质量关系如下表:
【答案】B
典例精讲
根据上表信息判断,下列说法中不正确的是( )
A.a=10 B.该反应属于置换反应
C.Z为化合物 D.反应中Y、W两种物质发生改变的质量比为22:9
物质 X Y Z W
反应前质量/g 5 2.2 16.2 0.9
反应后质量/g a 4.4 8.1 1.8
例8.(2023·黑龙江绥化·中考真题)在化学反应A+2B=C+2D中:已知C和D的相对分子质量之比是22:9,当6.4gB与足量A完全反应后,生成3.6gD。则在此反应中,B和C的质量比是( )
A.8:11 B.2:11
C.16:11 D.16:9
【答案】C
典例精讲
典例精讲
例9. (2023·广东·中考真题)梦天舱燃烧科学柜采用a作燃料成功实施首次在轨点火实验。a完全燃烧的反应微观示意图如图所示。下列说法错误的是( )
A.反应前后元素种类不变
B.反应前后分子个数不变
C.a分子中C、H原子个数比为1:4
D.反应生成c、d的质量比为 22:9
【答案】D
典例精讲
例10 .(2023·湖北武汉·中考真题)以CO2和H2为原料合成C2H4是综合利用二氧化碳、实现“碳中和”的研究热点。相关反应的微观示意图如下所示。
关于该反应,下列说法正滩的是( )
A.参加反成的甲和乙的质量比为11:1
B.生成丙和丁的分子个数比为1:2
C.反应物和生成物共涉及两种氧化物
D.反应前后元素的化合价都不变
【答案】C
例11.(2023云南昆明一模)自来水厂净化水的过程为:取水→沉降→过滤→吸附→消毒,高铁酸钾(K2FeO4)能用作絮凝剂。制备K2FeO4的化学方程式为:2Fe(OH)3+3Cl2+10KOH 2K2FeO4+6X+8H2O,则X的化学式为________。
KCl
典例精讲
例12. (2023陕西咸阳二模)关于以下三个反应的相关说法正确的是( )
① CaCO3 CaO+CO2↑
② 2NaHCO3 Na2CO3+H2O+CO2↑
③ NH4HCO3 NH3↑+H2O+CO2↑
A. 三种反应物均可在食品加工中用作膨松剂
B. 用加热的方法无法区分NaHCO3和NH4HCO3
C. 充分加热等质量的三种反应物生成CO2的质量相等
D. 三个反应均属于分解反应
【答案】D
典例精讲
典例精讲
例13. (2023·新疆·中考真题)《天工开物》中有“煤饼烧石成灰”的记载,“烧石成灰”发生的反应为: 。请根据此化学方程式计算,实验室中10g碳酸钙充分反应后。可制得氧化钙的质量是多少?
答案:5.6g
例14.(2023·山西·中考真题)“侯氏制碱法”是我国著名制碱专家侯德榜经过多年研究做出的杰出贡献,其最大的优点是降低了成本,大大提高了NaCl的利用率。
(1)“侯氏制碱法”的原理可表示为: ,X的化学式是_______,X中一种元素的质量分数为__________(精确到0.1%)。
(2)用58.5tNaCl(其利用率在96%以上)制碱,至少能生成Na2CO3的质量是多少?
【答案】(1)NH3 ; 氮元素的质量分数为82.4%或氢元素的质量分数为17.6%;(2)101.76t
典例精讲
例15.有资料表明,氧化铜对氯酸钾(KClO3)的分解有催化作用,现将2.4 g CuO与W g氯酸钾的混合物充分加热,使其不再产生气体后,残留固体经冷却、称量质量为W g。
(1)写出该反应的化学方程式;
(2)求生成O2的质量;
(3)求W的值。
典例精讲
【答案】(1)2KClO3 2KCl + 3O2↑
(2)2.4g;(3)6.125。
CuO
△
====
1.完成配套练习册;
2.完成单元检测卷 。
典例精讲
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
