【核心素养】2.3.1 物质的量的单位——摩尔课件(共41页)2023-2024学年高一化学人教版必修1
文档属性
| 名称 | 【核心素养】2.3.1 物质的量的单位——摩尔课件(共41页)2023-2024学年高一化学人教版必修1 |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-10 00:00:00 | ||
图片预览









文档简介
(共41张PPT)
第二章
第三节 第1课时 物质的量的单位——摩尔
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
学以致用·随堂检测全达标
素养 目标 1.通过对比、类比、归纳、演绎等多种思维方法,了解物质的量、摩尔质量的含义,体会从物质的量层次定量研究化学问题的意义,发展宏观辨识与微观探析的学科核心素养。
2.能基于物质的量认识物质组成及其变化,知道从定量的角度认识宏观物质和微观粒子的相互关系是研究化学问题的科学方法之一,发展宏观辨识与微观探析的学科核心素养。
基础落实·必备知识全过关
一、物质的量的单位——摩尔
1.概念 联系宏观物质与微观粒子的“桥梁”
物质的量是一个物理量,它表示含有 的集合体,符号为 。
2.摩尔
一定数目粒子
n
摩尔
mol
6.02×1023
原子
分子
离子
质子
3.规范表示
使用摩尔作单位时,所指粒子必须十分明确,且粒子的种类要用 表示,如下:
x + mol ―→ H2SO4
↓ ↓ ↓
数值 单位 指定化学式或微粒符号
例如,2 mol H、1 mol H2、1.5 mol NaOH、1 mol OH-等。
微点归纳 表示某物质(或粒子)的物质的量,可用“n(粒子符号)”表示。例如,H2O、CO2的物质的量分别表示为n(H2O)、n(CO2)。
化学式
4.阿伏加德罗常数
(1)概念
1 mol任何粒子的 叫做阿伏加德罗常数,符号为NA,通常用
表示。
(2)物质的量(n)、阿伏加德罗常数(NA)与粒子数(N)之间的关系:
。
粒子数
6.02×1023 mol-1
二、摩尔质量
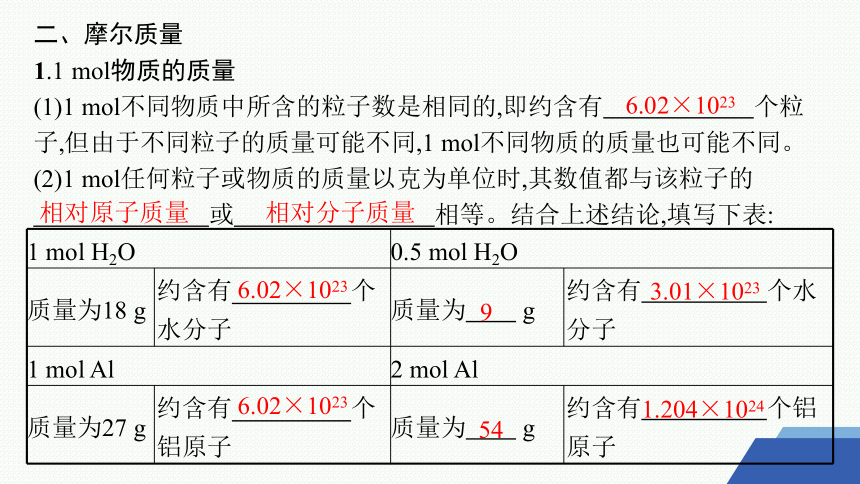
1.1 mol物质的质量
(1)1 mol不同物质中所含的粒子数是相同的,即约含有 个粒子,但由于不同粒子的质量可能不同,1 mol不同物质的质量也可能不同。
(2)1 mol任何粒子或物质的质量以克为单位时,其数值都与该粒子的
或 相等。结合上述结论,填写下表:
1 mol H2O 0.5 mol H2O
质量为18 g 约含有 个水分子 质量为 g 约含有 个水分子
1 mol Al 2 mol Al
质量为27 g 约含有 个铝原子 质量为 g 约含有 个铝原子
6.02×1023
相对原子质量
相对分子质量
6.02×1023
9
3.01×1023
6.02×1023
54
1.204×1024
2.摩尔质量 摩尔质量是定值,不随物质的量发生变化
(1)概念
微点归纳 表示某物质(或粒子)的摩尔质量,可用“M(粒子符号)”表示。例如,H2O、CO2的摩尔质量分别表示为M(H2O)=18 g·mol-1、
M(CO2)=44 g·mol-1。
(2)物质的量(n)、质量(m)与摩尔质量(M)之间的关系: 。
物质的量
M
g·mol-1
相对原子质量
相对分子质量
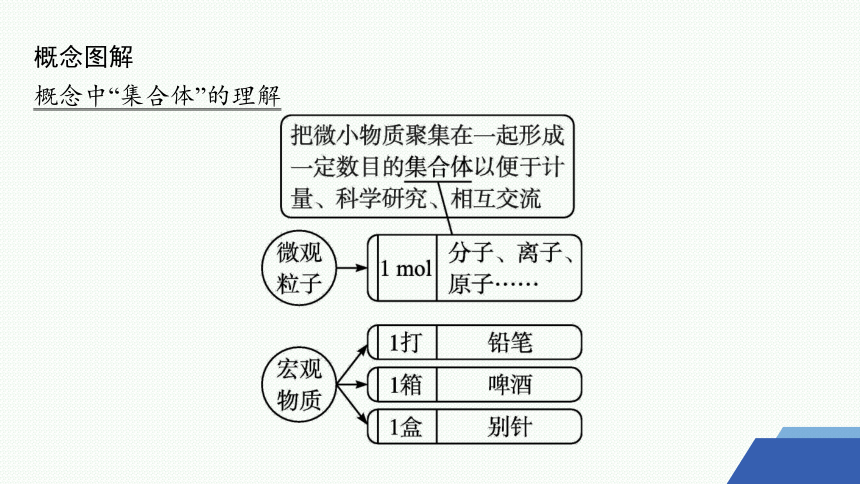
概念图解
概念中“集合体”的理解
归纳总结
物质的量及其单位(摩尔)
(1)“物质的量”是一个基本物理量,四个字是一个整体,不能拆开理解,也不能压缩为“物质量”。
(2)“摩尔”是“物质的量”的单位,不能将二者混淆,如“某物质的物质的量”不能说成“某物质的摩尔数”。
(3)物质的量及摩尔都用于计量微观粒子,不能用于计量宏观物质。
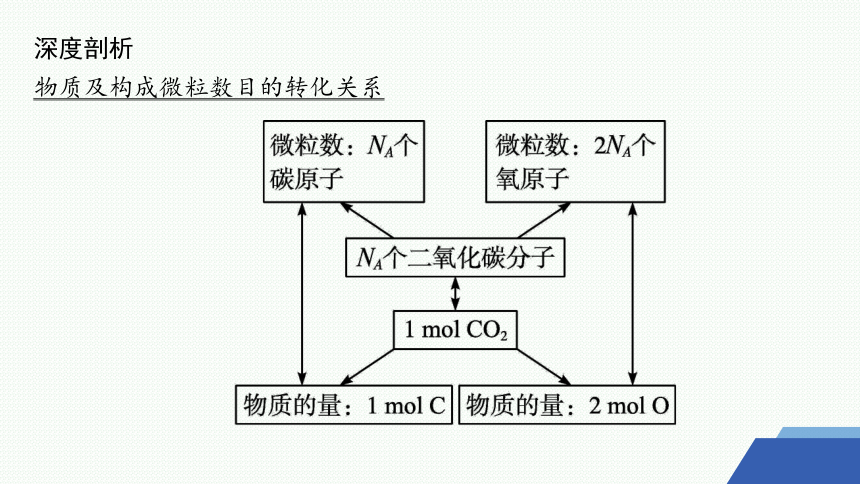
深度剖析
物质及构成微粒数目的转化关系
归纳总结
对摩尔质量的理解
(1)摩尔质量是物质的固有属性,不随物质的状态、物质的量的多少而发生变化。对于指定物质(组成固定)来说,其摩尔质量是固定值。
(2)摩尔质量只有以g·mol-1为单位时,其在数值上才等于该微观粒子的相对原子(或分子)质量。
(3)由于电子的质量较小,确定离子的摩尔质量时,不必考虑离子所带电荷数。例如,
深度思考
假设1个H2O分子的质量为ma g,试求出H2O的摩尔质量(用含ma、NA的代数式表示)。
提示 (NA·ma) g·mol-1
重难探究·能力素养全提升
探究一 物质的量的有关概念及理解
情境探究
从宏观角度看,矿泉水的质量和体积都可以测量,那么这瓶矿泉水中有多少个水分子呢 一滴水(约0.05 mL)大约含有17万亿亿个水分子。若一个个地去数这瓶矿泉水中含有的水分子,即使分秒不停,一个人穷其一生也无法完成这项工作。
(1)已知:1个水分子的质量约为2.99×10-23 g,试计算这瓶矿泉水(500 mL)中含有水分子的数目。
提示 1个水分子的质量约为2.99×10-23 g,500 mL矿泉水的质量约为500 g,则含有水分子的数目约为 ≈1.67×1025。
(2)1 mol H2O的摩尔质量是0.5 mol H2O的摩尔质量的2倍,这种观点正确吗 为什么
提示 不正确;物质的组成确定,其摩尔质量就是确定值,H2O的摩尔质量为18 g·mol-1,与其物质的量的大小无关。
方法突破
1.抓住“四化”,
准确理解
“物质的量”
2.基于“三性”,认识“摩尔质量”
应用体验
1.[2023江西上饶高一期中]草酸(H2C2O4)是生物体的一种代谢产物,广泛分布于植物、动物和真菌体中,并在不同的生命体中发挥不同的功能。下列关于草酸的说法错误的是( )
A.1 mol草酸含有2 mol H、2 mol C和4 mol O
B.含2 mol O的草酸的摩尔质量为90 g·mol-1
C.45 g草酸中含有的原子总数为4NA(设NA为阿伏加德罗常数的值)
D.117 g草酸完全燃烧生成CO2和H2O,转移电子为1.3 mol
D
解析 1个草酸分子含2个H、2个C和4个O,则1 mol草酸含有2 mol H、2 mol C和4 mol O,A正确;H2C2O4的相对分子质量为90,则其摩尔质量为90 g·mol-1,与含有的O原子数无关,B正确;1个草酸分子含有8个原子,45 g草酸为0.5 mol,则含有4 mol原子,故含有的原子总数为4NA,C正确;H2C2O4→CO2, C元素由+3价升高到+4价,117 g草酸的物质的量为1.3 mol,完全燃烧时转移电子为1.3 mol×2×(4-3)=2.6 mol,D错误。
思路分析 解答本题的思路如下:
(1)H2C2O4的相对分子质量为90 摩尔质量为90 g·mol-1;
(2)分析H2C2O4的组成 1个分子含2个H、2个C和4个O;
(3)分析H2C2O4中C化合价 生成CO2时化合价变化 转移电子的物质的量。
2.云南的普洱茶随我国的航天员登上了太空。茶叶装在特制包装袋中,注水后用加热器进行加热就可以喝了。下列说法正确的是( )
A.4 ℃、101 kPa时,18 mL水的物质的量为1 mol
B.航天员喝茶时注入的2 mol H2O的摩尔质量是36
C.1 mol H2O中含有3 mol电子
D.在太空中0.5 mol H2O的摩尔质量为9 g·mol-1
A
解析 4 ℃、101 kPa时,水的密度为1 g·cm-3,18 mL 水的质量为18 g,则其物质的量为 =1 mol,A正确;H2O的摩尔质量与其物质的量无关,
2 mol H2O的摩尔质量仍为18 g·mol-1,B错误;1个H2O分子含有10个电子,则1 mol H2O中含有10 mol电子,C错误;摩尔质量可看作物质的属性,在太空中H2O的摩尔质量仍为18 g·mol-1,D错误。
探究二 物质的量、质量和粒子数之间的换算关系
情境探究
国际知名期刊《Science》杂志发表论文称,我国科学家利用二氧化碳在实验室成功实现淀粉的合成,这是继20世纪60年代我国人工合成结晶牛胰岛素后的再一次重大突破。利用CO2人工合成淀粉技术的主要流程如下:
(1)等物质的量的H2O和H2O2,所含分子数之比为 ,所含O原子数之比为 。
(2)与16 g CH3OH所含碳原子数相同的CO2的质量为 ;3.0 g HCHO所含H原子数目为 。
1∶1
1∶2
22 g
1.204×1023
方法突破
物质的量、质量和粒子数目之间的换算关系及应用
名师点拨 (1)分析物质的组成,明确分子与原子(或离子)的数量关系;
(2)看清题目所求的是粒子的物质的量、数目还是粒子的质量;
(3)依据恒等关系式“ ”进行计算。
应用体验
1.实现“碳中和”的关键是控制碳氧化物的排放,CO和CO2是碳的两种重要氧化物,用NA表示阿伏加德罗常数的值,下列说法错误的是( )
A.NA个CO和1 mol CO2所含分子数相等
B.相同质量的CO和CO2所含的氧原子数之比为1∶2
C.相同物质的量的CO和CO2所含碳原子数之比为1∶1
D.28 g CO全部转化为CO2,所转移的电子数为2NA
B
解析 1 mol CO2含有NA个CO2分子,故与NA个CO所含分子数相同,A正确; CO和CO2的摩尔质量分别为28 g·mol-1、44 g·mol-1,二者等质量时,其物质的量之比为44∶28=11∶7,则所含氧原子数之比为11∶14,B错误;1个CO和1个CO2分子均含1个碳原子,相同物质的量时,二者所含碳原子的物质的量相等,则其数目之比为1∶1,C正确;CO转化为CO2时,1个CO失去2个电子, 28 g CO的物质的量为1 mol,则转移电子数为2NA,D正确。
【变式设问】
若CO2和CO所含氧原子数相同,试求二者的质量之比。
提示 CO2和CO所含氧原子数相同,其物质的量之比为1∶2,则CO2和CO的质量之比为(1×44)∶(2×28)=11∶14。
2.[2023山西太原高一期中]等质量的CH4和NH3相比较,下列结论错误的是
( )
A.分子个数之比为17∶16
B.原子个数之比为17∶16
C.氢原子个数之比为17∶12
D.电子个数之比为17∶16
B
解析 CH4和NH3的摩尔质量分别为16 g·mol-1、17 g·mol-1,等质量时二者的物质的量之比为17∶16,故分子个数之比为17∶16,A正确;CH4和NH3的原子个数之比为(17×5)∶(16×4)=85∶64,B错误;CH4和NH3的氢原子个数之比为(17×4)∶(16×3)=17∶12,C正确;1个CH4和1个NH3分子均含10个电子,故二者所含电子数之比为17∶16,D正确。
学以致用·随堂检测全达标
1
2
3
4
5
1.下列说法中,正确的是( )
A.Mg的摩尔质量为24
B.物质的量的基本单位是摩尔
C.1 mol CO2中含有的氧原子数约为6.02×1023
D.0.5 mol NaCl晶体中含有的分子数约为3.01×1023
B
解析 摩尔质量的单位是g·mol-1,A错误;1个CO2分子含2个氧原子,则1 mol CO2中含有的氧原子数约为1.204×1024,C错误;NaCl晶体是由Na+和Cl-构成的,不含NaCl分子,D错误。
1
2
3
4
5
2.1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为( )
A.64 g B.64
C.64 g·mol-1 D.32 g·mol-1
C
解析 某气体含有的分子数目为1.204×1022,则其物质的量为0.02 mol,又知该气体的质量为1.28 g,故该气体的摩尔质量为 =64 g·mol-1。
1
2
3
4
5
3.[2023河北廊坊高一期中]a mol H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为( )
B
解析 每个H2SO4分子中含有4个氧原子,a mol H2SO4中含有b个氧原子,则4a mol×NA=b,NA= mol-1。
1
2
3
4
5
4.顺铂是一种用于治疗癌症的药物,其结构如图所示。关于1 mol 顺铂的下列说法正确的是( )
A.含氮元素的质量为14 g
B.含铂原子的数目约为6.02×1022
C.含氯元素的质量为35.5 g
D.含氢原子的物质的量为6 mol
D
解析 由顺铂的结构可知,其化学式为PtH6N2Cl2,则1 mol 顺铂含有1 mol Pt、6 mol H、2 mol N和2 mol Cl,D正确;含氮元素的质量为2 mol×14 g·mol-1 =28 g,A错误;含1 mol Pt,则Pt原子的数目约为6.02×1023,B错误;含氯元素的质量为2 mol×35.5 g·mol-1=71 g,C错误。
1
2
3
4
5
5.近日,甘肃兰州建成千吨级二氧化碳加氢合成甲醇(CH3OH)项目,该项目依托中科院大连化物所专家工作站的科技成果,利用光伏发电和新型高效催化剂电解制备氢气,然后采用新型高效催化剂合成甲醇。回答下列问题:
(1)CH3OH的摩尔质量是 g·mol-1。
(2)2 mol H2O中所含原子的物质的量为 mol。
(3) g氢气中所含H原子的数目与1 mol CH3OH所含的H原子数相同。
(4)含0.1NA个O原子的CO2中有 个电子(设NA为阿伏加德罗常数的值)。
1
2
3
4
5
答案 (1)32 (2)6 (3)4 (4)1.1NA
解析 (3)1 mol CH3OH含有4 mol H原子,而含有4 mol H原子的H2的物质的量为2 mol,其质量为2 mol×2 g·mol-1=4 g。
(4)1个CO2分子含有22个电子,含0.1NA个O原子的CO2的物质的量为0.05 mol,则含有1.1 mol电子,故所含电子数为1.1NA。
本 课 结 束
第二章
第三节 第1课时 物质的量的单位——摩尔
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
学以致用·随堂检测全达标
素养 目标 1.通过对比、类比、归纳、演绎等多种思维方法,了解物质的量、摩尔质量的含义,体会从物质的量层次定量研究化学问题的意义,发展宏观辨识与微观探析的学科核心素养。
2.能基于物质的量认识物质组成及其变化,知道从定量的角度认识宏观物质和微观粒子的相互关系是研究化学问题的科学方法之一,发展宏观辨识与微观探析的学科核心素养。
基础落实·必备知识全过关
一、物质的量的单位——摩尔
1.概念 联系宏观物质与微观粒子的“桥梁”
物质的量是一个物理量,它表示含有 的集合体,符号为 。
2.摩尔
一定数目粒子
n
摩尔
mol
6.02×1023
原子
分子
离子
质子
3.规范表示
使用摩尔作单位时,所指粒子必须十分明确,且粒子的种类要用 表示,如下:
x + mol ―→ H2SO4
↓ ↓ ↓
数值 单位 指定化学式或微粒符号
例如,2 mol H、1 mol H2、1.5 mol NaOH、1 mol OH-等。
微点归纳 表示某物质(或粒子)的物质的量,可用“n(粒子符号)”表示。例如,H2O、CO2的物质的量分别表示为n(H2O)、n(CO2)。
化学式
4.阿伏加德罗常数
(1)概念
1 mol任何粒子的 叫做阿伏加德罗常数,符号为NA,通常用
表示。
(2)物质的量(n)、阿伏加德罗常数(NA)与粒子数(N)之间的关系:
。
粒子数
6.02×1023 mol-1
二、摩尔质量
1.1 mol物质的质量
(1)1 mol不同物质中所含的粒子数是相同的,即约含有 个粒子,但由于不同粒子的质量可能不同,1 mol不同物质的质量也可能不同。
(2)1 mol任何粒子或物质的质量以克为单位时,其数值都与该粒子的
或 相等。结合上述结论,填写下表:
1 mol H2O 0.5 mol H2O
质量为18 g 约含有 个水分子 质量为 g 约含有 个水分子
1 mol Al 2 mol Al
质量为27 g 约含有 个铝原子 质量为 g 约含有 个铝原子
6.02×1023
相对原子质量
相对分子质量
6.02×1023
9
3.01×1023
6.02×1023
54
1.204×1024
2.摩尔质量 摩尔质量是定值,不随物质的量发生变化
(1)概念
微点归纳 表示某物质(或粒子)的摩尔质量,可用“M(粒子符号)”表示。例如,H2O、CO2的摩尔质量分别表示为M(H2O)=18 g·mol-1、
M(CO2)=44 g·mol-1。
(2)物质的量(n)、质量(m)与摩尔质量(M)之间的关系: 。
物质的量
M
g·mol-1
相对原子质量
相对分子质量
概念图解
概念中“集合体”的理解
归纳总结
物质的量及其单位(摩尔)
(1)“物质的量”是一个基本物理量,四个字是一个整体,不能拆开理解,也不能压缩为“物质量”。
(2)“摩尔”是“物质的量”的单位,不能将二者混淆,如“某物质的物质的量”不能说成“某物质的摩尔数”。
(3)物质的量及摩尔都用于计量微观粒子,不能用于计量宏观物质。
深度剖析
物质及构成微粒数目的转化关系
归纳总结
对摩尔质量的理解
(1)摩尔质量是物质的固有属性,不随物质的状态、物质的量的多少而发生变化。对于指定物质(组成固定)来说,其摩尔质量是固定值。
(2)摩尔质量只有以g·mol-1为单位时,其在数值上才等于该微观粒子的相对原子(或分子)质量。
(3)由于电子的质量较小,确定离子的摩尔质量时,不必考虑离子所带电荷数。例如,
深度思考
假设1个H2O分子的质量为ma g,试求出H2O的摩尔质量(用含ma、NA的代数式表示)。
提示 (NA·ma) g·mol-1
重难探究·能力素养全提升
探究一 物质的量的有关概念及理解
情境探究
从宏观角度看,矿泉水的质量和体积都可以测量,那么这瓶矿泉水中有多少个水分子呢 一滴水(约0.05 mL)大约含有17万亿亿个水分子。若一个个地去数这瓶矿泉水中含有的水分子,即使分秒不停,一个人穷其一生也无法完成这项工作。
(1)已知:1个水分子的质量约为2.99×10-23 g,试计算这瓶矿泉水(500 mL)中含有水分子的数目。
提示 1个水分子的质量约为2.99×10-23 g,500 mL矿泉水的质量约为500 g,则含有水分子的数目约为 ≈1.67×1025。
(2)1 mol H2O的摩尔质量是0.5 mol H2O的摩尔质量的2倍,这种观点正确吗 为什么
提示 不正确;物质的组成确定,其摩尔质量就是确定值,H2O的摩尔质量为18 g·mol-1,与其物质的量的大小无关。
方法突破
1.抓住“四化”,
准确理解
“物质的量”
2.基于“三性”,认识“摩尔质量”
应用体验
1.[2023江西上饶高一期中]草酸(H2C2O4)是生物体的一种代谢产物,广泛分布于植物、动物和真菌体中,并在不同的生命体中发挥不同的功能。下列关于草酸的说法错误的是( )
A.1 mol草酸含有2 mol H、2 mol C和4 mol O
B.含2 mol O的草酸的摩尔质量为90 g·mol-1
C.45 g草酸中含有的原子总数为4NA(设NA为阿伏加德罗常数的值)
D.117 g草酸完全燃烧生成CO2和H2O,转移电子为1.3 mol
D
解析 1个草酸分子含2个H、2个C和4个O,则1 mol草酸含有2 mol H、2 mol C和4 mol O,A正确;H2C2O4的相对分子质量为90,则其摩尔质量为90 g·mol-1,与含有的O原子数无关,B正确;1个草酸分子含有8个原子,45 g草酸为0.5 mol,则含有4 mol原子,故含有的原子总数为4NA,C正确;H2C2O4→CO2, C元素由+3价升高到+4价,117 g草酸的物质的量为1.3 mol,完全燃烧时转移电子为1.3 mol×2×(4-3)=2.6 mol,D错误。
思路分析 解答本题的思路如下:
(1)H2C2O4的相对分子质量为90 摩尔质量为90 g·mol-1;
(2)分析H2C2O4的组成 1个分子含2个H、2个C和4个O;
(3)分析H2C2O4中C化合价 生成CO2时化合价变化 转移电子的物质的量。
2.云南的普洱茶随我国的航天员登上了太空。茶叶装在特制包装袋中,注水后用加热器进行加热就可以喝了。下列说法正确的是( )
A.4 ℃、101 kPa时,18 mL水的物质的量为1 mol
B.航天员喝茶时注入的2 mol H2O的摩尔质量是36
C.1 mol H2O中含有3 mol电子
D.在太空中0.5 mol H2O的摩尔质量为9 g·mol-1
A
解析 4 ℃、101 kPa时,水的密度为1 g·cm-3,18 mL 水的质量为18 g,则其物质的量为 =1 mol,A正确;H2O的摩尔质量与其物质的量无关,
2 mol H2O的摩尔质量仍为18 g·mol-1,B错误;1个H2O分子含有10个电子,则1 mol H2O中含有10 mol电子,C错误;摩尔质量可看作物质的属性,在太空中H2O的摩尔质量仍为18 g·mol-1,D错误。
探究二 物质的量、质量和粒子数之间的换算关系
情境探究
国际知名期刊《Science》杂志发表论文称,我国科学家利用二氧化碳在实验室成功实现淀粉的合成,这是继20世纪60年代我国人工合成结晶牛胰岛素后的再一次重大突破。利用CO2人工合成淀粉技术的主要流程如下:
(1)等物质的量的H2O和H2O2,所含分子数之比为 ,所含O原子数之比为 。
(2)与16 g CH3OH所含碳原子数相同的CO2的质量为 ;3.0 g HCHO所含H原子数目为 。
1∶1
1∶2
22 g
1.204×1023
方法突破
物质的量、质量和粒子数目之间的换算关系及应用
名师点拨 (1)分析物质的组成,明确分子与原子(或离子)的数量关系;
(2)看清题目所求的是粒子的物质的量、数目还是粒子的质量;
(3)依据恒等关系式“ ”进行计算。
应用体验
1.实现“碳中和”的关键是控制碳氧化物的排放,CO和CO2是碳的两种重要氧化物,用NA表示阿伏加德罗常数的值,下列说法错误的是( )
A.NA个CO和1 mol CO2所含分子数相等
B.相同质量的CO和CO2所含的氧原子数之比为1∶2
C.相同物质的量的CO和CO2所含碳原子数之比为1∶1
D.28 g CO全部转化为CO2,所转移的电子数为2NA
B
解析 1 mol CO2含有NA个CO2分子,故与NA个CO所含分子数相同,A正确; CO和CO2的摩尔质量分别为28 g·mol-1、44 g·mol-1,二者等质量时,其物质的量之比为44∶28=11∶7,则所含氧原子数之比为11∶14,B错误;1个CO和1个CO2分子均含1个碳原子,相同物质的量时,二者所含碳原子的物质的量相等,则其数目之比为1∶1,C正确;CO转化为CO2时,1个CO失去2个电子, 28 g CO的物质的量为1 mol,则转移电子数为2NA,D正确。
【变式设问】
若CO2和CO所含氧原子数相同,试求二者的质量之比。
提示 CO2和CO所含氧原子数相同,其物质的量之比为1∶2,则CO2和CO的质量之比为(1×44)∶(2×28)=11∶14。
2.[2023山西太原高一期中]等质量的CH4和NH3相比较,下列结论错误的是
( )
A.分子个数之比为17∶16
B.原子个数之比为17∶16
C.氢原子个数之比为17∶12
D.电子个数之比为17∶16
B
解析 CH4和NH3的摩尔质量分别为16 g·mol-1、17 g·mol-1,等质量时二者的物质的量之比为17∶16,故分子个数之比为17∶16,A正确;CH4和NH3的原子个数之比为(17×5)∶(16×4)=85∶64,B错误;CH4和NH3的氢原子个数之比为(17×4)∶(16×3)=17∶12,C正确;1个CH4和1个NH3分子均含10个电子,故二者所含电子数之比为17∶16,D正确。
学以致用·随堂检测全达标
1
2
3
4
5
1.下列说法中,正确的是( )
A.Mg的摩尔质量为24
B.物质的量的基本单位是摩尔
C.1 mol CO2中含有的氧原子数约为6.02×1023
D.0.5 mol NaCl晶体中含有的分子数约为3.01×1023
B
解析 摩尔质量的单位是g·mol-1,A错误;1个CO2分子含2个氧原子,则1 mol CO2中含有的氧原子数约为1.204×1024,C错误;NaCl晶体是由Na+和Cl-构成的,不含NaCl分子,D错误。
1
2
3
4
5
2.1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为( )
A.64 g B.64
C.64 g·mol-1 D.32 g·mol-1
C
解析 某气体含有的分子数目为1.204×1022,则其物质的量为0.02 mol,又知该气体的质量为1.28 g,故该气体的摩尔质量为 =64 g·mol-1。
1
2
3
4
5
3.[2023河北廊坊高一期中]a mol H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为( )
B
解析 每个H2SO4分子中含有4个氧原子,a mol H2SO4中含有b个氧原子,则4a mol×NA=b,NA= mol-1。
1
2
3
4
5
4.顺铂是一种用于治疗癌症的药物,其结构如图所示。关于1 mol 顺铂的下列说法正确的是( )
A.含氮元素的质量为14 g
B.含铂原子的数目约为6.02×1022
C.含氯元素的质量为35.5 g
D.含氢原子的物质的量为6 mol
D
解析 由顺铂的结构可知,其化学式为PtH6N2Cl2,则1 mol 顺铂含有1 mol Pt、6 mol H、2 mol N和2 mol Cl,D正确;含氮元素的质量为2 mol×14 g·mol-1 =28 g,A错误;含1 mol Pt,则Pt原子的数目约为6.02×1023,B错误;含氯元素的质量为2 mol×35.5 g·mol-1=71 g,C错误。
1
2
3
4
5
5.近日,甘肃兰州建成千吨级二氧化碳加氢合成甲醇(CH3OH)项目,该项目依托中科院大连化物所专家工作站的科技成果,利用光伏发电和新型高效催化剂电解制备氢气,然后采用新型高效催化剂合成甲醇。回答下列问题:
(1)CH3OH的摩尔质量是 g·mol-1。
(2)2 mol H2O中所含原子的物质的量为 mol。
(3) g氢气中所含H原子的数目与1 mol CH3OH所含的H原子数相同。
(4)含0.1NA个O原子的CO2中有 个电子(设NA为阿伏加德罗常数的值)。
1
2
3
4
5
答案 (1)32 (2)6 (3)4 (4)1.1NA
解析 (3)1 mol CH3OH含有4 mol H原子,而含有4 mol H原子的H2的物质的量为2 mol,其质量为2 mol×2 g·mol-1=4 g。
(4)1个CO2分子含有22个电子,含0.1NA个O原子的CO2的物质的量为0.05 mol,则含有1.1 mol电子,故所含电子数为1.1NA。
本 课 结 束
