3.2.2 水解平衡的移动 教学课件(共19张PPT)
文档属性
| 名称 | 3.2.2 水解平衡的移动 教学课件(共19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-10 00:00:00 | ||
图片预览





文档简介
(共19张PPT)
第二课时 水解平衡的移动
盐类的水解
泡沫灭火器
已知:泡沫灭火器里的药品是NaHCO3和Al2(SO4)3溶液。
为什么两种物质混合时为什么产生了大量沉淀和气泡?
任务一:探究盐类水解平衡的影响因素
【实验探究】
设计实验方案探究温度升高,盐溶液浓度降低时醋酸钠溶液水解平衡的移动情况及水解程度的变化。
试剂:1mol/l醋酸钠溶液 蒸馏水 酚酞溶液 酒精灯
影响因素 实验方案 实验现象 实验结论
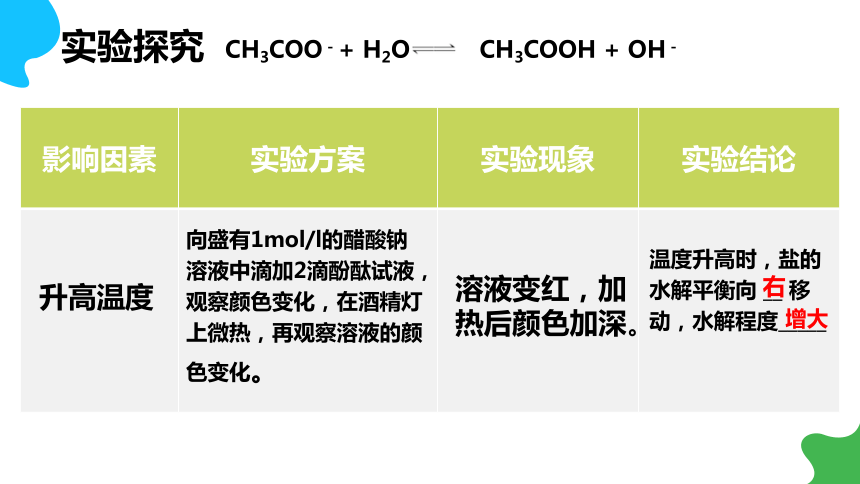
溶液变红,加热后颜色加深。
温度升高时,盐的水解平衡向 __ 移动,水解程度_____
向盛有1mol/l的醋酸钠溶液中滴加2滴酚酞试液,观察颜色变化,在酒精灯上微热,再观察溶液的颜色变化。
CH3COO-+ H2O CH3COOH + OH-
实验探究
升高温度
右
增大
深度思考
温度改变使水解平衡移动的根本原因是什么?
温度改变了Kh,使Q和Kh不再相等.
影响因素 实验方案 实验现象 实验结论
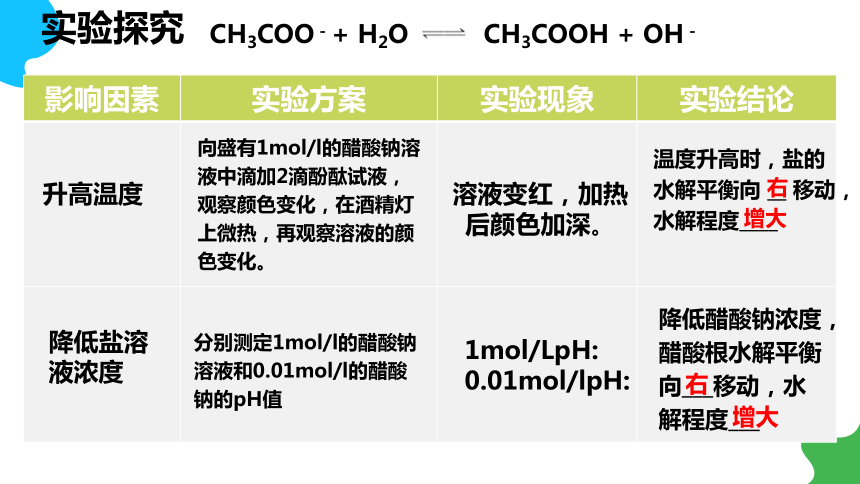
分别测定1mol/l的醋酸钠溶液和0.01mol/l的醋酸钠的pH值
溶液变红,加热后颜色加深。
温度升高时,盐的水解平衡向 __ 移动,水解程度____
向盛有1mol/l的醋酸钠溶液中滴加2滴酚酞试液,观察颜色变化,在酒精灯上微热,再观察溶液的颜色变化。
1mol/LpH:
0.01mol/lpH:
降低醋酸钠浓度,醋酸根水解平衡向___移动,水解程度___
CH3COO-+ H2O CH3COOH + OH-
实验探究
升高温度
右
增大
降低盐溶液浓度
右
增大
深度思考
盐溶液浓度改变使水解平衡移动的根本原因是什么?
浓度的大小使Q大小发生变化, Q和Kh不再相等
请小组内合作讨论分析下列外界条件变化时Q与K关系,并分析醋酸根的水解移动情况和水解程度变化
Q与K关系 移动方向 水解程度
CH3COO-+ H2O CH3COOH + OH-
理论探究1
增加溶液中溶质的量,使盐的浓度增大一倍
Q与K关系 移动方向 水解程度
向溶液中加酸增加氢离子浓度
请分析泡沫灭火器的成分之一硫酸铝溶液在下述条件下的平衡移动情况。
Al 3++3H2O Al(OH)3+3H+
理论探究2
小结
盐的浓度
溶液的温度
外加酸碱
Q与K关系
水解平衡的移动
升温,促进水解反应
盐越稀,水解程度越大
加酸抑制弱碱阳离子水解
加碱抑制弱酸阴离子水解
【合作讨论】
碳酸氢钠浓溶液和硫酸铝浓溶液混合后为什么发生剧烈反应,产生气体和沉淀分别是什么?请运用盐类水解的相关知识进行分析。
任务二 含有多种溶质的复杂体系溶液分析
体系中含有哪些微粒?
哪些微粒可以水解?
水解的微粒间如何相互影响?
分析溶液的组成
分析相互作用
分析作用结果
多种溶质复杂体系水解实际问题思维模型:
NaHCO3
Na+ HCO3-
Al2(SO4)3
Al3+ SO42-
HCO3- + H2O H2CO3 + OH-
Al3+ + 3H2O Al(OH)3 + 3H+
Al3+ +3HCO3- = Al(OH)3↓+3CO2↑
泡沫灭火器的原理
H2O
CH3COONH4溶液中的微粒水解情况分析
CH3COO- NH4+
CH3COO-+ H2O CH3COOH + OH-
NH4+ + H2O NH3·H2O + H+
CH3COO-+ NH4+ + H2O CH3COOH + NH3·H2O
分析溶液的组成
分析相互作用
分析作用结果
应用模型
H2O
氯化铝溶液和硫化钠溶液混合是否可以制得硫化铝固体?
【思考】
学以致用:泡沫灭火器反应物的选择
泡沫灭火器中可以用碳酸钠溶液代替碳酸氢钠吗?请先分析碳酸钠与硫酸铝的混合体系微粒的水解情况,然后说明你的预测理由。
预测 分析 实验验证设计
可以
不可以
混合0.5mol/l硫酸铝溶液与0.5mol/l碳酸钠溶液,对比硫酸铝与碳酸氢钠的反应观察现象
实验现象 结论及分析
硫酸铝溶液与碳酸钠溶液比与碳酸氢钠 产生气泡速率慢很多
不可以替换
小结
模型认知
平衡思想
水解平衡移动
解决实际问题
影响水解平衡的因素
1、对滴有酚酞溶液的下列溶液,操作后颜色变深的是( )
A.明矾溶液加热
B.CH3COONa溶液加热
C.氨水中加入少量NH4Cl固体
D.小苏打溶液中加入少量NaCl固体
检测题
B
2.在一定条件下,Na2CO3溶液中存在水解平衡:CO32-+H2O HCO3-+OH-下列说法正确的是( )
A.加水稀释,水解平衡正向移动,溶液中c(OH-)增大
B.加入少量NH4Cl固体,平衡向正反应方向移动
C.升高温度,减小
D.加入NaOH固体,溶液pH减小
B
第二课时 水解平衡的移动
盐类的水解
泡沫灭火器
已知:泡沫灭火器里的药品是NaHCO3和Al2(SO4)3溶液。
为什么两种物质混合时为什么产生了大量沉淀和气泡?
任务一:探究盐类水解平衡的影响因素
【实验探究】
设计实验方案探究温度升高,盐溶液浓度降低时醋酸钠溶液水解平衡的移动情况及水解程度的变化。
试剂:1mol/l醋酸钠溶液 蒸馏水 酚酞溶液 酒精灯
影响因素 实验方案 实验现象 实验结论
溶液变红,加热后颜色加深。
温度升高时,盐的水解平衡向 __ 移动,水解程度_____
向盛有1mol/l的醋酸钠溶液中滴加2滴酚酞试液,观察颜色变化,在酒精灯上微热,再观察溶液的颜色变化。
CH3COO-+ H2O CH3COOH + OH-
实验探究
升高温度
右
增大
深度思考
温度改变使水解平衡移动的根本原因是什么?
温度改变了Kh,使Q和Kh不再相等.
影响因素 实验方案 实验现象 实验结论
分别测定1mol/l的醋酸钠溶液和0.01mol/l的醋酸钠的pH值
溶液变红,加热后颜色加深。
温度升高时,盐的水解平衡向 __ 移动,水解程度____
向盛有1mol/l的醋酸钠溶液中滴加2滴酚酞试液,观察颜色变化,在酒精灯上微热,再观察溶液的颜色变化。
1mol/LpH:
0.01mol/lpH:
降低醋酸钠浓度,醋酸根水解平衡向___移动,水解程度___
CH3COO-+ H2O CH3COOH + OH-
实验探究
升高温度
右
增大
降低盐溶液浓度
右
增大
深度思考
盐溶液浓度改变使水解平衡移动的根本原因是什么?
浓度的大小使Q大小发生变化, Q和Kh不再相等
请小组内合作讨论分析下列外界条件变化时Q与K关系,并分析醋酸根的水解移动情况和水解程度变化
Q与K关系 移动方向 水解程度
CH3COO-+ H2O CH3COOH + OH-
理论探究1
增加溶液中溶质的量,使盐的浓度增大一倍
Q与K关系 移动方向 水解程度
向溶液中加酸增加氢离子浓度
请分析泡沫灭火器的成分之一硫酸铝溶液在下述条件下的平衡移动情况。
Al 3++3H2O Al(OH)3+3H+
理论探究2
小结
盐的浓度
溶液的温度
外加酸碱
Q与K关系
水解平衡的移动
升温,促进水解反应
盐越稀,水解程度越大
加酸抑制弱碱阳离子水解
加碱抑制弱酸阴离子水解
【合作讨论】
碳酸氢钠浓溶液和硫酸铝浓溶液混合后为什么发生剧烈反应,产生气体和沉淀分别是什么?请运用盐类水解的相关知识进行分析。
任务二 含有多种溶质的复杂体系溶液分析
体系中含有哪些微粒?
哪些微粒可以水解?
水解的微粒间如何相互影响?
分析溶液的组成
分析相互作用
分析作用结果
多种溶质复杂体系水解实际问题思维模型:
NaHCO3
Na+ HCO3-
Al2(SO4)3
Al3+ SO42-
HCO3- + H2O H2CO3 + OH-
Al3+ + 3H2O Al(OH)3 + 3H+
Al3+ +3HCO3- = Al(OH)3↓+3CO2↑
泡沫灭火器的原理
H2O
CH3COONH4溶液中的微粒水解情况分析
CH3COO- NH4+
CH3COO-+ H2O CH3COOH + OH-
NH4+ + H2O NH3·H2O + H+
CH3COO-+ NH4+ + H2O CH3COOH + NH3·H2O
分析溶液的组成
分析相互作用
分析作用结果
应用模型
H2O
氯化铝溶液和硫化钠溶液混合是否可以制得硫化铝固体?
【思考】
学以致用:泡沫灭火器反应物的选择
泡沫灭火器中可以用碳酸钠溶液代替碳酸氢钠吗?请先分析碳酸钠与硫酸铝的混合体系微粒的水解情况,然后说明你的预测理由。
预测 分析 实验验证设计
可以
不可以
混合0.5mol/l硫酸铝溶液与0.5mol/l碳酸钠溶液,对比硫酸铝与碳酸氢钠的反应观察现象
实验现象 结论及分析
硫酸铝溶液与碳酸钠溶液比与碳酸氢钠 产生气泡速率慢很多
不可以替换
小结
模型认知
平衡思想
水解平衡移动
解决实际问题
影响水解平衡的因素
1、对滴有酚酞溶液的下列溶液,操作后颜色变深的是( )
A.明矾溶液加热
B.CH3COONa溶液加热
C.氨水中加入少量NH4Cl固体
D.小苏打溶液中加入少量NaCl固体
检测题
B
2.在一定条件下,Na2CO3溶液中存在水解平衡:CO32-+H2O HCO3-+OH-下列说法正确的是( )
A.加水稀释,水解平衡正向移动,溶液中c(OH-)增大
B.加入少量NH4Cl固体,平衡向正反应方向移动
C.升高温度,减小
D.加入NaOH固体,溶液pH减小
B
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
