2.1 钠及其化合物 同步练习题(含答案)2023-2024学年高一上学期人教版(2019)化学必修第一册
文档属性
| 名称 | 2.1 钠及其化合物 同步练习题(含答案)2023-2024学年高一上学期人教版(2019)化学必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 545.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-11 00:00:00 | ||
图片预览


文档简介
2.1 钠及其化合物 同步练习题
一、选择题
1.下列各物质的分类、名称(或俗名)、化学式都正确的是
A.酸性氧化物 干冰 CO2 B.碱性氧化物 氧化铁 FeO
C.酸 硫酸 H2S D.碱 纯碱 Na2CO3
2.下列用品的有效成分及用途对应不正确的是
A B C D
用品
有效成分 NaCl NaClO
用途 调味品 发酵粉 制氧剂 消毒剂
A.A B.B C.C D.D
3.在化学实验中,具有安全和环保意识是重要的科学素养。下列做法不正确的是
A.酒精灯失火用湿抹布灭火 B.可用手直接取用金属钠
C.用点燃的方法处理CO尾气 D.、等固体不能随便丢弃
4.鉴别下列各组物质,只能采用焰色试验的是
A.和NaCl B.NaCl和KCl
C.和 D.KCl和
5.下列各组物质反应,条件(温度、浓度、反应物用量等)改变,不会引起产物改变的是
A.NaHCO3和HCl B.Na和O2
C.AlCl3与NaOH D.Na2CO3和HCl
6.钠在空气中燃烧的实验,下列不需要的仪器是
A. B. C. D.
7.通常需用焰色反应才能鉴别的一组物质是
A.丝绸与棉布 B.氯化钠与氯化钾
C.硫酸铵与氯化铵 D.碳酸钠与硝酸钠
8.下列操作不符合实验安全规范的是
A.熄灭酒精灯时,用嘴吹灭
B.金属钠不慎着火时,立即用沙土覆盖
C.制备有毒气体时,在通风橱内进行
D.盐酸沾到皮肤上,立即用大量水冲洗后用稀溶液冲洗
二、非选择题
9.卫生部曾发出公告,禁止在面粉生产中添加过氧化钙等食品添加剂。与在结构和性质上有很多相似的地方。请回答下列问题:
(1)中阴阳离子个数之比为___________。
(2)与足量水反应的离子方程式为___________,反应过程中断裂的化学键有___________(填序号)
A.离子键 B.极性共价键 C.非极性共价键
(3)与二氧化碳反应中氧化剂与还原剂的物质的量之比为___________。
10.我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如下:
(1)粗盐水中主要含有Ca2+、Mg2+、SO42﹣等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为______、盐酸(只写一种)。加盐酸的作用是(用化学方程式表示)____________、____________。
(2)制碱原理为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,该反应原理可看作是由:①CO2+NH3+H2O=NH4HCO3和②NaCl+NH4HCO3=NaHCO3↓+NH4Cl两个反应加合而成,则该反应类型为______________。
(3)X的化学式为__________________。
(4)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为____________,Y的化学式为____________,写出Y的一种用途_______________。
11.向含有mmolNaOH的溶液中通入nmolCO2气体,若生成碳酸钠和碳酸氢钠两种盐,计算碳酸钠和碳酸氢钠的物质的量分别是___________、___________。
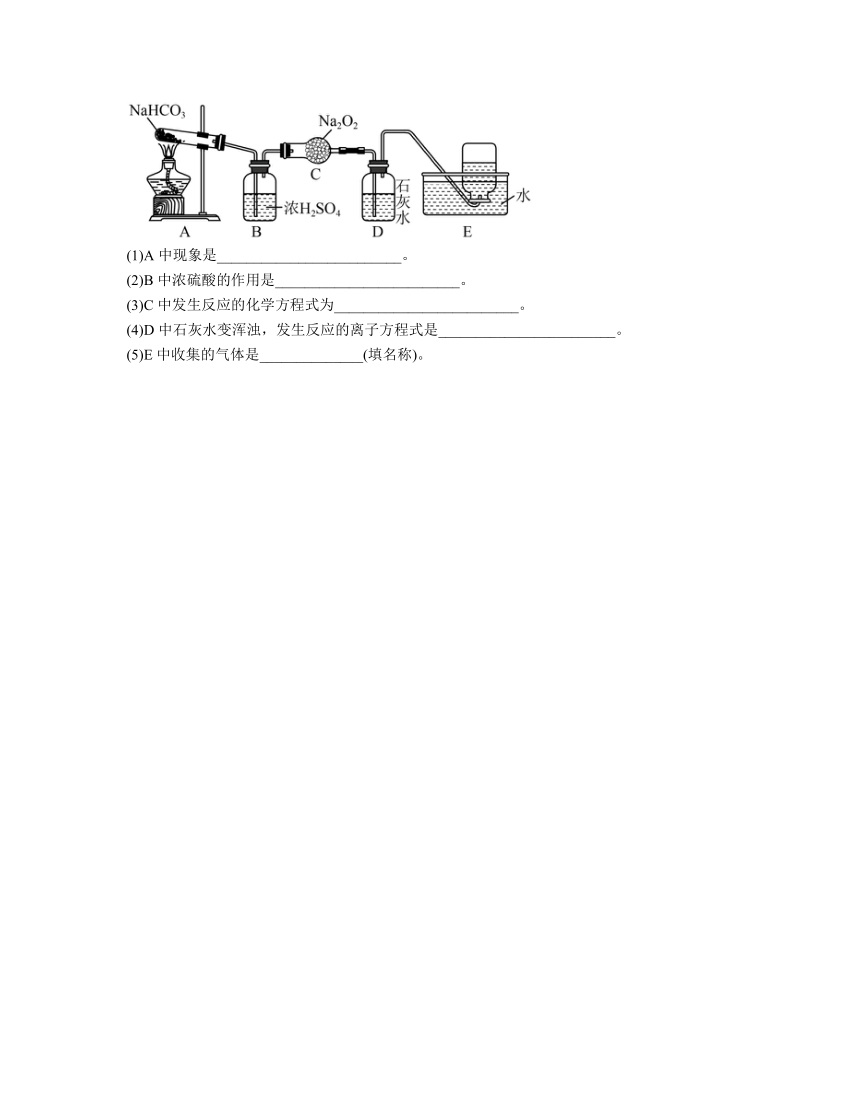
12.按照如图所示装置进行实验,填写有关现象及化学方程式。
(1)A中现象是_________________________。
(2)B中浓硫酸的作用是_________________________。
(3)C中发生反应的化学方程式为_________________________。
(4)D中石灰水变浑浊,发生反应的离子方程式是________________________。
(5)E中收集的气体是______________(填名称)。
【参考答案】
一、选择题
1.A
解析:A.固体CO2的俗称为干冰,是酸性氧化物,A正确;
B.氧化铁的化学式为Fe2O3,是碱性氧化物,B错误;
C.H2S为硫化氢,是酸,C错误;
D.Na2CO3俗名是纯碱,属于盐类,D错误;
故答案为:A。
2.B
解析:A.食盐主要成分NaCl,作调味品,A正确;
B.小苏打有效成分NaHCO3,B错误;
C.Na2O2做制氧剂,C正确;
D.消毒剂主要成分NaClO,D正确;
故答案为:B。
3.B
解析:A. 酒精灯失火用湿抹布灭火,故A正确;
B. 不可用手直接取用金属钠,应用镊子取用,故B错误;
C. CO燃烧生成二氧化碳,则可用点燃的方法处理CO尾气,故C正确;
D. 、等固体不能随便丢弃,应放到指定容器中,故D正确;
故选B。
4.B
解析:A.和NaCl可用氯化钡鉴别,出现白色沉淀的为K2SO4,故A不符合题意;
B.NaCl和KCl的阴离子相同,阳离子均为碱金属离子,只能利用焰色反应鉴别,故B符合题意;
C.和可用NaOH鉴别,与NaOH反应生成白色沉淀的为氯化镁,无现象的为NaCl,故C不符合题意;
D.KCl和可用盐酸检验,与盐酸反应生成气体的为碳酸钙,无现象的为KCl,故D不符合题意;
故答案选B。
5.A
解析:A.NaHCO3和HCl反应只生成氯化钠、水和CO2,与条件无关,故A选;
B.常温下Na和O2反应生成氧化钠,点燃或加热反应生成过氧化钠,反应温度不同其产物不同,故B不选;
C.AlCl3和NaOH反应产物与氢氧化钠用量有关,氢氧化钠少量生成氢氧化铝沉淀,氢氧化钠过量生成偏铝酸钠,故C不选;
D.Na2CO3和少量HCl反应生成碳酸氢钠和氯化钠,和过量HCl反应生成氯化钠、水和CO2,反应物用量不同其产物不同,故D不选;
故选:A。
6.A
解析:完成钠在空气中燃烧的实验,应该在坩埚中进行,A所示仪器是玻璃棒,B中所示仪器是泥三角,C所示仪器是三角架,D所示仪器是坩埚,用不到的仪器为玻璃棒,故选A。
7.B
【分析】焰色反应,也称作焰色测试及焰色试验,是某些金属或它们的化合物在无色火焰中灼烧时使火焰呈现特殊颜色的反应;
解析:A.丝绸含有蛋白质,灼烧有烧焦羽毛味;棉为植物纤维,灼烧无烧焦羽毛味,无需用焰色反应;故A错误;
B.钠元素焰色反应为黄色、钾元素焰色反应为紫色,故B正确;
C.两者不含金属元素,故C错误;
D.碳酸钠与硝酸钠均含有钠元素,焰色反应均为黄色,故D错误;
故选B。
8.A
解析:A.酒精灯内有酒精蒸气,用嘴吹灭时,会把火吹入灯内,引起灯内酒精与空气的混合气体爆炸,故A错误;
B.钠与水反应生成氢氧化钠和氢气,所以金属钠不慎着火时,立即用沙土覆盖,故B正确;
C.制备有毒气体时,在通风橱内进行,防止中毒,故C正确;
D.盐酸是一元强酸,盐酸沾到皮肤上,立即用大量水冲洗后用稀溶液冲洗,故D正确。
故选A。
二、非选择题
9.(1)1∶1
(2) ABC
(3)1∶1
解析:(1)是由钙离子(Ca2+)与过氧根离子()构成,所以阴阳离子个数之比为1∶1;
(2)与化学性质相似,根据过氧化钠与水的反应原理可知,过氧化钙与水反应生成氢氧化钙与氧气,其离子方程式为:;
(3)与化学性质相似,根据过氧化钠与二氧化碳的反应原理可知,与二氧化碳反应生成碳酸钠与氧气,其化学方程式为:,所以反应中氧化剂与还原剂均为,其物质的量之比为1∶1。
10. BaCl2溶液、NaOH溶液、Na2CO3溶液 NaOH+HCl=NaCl+H2O Na2CO3+2HCl=2NaCl+CO2+H2O 化合反应、复分解 CO2 氨气 NH4Cl 氮肥
【分析】粗盐水精制后得到饱和溶液,通入氨气使溶液显碱性,之后通入过量的二氧化碳,发生反应NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,过滤得到碳酸氢钠晶体,煅烧得到碳酸钠、二氧化碳和水,滤液中主要含有氯化铵,加入氢氧化钙加热可产生氨气循环使用。
解析:(1)加入碳酸钠的作用有两个:一个是除去溶液中的Ca2+、另一个是除去过量的氯化钡,所以加入的碳酸钠必须排在氯化钡的后面,所以顺序是NaOH、BaCl2、Na2CO3;加入盐酸的目的是除去过量的氢氧化钠和过量的碳酸钠,方程式为NaOH+HCl===NaCl+H2O、Na2CO3+2HCl===2NaCl+H2O+CO2;
(2)反应①为化合反应,反应②为复分解反应,则该反为化合反应、复分解;
(3)煅烧碳酸氢钠可以得到碳酸钠、二氧化碳和水,所以X的化学式为CO2;
(4)滤液中主要成分为NH4Cl,在加热条件下与氢氧化钙反应可以生成氨气,氨气可循环使用,NH4Cl含有氮元素可以做氮肥。
【点睛】粗盐提纯时加入碳酸钠的作用有两个:一个是除去溶液中的Ca2+、另一个是除去过量的氯化钡,所以加入的碳酸钠必须排在氯化钡的后面。
11. Na2CO3,(m-n) mol NaHCO3,(2n-m) mol
解析:设Na2CO3为x mol,NaHCO3为y mol,根据钠元素的守恒,得2x+y=m,再根据碳元素的守恒得x+y=n,联立解出x=(m-n)mol、y=(2n-m)mol。
12.(1)试管口有无色液体生成
(2)干燥CO2气体
(3)2CO2+2Na2O2=2Na2CO3+O2
(4)CO2+Ca2++2OH-=CaCO3↓+H2O
(5)氧气
【分析】碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,浓硫酸干燥二氧化碳,人氧化碳和过氧化钠反应生成碳酸钠和氧气,澄清石灰水变浑浊,说明二氧化碳和氢氧化钙反应,E中收集到氧气。
解析:(1)碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,水蒸气冷凝在试管口,因此A中现象是试管口有无色液体生成;故答案为:试管口有无色液体生成。
(2)A中出现的气体有二氧化碳和水蒸气,因此B中浓硫酸的作用是干燥CO2气体;故答案为:干燥CO2气体。
(3)C中发生反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2;故答案为:2CO2+2Na2O2=2Na2CO3+O2。
(4)D中石灰水变浑浊,是氢氧化钙和二氧化碳反应生成碳酸钙和水,其发生反应的离子方程式是CO2+Ca2++2OH-=CaCO3↓+H2O;故答案为:CO2+Ca2++2OH-=CaCO3↓+H2O。
(5)C中生成了氧气,氧气难溶于水,用排水法收集,因此E中收集的气体是氧气;故答案为:氧气
一、选择题
1.下列各物质的分类、名称(或俗名)、化学式都正确的是
A.酸性氧化物 干冰 CO2 B.碱性氧化物 氧化铁 FeO
C.酸 硫酸 H2S D.碱 纯碱 Na2CO3
2.下列用品的有效成分及用途对应不正确的是
A B C D
用品
有效成分 NaCl NaClO
用途 调味品 发酵粉 制氧剂 消毒剂
A.A B.B C.C D.D
3.在化学实验中,具有安全和环保意识是重要的科学素养。下列做法不正确的是
A.酒精灯失火用湿抹布灭火 B.可用手直接取用金属钠
C.用点燃的方法处理CO尾气 D.、等固体不能随便丢弃
4.鉴别下列各组物质,只能采用焰色试验的是
A.和NaCl B.NaCl和KCl
C.和 D.KCl和
5.下列各组物质反应,条件(温度、浓度、反应物用量等)改变,不会引起产物改变的是
A.NaHCO3和HCl B.Na和O2
C.AlCl3与NaOH D.Na2CO3和HCl
6.钠在空气中燃烧的实验,下列不需要的仪器是
A. B. C. D.
7.通常需用焰色反应才能鉴别的一组物质是
A.丝绸与棉布 B.氯化钠与氯化钾
C.硫酸铵与氯化铵 D.碳酸钠与硝酸钠
8.下列操作不符合实验安全规范的是
A.熄灭酒精灯时,用嘴吹灭
B.金属钠不慎着火时,立即用沙土覆盖
C.制备有毒气体时,在通风橱内进行
D.盐酸沾到皮肤上,立即用大量水冲洗后用稀溶液冲洗
二、非选择题
9.卫生部曾发出公告,禁止在面粉生产中添加过氧化钙等食品添加剂。与在结构和性质上有很多相似的地方。请回答下列问题:
(1)中阴阳离子个数之比为___________。
(2)与足量水反应的离子方程式为___________,反应过程中断裂的化学键有___________(填序号)
A.离子键 B.极性共价键 C.非极性共价键
(3)与二氧化碳反应中氧化剂与还原剂的物质的量之比为___________。
10.我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如下:
(1)粗盐水中主要含有Ca2+、Mg2+、SO42﹣等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为______、盐酸(只写一种)。加盐酸的作用是(用化学方程式表示)____________、____________。
(2)制碱原理为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,该反应原理可看作是由:①CO2+NH3+H2O=NH4HCO3和②NaCl+NH4HCO3=NaHCO3↓+NH4Cl两个反应加合而成,则该反应类型为______________。
(3)X的化学式为__________________。
(4)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为____________,Y的化学式为____________,写出Y的一种用途_______________。
11.向含有mmolNaOH的溶液中通入nmolCO2气体,若生成碳酸钠和碳酸氢钠两种盐,计算碳酸钠和碳酸氢钠的物质的量分别是___________、___________。
12.按照如图所示装置进行实验,填写有关现象及化学方程式。
(1)A中现象是_________________________。
(2)B中浓硫酸的作用是_________________________。
(3)C中发生反应的化学方程式为_________________________。
(4)D中石灰水变浑浊,发生反应的离子方程式是________________________。
(5)E中收集的气体是______________(填名称)。
【参考答案】
一、选择题
1.A
解析:A.固体CO2的俗称为干冰,是酸性氧化物,A正确;
B.氧化铁的化学式为Fe2O3,是碱性氧化物,B错误;
C.H2S为硫化氢,是酸,C错误;
D.Na2CO3俗名是纯碱,属于盐类,D错误;
故答案为:A。
2.B
解析:A.食盐主要成分NaCl,作调味品,A正确;
B.小苏打有效成分NaHCO3,B错误;
C.Na2O2做制氧剂,C正确;
D.消毒剂主要成分NaClO,D正确;
故答案为:B。
3.B
解析:A. 酒精灯失火用湿抹布灭火,故A正确;
B. 不可用手直接取用金属钠,应用镊子取用,故B错误;
C. CO燃烧生成二氧化碳,则可用点燃的方法处理CO尾气,故C正确;
D. 、等固体不能随便丢弃,应放到指定容器中,故D正确;
故选B。
4.B
解析:A.和NaCl可用氯化钡鉴别,出现白色沉淀的为K2SO4,故A不符合题意;
B.NaCl和KCl的阴离子相同,阳离子均为碱金属离子,只能利用焰色反应鉴别,故B符合题意;
C.和可用NaOH鉴别,与NaOH反应生成白色沉淀的为氯化镁,无现象的为NaCl,故C不符合题意;
D.KCl和可用盐酸检验,与盐酸反应生成气体的为碳酸钙,无现象的为KCl,故D不符合题意;
故答案选B。
5.A
解析:A.NaHCO3和HCl反应只生成氯化钠、水和CO2,与条件无关,故A选;
B.常温下Na和O2反应生成氧化钠,点燃或加热反应生成过氧化钠,反应温度不同其产物不同,故B不选;
C.AlCl3和NaOH反应产物与氢氧化钠用量有关,氢氧化钠少量生成氢氧化铝沉淀,氢氧化钠过量生成偏铝酸钠,故C不选;
D.Na2CO3和少量HCl反应生成碳酸氢钠和氯化钠,和过量HCl反应生成氯化钠、水和CO2,反应物用量不同其产物不同,故D不选;
故选:A。
6.A
解析:完成钠在空气中燃烧的实验,应该在坩埚中进行,A所示仪器是玻璃棒,B中所示仪器是泥三角,C所示仪器是三角架,D所示仪器是坩埚,用不到的仪器为玻璃棒,故选A。
7.B
【分析】焰色反应,也称作焰色测试及焰色试验,是某些金属或它们的化合物在无色火焰中灼烧时使火焰呈现特殊颜色的反应;
解析:A.丝绸含有蛋白质,灼烧有烧焦羽毛味;棉为植物纤维,灼烧无烧焦羽毛味,无需用焰色反应;故A错误;
B.钠元素焰色反应为黄色、钾元素焰色反应为紫色,故B正确;
C.两者不含金属元素,故C错误;
D.碳酸钠与硝酸钠均含有钠元素,焰色反应均为黄色,故D错误;
故选B。
8.A
解析:A.酒精灯内有酒精蒸气,用嘴吹灭时,会把火吹入灯内,引起灯内酒精与空气的混合气体爆炸,故A错误;
B.钠与水反应生成氢氧化钠和氢气,所以金属钠不慎着火时,立即用沙土覆盖,故B正确;
C.制备有毒气体时,在通风橱内进行,防止中毒,故C正确;
D.盐酸是一元强酸,盐酸沾到皮肤上,立即用大量水冲洗后用稀溶液冲洗,故D正确。
故选A。
二、非选择题
9.(1)1∶1
(2) ABC
(3)1∶1
解析:(1)是由钙离子(Ca2+)与过氧根离子()构成,所以阴阳离子个数之比为1∶1;
(2)与化学性质相似,根据过氧化钠与水的反应原理可知,过氧化钙与水反应生成氢氧化钙与氧气,其离子方程式为:;
(3)与化学性质相似,根据过氧化钠与二氧化碳的反应原理可知,与二氧化碳反应生成碳酸钠与氧气,其化学方程式为:,所以反应中氧化剂与还原剂均为,其物质的量之比为1∶1。
10. BaCl2溶液、NaOH溶液、Na2CO3溶液 NaOH+HCl=NaCl+H2O Na2CO3+2HCl=2NaCl+CO2+H2O 化合反应、复分解 CO2 氨气 NH4Cl 氮肥
【分析】粗盐水精制后得到饱和溶液,通入氨气使溶液显碱性,之后通入过量的二氧化碳,发生反应NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,过滤得到碳酸氢钠晶体,煅烧得到碳酸钠、二氧化碳和水,滤液中主要含有氯化铵,加入氢氧化钙加热可产生氨气循环使用。
解析:(1)加入碳酸钠的作用有两个:一个是除去溶液中的Ca2+、另一个是除去过量的氯化钡,所以加入的碳酸钠必须排在氯化钡的后面,所以顺序是NaOH、BaCl2、Na2CO3;加入盐酸的目的是除去过量的氢氧化钠和过量的碳酸钠,方程式为NaOH+HCl===NaCl+H2O、Na2CO3+2HCl===2NaCl+H2O+CO2;
(2)反应①为化合反应,反应②为复分解反应,则该反为化合反应、复分解;
(3)煅烧碳酸氢钠可以得到碳酸钠、二氧化碳和水,所以X的化学式为CO2;
(4)滤液中主要成分为NH4Cl,在加热条件下与氢氧化钙反应可以生成氨气,氨气可循环使用,NH4Cl含有氮元素可以做氮肥。
【点睛】粗盐提纯时加入碳酸钠的作用有两个:一个是除去溶液中的Ca2+、另一个是除去过量的氯化钡,所以加入的碳酸钠必须排在氯化钡的后面。
11. Na2CO3,(m-n) mol NaHCO3,(2n-m) mol
解析:设Na2CO3为x mol,NaHCO3为y mol,根据钠元素的守恒,得2x+y=m,再根据碳元素的守恒得x+y=n,联立解出x=(m-n)mol、y=(2n-m)mol。
12.(1)试管口有无色液体生成
(2)干燥CO2气体
(3)2CO2+2Na2O2=2Na2CO3+O2
(4)CO2+Ca2++2OH-=CaCO3↓+H2O
(5)氧气
【分析】碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,浓硫酸干燥二氧化碳,人氧化碳和过氧化钠反应生成碳酸钠和氧气,澄清石灰水变浑浊,说明二氧化碳和氢氧化钙反应,E中收集到氧气。
解析:(1)碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,水蒸气冷凝在试管口,因此A中现象是试管口有无色液体生成;故答案为:试管口有无色液体生成。
(2)A中出现的气体有二氧化碳和水蒸气,因此B中浓硫酸的作用是干燥CO2气体;故答案为:干燥CO2气体。
(3)C中发生反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2;故答案为:2CO2+2Na2O2=2Na2CO3+O2。
(4)D中石灰水变浑浊,是氢氧化钙和二氧化碳反应生成碳酸钙和水,其发生反应的离子方程式是CO2+Ca2++2OH-=CaCO3↓+H2O;故答案为:CO2+Ca2++2OH-=CaCO3↓+H2O。
(5)C中生成了氧气,氧气难溶于水,用排水法收集,因此E中收集的气体是氧气;故答案为:氧气
