3.2.1铁合金 铝和铝合金 新型合金课件(共25张PPT)2023-2024学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 3.2.1铁合金 铝和铝合金 新型合金课件(共25张PPT)2023-2024学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 14.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-13 00:00:00 | ||
图片预览







文档简介
(共25张PPT)
第二节 金属材料
第三章 铁 金属材料
第1课时:铁合金 铝和铝合金 新型合金
目 录
CONTENTS
01
金属材料 铁合金
02
铝和铝合金
03
新型合金
学习目标
1.认识合金的特征性质,了解常见合金的分类、组成和用途。
2.掌握Al与O2反应及Al与NaOH溶液反应的产物和本质。
3.正确认识氧化铝的两性。
4.能说明常见金属材料对社会发展的价值及对环境的影响。
(本页可根据需要自行删除)
①由于ppt含较多高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有1个视频,根据需要选择即时播放。
视频清单
①铝、氧化铝与盐酸的反应
②铝、氧化铝与氢氧化钠溶液的反应
致老师和同学们
新课导入
生活中常见的金属材料
1
金属材料 铁合金
合金是由两种或两种以上的金属或金属与非金属熔合而成的具有金属特性的物质。
金属材料
纯金属
合金
80多种
几千种
生活中用到的金属材料是纯金属较多还是合金较多?为什么?
合金多
合金的性能比纯金属更优良
常见合金的硬度会比其成分金属大,合金的熔点一般比成分金属低。
一、金属材料 铁合金
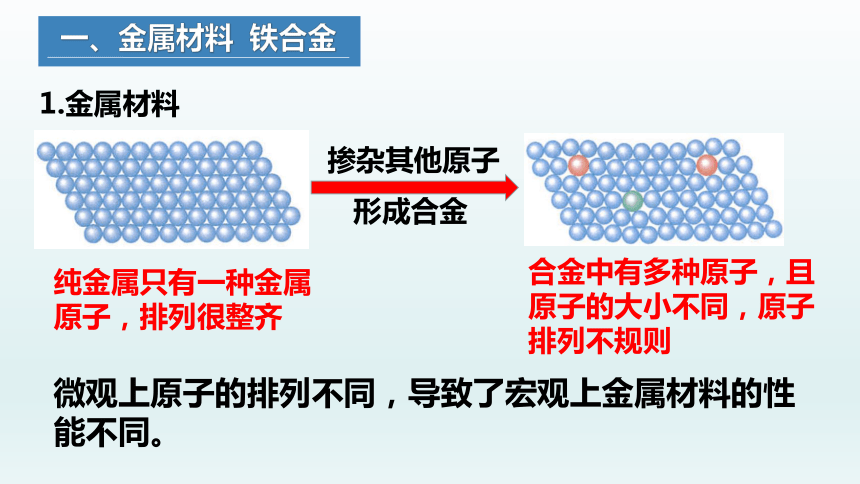
1.金属材料
纯金属只有一种金属原子,排列很整齐
合金中有多种原子,且原子的大小不同,原子排列不规则
掺杂其他原子
形成合金
微观上原子的排列不同,导致了宏观上金属材料的性能不同。
一、金属材料 铁合金
1.金属材料
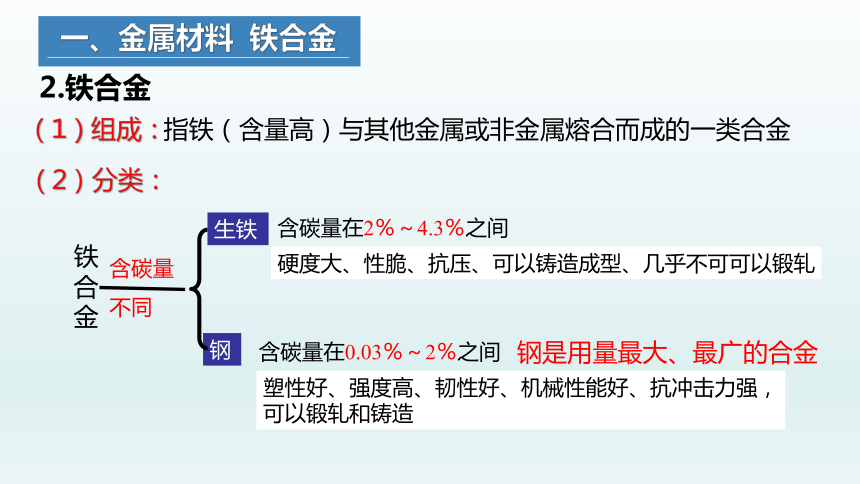
(1)组成:
指铁(含量高)与其他金属或非金属熔合而成的一类合金
(2)分类:
生铁
钢
铁合金
含碳量不同
含碳量在2%~4.3%之间
含碳量在0.03%~2%之间
硬度大、性脆、抗压、可以铸造成型、几乎不可可以锻轧
塑性好、强度高、韧性好、机械性能好、抗冲击力强,
可以锻轧和铸造
一、金属材料 铁合金
2.铁合金
钢是用量最大、最广的合金
钢
碳素钢
低碳钢
(含碳0.3%~0.6%)
高碳钢
(含碳0.03%~0.3%)
中碳钢
(含碳0.6%~2% )
合金钢
(特种钢)
在碳素钢中加入铬、锰、钨、硅等合金元素,使其具有特殊性能
钢板、钢丝、钢管
钢轨、车轮、建材
器械、弹簧、刀具
不锈钢是最常见的合金钢,其合金元素是Cr和Ni
一、金属材料 铁合金
2.铁合金
2
铝和铝合金
二、铝和铝合金
(1)铝是地壳中含量最多的金属元素。
(2)铝是一种活泼金属,在常温下就能与空气中的O2发生
反应,表面生成一层致密的氧化铝薄膜。日常常用的铝制
品通常都是由铝合金制造的,其表面总是覆盖着致密的氧
化铝薄膜,保护内部金属不受腐蚀。
1.铝
meiyangyang8602
二、铝和铝合金
2.铝、氧化铝的性质
【实验3-4】 在一支试管中加入5 mL盐酸,再向试管中放入一小块铝片。观察现象。过一段时间后,将点燃的木条放在试管口,你观察到什么现象?
meiyangyang8602
二、铝和铝合金
2.铝、氧化铝的性质
实验现象 铝片逐渐溶解,有无色气泡冒出,将点燃的木条放在试管口有爆鸣声
化学方程式 Al2O3+6HCl=2AlCl3+3H2O
2Al+6HCl=2AlCl3+3H2↑
结论 Al2O3和铝均能与盐酸发生反应
(1)与盐酸反应
meiyangyang8602
二、铝和铝合金
2.铝、氧化铝的性质
【实验3-5】在两支试管中分别加入少量的 NaOH溶液,然后向其中一支试管中放入一小块铝片,向另一支试管中放入用砂纸仔细打磨过(除去表面的氧化膜)的一小块铝片。观察现象。过一段时间后,将点燃的木条分别放在两支试管口,
你观察到什么现象?
meiyangyang8602
二、铝和铝合金
2.铝、氧化铝的性质
实验现象 试管①中铝片逐渐溶解,一开始无气泡产生,一段时间后,有无色气泡冒出,试管②中铝片逐渐溶解,立即产生无色气泡,将点燃的木条放在试管口,都有爆鸣声
化学方程式 Al2O3+2NaOH=2NaAlO2+H2O
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
结论 Al2O3和铝均能与NaOH溶液发生反应
(2)与氢氧化钠溶液反应
两性氧化物:既能与酸反应,又能与碱反应生成盐和水,如:Al2O3。
不可以
meiyangyang8602
氧化物
酸性氧化物
(例如CO2、SO2……)
碱性氧化物
(例如CaO、Na2O、Fe2O3、FeO……)
两性氧化物
(例如Al2O3……)
铝既能与稀盐酸反应又能与NaOH溶液反应,都生成___和氢气。
氧化铝既能与稀盐酸反应又能与NaOH溶液反应,都生成___和水。
盐
盐
Al2O3+6H+===2Al3++3H2O
Al2O3+2OH-===2AlO2-+H2O
2Al+6H+===2Al3++3H2↑
2Al+2OH-+2H2O===2AlO2-+3H2↑
2.铝、氧化铝的性质
二、铝和铝合金
meiyangyang8602
二、铝和铝合金
3.铝合金
向铝中加入少量的合金元素,如Cu、Mg、Si、Mn、Zn及稀土元素等,可制成铝合金。铝合金是目前用途广泛的合金之一。例如,硬铝的密度小、强度高,具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料。
“会飞的金属”
3
新型合金
三、新型合金
近年来,为满足某些尖端技术发展的需要,人们又设计和 合成了许
多新型合金。如:用于贮氢的新型合金Ti Fe合金和La Ni合金;钛
合金、耐热合金和形状记忆合金等广泛应用于航空航天、生物工程
和电子工业等领域。
耐热合金
答案 (1)× (2)× (3)× (4)√ (5)× (6)√ (7)×
对 点 训 练
1.判断正误,正确的打“√”,错误的打“×”。(1)合金中不可能含有非金属元素。( )(2)合金中的金属元素以化合物的形式存在。( )(3)合金中各元素的含量一定,所以合金是纯净物。( )(4)生铁的熔点比铁低,但机械强度和硬度比铁高。( )(5)两性氧化物是既有酸性又有碱性的氧化物。( )(6)等质量的Al与足量的盐酸、NaOH溶液充分反应,生成的H2的物质的量相同。( )(7)等物质的量的盐酸、NaOH溶液与足量Al充分反应,生成的H2的物质的量相同。( )
A
对 点 训 练
2.不锈钢通常不与酸、碱、盐反应,是因为加入了( )A.Ni和Cr B.Ni和AuC.Cr和Au D.Cr和Pt
C
对 点 训 练
3.日常生活中使用的钥匙是由铝合金制成的,而不是由纯铝所制,这主要是因为铝合金的( )A.熔点低 B.耐腐蚀性强C.硬度大 D.密度小
对 点 训 练
4.将未经打磨的铝条分别浸入足量的NaOH溶液和稀硫酸中,写出实验过程中反应的离子方程式:________________________________________。
Al2O3+2OH-===2AlO2-+H2O,
2Al+2OH-+2H2O===2AlO2-+3H2↑,
Al2O3+6H+===2Al3++3H2O,
2Al+6H+===2Al3++3H2↑
谢谢观赏
第二节 金属材料
第三章 铁 金属材料
第1课时:铁合金 铝和铝合金 新型合金
目 录
CONTENTS
01
金属材料 铁合金
02
铝和铝合金
03
新型合金
学习目标
1.认识合金的特征性质,了解常见合金的分类、组成和用途。
2.掌握Al与O2反应及Al与NaOH溶液反应的产物和本质。
3.正确认识氧化铝的两性。
4.能说明常见金属材料对社会发展的价值及对环境的影响。
(本页可根据需要自行删除)
①由于ppt含较多高质量素材和视频,故资源比较大。
②所用视频均内嵌在ppt中,不需要另外下载。本节共有1个视频,根据需要选择即时播放。
视频清单
①铝、氧化铝与盐酸的反应
②铝、氧化铝与氢氧化钠溶液的反应
致老师和同学们
新课导入
生活中常见的金属材料
1
金属材料 铁合金
合金是由两种或两种以上的金属或金属与非金属熔合而成的具有金属特性的物质。
金属材料
纯金属
合金
80多种
几千种
生活中用到的金属材料是纯金属较多还是合金较多?为什么?
合金多
合金的性能比纯金属更优良
常见合金的硬度会比其成分金属大,合金的熔点一般比成分金属低。
一、金属材料 铁合金
1.金属材料
纯金属只有一种金属原子,排列很整齐
合金中有多种原子,且原子的大小不同,原子排列不规则
掺杂其他原子
形成合金
微观上原子的排列不同,导致了宏观上金属材料的性能不同。
一、金属材料 铁合金
1.金属材料
(1)组成:
指铁(含量高)与其他金属或非金属熔合而成的一类合金
(2)分类:
生铁
钢
铁合金
含碳量不同
含碳量在2%~4.3%之间
含碳量在0.03%~2%之间
硬度大、性脆、抗压、可以铸造成型、几乎不可可以锻轧
塑性好、强度高、韧性好、机械性能好、抗冲击力强,
可以锻轧和铸造
一、金属材料 铁合金
2.铁合金
钢是用量最大、最广的合金
钢
碳素钢
低碳钢
(含碳0.3%~0.6%)
高碳钢
(含碳0.03%~0.3%)
中碳钢
(含碳0.6%~2% )
合金钢
(特种钢)
在碳素钢中加入铬、锰、钨、硅等合金元素,使其具有特殊性能
钢板、钢丝、钢管
钢轨、车轮、建材
器械、弹簧、刀具
不锈钢是最常见的合金钢,其合金元素是Cr和Ni
一、金属材料 铁合金
2.铁合金
2
铝和铝合金
二、铝和铝合金
(1)铝是地壳中含量最多的金属元素。
(2)铝是一种活泼金属,在常温下就能与空气中的O2发生
反应,表面生成一层致密的氧化铝薄膜。日常常用的铝制
品通常都是由铝合金制造的,其表面总是覆盖着致密的氧
化铝薄膜,保护内部金属不受腐蚀。
1.铝
meiyangyang8602
二、铝和铝合金
2.铝、氧化铝的性质
【实验3-4】 在一支试管中加入5 mL盐酸,再向试管中放入一小块铝片。观察现象。过一段时间后,将点燃的木条放在试管口,你观察到什么现象?
meiyangyang8602
二、铝和铝合金
2.铝、氧化铝的性质
实验现象 铝片逐渐溶解,有无色气泡冒出,将点燃的木条放在试管口有爆鸣声
化学方程式 Al2O3+6HCl=2AlCl3+3H2O
2Al+6HCl=2AlCl3+3H2↑
结论 Al2O3和铝均能与盐酸发生反应
(1)与盐酸反应
meiyangyang8602
二、铝和铝合金
2.铝、氧化铝的性质
【实验3-5】在两支试管中分别加入少量的 NaOH溶液,然后向其中一支试管中放入一小块铝片,向另一支试管中放入用砂纸仔细打磨过(除去表面的氧化膜)的一小块铝片。观察现象。过一段时间后,将点燃的木条分别放在两支试管口,
你观察到什么现象?
meiyangyang8602
二、铝和铝合金
2.铝、氧化铝的性质
实验现象 试管①中铝片逐渐溶解,一开始无气泡产生,一段时间后,有无色气泡冒出,试管②中铝片逐渐溶解,立即产生无色气泡,将点燃的木条放在试管口,都有爆鸣声
化学方程式 Al2O3+2NaOH=2NaAlO2+H2O
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
结论 Al2O3和铝均能与NaOH溶液发生反应
(2)与氢氧化钠溶液反应
两性氧化物:既能与酸反应,又能与碱反应生成盐和水,如:Al2O3。
不可以
meiyangyang8602
氧化物
酸性氧化物
(例如CO2、SO2……)
碱性氧化物
(例如CaO、Na2O、Fe2O3、FeO……)
两性氧化物
(例如Al2O3……)
铝既能与稀盐酸反应又能与NaOH溶液反应,都生成___和氢气。
氧化铝既能与稀盐酸反应又能与NaOH溶液反应,都生成___和水。
盐
盐
Al2O3+6H+===2Al3++3H2O
Al2O3+2OH-===2AlO2-+H2O
2Al+6H+===2Al3++3H2↑
2Al+2OH-+2H2O===2AlO2-+3H2↑
2.铝、氧化铝的性质
二、铝和铝合金
meiyangyang8602
二、铝和铝合金
3.铝合金
向铝中加入少量的合金元素,如Cu、Mg、Si、Mn、Zn及稀土元素等,可制成铝合金。铝合金是目前用途广泛的合金之一。例如,硬铝的密度小、强度高,具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料。
“会飞的金属”
3
新型合金
三、新型合金
近年来,为满足某些尖端技术发展的需要,人们又设计和 合成了许
多新型合金。如:用于贮氢的新型合金Ti Fe合金和La Ni合金;钛
合金、耐热合金和形状记忆合金等广泛应用于航空航天、生物工程
和电子工业等领域。
耐热合金
答案 (1)× (2)× (3)× (4)√ (5)× (6)√ (7)×
对 点 训 练
1.判断正误,正确的打“√”,错误的打“×”。(1)合金中不可能含有非金属元素。( )(2)合金中的金属元素以化合物的形式存在。( )(3)合金中各元素的含量一定,所以合金是纯净物。( )(4)生铁的熔点比铁低,但机械强度和硬度比铁高。( )(5)两性氧化物是既有酸性又有碱性的氧化物。( )(6)等质量的Al与足量的盐酸、NaOH溶液充分反应,生成的H2的物质的量相同。( )(7)等物质的量的盐酸、NaOH溶液与足量Al充分反应,生成的H2的物质的量相同。( )
A
对 点 训 练
2.不锈钢通常不与酸、碱、盐反应,是因为加入了( )A.Ni和Cr B.Ni和AuC.Cr和Au D.Cr和Pt
C
对 点 训 练
3.日常生活中使用的钥匙是由铝合金制成的,而不是由纯铝所制,这主要是因为铝合金的( )A.熔点低 B.耐腐蚀性强C.硬度大 D.密度小
对 点 训 练
4.将未经打磨的铝条分别浸入足量的NaOH溶液和稀硫酸中,写出实验过程中反应的离子方程式:________________________________________。
Al2O3+2OH-===2AlO2-+H2O,
2Al+2OH-+2H2O===2AlO2-+3H2↑,
Al2O3+6H+===2Al3++3H2O,
2Al+6H+===2Al3++3H2↑
谢谢观赏
