1.1.1 反应热 焓变 课件(共42张PPT) 2023-2024学年高二化学人教版选择性必修1
文档属性
| 名称 | 1.1.1 反应热 焓变 课件(共42张PPT) 2023-2024学年高二化学人教版选择性必修1 |  | |
| 格式 | pptx | ||
| 文件大小 | 6.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-13 12:33:46 | ||
图片预览










文档简介
(共42张PPT)
第一章
第一节 第1课时 反应热 焓变
素养 目标
1.能辨识化学反应中的能量转化形式,知道内能是体系内物质的各种能量的总和,能解释化学反应中能量变化的本质,培养宏观辨识与微观探析的化学核心素养。
2.认识化学能与热能的相互转化,知道恒温恒压条件下化学反应的反应热可以用焓变表示。
3.通过实验探究学会测定中和反应的反应热,会分析测定反应热时误差产生的原因,并能采取适当措施减小实验误差,培养学生的科学探究与创新意识。
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
基础落实·必备知识全过关
一、反应热及其测定
1.体系与环境
以盐酸与NaOH溶液的反应为例,我们将试管中的盐酸、NaOH溶液及发生的反应等看作一个反应 ,简称 (又称 ),盛溶液的试管和溶液之外的空气等看作 。
2.反应热
在 条件下,化学反应体系向环境释放或从环境吸收的 ,称为化学反应的 ,简称反应热。
体系
体系
系统
环境
等温
热量
热效应
3.中和反应反应热的测定
(1)原理:根据体系的 和有关物质的 来计算反应热。Q= 。
(2)测定过程
温度变化
比热容
cmΔt
体系的温度
(3)数据处理
某小组用50 mL 0.5 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液进行实验。
设溶液的密度均为1 g·cm-3,反应后溶液的比热容c=4.18 J·g-1·℃-1,反应前体系温度为t1 ℃,反应后体系温度为t2 ℃,则反应放出的热量Q=cmΔt=c·[m(盐酸)+m(NaOH溶液)]·(t2-t1)≈ kJ,那么生成1 mol H2O放出的热量为
常采用碱稍过量的方法保证酸完全中和
4.大量实验测得,在25 ℃和101 kPa下,强酸的稀溶液与强碱的稀溶液发生中和反应生成1 mol H2O时,放出 的热量。
0.418(t2-t1)
16.72(t2-t1) kJ
57.3 kJ
二、反应热与焓变
1.化学反应产生反应热的原因:化学反应前后体系的 发生了变化。内能受 、 和物质的 等影响。
2.焓与焓变
内能
温度
压强
聚集状态
H
生成物
反应物
kJ·mol-1
3.ΔH的正、负规定
放热反应:其焓减小,ΔH为 ,即ΔH 0;
吸热反应:其焓增大,ΔH为 ,即ΔH 0。
4.从微观角度认识反应热的实质
(1)实例:
反应H2(g)+Cl2(g)===2HCl(g)的能量变化如图所示:
负值
<
正值
>
由图可知:
化学键 反应中能量变化 结论
断裂或形成1 mol化学键的能量变化 断裂或形成化学键的总能量变化
H—H 吸收 kJ 共吸收 kJ H2(g)+Cl2(g)
===2HCl(g)的反应热ΔH=
Cl—Cl 吸收 kJ
H—Cl 放出 kJ 共放出 kJ
(2)结论: 时的能量变化是化学反应中能量变化的主要原因。
436
243
679
431
862
-183 kJ· mol-1
化学键断裂和形成
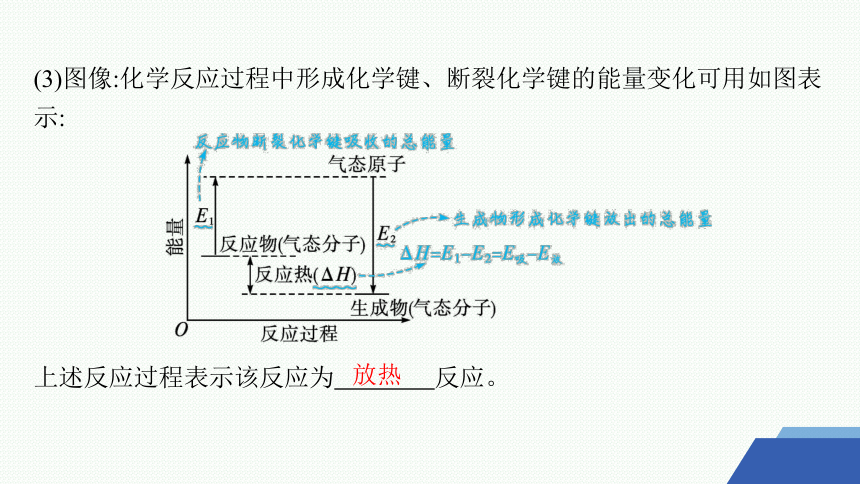
(3)图像:化学反应过程中形成化学键、断裂化学键的能量变化可用如图表示:
上述反应过程表示该反应为 反应。
放热
深化理解
体系与环境只是为了方便人们在研究具体事物时确定所研究的对象而人为划分的,二者并无本质上的区别,也不要求一定存在实际的界面。
反应热概念中的“等温条件下”理解:是指化学反应发生后,使反应体系的温度恢复到反应前体系的温度,即反应前后体系的温度相等。
微思考1
阅读教材“探究——中和反应反应热的测定”。思考:
(1)简易量热计中玻璃搅拌器能否改为金属搅拌器
(2)在盛有盐酸的内筒中加入NaOH溶液时为防止液体溅出而缓慢倒入,是否正确
提示 若把玻璃搅拌器改为金属搅拌器,金属导热性强,导致热量损失多。
提示 在盛有盐酸的内筒中加入NaOH溶液时要迅速倒入,减少溶液混合过程中热量的损失。
易错辨析1
(1)中和反应反应热的测定实验中,一组完整的实验数据至少需要测三次温度。( )
(2)浓硫酸与NaOH溶液反应生成1 mol H2O(l),放出的热量为57.3 kJ。( )
(3)中和反应反应热的测定实验中,应将50 mL 0.55 mol·L-1 NaOH溶液分多次倒入内筒。( )
√
×
提示 浓硫酸稀释时要放出热量,因此浓硫酸与NaOH溶液反应生成1 mol H2O(l),放出的热量大于57.3 kJ。
×
提示 NaOH溶液应一次迅速加入内筒。
(4)中和反应反应热的测定实验中,测定盐酸后的温度计没有冲洗干净,立即测NaOH溶液的温度。( )
×
提示 测量完盐酸的温度后,温度计应冲洗干净并擦干再测NaOH溶液的温度。
微思考2
自学教材“1 mol H2与1 mol Cl2反应生成2 mol HCl时的反应热”一段。思考:
1 mol气态分子AB离解成气态原子A和B所吸收的能量称为键能。试分析如何通过反应物和生成物键能推断反应热ΔH。
提示 ΔH=E(反应物的总键能)-E(生成物的总键能)。
易错辨析2
(1)化学变化中的能量变化都是化学能与热能间的相互转化。( )
(2)所有的化学反应都伴有能量的变化。( )
(3)H2与O2反应生成水、NaOH溶于水都是放热反应。( )
(4)吸热反应的ΔH<0,放热反应的ΔH>0。( )
×
提示 化学变化中的能量变化不仅仅是化学能与热能间的相互转化,还可以存在化学能与光能、电能等能量间的转化。
√
×
提示 NaOH溶于水不是化学反应,不属于放热反应。
×
提示 吸热反应:ΔH>0,放热反应:ΔH<0。
知识拓展
H=U+pV,式中:U为内能,p为压强,V为体积,则有ΔH=ΔU+VΔp+pΔV。
化学反应体系与环境进行能量交换有功和热两种形式。根据能量守恒定律,化学反应中内能的变化等于反应热(Q)和功(W)的加和,即ΔU=Q+W。
当反应中物质的能量变化没有与电能、光能等其他形式的能量发生变化,则有W=-pΔV,此时有ΔH=Q+VΔp,且当反应同时处于等压条件时,即Δp=0,则有ΔH=Q。
重难探究·能力素养全提升
探究一 中和反应反应热的测定
情境探究
在实验室用如图所示装置测定中和反应反应热。
(1)用50 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液,在如图所示的装置中分别进行中和反应反应热的测定,测定的结果是否相同 哪个结果更接近于真实值 为什么
(2)在图2装置中用50 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液、50 mL 0.50 mol·L-1的硝酸与50 mL 0.55 mol·L-1的KOH溶液,分别进行中和反应反应热的测定,测定的结果是否相同
提示 两种装置测定的结果不同。用题图2装置测定的中和反应反应热更接近于真实值。因为题图2装置热量损失少。
提示 相同。盐酸、硝酸都是一元强酸,NaOH和KOH均为一元强碱,反应实质为H++OH-===H2O,上述两组实验中,强酸和强碱的稀溶液反应均生成0.025 mol H2O,因此反应放出热量相同。
(3)谈一谈中和反应反应热的测定实验成功的关键。
提示 中和反应反应热的测定实验成功的关键是比较准确地配制一定物质的量浓度的溶液,量热计要尽量做到保温、绝热且可使体系温度尽快达到一致;在量热的过程中要尽量避免热量的散失。
方法突破
中和反应反应热的测定减少实验误差的方法
名师点拨 测定中和反应反应热的易错点
(1)实验中不能用弱酸或弱碱,因为弱酸、弱碱电离时吸收热量,会使测得的热量数值偏低,ΔH偏高。
(2)不能用浓硫酸代替稀硫酸,因为浓硫酸稀释放热,会使测得的热量数值偏高,ΔH偏低。
(3)在25 ℃和101 kPa下,强酸的稀溶液和强碱的稀溶液发生中和反应生成1 mol H2O放出57.3 kJ的热量,与测定时强酸或强碱的种类、用量无关。
应用体验
视角1中和反应反应热的测定实验
1.50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算中和反应反应热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 。
(2)隔热层的作用是 。
玻璃搅拌器
减少实验过程中的热量损失
(3)倒入NaOH溶液的正确操作是 (填字母)。
a.沿玻璃棒缓慢倒入
b.分三次少量倒入
c.一次迅速倒入
(4)若实验过程中,内筒未加杯盖,求得的中和反应反应热数值 (填“偏大”“偏小”或“无影响”)。
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成的溶液的比热容c=4.18 J·g-1· ℃-1。为了计算中和反应反应热,某学生的实验记录数据如下:
c
偏小
实验 序号 反应物的温度/℃ 反应前体系的温度 t1/℃ 反应后体系的温度t2/℃
盐酸 氢氧化钠溶液
1 20.0 20.1 23.2
2 20.2 20.4 23.4
3 20.3 20.3 24.2
4 20.5 20.6 23.6
完成表格并依据该学生的实验数据计算,该实验中生成1 mol H2O时放出的热量为 kJ(结果保留一位小数)。
20.05
20.3
20.3
20.55
51.8
解析 (5)四次实验(t2-t1)的值分别为3.15、3.1、3.9、3.05,第三次明显偏大,
J=51 832 J≈51.8 kJ。
视角2中和反应热量或反应热大小的比较
2.已知在25 ℃和101 kPa下,强酸的稀溶液和强碱的稀溶液发生中和反应生成1 mol H2O放出57.3 kJ的热量。现分别向1 L 0.5 mol·L-1的Ba(OH)2溶液中加入①浓硫酸、②稀硝酸、③稀醋酸,恰好完全反应的热效应分别为ΔH1、ΔH2、ΔH3,下列关系正确的是( )
A.ΔH1>ΔH2>ΔH3 B.ΔH1<ΔH2<ΔH3
C.ΔH1>ΔH2=ΔH3 D.ΔH1=ΔH2<ΔH3
B
解析 因为浓硫酸溶于水放热,醋酸作为弱酸,电离吸热,则恰好完全反应时放出的热量为①>②>③,所以ΔH1<ΔH2<ΔH3,故B正确。
易错提醒 比较反应热的大小时,应注意反应热ΔH存在“+”“-”号,放热反应ΔH为负值,放出热量越多ΔH越小。
探究二 反应热与焓变
情境探究
1 mol N2(g)和1 mol O2(g)反应生成2 mol NO(g)的能量转化关系如图所示:
(1)根据上图分析N≡N的键能是多少
(2)1 mol NO(g)断键生成N(g)、O(g)所吸收的能量是多少
(3)该反应是吸热反应还是放热反应 (通过计算回答)
提示 946 kJ·mol-1。N、O为同周期元素,原子半径N>O,因此题图中灰球表示N原子。
提示 NO的键能为632 kJ· mol-1,则1 mol NO(g)断键生成N(g)、O(g)吸收632 kJ的能量。
提示 ΔH=946 kJ· mol-1+498 kJ· mol-1-2×632 kJ· mol-1=+180 kJ· mol-1>0,故该反应为吸热反应。
方法突破
1.化学反应的实质和特征
2.吸热反应和放热反应的图像及反应热
名师点拨 反应热计算公式
(1)根据反应物和生成物的焓(或相对能量)计算,公式为
ΔH=H(生成物)-H(反应物);
(2)根据键能或热量变化计算,公式为ΔH=反应物的键能和-生成物的键能和=反应吸收的能量-反应放出的能量。
应用体验
视角1利用键能计算焓变
1.[2023湖南长沙适应性考试]工业上,在一定条件下用乙烯水化法制备乙醇,其化学方程式为CH2==CH2(g)+H2O(g) CH3CH2OH(g)。已知几种化学键的键能如表所示。
化学键 H—C C==C H—O C—O C—C
413.4 615 462.8 351 347.7
根据键能估算该反应的ΔH为( )
A.-34.3 kJ·mol-1 B.+34.3 kJ·mol-1
C.-66 kJ·mol-1 D.+66 kJ·mol-1
A
解析 CH2==CH2(g)+H2O(g) CH3CH2OH(g)的焓变ΔH=反应物总键能之和-生成物总键能之和,结合图表提供的化学键的键能,则
ΔH=615 kJ·mol-1+4×413.4 kJ·mol-1+2×462.8 kJ·mol-1-(5×413.4 kJ·mol-1
+347.7 kJ·mol-1+351 kJ·mol-1+462.8 kJ·mol-1)=-34.3 kJ·mol-1,故选A。
归纳总结 依据键能计算反应热的方法
(1)计算公式:ΔH=反应物的键能和-生成物的键能和。
(2)根据键能计算反应热的关键是正确分析反应物和生成物中所含共价键数目。如:1 mol NH3中含有3 mol N—H。
(3)理解常见物质结构,正确分析物质中化学键数目。如P4结构为
,则1 mol P4中含有6 mol P—P;S8结构为 ,则1 mol S8中含有8 mol S—S;P4O10结构为 ,则1 mol P4O10中含有12 mol P—O和4 mol P==O。
视角2根据图像计算焓变
2.[根据热量变化计算]已知N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量变化如图所示,则该反应的ΔH= ,根据下列已知键能数据计算N—H键能为 kJ·mol-1。
化学键 N≡N H—H
键能/(kJ·mol-1) 946 436.0
-46 kJ·mol-1
391
3.[根据相对能量计算]CO还原NO的反应历程分三步,其中相对能量变化如图:
(1)第一步反应为 (填“吸”或“放”,下同)热反应,第三步反应为______ 热反应。
(2)第二步反应的ΔH= ,总反应的ΔH= 。
吸
放
-513.5 kJ·mol-1
-373.6 kJ·mol-1
易错提醒 根据图像计算反应热时,根据热量数值计算ΔH=E吸-E放,即前-后;根据相对能量计算ΔH=E(生成物)-E(反应物),即后-前。
本 课 结 束
第一章
第一节 第1课时 反应热 焓变
素养 目标
1.能辨识化学反应中的能量转化形式,知道内能是体系内物质的各种能量的总和,能解释化学反应中能量变化的本质,培养宏观辨识与微观探析的化学核心素养。
2.认识化学能与热能的相互转化,知道恒温恒压条件下化学反应的反应热可以用焓变表示。
3.通过实验探究学会测定中和反应的反应热,会分析测定反应热时误差产生的原因,并能采取适当措施减小实验误差,培养学生的科学探究与创新意识。
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
基础落实·必备知识全过关
一、反应热及其测定
1.体系与环境
以盐酸与NaOH溶液的反应为例,我们将试管中的盐酸、NaOH溶液及发生的反应等看作一个反应 ,简称 (又称 ),盛溶液的试管和溶液之外的空气等看作 。
2.反应热
在 条件下,化学反应体系向环境释放或从环境吸收的 ,称为化学反应的 ,简称反应热。
体系
体系
系统
环境
等温
热量
热效应
3.中和反应反应热的测定
(1)原理:根据体系的 和有关物质的 来计算反应热。Q= 。
(2)测定过程
温度变化
比热容
cmΔt
体系的温度
(3)数据处理
某小组用50 mL 0.5 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液进行实验。
设溶液的密度均为1 g·cm-3,反应后溶液的比热容c=4.18 J·g-1·℃-1,反应前体系温度为t1 ℃,反应后体系温度为t2 ℃,则反应放出的热量Q=cmΔt=c·[m(盐酸)+m(NaOH溶液)]·(t2-t1)≈ kJ,那么生成1 mol H2O放出的热量为
常采用碱稍过量的方法保证酸完全中和
4.大量实验测得,在25 ℃和101 kPa下,强酸的稀溶液与强碱的稀溶液发生中和反应生成1 mol H2O时,放出 的热量。
0.418(t2-t1)
16.72(t2-t1) kJ
57.3 kJ
二、反应热与焓变
1.化学反应产生反应热的原因:化学反应前后体系的 发生了变化。内能受 、 和物质的 等影响。
2.焓与焓变
内能
温度
压强
聚集状态
H
生成物
反应物
kJ·mol-1
3.ΔH的正、负规定
放热反应:其焓减小,ΔH为 ,即ΔH 0;
吸热反应:其焓增大,ΔH为 ,即ΔH 0。
4.从微观角度认识反应热的实质
(1)实例:
反应H2(g)+Cl2(g)===2HCl(g)的能量变化如图所示:
负值
<
正值
>
由图可知:
化学键 反应中能量变化 结论
断裂或形成1 mol化学键的能量变化 断裂或形成化学键的总能量变化
H—H 吸收 kJ 共吸收 kJ H2(g)+Cl2(g)
===2HCl(g)的反应热ΔH=
Cl—Cl 吸收 kJ
H—Cl 放出 kJ 共放出 kJ
(2)结论: 时的能量变化是化学反应中能量变化的主要原因。
436
243
679
431
862
-183 kJ· mol-1
化学键断裂和形成
(3)图像:化学反应过程中形成化学键、断裂化学键的能量变化可用如图表示:
上述反应过程表示该反应为 反应。
放热
深化理解
体系与环境只是为了方便人们在研究具体事物时确定所研究的对象而人为划分的,二者并无本质上的区别,也不要求一定存在实际的界面。
反应热概念中的“等温条件下”理解:是指化学反应发生后,使反应体系的温度恢复到反应前体系的温度,即反应前后体系的温度相等。
微思考1
阅读教材“探究——中和反应反应热的测定”。思考:
(1)简易量热计中玻璃搅拌器能否改为金属搅拌器
(2)在盛有盐酸的内筒中加入NaOH溶液时为防止液体溅出而缓慢倒入,是否正确
提示 若把玻璃搅拌器改为金属搅拌器,金属导热性强,导致热量损失多。
提示 在盛有盐酸的内筒中加入NaOH溶液时要迅速倒入,减少溶液混合过程中热量的损失。
易错辨析1
(1)中和反应反应热的测定实验中,一组完整的实验数据至少需要测三次温度。( )
(2)浓硫酸与NaOH溶液反应生成1 mol H2O(l),放出的热量为57.3 kJ。( )
(3)中和反应反应热的测定实验中,应将50 mL 0.55 mol·L-1 NaOH溶液分多次倒入内筒。( )
√
×
提示 浓硫酸稀释时要放出热量,因此浓硫酸与NaOH溶液反应生成1 mol H2O(l),放出的热量大于57.3 kJ。
×
提示 NaOH溶液应一次迅速加入内筒。
(4)中和反应反应热的测定实验中,测定盐酸后的温度计没有冲洗干净,立即测NaOH溶液的温度。( )
×
提示 测量完盐酸的温度后,温度计应冲洗干净并擦干再测NaOH溶液的温度。
微思考2
自学教材“1 mol H2与1 mol Cl2反应生成2 mol HCl时的反应热”一段。思考:
1 mol气态分子AB离解成气态原子A和B所吸收的能量称为键能。试分析如何通过反应物和生成物键能推断反应热ΔH。
提示 ΔH=E(反应物的总键能)-E(生成物的总键能)。
易错辨析2
(1)化学变化中的能量变化都是化学能与热能间的相互转化。( )
(2)所有的化学反应都伴有能量的变化。( )
(3)H2与O2反应生成水、NaOH溶于水都是放热反应。( )
(4)吸热反应的ΔH<0,放热反应的ΔH>0。( )
×
提示 化学变化中的能量变化不仅仅是化学能与热能间的相互转化,还可以存在化学能与光能、电能等能量间的转化。
√
×
提示 NaOH溶于水不是化学反应,不属于放热反应。
×
提示 吸热反应:ΔH>0,放热反应:ΔH<0。
知识拓展
H=U+pV,式中:U为内能,p为压强,V为体积,则有ΔH=ΔU+VΔp+pΔV。
化学反应体系与环境进行能量交换有功和热两种形式。根据能量守恒定律,化学反应中内能的变化等于反应热(Q)和功(W)的加和,即ΔU=Q+W。
当反应中物质的能量变化没有与电能、光能等其他形式的能量发生变化,则有W=-pΔV,此时有ΔH=Q+VΔp,且当反应同时处于等压条件时,即Δp=0,则有ΔH=Q。
重难探究·能力素养全提升
探究一 中和反应反应热的测定
情境探究
在实验室用如图所示装置测定中和反应反应热。
(1)用50 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液,在如图所示的装置中分别进行中和反应反应热的测定,测定的结果是否相同 哪个结果更接近于真实值 为什么
(2)在图2装置中用50 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液、50 mL 0.50 mol·L-1的硝酸与50 mL 0.55 mol·L-1的KOH溶液,分别进行中和反应反应热的测定,测定的结果是否相同
提示 两种装置测定的结果不同。用题图2装置测定的中和反应反应热更接近于真实值。因为题图2装置热量损失少。
提示 相同。盐酸、硝酸都是一元强酸,NaOH和KOH均为一元强碱,反应实质为H++OH-===H2O,上述两组实验中,强酸和强碱的稀溶液反应均生成0.025 mol H2O,因此反应放出热量相同。
(3)谈一谈中和反应反应热的测定实验成功的关键。
提示 中和反应反应热的测定实验成功的关键是比较准确地配制一定物质的量浓度的溶液,量热计要尽量做到保温、绝热且可使体系温度尽快达到一致;在量热的过程中要尽量避免热量的散失。
方法突破
中和反应反应热的测定减少实验误差的方法
名师点拨 测定中和反应反应热的易错点
(1)实验中不能用弱酸或弱碱,因为弱酸、弱碱电离时吸收热量,会使测得的热量数值偏低,ΔH偏高。
(2)不能用浓硫酸代替稀硫酸,因为浓硫酸稀释放热,会使测得的热量数值偏高,ΔH偏低。
(3)在25 ℃和101 kPa下,强酸的稀溶液和强碱的稀溶液发生中和反应生成1 mol H2O放出57.3 kJ的热量,与测定时强酸或强碱的种类、用量无关。
应用体验
视角1中和反应反应热的测定实验
1.50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算中和反应反应热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 。
(2)隔热层的作用是 。
玻璃搅拌器
减少实验过程中的热量损失
(3)倒入NaOH溶液的正确操作是 (填字母)。
a.沿玻璃棒缓慢倒入
b.分三次少量倒入
c.一次迅速倒入
(4)若实验过程中,内筒未加杯盖,求得的中和反应反应热数值 (填“偏大”“偏小”或“无影响”)。
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成的溶液的比热容c=4.18 J·g-1· ℃-1。为了计算中和反应反应热,某学生的实验记录数据如下:
c
偏小
实验 序号 反应物的温度/℃ 反应前体系的温度 t1/℃ 反应后体系的温度t2/℃
盐酸 氢氧化钠溶液
1 20.0 20.1 23.2
2 20.2 20.4 23.4
3 20.3 20.3 24.2
4 20.5 20.6 23.6
完成表格并依据该学生的实验数据计算,该实验中生成1 mol H2O时放出的热量为 kJ(结果保留一位小数)。
20.05
20.3
20.3
20.55
51.8
解析 (5)四次实验(t2-t1)的值分别为3.15、3.1、3.9、3.05,第三次明显偏大,
J=51 832 J≈51.8 kJ。
视角2中和反应热量或反应热大小的比较
2.已知在25 ℃和101 kPa下,强酸的稀溶液和强碱的稀溶液发生中和反应生成1 mol H2O放出57.3 kJ的热量。现分别向1 L 0.5 mol·L-1的Ba(OH)2溶液中加入①浓硫酸、②稀硝酸、③稀醋酸,恰好完全反应的热效应分别为ΔH1、ΔH2、ΔH3,下列关系正确的是( )
A.ΔH1>ΔH2>ΔH3 B.ΔH1<ΔH2<ΔH3
C.ΔH1>ΔH2=ΔH3 D.ΔH1=ΔH2<ΔH3
B
解析 因为浓硫酸溶于水放热,醋酸作为弱酸,电离吸热,则恰好完全反应时放出的热量为①>②>③,所以ΔH1<ΔH2<ΔH3,故B正确。
易错提醒 比较反应热的大小时,应注意反应热ΔH存在“+”“-”号,放热反应ΔH为负值,放出热量越多ΔH越小。
探究二 反应热与焓变
情境探究
1 mol N2(g)和1 mol O2(g)反应生成2 mol NO(g)的能量转化关系如图所示:
(1)根据上图分析N≡N的键能是多少
(2)1 mol NO(g)断键生成N(g)、O(g)所吸收的能量是多少
(3)该反应是吸热反应还是放热反应 (通过计算回答)
提示 946 kJ·mol-1。N、O为同周期元素,原子半径N>O,因此题图中灰球表示N原子。
提示 NO的键能为632 kJ· mol-1,则1 mol NO(g)断键生成N(g)、O(g)吸收632 kJ的能量。
提示 ΔH=946 kJ· mol-1+498 kJ· mol-1-2×632 kJ· mol-1=+180 kJ· mol-1>0,故该反应为吸热反应。
方法突破
1.化学反应的实质和特征
2.吸热反应和放热反应的图像及反应热
名师点拨 反应热计算公式
(1)根据反应物和生成物的焓(或相对能量)计算,公式为
ΔH=H(生成物)-H(反应物);
(2)根据键能或热量变化计算,公式为ΔH=反应物的键能和-生成物的键能和=反应吸收的能量-反应放出的能量。
应用体验
视角1利用键能计算焓变
1.[2023湖南长沙适应性考试]工业上,在一定条件下用乙烯水化法制备乙醇,其化学方程式为CH2==CH2(g)+H2O(g) CH3CH2OH(g)。已知几种化学键的键能如表所示。
化学键 H—C C==C H—O C—O C—C
413.4 615 462.8 351 347.7
根据键能估算该反应的ΔH为( )
A.-34.3 kJ·mol-1 B.+34.3 kJ·mol-1
C.-66 kJ·mol-1 D.+66 kJ·mol-1
A
解析 CH2==CH2(g)+H2O(g) CH3CH2OH(g)的焓变ΔH=反应物总键能之和-生成物总键能之和,结合图表提供的化学键的键能,则
ΔH=615 kJ·mol-1+4×413.4 kJ·mol-1+2×462.8 kJ·mol-1-(5×413.4 kJ·mol-1
+347.7 kJ·mol-1+351 kJ·mol-1+462.8 kJ·mol-1)=-34.3 kJ·mol-1,故选A。
归纳总结 依据键能计算反应热的方法
(1)计算公式:ΔH=反应物的键能和-生成物的键能和。
(2)根据键能计算反应热的关键是正确分析反应物和生成物中所含共价键数目。如:1 mol NH3中含有3 mol N—H。
(3)理解常见物质结构,正确分析物质中化学键数目。如P4结构为
,则1 mol P4中含有6 mol P—P;S8结构为 ,则1 mol S8中含有8 mol S—S;P4O10结构为 ,则1 mol P4O10中含有12 mol P—O和4 mol P==O。
视角2根据图像计算焓变
2.[根据热量变化计算]已知N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量变化如图所示,则该反应的ΔH= ,根据下列已知键能数据计算N—H键能为 kJ·mol-1。
化学键 N≡N H—H
键能/(kJ·mol-1) 946 436.0
-46 kJ·mol-1
391
3.[根据相对能量计算]CO还原NO的反应历程分三步,其中相对能量变化如图:
(1)第一步反应为 (填“吸”或“放”,下同)热反应,第三步反应为______ 热反应。
(2)第二步反应的ΔH= ,总反应的ΔH= 。
吸
放
-513.5 kJ·mol-1
-373.6 kJ·mol-1
易错提醒 根据图像计算反应热时,根据热量数值计算ΔH=E吸-E放,即前-后;根据相对能量计算ΔH=E(生成物)-E(反应物),即后-前。
本 课 结 束
