2.2.1.氯气的性质课件(共21张PPT)2023-2024学年高一上学期人教版(2019)必修第一册
文档属性
| 名称 | 2.2.1.氯气的性质课件(共21张PPT)2023-2024学年高一上学期人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 14.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-13 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
氯气的性质(第一课时)
年 级:高一 学 科:化学(人教版)
主讲人: 学 校:
学习目标 学习重难点
1.通过实验探究氯气的主要化学性质 2.能正确写出氯气与金属、与氢气反应的化学方程式 3.学会对实验现象进行描述 重点:认识氯气的相关性质
难点:掌握研究物质性质的方法
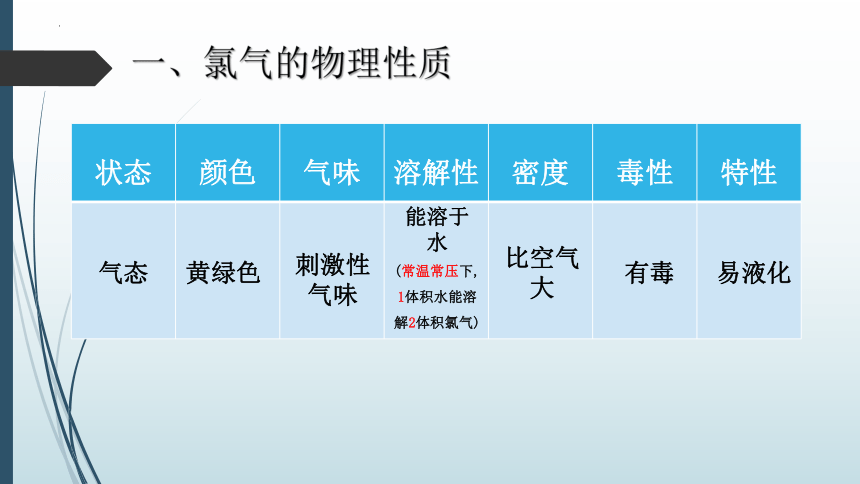
一、氯气的物理性质
状态 颜色 气味 溶解性 密度 毒性 特性
气态
黄绿色
刺激性
气味
能溶于水
(常温常压下,
1体积水能溶解2体积氯气)
比空气大
有毒
易液化
【自主思考】
1.你知道通常从哪些方面认识物质的物理性质吗?
物理性质一般包括颜色、状态、气味、密度、硬度、熔点、沸点等。所以在观察时要客观地全方位地观察,如果使用的药品有毒或有腐蚀性,取用时要注意安全。
2.实验室中怎样安全地闻气体气味?
稍打开集气瓶的玻璃片,用手轻轻在瓶口扇动,仅使极少量的气体飘进鼻孔。
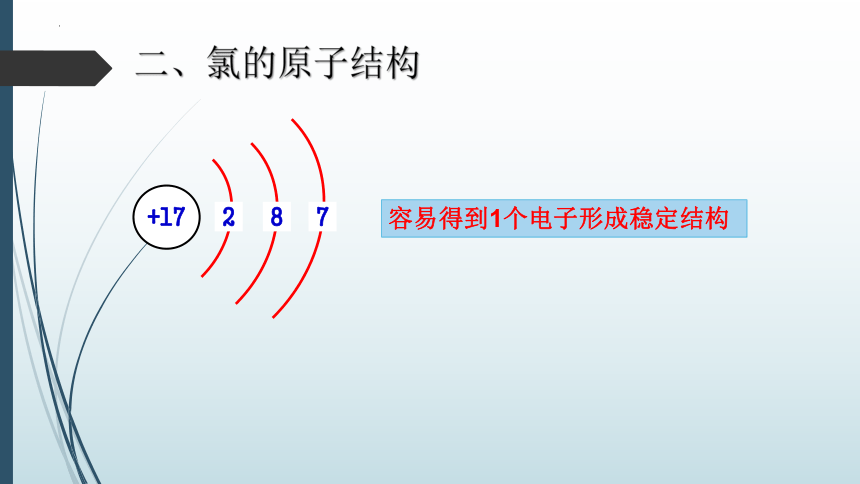
二、氯的原子结构
+17
2
8
7
容易得到1个电子形成稳定结构
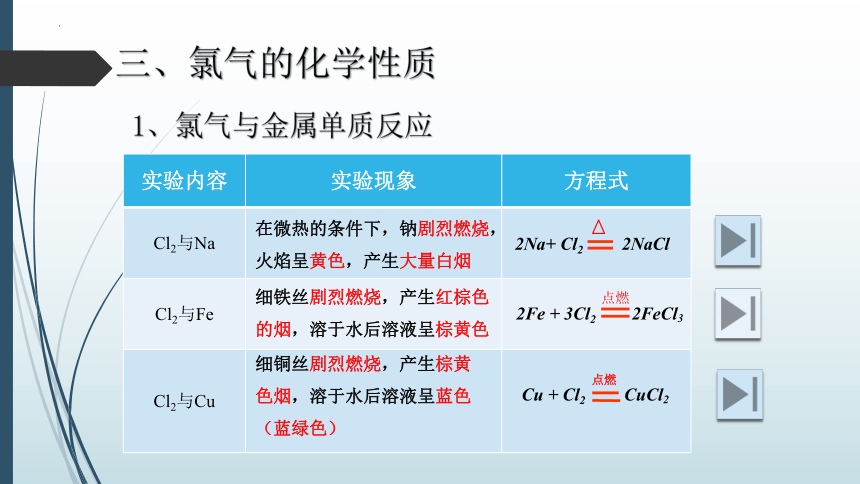
三、氯气的化学性质
1、氯气与金属单质反应
实验内容 实验现象 方程式
Cl2与Na
Cl2与Fe
Cl2与Cu
2Fe + 3Cl2 2FeCl3
点燃
Cu + Cl2 CuCl2
点燃
在微热的条件下,钠剧烈燃烧,火焰呈黄色,产生大量白烟
细铁丝剧烈燃烧,产生红棕色的烟,溶于水后溶液呈棕黄色
细铜丝剧烈燃烧,产生棕黄色烟,溶于水后溶液呈蓝色(蓝绿色)
2Na+ Cl2 2NaCl
【注意】
氯气与除金、铂以外的绝大多数金属都能反应。变价金属单质与氯气反应,一般生成最高价氯化物,例:过量的铁丝在氯气中燃烧时,生成FeCl3而不生成FeCl2.
常温下,干燥的Cl2不与铁反应,故工业上常用钢瓶贮存液氯。
实验内容 实验现象 方程式
H2在Cl2中点燃
H2与Cl2的混合气体光照
H2 + Cl2 === 2HCl
点燃
H2 + Cl2 === 2HCl
光照
2、氯气与非金属单质反应
安静的燃烧,发出苍白色火焰,集气瓶口有白雾
剧烈反应,发生爆炸
【注意】
为了保证实验安全,氢气在点燃之前必须验纯,只有符合点燃纯度要求的氢气才能点燃。
H2和Cl2混合,在强光照射下会发生反应,但容易爆炸,因此实际工业生产中,用点燃的方法生产HCl, HCl溶于水即得盐酸。
【自主思考】
1.燃烧反应必须有氧气参加么?
可燃物与氧化剂(如:O2、Cl2等)在一定条件下(点燃、灼烧等)发生发光、发热的剧烈反应都可以称为燃烧。
即燃烧不一定有氧气参与。如:Na、Fe、Cu等均可以在氯气中燃烧。
2.为什么有的实验看到的是烟,有的是雾?
物质 成分 举例
烟
雾
固体小颗粒
液体小液滴
Fe在氯气中燃烧产生红棕色的烟——FeCl3固体颗粒
H2在Cl2中燃烧生成的HCl气体遇到水蒸气形成白雾
【典题例证3】下列氯的化合物中,不能由氯气和相应的金属反应来制取的是( )
A、FeCl3 B、CaCl2 C、FeCl2 D、KCl
解析 变价金属单质与氯气反应,一般生成最高价氯化物
答案 C
四、总结
1、氯气的物理性质
四、总结
2、氯气的化学性质
四、总结
2、氯气的化学性质
氯气的性质(第一课时)
年 级:高一 学 科:化学(人教版)
主讲人: 学 校:
学习目标 学习重难点
1.通过实验探究氯气的主要化学性质 2.能正确写出氯气与金属、与氢气反应的化学方程式 3.学会对实验现象进行描述 重点:认识氯气的相关性质
难点:掌握研究物质性质的方法
一、氯气的物理性质
状态 颜色 气味 溶解性 密度 毒性 特性
气态
黄绿色
刺激性
气味
能溶于水
(常温常压下,
1体积水能溶解2体积氯气)
比空气大
有毒
易液化
【自主思考】
1.你知道通常从哪些方面认识物质的物理性质吗?
物理性质一般包括颜色、状态、气味、密度、硬度、熔点、沸点等。所以在观察时要客观地全方位地观察,如果使用的药品有毒或有腐蚀性,取用时要注意安全。
2.实验室中怎样安全地闻气体气味?
稍打开集气瓶的玻璃片,用手轻轻在瓶口扇动,仅使极少量的气体飘进鼻孔。
二、氯的原子结构
+17
2
8
7
容易得到1个电子形成稳定结构
三、氯气的化学性质
1、氯气与金属单质反应
实验内容 实验现象 方程式
Cl2与Na
Cl2与Fe
Cl2与Cu
2Fe + 3Cl2 2FeCl3
点燃
Cu + Cl2 CuCl2
点燃
在微热的条件下,钠剧烈燃烧,火焰呈黄色,产生大量白烟
细铁丝剧烈燃烧,产生红棕色的烟,溶于水后溶液呈棕黄色
细铜丝剧烈燃烧,产生棕黄色烟,溶于水后溶液呈蓝色(蓝绿色)
2Na+ Cl2 2NaCl
【注意】
氯气与除金、铂以外的绝大多数金属都能反应。变价金属单质与氯气反应,一般生成最高价氯化物,例:过量的铁丝在氯气中燃烧时,生成FeCl3而不生成FeCl2.
常温下,干燥的Cl2不与铁反应,故工业上常用钢瓶贮存液氯。
实验内容 实验现象 方程式
H2在Cl2中点燃
H2与Cl2的混合气体光照
H2 + Cl2 === 2HCl
点燃
H2 + Cl2 === 2HCl
光照
2、氯气与非金属单质反应
安静的燃烧,发出苍白色火焰,集气瓶口有白雾
剧烈反应,发生爆炸
【注意】
为了保证实验安全,氢气在点燃之前必须验纯,只有符合点燃纯度要求的氢气才能点燃。
H2和Cl2混合,在强光照射下会发生反应,但容易爆炸,因此实际工业生产中,用点燃的方法生产HCl, HCl溶于水即得盐酸。
【自主思考】
1.燃烧反应必须有氧气参加么?
可燃物与氧化剂(如:O2、Cl2等)在一定条件下(点燃、灼烧等)发生发光、发热的剧烈反应都可以称为燃烧。
即燃烧不一定有氧气参与。如:Na、Fe、Cu等均可以在氯气中燃烧。
2.为什么有的实验看到的是烟,有的是雾?
物质 成分 举例
烟
雾
固体小颗粒
液体小液滴
Fe在氯气中燃烧产生红棕色的烟——FeCl3固体颗粒
H2在Cl2中燃烧生成的HCl气体遇到水蒸气形成白雾
【典题例证3】下列氯的化合物中,不能由氯气和相应的金属反应来制取的是( )
A、FeCl3 B、CaCl2 C、FeCl2 D、KCl
解析 变价金属单质与氯气反应,一般生成最高价氯化物
答案 C
四、总结
1、氯气的物理性质
四、总结
2、氯气的化学性质
四、总结
2、氯气的化学性质
