2.3 芳香烃课件(共53张PPT) 2023-2024学年高二化学人教版选择性必修3
文档属性
| 名称 | 2.3 芳香烃课件(共53张PPT) 2023-2024学年高二化学人教版选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-13 00:00:00 | ||
图片预览









文档简介
(共53张PPT)
第二章
第三节 芳香烃
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
素养目标 1.通过化学键的特殊性理解苯及其同系物的结构特点,进而理解苯和苯的同系物的性质及应用,理解有机反应类型与分子结构特点的关系,形成宏观辨识与微观探析的学科核心素养。
2.通过采用模型、符号等多种方式对苯及其同系物的空间结构进行综合表征,形成证据推理与模型认知的学科核心素养。
3.根据预测设计实验探究芳香烃可能具有的化学性质,完成实验操作,能对观察记录的实验信息进行分析、归纳、总结,得出实验结论,形成科学探究与创新意识的学科核心素养。
基础落实·必备知识全过关
一、苯的结构和性质
1.物理性质
颜色、状态 气味 密度 溶解性 挥发性
色液体 有特殊气味 比水 溶于水, 溶于有机溶剂 沸点较低,
挥发
无
小
不
易
易
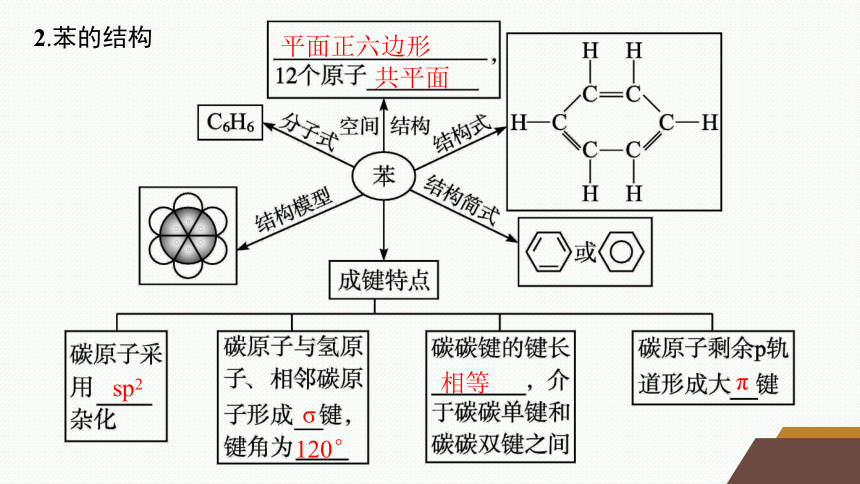
2.苯的结构
平面正六边形
共平面
sp2
σ
120°
相等
π
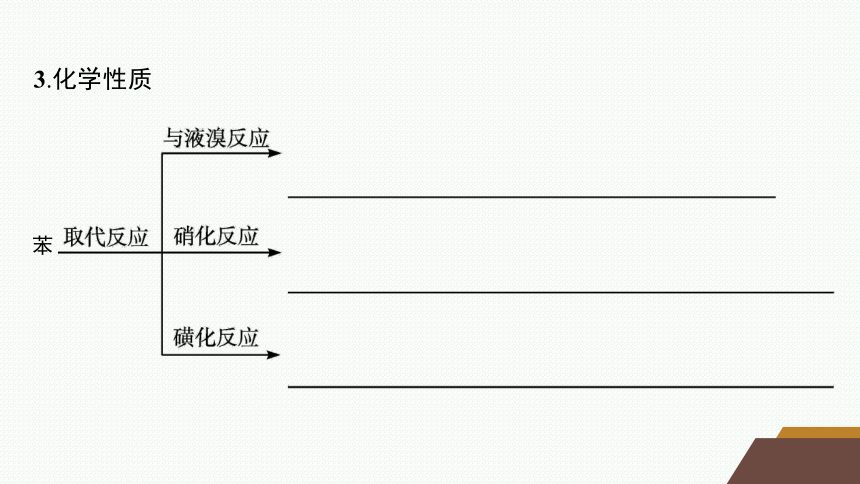
3.化学性质
苯
火焰明亮,产生浓重的黑烟
二、苯的同系物
1.组成和结构特点
烷基
一
烷基
CnH2n-6(n>6)
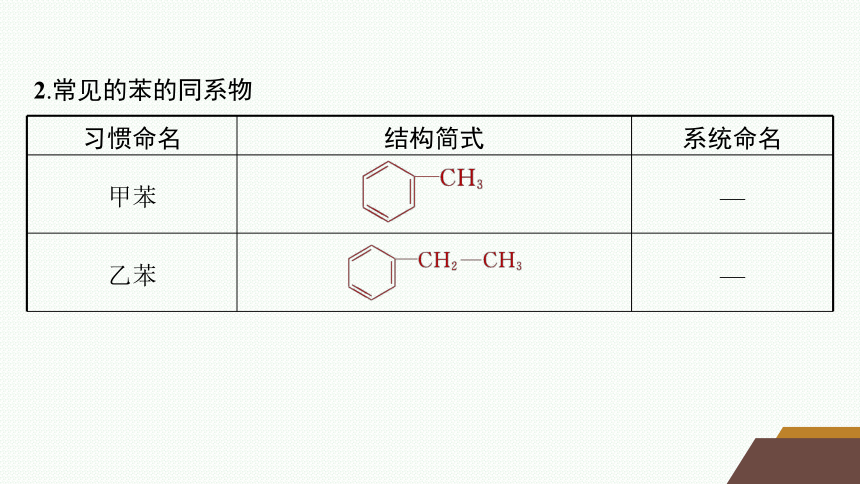
2.常见的苯的同系物
习惯命名 结构简式 系统命名
甲苯 —
乙苯 —
习惯命名 结构简式 系统命名
二 甲 苯 邻二甲苯
间二甲苯
对二甲苯
1,2-二甲苯
1,3-二甲苯
1,4-二甲苯
3.物理性质
颜色、状态 气味 密度 溶解性
一般为 色液体 有类似苯的气味 比水 溶于水, 溶于有机溶剂
无
小
不
易
4.化学性质(以甲苯为例)
甲苯
紫红色褪去
甲基
深度思考1
提示 苯乙烯属于芳香烃,苯甲酸除含有C、H元素外,还含有O元素,不属于烃类。
(2)苯的结构简式可写为“ ”,说明苯分子中碳碳单键和碳碳双键是交替排列的。这种说法是否正确
(3) 分子中共面的碳原子最多有几个
提示 不正确。苯分子中不存在典型的碳碳单键和碳碳双键。
提示 8。苯环上的6个C原子一定共面,碳碳双键上的两个C原子共面,单键可以旋转,所以最多可有8个碳原子共面。
易错辨析1
(1)标准状况下,22.4 L苯含有碳碳双键的数目为3NA(NA表示阿伏加德罗常数的值)。( )
(2)一般用分液的方法分离苯和水的混合物。( )
(3)苯与液溴混合后加入铁粉可发生取代反应。( )
(4) 是芳香族化合物,但不是芳香烃。( )
×
提示 标准状况下,苯为液态且苯分子结构中不含有典型的碳碳双键。
√
√
√
教材拓展
苯的同系物的命名
采用系统命名法命名,当苯环上有多个取代基时,苯环上的编号必须符合取代基位次之和最小的原则。而当用取代基位次之和最小原则无法确定哪一种编号正确时,应保证较简单的取代基位次尽可能小。例如:
4-甲基-2-乙基-1-丙基苯
1-甲基-3,5-二乙基苯
深度思考2
(1)怎样通过实验来区别苯和甲苯
(2)写出甲苯和氯气在光照下反应生成一氯代物的化学方程式。
提示 分别取两种液体少量,加入酸性KMnO4溶液,使其褪色的为甲苯,不褪色的为苯。
易错辨析2
(1)苯的邻位二元取代物只有一种,能证明苯分子中不存在单、双键交替结构。( )
(2)符合CnH2n-6(n≥6)通式的有机化合物一定是苯及其同系物。( )
(3)甲苯分子中所有的原子在同一平面上。( )
√
×
提示 符合CnH2n-6(n≥6)通式的有机化合物分子中可能含有多个碳碳双键或碳碳三键,如CH≡C—CH2—C≡C—CH3。
×
提示 甲苯分子的甲基中至少有2个氢原子与其他原子不在同一平面上。
(4)乙苯的一氯代物有5种。( )
(5)等物质的量的苯、甲苯与足量H2加成时,消耗H2的量相同。( )
√
提示 乙苯的一氯代物有5种,氯原子取代位置如图: 。
√
提示 苯、甲苯与H2加成时,都是苯环发生反应。
重难探究·能力素养全提升
情境探究
探究一 苯的分子结构和性质
科学家通过蒸馏苯甲酸和石灰的混合物,将得到的一种液体命名为苯,又通过实验确定了苯的相对分子质量为78,分子式为C6H6。对于如何确定苯的结构式,却成了摆在化学家们面前的难题:苯的碳、氢比值如此之大,表明苯是高度不饱和的化合物,但它又不具有典型的不饱和化合物应具有的易发生加成反应的性质。
思考交流:
1.苯和乙烯都能使溴水褪色,二者褪色的原理相同吗
提示 不相同。苯因萃取溴水中的Br2而使溴水褪色,而乙烯因与Br2发生加成反应而使溴水褪色,二者褪色的原理不相同。
2.一定条件下,苯、甲烷和乙烯均能与溴反应,条件相同吗 反应类型相同吗
提示 苯与液溴在FeBr3作催化剂时才能反应,甲烷与溴蒸气在光照时反应,乙烯与溴水或溴的CCl4溶液在常温下反应,三者反应类型分别是取代反应、取代反应和加成反应。
3.苯分子实际上不具有碳碳单键和碳碳双键的简单交替结构,可以作为证据的事实有哪些
①苯的间位二元取代物只有一种。
②苯的邻位二元取代物只有一种。
③苯不能使酸性KMnO4溶液褪色。
④苯能在一定条件下与氢气反应生成环己烷。
⑤苯在FeBr3存在的条件下与液溴发生取代反应。
方法突破
1.苯的分子结构
(1)苯分子中碳原子采取sp2杂化,除σ键外还含有大π键。苯分子为平面形结构,分子中的6个碳原子和6个氢原子共平面。
(2)苯分子不存在单双键交替结构,可以从以下几个方面证明:
①苯分子中六个碳碳键均等长,六元碳环呈平面正六边形;
②碳碳双键能使酸性KMnO4溶液褪色,但苯不能;
③邻二氯苯只有一种结构,而若为单双键交替应有两种结构
2.苯的化学性质
应用体验
视角1苯分子的结构
1.下列关于苯的说法正确的是( )
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式( )看,苯分子中含有碳碳双键,应属于烯烃
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同
D
解析 苯的分子式是C6H6,不能使酸性KMnO4溶液褪色,属于不饱和烃,故A错误;苯分子中不含有碳碳双键,不属于烯烃,故B错误;在催化剂作用下,苯与液溴反应生成溴苯,发生取代反应,故C错误;苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的化学键,故D正确。
视角2苯和烷烃性质的比较
2.下列反应中,属于取代反应的是( )
A.苯在氯化铁存在时与氯单质的反应
B.苯在镍作催化剂时与氢气的反应
C.苯在空气中燃烧
D.苯与碘水混合振荡
A
解析 A项是取代反应;B项是加成反应;C项是氧化反应;D项是物理过程。
【变式设问】
(1)将苯加入碘水中,充分振荡,有什么现象
(2)将苯加入碘水中,充分振荡后出现的现象是发生化学变化产生的吗
提示 液体分层,上层呈紫红色。
提示 不是。是苯萃取了碘水中的碘单质,发生了物理变化。
3.下列关于苯的叙述正确的是( )
A.反应①为加成反应
B.反应④中1 mol苯最多与3 mol H2发生加成反应,是因为苯分子含有三个碳碳双键
C.反应③为取代反应,有机产物是一种烃
D.反应②为氧化反应,反应现象是火焰明亮并带有浓烟
D
解析 反应①是苯和液溴在FeBr3的催化作用下生成溴苯和溴化氢,故为取代反应,A错误;苯分子中不存在碳碳单键和碳碳双键的交替现象,苯环上的6个碳碳键均为介于碳碳单键和碳碳双键之间独特的键,B错误;反应③是苯在浓硫酸作用下与浓硝酸反应生成硝基苯和水,故为取代反应,有机产物是硝基苯,不属于烃,而是烃的衍生物,C错误;反应②是苯的燃烧反应,故为氧化反应,反应现象是火焰明亮并带有浓烟,D正确。
视角3苯和烯烃性质的比较
4.科学家对物质性质的推断一般要基于一些实验事实。下列能说明苯与一般的烯烃性质不同的事实是( )
A.苯分子是高度对称的平面形分子
B.苯不溶于水
C.苯不与酸性KMnO4溶液反应
D.1 mol苯在一定条件下可与3 mol氯气发生加成反应
C
解析 乙烯的分子结构也是一个高度对称的平面形结构,故A不符合题意;苯是芳香烃,不溶于水,故B不符合题意;苯中不含碳碳双键,因此不能被酸性高锰酸钾溶液氧化,故C符合题意;苯和含三个碳碳双键的烯烃均可以与氯气发生加成反应,而且比例一致,故D不符合题意。
5.下列区分苯和己烯的实验方法和判断正确的是( )
A.分别点燃,没有烟生成的是苯
B.分别加入少量溴水振荡,静置后分层,下层橙黄色消失的是己烯
C.分别加入溴的CCl4溶液振荡,静置后分层,上下两层均为无色的是己烯
D.分别加入酸性KMnO4溶液振荡,紫红色消失的是己烯
D
解析 苯、己烯燃烧时都会产生烟,A错误;分别加入溴水振荡,下层橙黄色均消失,B错误;分别加入溴的CCl4溶液都不分层,C错误;苯不能使酸性KMnO4溶液褪色,但己烯可以,D正确。
情境探究
探究二 苯和苯的同系物性质的差异
实验1:向两支分别盛有少量酸性KMnO4溶液和溴的四氯化碳溶液的试管中滴入苯,振荡试管,静置。
实验2:向盛有少量酸性KMnO4溶液和溴的四氯化碳溶液的试管中滴入甲苯,振荡试管,静置。
1.向盛有酸性KMnO4溶液的试管中分别滴加苯和甲苯,用力振荡,静置,观察到的现象是什么 为什么
2.向盛有溴的四氯化碳溶液的试管中分别滴加苯和甲苯,用力振荡,静置,观察到的现象是什么 为什么 若将溴的四氯化碳溶液改为溴水呢
提示 滴加苯的试管,溶液分层,上层无色,下层为紫红色;滴加甲苯的试管,溶液不分层,为无色。原因:苯不能被酸性KMnO4溶液氧化;甲苯中苯环使甲基活化,能被酸性KMnO4溶液氧化,紫红色褪去。
提示 两试管中均得到均一、稳定的橙红色液体。原因:苯和甲苯均能溶于四氯化碳得到均一、稳定的液体混合物。若将溴的四氯化碳溶液改为溴水,两试管中液体分层,上层为橙红色,下层无色。原因:苯和甲苯能萃取溴水中的溴。
3.常见的烃中,能使酸性KMnO4溶液褪色的有哪些
提示 烯烃、炔烃、苯的某些同系物。
方法突破
苯和苯的同系物的比较
类别 苯 苯的同系物
相 同 点 分子 构成 ①分子中都含有一个苯环 ②都符合分子式通式CnH2n-6
化学 性质 ①燃烧时现象相同,火焰明亮,伴有浓烟 ②都易发生苯环上的取代反应 ③都能发生苯环的加成反应,但反应都比较困难
类别 苯 苯的同系物
不 同 点 易发生取代反应主要得到一元取代产物 更容易发生取代反应常得到多元取代产物
难被氧化,不能使酸性KMnO4溶液褪色 易被氧化,能使酸性KMnO4溶液褪色
差异 原因 苯的同系物分子中,苯环与侧链相互影响,苯环影响侧链,使侧链烃基性质活泼而易被氧化。侧链烃基影响苯环,使苯环邻、对位的氢更活泼而易被取代
应用体验
视角1苯的同系物的判断
1.下列有机化合物中,属于苯的同系物的是( )
D
解析 同系物是指结构相似,在分子组成上相差若干个CH2原子团的物质。A项,该结构是苯,不符合题意;B项,除了苯环,还含有碳碳双键,不饱和度与苯不同,不符合题意;C项,没有苯环,与苯结构不相似,不符合题意;D项,符合同系物的定义,符合题意。
视角2苯和苯的同系物性质的比较
2.下列反应只能得到一种有机化合物的是( )
A.丙烯与HCl发生反应
B.在FeBr3催化下,甲苯与液溴反应
C.乙苯与酸性高锰酸钾溶液反应
D.甲苯在光照条件下与Cl2反应
C
解析 丙烯和HCl发生加成反应生成1-氯丙烷或2-氯丙烷,所以有两种有机化合物生成,A不符合题意;在FeBr3催化下,甲苯与液溴反应可以生成邻溴甲苯、对溴甲苯或二溴甲苯、三溴甲苯等,B不符合题意;乙苯与酸性高锰酸钾溶液反应只生成一种有机化合物苯甲酸,C符合题意;甲苯与氯气在光照条件下发生取代反应,甲基上的氢原子可能有一个被取代、两个被取代或三个被取代,产物有多种,D不符合题意。
3.甲苯是苯的同系物,化学性质与苯相似,但由于基团之间的相互影响,使甲苯的某些性质又与苯不同。下列有关推断及解释都正确的是( )
A.苯不能通过化学反应使溴水褪色,但甲苯可以,这是甲基对苯环影响的结果
B.苯不能在光照下与Cl2发生取代反应,但甲苯可以,这是苯环对甲基影响的结果
C.苯的一氯代物只有一种,而甲苯的苯环上一氯代物有3种,这是苯环对甲基影响的结果
D.甲烷不能使酸性KMnO4溶液褪色,但甲苯可以,这是苯环对甲基影响的结果
D
解析 苯与甲苯均不含碳碳双键,都不能使溴水褪色,故A错误;苯不能在光照下与Cl2发生取代反应,但甲苯可以,是因为甲基上的氢原子容易被取代,与苯环的影响无关,故B错误;苯的一氯代物只有一种,而甲苯苯环上的一氯代物有3种,是因为苯分子中的氢原子完全相同,而甲苯苯环上有3种不同环境下的氢原子,与苯环对甲基影响无关,故C错误;甲烷不能使酸性KMnO4溶液褪色,但甲苯可以,这是苯环对甲基影响的结果,故D正确。
视角3与芳香烃有关的鉴别与除杂
4.下列有机化合物鉴别方法不正确的是( )
A.将乙烯和甲烷分别通入酸性高锰酸钾溶液中,观察溶液颜色是否变化
B.将溴水分别加入四氯化碳和苯中,观察溶液颜色及是否分层
C.苯和己烷分别放入水中,观察液体是否分层
D.甲苯和硝基苯分别放入水中,观察液体是否分层
C
解析 乙烯能与酸性高锰酸钾溶液反应并使其褪色,而甲烷不能,可鉴别,故A正确;Br2易溶于四氯化碳和苯,四氯化碳和苯都不溶于水,可从溴水中萃取出Br2,但四氯化碳的密度比水大,苯的密度比水小,分层后有机层(含Br2)位置不同,可鉴别,故B正确;苯和己烷都不溶于水,密度均比水小,放入水中都分层,现象相同,不能鉴别,故C错误;甲苯和硝基苯都不溶于水,但硝基苯的密度比水大,甲苯的密度比水小,分层后有机层位置不同,可鉴别,故D正确。
视角3苯的同系物的结构
5.[2023江西南昌高二检测]某烃的分子式为C10H14,它不能使溴水因发生化学反应而褪色,但可使酸性KMnO4溶液褪色,分子结构中只含有两个不相同烷基,符合条件的烃有( )
A.3种 B.4种 C.5种 D.6种
D
解析 该烃不能使溴水因发生化学反应而褪色,可使酸性KMnO4溶液褪色,可判断该烃为苯的同系物;分子结构中含有两个不相同的烷基,则一个为甲基,另一个为丙基(—CH2—CH2—CH3、 ),而两个烷基在苯环上
有邻、间、对三种位置,故符合条件的烃共有6种。
【变式设问】
C10H14的一种同系物为C9H12,含有苯环,核磁共振氢谱只有两种氢原子,且所有碳原子共平面,写出其结构简式。
本 课 结 束
第二章
第三节 芳香烃
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
素养目标 1.通过化学键的特殊性理解苯及其同系物的结构特点,进而理解苯和苯的同系物的性质及应用,理解有机反应类型与分子结构特点的关系,形成宏观辨识与微观探析的学科核心素养。
2.通过采用模型、符号等多种方式对苯及其同系物的空间结构进行综合表征,形成证据推理与模型认知的学科核心素养。
3.根据预测设计实验探究芳香烃可能具有的化学性质,完成实验操作,能对观察记录的实验信息进行分析、归纳、总结,得出实验结论,形成科学探究与创新意识的学科核心素养。
基础落实·必备知识全过关
一、苯的结构和性质
1.物理性质
颜色、状态 气味 密度 溶解性 挥发性
色液体 有特殊气味 比水 溶于水, 溶于有机溶剂 沸点较低,
挥发
无
小
不
易
易
2.苯的结构
平面正六边形
共平面
sp2
σ
120°
相等
π
3.化学性质
苯
火焰明亮,产生浓重的黑烟
二、苯的同系物
1.组成和结构特点
烷基
一
烷基
CnH2n-6(n>6)
2.常见的苯的同系物
习惯命名 结构简式 系统命名
甲苯 —
乙苯 —
习惯命名 结构简式 系统命名
二 甲 苯 邻二甲苯
间二甲苯
对二甲苯
1,2-二甲苯
1,3-二甲苯
1,4-二甲苯
3.物理性质
颜色、状态 气味 密度 溶解性
一般为 色液体 有类似苯的气味 比水 溶于水, 溶于有机溶剂
无
小
不
易
4.化学性质(以甲苯为例)
甲苯
紫红色褪去
甲基
深度思考1
提示 苯乙烯属于芳香烃,苯甲酸除含有C、H元素外,还含有O元素,不属于烃类。
(2)苯的结构简式可写为“ ”,说明苯分子中碳碳单键和碳碳双键是交替排列的。这种说法是否正确
(3) 分子中共面的碳原子最多有几个
提示 不正确。苯分子中不存在典型的碳碳单键和碳碳双键。
提示 8。苯环上的6个C原子一定共面,碳碳双键上的两个C原子共面,单键可以旋转,所以最多可有8个碳原子共面。
易错辨析1
(1)标准状况下,22.4 L苯含有碳碳双键的数目为3NA(NA表示阿伏加德罗常数的值)。( )
(2)一般用分液的方法分离苯和水的混合物。( )
(3)苯与液溴混合后加入铁粉可发生取代反应。( )
(4) 是芳香族化合物,但不是芳香烃。( )
×
提示 标准状况下,苯为液态且苯分子结构中不含有典型的碳碳双键。
√
√
√
教材拓展
苯的同系物的命名
采用系统命名法命名,当苯环上有多个取代基时,苯环上的编号必须符合取代基位次之和最小的原则。而当用取代基位次之和最小原则无法确定哪一种编号正确时,应保证较简单的取代基位次尽可能小。例如:
4-甲基-2-乙基-1-丙基苯
1-甲基-3,5-二乙基苯
深度思考2
(1)怎样通过实验来区别苯和甲苯
(2)写出甲苯和氯气在光照下反应生成一氯代物的化学方程式。
提示 分别取两种液体少量,加入酸性KMnO4溶液,使其褪色的为甲苯,不褪色的为苯。
易错辨析2
(1)苯的邻位二元取代物只有一种,能证明苯分子中不存在单、双键交替结构。( )
(2)符合CnH2n-6(n≥6)通式的有机化合物一定是苯及其同系物。( )
(3)甲苯分子中所有的原子在同一平面上。( )
√
×
提示 符合CnH2n-6(n≥6)通式的有机化合物分子中可能含有多个碳碳双键或碳碳三键,如CH≡C—CH2—C≡C—CH3。
×
提示 甲苯分子的甲基中至少有2个氢原子与其他原子不在同一平面上。
(4)乙苯的一氯代物有5种。( )
(5)等物质的量的苯、甲苯与足量H2加成时,消耗H2的量相同。( )
√
提示 乙苯的一氯代物有5种,氯原子取代位置如图: 。
√
提示 苯、甲苯与H2加成时,都是苯环发生反应。
重难探究·能力素养全提升
情境探究
探究一 苯的分子结构和性质
科学家通过蒸馏苯甲酸和石灰的混合物,将得到的一种液体命名为苯,又通过实验确定了苯的相对分子质量为78,分子式为C6H6。对于如何确定苯的结构式,却成了摆在化学家们面前的难题:苯的碳、氢比值如此之大,表明苯是高度不饱和的化合物,但它又不具有典型的不饱和化合物应具有的易发生加成反应的性质。
思考交流:
1.苯和乙烯都能使溴水褪色,二者褪色的原理相同吗
提示 不相同。苯因萃取溴水中的Br2而使溴水褪色,而乙烯因与Br2发生加成反应而使溴水褪色,二者褪色的原理不相同。
2.一定条件下,苯、甲烷和乙烯均能与溴反应,条件相同吗 反应类型相同吗
提示 苯与液溴在FeBr3作催化剂时才能反应,甲烷与溴蒸气在光照时反应,乙烯与溴水或溴的CCl4溶液在常温下反应,三者反应类型分别是取代反应、取代反应和加成反应。
3.苯分子实际上不具有碳碳单键和碳碳双键的简单交替结构,可以作为证据的事实有哪些
①苯的间位二元取代物只有一种。
②苯的邻位二元取代物只有一种。
③苯不能使酸性KMnO4溶液褪色。
④苯能在一定条件下与氢气反应生成环己烷。
⑤苯在FeBr3存在的条件下与液溴发生取代反应。
方法突破
1.苯的分子结构
(1)苯分子中碳原子采取sp2杂化,除σ键外还含有大π键。苯分子为平面形结构,分子中的6个碳原子和6个氢原子共平面。
(2)苯分子不存在单双键交替结构,可以从以下几个方面证明:
①苯分子中六个碳碳键均等长,六元碳环呈平面正六边形;
②碳碳双键能使酸性KMnO4溶液褪色,但苯不能;
③邻二氯苯只有一种结构,而若为单双键交替应有两种结构
2.苯的化学性质
应用体验
视角1苯分子的结构
1.下列关于苯的说法正确的是( )
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式( )看,苯分子中含有碳碳双键,应属于烯烃
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同
D
解析 苯的分子式是C6H6,不能使酸性KMnO4溶液褪色,属于不饱和烃,故A错误;苯分子中不含有碳碳双键,不属于烯烃,故B错误;在催化剂作用下,苯与液溴反应生成溴苯,发生取代反应,故C错误;苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的化学键,故D正确。
视角2苯和烷烃性质的比较
2.下列反应中,属于取代反应的是( )
A.苯在氯化铁存在时与氯单质的反应
B.苯在镍作催化剂时与氢气的反应
C.苯在空气中燃烧
D.苯与碘水混合振荡
A
解析 A项是取代反应;B项是加成反应;C项是氧化反应;D项是物理过程。
【变式设问】
(1)将苯加入碘水中,充分振荡,有什么现象
(2)将苯加入碘水中,充分振荡后出现的现象是发生化学变化产生的吗
提示 液体分层,上层呈紫红色。
提示 不是。是苯萃取了碘水中的碘单质,发生了物理变化。
3.下列关于苯的叙述正确的是( )
A.反应①为加成反应
B.反应④中1 mol苯最多与3 mol H2发生加成反应,是因为苯分子含有三个碳碳双键
C.反应③为取代反应,有机产物是一种烃
D.反应②为氧化反应,反应现象是火焰明亮并带有浓烟
D
解析 反应①是苯和液溴在FeBr3的催化作用下生成溴苯和溴化氢,故为取代反应,A错误;苯分子中不存在碳碳单键和碳碳双键的交替现象,苯环上的6个碳碳键均为介于碳碳单键和碳碳双键之间独特的键,B错误;反应③是苯在浓硫酸作用下与浓硝酸反应生成硝基苯和水,故为取代反应,有机产物是硝基苯,不属于烃,而是烃的衍生物,C错误;反应②是苯的燃烧反应,故为氧化反应,反应现象是火焰明亮并带有浓烟,D正确。
视角3苯和烯烃性质的比较
4.科学家对物质性质的推断一般要基于一些实验事实。下列能说明苯与一般的烯烃性质不同的事实是( )
A.苯分子是高度对称的平面形分子
B.苯不溶于水
C.苯不与酸性KMnO4溶液反应
D.1 mol苯在一定条件下可与3 mol氯气发生加成反应
C
解析 乙烯的分子结构也是一个高度对称的平面形结构,故A不符合题意;苯是芳香烃,不溶于水,故B不符合题意;苯中不含碳碳双键,因此不能被酸性高锰酸钾溶液氧化,故C符合题意;苯和含三个碳碳双键的烯烃均可以与氯气发生加成反应,而且比例一致,故D不符合题意。
5.下列区分苯和己烯的实验方法和判断正确的是( )
A.分别点燃,没有烟生成的是苯
B.分别加入少量溴水振荡,静置后分层,下层橙黄色消失的是己烯
C.分别加入溴的CCl4溶液振荡,静置后分层,上下两层均为无色的是己烯
D.分别加入酸性KMnO4溶液振荡,紫红色消失的是己烯
D
解析 苯、己烯燃烧时都会产生烟,A错误;分别加入溴水振荡,下层橙黄色均消失,B错误;分别加入溴的CCl4溶液都不分层,C错误;苯不能使酸性KMnO4溶液褪色,但己烯可以,D正确。
情境探究
探究二 苯和苯的同系物性质的差异
实验1:向两支分别盛有少量酸性KMnO4溶液和溴的四氯化碳溶液的试管中滴入苯,振荡试管,静置。
实验2:向盛有少量酸性KMnO4溶液和溴的四氯化碳溶液的试管中滴入甲苯,振荡试管,静置。
1.向盛有酸性KMnO4溶液的试管中分别滴加苯和甲苯,用力振荡,静置,观察到的现象是什么 为什么
2.向盛有溴的四氯化碳溶液的试管中分别滴加苯和甲苯,用力振荡,静置,观察到的现象是什么 为什么 若将溴的四氯化碳溶液改为溴水呢
提示 滴加苯的试管,溶液分层,上层无色,下层为紫红色;滴加甲苯的试管,溶液不分层,为无色。原因:苯不能被酸性KMnO4溶液氧化;甲苯中苯环使甲基活化,能被酸性KMnO4溶液氧化,紫红色褪去。
提示 两试管中均得到均一、稳定的橙红色液体。原因:苯和甲苯均能溶于四氯化碳得到均一、稳定的液体混合物。若将溴的四氯化碳溶液改为溴水,两试管中液体分层,上层为橙红色,下层无色。原因:苯和甲苯能萃取溴水中的溴。
3.常见的烃中,能使酸性KMnO4溶液褪色的有哪些
提示 烯烃、炔烃、苯的某些同系物。
方法突破
苯和苯的同系物的比较
类别 苯 苯的同系物
相 同 点 分子 构成 ①分子中都含有一个苯环 ②都符合分子式通式CnH2n-6
化学 性质 ①燃烧时现象相同,火焰明亮,伴有浓烟 ②都易发生苯环上的取代反应 ③都能发生苯环的加成反应,但反应都比较困难
类别 苯 苯的同系物
不 同 点 易发生取代反应主要得到一元取代产物 更容易发生取代反应常得到多元取代产物
难被氧化,不能使酸性KMnO4溶液褪色 易被氧化,能使酸性KMnO4溶液褪色
差异 原因 苯的同系物分子中,苯环与侧链相互影响,苯环影响侧链,使侧链烃基性质活泼而易被氧化。侧链烃基影响苯环,使苯环邻、对位的氢更活泼而易被取代
应用体验
视角1苯的同系物的判断
1.下列有机化合物中,属于苯的同系物的是( )
D
解析 同系物是指结构相似,在分子组成上相差若干个CH2原子团的物质。A项,该结构是苯,不符合题意;B项,除了苯环,还含有碳碳双键,不饱和度与苯不同,不符合题意;C项,没有苯环,与苯结构不相似,不符合题意;D项,符合同系物的定义,符合题意。
视角2苯和苯的同系物性质的比较
2.下列反应只能得到一种有机化合物的是( )
A.丙烯与HCl发生反应
B.在FeBr3催化下,甲苯与液溴反应
C.乙苯与酸性高锰酸钾溶液反应
D.甲苯在光照条件下与Cl2反应
C
解析 丙烯和HCl发生加成反应生成1-氯丙烷或2-氯丙烷,所以有两种有机化合物生成,A不符合题意;在FeBr3催化下,甲苯与液溴反应可以生成邻溴甲苯、对溴甲苯或二溴甲苯、三溴甲苯等,B不符合题意;乙苯与酸性高锰酸钾溶液反应只生成一种有机化合物苯甲酸,C符合题意;甲苯与氯气在光照条件下发生取代反应,甲基上的氢原子可能有一个被取代、两个被取代或三个被取代,产物有多种,D不符合题意。
3.甲苯是苯的同系物,化学性质与苯相似,但由于基团之间的相互影响,使甲苯的某些性质又与苯不同。下列有关推断及解释都正确的是( )
A.苯不能通过化学反应使溴水褪色,但甲苯可以,这是甲基对苯环影响的结果
B.苯不能在光照下与Cl2发生取代反应,但甲苯可以,这是苯环对甲基影响的结果
C.苯的一氯代物只有一种,而甲苯的苯环上一氯代物有3种,这是苯环对甲基影响的结果
D.甲烷不能使酸性KMnO4溶液褪色,但甲苯可以,这是苯环对甲基影响的结果
D
解析 苯与甲苯均不含碳碳双键,都不能使溴水褪色,故A错误;苯不能在光照下与Cl2发生取代反应,但甲苯可以,是因为甲基上的氢原子容易被取代,与苯环的影响无关,故B错误;苯的一氯代物只有一种,而甲苯苯环上的一氯代物有3种,是因为苯分子中的氢原子完全相同,而甲苯苯环上有3种不同环境下的氢原子,与苯环对甲基影响无关,故C错误;甲烷不能使酸性KMnO4溶液褪色,但甲苯可以,这是苯环对甲基影响的结果,故D正确。
视角3与芳香烃有关的鉴别与除杂
4.下列有机化合物鉴别方法不正确的是( )
A.将乙烯和甲烷分别通入酸性高锰酸钾溶液中,观察溶液颜色是否变化
B.将溴水分别加入四氯化碳和苯中,观察溶液颜色及是否分层
C.苯和己烷分别放入水中,观察液体是否分层
D.甲苯和硝基苯分别放入水中,观察液体是否分层
C
解析 乙烯能与酸性高锰酸钾溶液反应并使其褪色,而甲烷不能,可鉴别,故A正确;Br2易溶于四氯化碳和苯,四氯化碳和苯都不溶于水,可从溴水中萃取出Br2,但四氯化碳的密度比水大,苯的密度比水小,分层后有机层(含Br2)位置不同,可鉴别,故B正确;苯和己烷都不溶于水,密度均比水小,放入水中都分层,现象相同,不能鉴别,故C错误;甲苯和硝基苯都不溶于水,但硝基苯的密度比水大,甲苯的密度比水小,分层后有机层位置不同,可鉴别,故D正确。
视角3苯的同系物的结构
5.[2023江西南昌高二检测]某烃的分子式为C10H14,它不能使溴水因发生化学反应而褪色,但可使酸性KMnO4溶液褪色,分子结构中只含有两个不相同烷基,符合条件的烃有( )
A.3种 B.4种 C.5种 D.6种
D
解析 该烃不能使溴水因发生化学反应而褪色,可使酸性KMnO4溶液褪色,可判断该烃为苯的同系物;分子结构中含有两个不相同的烷基,则一个为甲基,另一个为丙基(—CH2—CH2—CH3、 ),而两个烷基在苯环上
有邻、间、对三种位置,故符合条件的烃共有6种。
【变式设问】
C10H14的一种同系物为C9H12,含有苯环,核磁共振氢谱只有两种氢原子,且所有碳原子共平面,写出其结构简式。
本 课 结 束
