4.1 糖类课件(共61张PPT) 2023-2024学年高二化学人教版选择性必修3
文档属性
| 名称 | 4.1 糖类课件(共61张PPT) 2023-2024学年高二化学人教版选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-13 00:00:00 | ||
图片预览








文档简介
(共61张PPT)
第四章
第一节 糖类
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
素养 目标 1.通过对糖类的官能团、结构特点的微观探析,了解糖类的分类,根据所学化合物的性质推测糖类的化学性质,形成宏观辨识与微观探析的学科核心素养。
2.通过实验探究糖的性质,发现问题并解决问题,设计出糖类水解程度判断的合理实验方案,形成科学探究与创新意识的学科核心素养。
3.通过阅读和查阅资料,了解糖类在人体供能、储能等方面的作用,了解糖类的摄入和代谢与人体健康之间的关系,并能科学合理地搭配饮食,形成科学态度与社会责任的学科核心素养。
基础落实·必备知识全过关
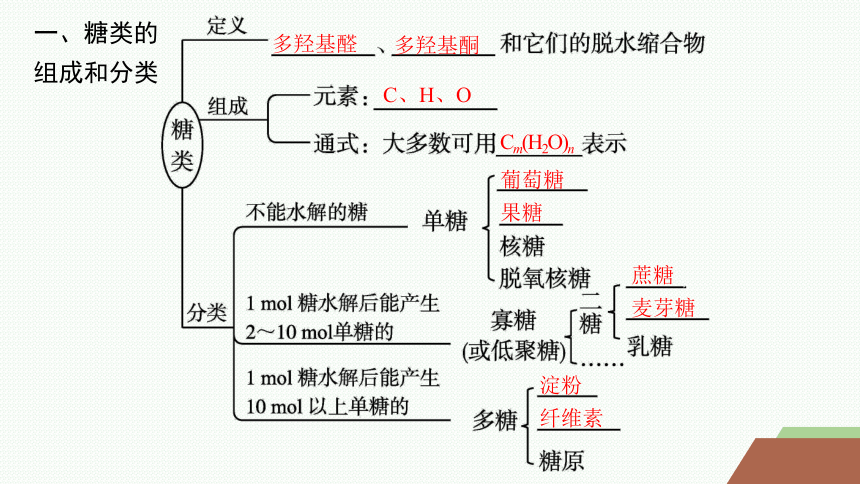
一、糖类的组成和分类
多羟基醛
多羟基酮
C、H、O
Cm(H2O)n
葡萄糖
果糖
蔗糖
麦芽糖
淀粉
纤维素
二、单糖
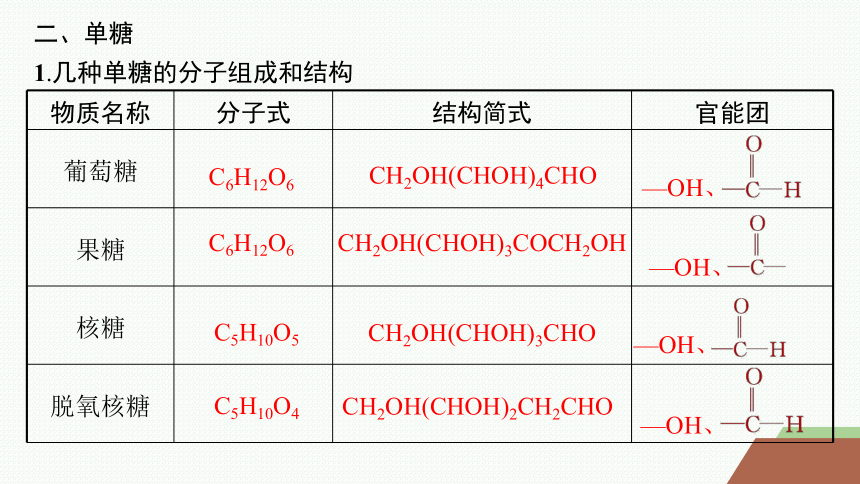
1.几种单糖的分子组成和结构
物质名称 分子式 结构简式 官能团
葡萄糖
果糖
核糖
脱氧核糖
C6H12O6
CH2OH(CHOH)4CHO
—OH、
C6H12O6
CH2OH(CHOH)3COCH2OH
—OH、
C5H10O5
CH2OH(CHOH)3CHO
—OH、
C5H10O4
CH2OH(CHOH)2CH2CHO
—OH、
物质名称 分子式 结构简式 官能团
相互关系 果糖与葡萄糖互为 ;核糖和脱氧核糖都是含有5个碳原子的单糖——戊糖
同分异构体
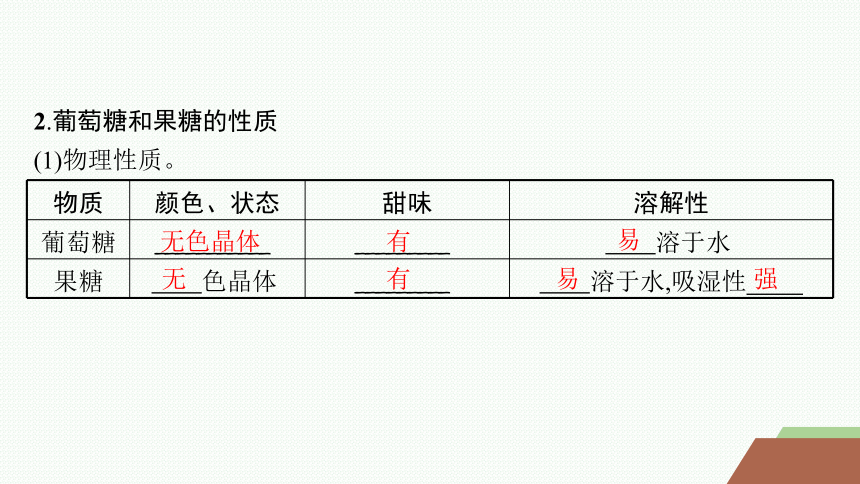
2.葡萄糖和果糖的性质
(1)物理性质。
物质 颜色、状态 甜味 溶解性
葡萄糖 ___________ _________ 溶于水
果糖 色晶体 _________ 溶于水,吸湿性
无色晶体
有
易
无
有
易
强
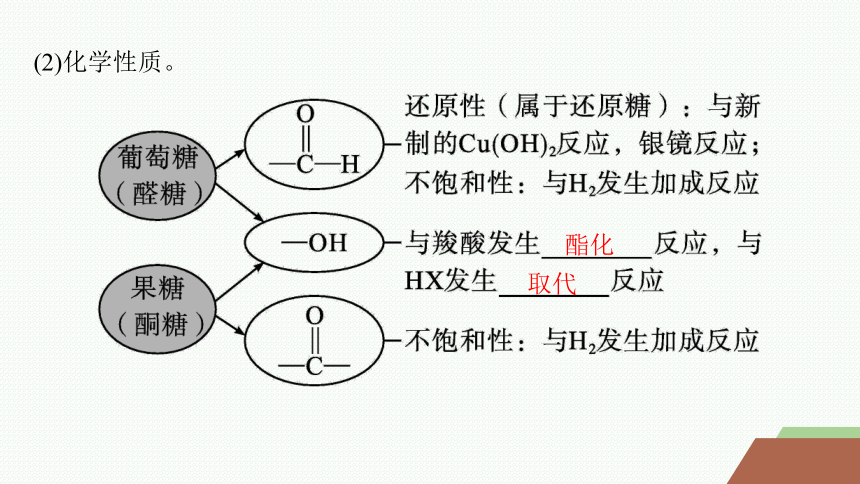
(2)化学性质。
酯化
取代
3.几种单糖的用途
(1)葡萄糖(重要的营养物质)和果糖广泛应用于食品和医药工业。
(2)核糖与脱氧核糖分别是生物体的遗传物质核糖核酸(RNA)与脱氧核糖核酸(DNA)的重要组成部分。
三、二糖
1.蔗糖和麦芽糖
类别 蔗糖 麦芽糖
分子式 _______________ ______________
物理性质 色晶体, 溶于水, 甜味 有甜味(不及蔗糖)
化学性质 水解反应,化学方程式: 水解反应,化学方程式:
C12H22O11
C12H22O11
无
易
有
2.乳糖
乳糖是一种常见的 ,主要存在于哺乳动物的乳汁中,经发酵产生 。
二糖
乳酸
四、多糖
1.组成和结构
名称 淀粉 纤维素
分子式 ____________________ __________________
n值大小 大 更大
类别 都属于
结构特点 ① —CHO,②有—OH
是否互为同分异构体 ___________
(C6H10O5)n
(C6H10O5)n
高分子化合物
无
否
2.物理性质
(1)淀粉: 物质, 甜味, 溶于冷水,热水中部分溶解,形成胶状的淀粉糊。
(2)纤维素: 物质, 甜味, 溶于水,也________ 一般的有机溶剂。
白色粉末状
没有
不
白色纤维状
没有
不
不溶于
3.化学性质
物质 淀粉 纤维素
相同点 水解反应 水解的化学方程式分别为: ;
氧化反应 都属于 糖, 被银氨溶液和新制的氢氧化铜等弱氧化剂氧化
酯化反应 由于分子中葡萄糖单元醇羟基的存在,故都能发生酯化反应
不同点 与碘作用 呈 无明显现象
非还原
不能
蓝色
深度思考1
葡萄糖、果糖、核糖和脱氧核糖分子分别有几个手性碳原子
提示 葡萄糖分子有4个,果糖分子有3个,核糖分子有3个,脱氧核糖分子有
2个。
图例展示
葡萄糖分子球棍模型
教材拓展1
糖尿病患者的尿液中含有的糖分(葡萄糖)较多,怎样检验一个病人是否患有糖尿病
提示 可用葡萄糖的特征反应进行检验。在患者的尿液中加入新制的氢氧化铜并加热,观察是否有砖红色沉淀生成。一般不用银镜反应,因为银氨溶液在配制、使用以及试管洗涤等方面均有不便。
易错辨析1
(1)糖类最早被称为“碳水化合物”,是因为糖的分子中含有水分子。( )
(2)糖类不一定都有甜味。( )
(3)葡萄糖和果糖分子式相同,结构不同,互为同分异构体;核糖与脱氧核糖分子式不同,不是同分异构体。( )
(4)能发生银镜反应,该化合物不一定属于醛。( )
(5)果糖为多羟基酮,能发生加成和酯化反应。( )
×
提示 不是;糖分子中的氢、氧原子并不是以水的形式存在,只是大多数糖类化合物中氢、氧原子的个数比是2∶1。
√
√
√
提示 葡萄糖、核糖、脱氧核糖不属于醛,也能发生银镜反应。
√
深度思考2
试分析如何利用实验方法区分蔗糖和麦芽糖
提示 蔗糖无醛基,麦芽糖有醛基,可以利用与银氨溶液或新制的氢氧化铜反应区分。
教材拓展2
中学阶段能发生银镜反应的物质:醛类、甲酸、甲酸酯类、甲酸盐、葡萄糖、麦芽糖等。
思考:能发生银镜反应的物质一定含有醛基吗
提示 不是。
教材拓展3
由淀粉制乙醇的多步反应
易错辨析2
(1)蔗糖是一种二糖,它的相对分子质量是葡萄糖的两倍。( )
(2)蔗糖、麦芽糖、淀粉水解的最终产物不相同。( )
(3)蔗糖和麦芽糖互为同分异构体,淀粉和纤维素也互为同分异构体。( )
(4)淀粉和纤维素在人体内最终都水解为葡萄糖。( )
(5)淀粉和纤维素的化学式都可以用(C6H10O5)n表示,二者是混合物。( )
×
提示 蔗糖的分子式为C12H22O11,而葡萄糖的分子式为C6H12O6。
√
提示 蔗糖水解的最终产物为葡萄糖和果糖,麦芽糖和淀粉水解的最终产物均为葡萄糖。
×
提示 淀粉和纤维素分子中n取值不同,不互为同分异构体。
×
提示 纤维素在人体内不能水解。
√
重难探究·能力素养全提升
情境探究
探究一 葡萄糖的结构与性质
按下图所示完成葡萄糖性质的两个探究实验:
实验2
请思考并回答以下问题。
1.总结反应现象,写出化学方程式。
提示
名称 实验现象 化学方程式
实验 1 试管壁上有银镜生成 CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
实验 2 试管中出现砖红色沉淀 CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH CH2OH(CHOH)4COONa+Cu2O↓+3H2O
2.根据上述实验现象得出什么结论
提示 葡萄糖中含有醛基。
3.已知葡萄糖的结构简式为 ,与乙酸反应生成酯,从理论上讲1 mol葡萄糖完全酯化需要多少乙酸
提示 1个葡萄糖分子中含有5个羟基,从理论上讲,1 mol葡萄糖完全酯化时需5 mol乙酸。
方法突破
1.葡萄糖的结构特点
2.葡萄糖的性质
反应类型 试剂或条件 表现性质的官能团
加成反应 H2/Ni 醛基
氧化反应 银氨溶液
新制的Cu(OH)2
使溴水、酸性高锰酸钾溶液褪色
生理氧化 —
酯化反应 乙酸等 羟基
应用体验
视角1糖类的组成与结构
1.对于糖类化合物的概念叙述正确的是( )
A.含有碳、氢、氧三种元素的有机化合物
B.是碳和水的化合物,又称碳水化合物
C.有甜味的物质
D.一般是多羟基醛或多羟基酮及它们的脱水缩合物
D
解析 含有C、H、O三种元素的有机物不一定是糖类,A项错误;糖类不是碳和水的化合物,B项错误;有甜味的物质不一定是糖类,C项错误。
2.葡萄糖是单糖的主要原因是( )
A.在糖类物质中含碳原子数最少
B.不能水解成更简单的糖
C.分子中有一个醛基( )
D.分子结构最简单
B
解析 从分类来看,不能再水解的糖是单糖,故答案为B。
3.下列关于核糖和脱氧核糖的说法正确的是( )
A.二者含有的官能团相同,互为同系物
B.二者分子式相同,互为同分异构体
C.核糖为五碳醛糖,脱氧核糖为五碳酮糖
D.二者均为生物体遗传物质的重要组成部分
D
解析
核糖是组成核糖核酸的成分,脱氧核糖是组成脱氧核糖核酸的成分,D项正确。
易错提醒 糖类判断的误区
(1)大多数糖类的组成可以用通式Cm(H2O)n表示;少数糖类不符合通式,如脱氧核糖(C5H10O4)、鼠李糖(C6H12O5);少数符合糖类通式的物质不是糖类,如乙酸(CH3COOH)、甲酸甲酯(HCOOCH3)。
(2)判断某物质是否属于糖类,要根据其结构特点,只有含有多羟基醛或多羟基酮以及能水解生成多羟基醛或多羟基酮的物质才属于糖类。
(3)葡萄糖和果糖属于单糖不是因为它们分子中碳原子数最少,而是因为不能水解。
4.葡萄糖作为维持生命的基础物质,下列叙述错误的是( )
A.加热条件下,葡萄糖遇到新制的氢氧化铜产生砖红色沉淀
B.工业上用葡萄糖的银镜反应生产镜子
C.葡萄糖与H2发生反应生成六羟基多元醇
D.1 mol葡萄糖最多与6 mol乙酸反应
D
解析 葡萄糖中含有醛基,加热时遇到新制的氢氧化铜会生成砖红色沉淀,故A正确;葡萄糖含有醛基,可以与银氨溶液发生银镜反应,可用于生产镜子,故B正确;葡萄糖的结构简式为CH2OH(CHOH)4CHO,醛基可以与氢气发生加成反应生成羟基,所以葡萄糖与H2发生反应生成六羟基多元醇,故C正确;1 mol葡萄糖含有5 mol羟基,最多与5 mol乙酸反应,故D错误。
【变式设问】
(1)B项中,葡萄糖发生银镜反应的实验操作是什么
(2)1 mol葡萄糖与足量的钠反应,产生标准状况下气体的体积是
L。
提示 在一支洁净的试管中配制2 mL的银氨溶液,加入1 mL 10%的葡萄糖溶液,振荡,在水浴中加热3~5 min。
提示 56 一个葡萄糖分子中含有5个羟基,1 mol葡萄糖与足量的钠反应,产生2.5 mol氢气,故在标准状况下气体的体积是56 L。
视角2单糖的性质
5.下列关于葡萄糖和果糖的说法错误的是( )
A.葡萄糖中含有醛基是还原糖,而果糖没有醛基是非还原糖
B.葡萄糖和果糖都能与H2在一定条件下作用生成己六醇
C.葡萄糖与乙酸作用生成葡萄糖五乙酸酯
D.葡萄糖和果糖都是单糖,互为同分异构体
A
解析 虽然果糖中不含有醛基,但是果糖在碱性条件下可以转化为醛糖,与葡萄糖一样也是还原糖,A错误;葡萄糖分子中含有5个—OH和1个—CHO,
果糖分子中含有5个—OH和1个 ,醛基和酮羰基都能与H2发生加成
反应,B正确;葡萄糖分子中含有5个—OH,与乙酸作用生成葡萄糖五乙酸酯,C正确;葡萄糖和果糖分子式相同,结构不同,互为同分异构体,D正确。
6.乙醇、乙酸和葡萄糖三种溶液,只用一种试剂就能将它们区别开来,该试剂是( )
A.金属钠
B.石蕊溶液
C.新制的Cu(OH)2
D.NaHCO3溶液
C
解析 新制的Cu(OH)2与乙醇不反应,可与葡萄糖溶液加热到沸腾有砖红色沉淀生成,新制的Cu(OH)2能溶于乙酸,溶液显蓝色,故能区分三种溶液。
情境探究
探究二 糖类的水解及水解产物的检验
实验1:按下表所示完成蔗糖和麦芽糖性质的探究实验
实验步骤 实验现象 实验结论
试管内无
明显现象
蔗糖分子中无醛基,是非还原糖;
实验步骤 实验现象 实验结论
试管内产生砖红色沉淀
麦芽糖分子中含有醛基,是还原糖
实验步骤 实验现象 实验结论
加入银氨溶液的试管中产生银镜;加入新制的Cu(OH)2的试管中出现砖红色沉淀
蔗糖能发生水解反应,其水解产物分子中含有醛基,具有还原性
实验2:完成如下有关淀粉水解的探究实验
(1)实验原理
判断淀粉水解的程度时,要注意检验产物中是否生成葡萄糖,同时还要确认淀粉是否水解完全。用银氨溶液或新制的Cu(OH)2和碘水来检验淀粉是否发生了水解及水解是否完全。
(2)实验步骤
请思考并回答以下问题:
1.总结实验1的实验现象及实验结论。
2.根据实验2的不同实验现象得出结论。
实验 现象A 现象B 结论
① 未出现银镜 溶液变蓝色
② 出现银镜 溶液变蓝色
③ 出现银镜 溶液不变蓝色
淀粉尚未水解
淀粉部分水解
淀粉完全水解
3.二糖水解用稀硫酸作催化剂还是用浓硫酸作催化剂
4.在检验两个实验的水解产物时,为什么不能向水解液中直接加入新制的氢氧化铜
5.实验2中,水解液中加入NaOH溶液的作用是什么 若在中和液中加入碘水,溶液不呈蓝色,能否说明淀粉已完全水解
提示 二糖水解用稀硫酸作催化剂,若用浓硫酸作催化剂,蔗糖易脱水炭化。
提示 用新制的氢氧化铜检验淀粉水解产物葡萄糖时,需在碱性条件下进行,所以需先加入过量的NaOH溶液中和掉催化剂稀硫酸后,才能加入新制的氢氧化铜进行后续实验。
提示 中和水解液中的稀硫酸,为醛基的检验创造碱性环境;中和液呈碱性, I2与NaOH可发生反应I2+2NaOH===NaI+NaIO+H2O,无法检验淀粉是否存在。
方法突破
1.糖类还原性的检验方法
2.水解产物中葡萄糖的检验
(1)水解条件
①蔗糖:稀硫酸作催化剂,水浴加热。
②纤维素:90%的浓硫酸作催化剂,小火微热。
③淀粉:稀硫酸或酶催化,水浴加热。
(2)水解产物中葡萄糖的检验:要检验糖类水解产物中的葡萄糖,必须先加入NaOH溶液中和其中的硫酸,再加入银氨溶液或新制的Cu(OH)2进行检验。
3.淀粉水解程度的判断
(1)实验原理
用银氨溶液或新制的Cu(OH)2和碘水来检验淀粉在水溶液中是否发生了水解及水解是否已进行完全。
(2)实验步骤
(3)实验现象及结论
实验 现象A 现象B 结论
1 未出现银镜 溶液变蓝色 淀粉尚未水解
2 出现银镜 溶液变蓝色 淀粉部分水解
3 出现银镜 溶液不变蓝色 淀粉完全水解
微点拨 (1)检验水解产物时需先中和再检验的:卤代烃中卤族元素的检验;糖类水解产物的检验。
(2)要检验淀粉是否水解,可以通过检验葡萄糖的存在来证明;要检验淀粉是否完全水解,除要检验葡萄糖存在外,还要检验淀粉是否还存在来证明。
应用体验
视角1二糖的结构与性质
1.下列关于蔗糖和麦芽糖的说法中,不正确的是( )
A.蔗糖与麦芽糖互为同分异构体
B.蔗糖与麦芽糖的分子式都是C12H22O11
C.蔗糖的水解产物是葡萄糖
D.麦芽糖能发生银镜反应,蔗糖不能发生银镜反应
C
解析 蔗糖与麦芽糖的分子式都是C12H22O11,二者互为同分异构体;麦芽糖是还原糖,而蔗糖是非还原糖;蔗糖的水解产物是果糖和葡萄糖。
2.下列关于蔗糖属于非还原糖而其水解产物具有还原性的实验方案的说法中正确的是( )
A.验证蔗糖属于非还原糖的操作顺序:④③
B.验证蔗糖属于非还原糖的操作顺序:③⑤
C.验证蔗糖水解产物具有还原性的操作顺序:①④⑤
D.验证蔗糖水解产物具有还原性的操作顺序:①⑤②④⑤
D
解析 在碱性条件下加银氨溶液,加热后产生光亮的银镜,可说明水解产物具有还原性,则水解后先加NaOH溶液至碱性,再加银氨溶液,验证蔗糖水解产物具有还原性的操作顺序为①⑤②④⑤,蔗糖属于非还原糖,不能发生银镜反应,则验证蔗糖属于非还原糖的操作顺序为④⑤。
视角2多糖的结构与应用
3.关于淀粉和纤维素两种物质,下列说法正确的是( )
A.二者都能水解,且水解的最终产物不相同
B.二者含C、H、O三种元素的质量分数相同,且互为同分异构体
C.它们都属于糖类,且都是有机高分子
D.都可用(C6H10O5)n表示,但淀粉能发生银镜反应,而纤维素不能
C
解析 淀粉和纤维素都是由葡萄糖单元相互连接组成的,因此水解的最终产物都是葡萄糖,A项错误;由于二者的n值都很大且不同,所以它们是有机高分子,但不互为同分异构体,B项错误、C项正确;二者都是非还原糖,D项错误。
4.生活中的一些问题常涉及化学知识,下列叙述正确的是( )
A.棉花的主要成分是纤维素
B.过多食用糖类物质如淀粉等不会导致人体发胖
C.淀粉在人体内直接水解生成葡萄糖,为人体组织提供营养
D.纤维素在人体消化过程中起重要作用,纤维素可以作为人类的营养物质
A
解析 人体中没有水解纤维素的酶,纤维素在人体中主要是加强胃肠蠕动,具有通便功能。
视角3二糖和多糖的水解实验
5.下列实验能获得成功的是( )
A.蔗糖溶液中加入稀硫酸,加热,然后加入银氨溶液,水浴加热,有银镜生成
B.在硫酸铜溶液中加入几滴稀NaOH溶液后,加入葡萄糖溶液,煮沸后,有砖红色沉淀析出
C.在淀粉溶液中加入唾液(含淀粉酶),水浴加热(36 ℃左右),冷却后加入银氨溶液,再水浴加热,有银镜生成
D.在淀粉溶液中加入稀硫酸,微热后,再加入新制的Cu(OH)2,无明显现象,说明淀粉没有水解
C
解析 A项银镜反应应在碱性环境下进行,应先加碱中和稀硫酸,再进行银镜实验;葡萄糖能与新制的Cu(OH)2反应,产生砖红色沉淀,B项NaOH用量太少;D项在加新制的Cu(OH)2之前应先加NaOH溶液,中和稀硫酸。
【变式设问】
(1)淀粉发生水解时的产物中会有蔗糖、麦芽糖吗
(2)选项D中微热后加入碘水后变蓝,能否说明淀粉没有水解
提示 有麦芽糖、没有蔗糖。根据淀粉水解的程度,其水解产物可能为麦芽糖或葡萄糖,不会生成蔗糖。
提示 不能。加入碘水后变蓝,说明还有淀粉,可能没有水解,也可能是部分水解。
6.某同学称取9 g淀粉溶于水,测定淀粉水解的百分率,其操作步骤如图所示。
提示:少量溶液计算时忽略不计。
试回答下列问题:
(1)所加试剂A是 ,B是 。只加A,不加B是否可以
(填“可以”或“不可以”),理由是 。
(2)当析出2.16 g Ag时,淀粉的水解百分率是 。
稀硫酸
NaOH溶液
不可以
银镜反应必须在碱性条件下进行
18%
解析 (1)淀粉在酸性条件下发生水解反应,故A可为稀硫酸;淀粉水解的最终产物是葡萄糖,葡萄糖分子中含有醛基,可与银氨溶液发生银镜反应,但银镜反应必须在碱性条件下进行,故B为NaOH溶液。
本 课 结 束
第四章
第一节 糖类
基础落实·必备知识全过关
重难探究·能力素养全提升
目录索引
素养 目标 1.通过对糖类的官能团、结构特点的微观探析,了解糖类的分类,根据所学化合物的性质推测糖类的化学性质,形成宏观辨识与微观探析的学科核心素养。
2.通过实验探究糖的性质,发现问题并解决问题,设计出糖类水解程度判断的合理实验方案,形成科学探究与创新意识的学科核心素养。
3.通过阅读和查阅资料,了解糖类在人体供能、储能等方面的作用,了解糖类的摄入和代谢与人体健康之间的关系,并能科学合理地搭配饮食,形成科学态度与社会责任的学科核心素养。
基础落实·必备知识全过关
一、糖类的组成和分类
多羟基醛
多羟基酮
C、H、O
Cm(H2O)n
葡萄糖
果糖
蔗糖
麦芽糖
淀粉
纤维素
二、单糖
1.几种单糖的分子组成和结构
物质名称 分子式 结构简式 官能团
葡萄糖
果糖
核糖
脱氧核糖
C6H12O6
CH2OH(CHOH)4CHO
—OH、
C6H12O6
CH2OH(CHOH)3COCH2OH
—OH、
C5H10O5
CH2OH(CHOH)3CHO
—OH、
C5H10O4
CH2OH(CHOH)2CH2CHO
—OH、
物质名称 分子式 结构简式 官能团
相互关系 果糖与葡萄糖互为 ;核糖和脱氧核糖都是含有5个碳原子的单糖——戊糖
同分异构体
2.葡萄糖和果糖的性质
(1)物理性质。
物质 颜色、状态 甜味 溶解性
葡萄糖 ___________ _________ 溶于水
果糖 色晶体 _________ 溶于水,吸湿性
无色晶体
有
易
无
有
易
强
(2)化学性质。
酯化
取代
3.几种单糖的用途
(1)葡萄糖(重要的营养物质)和果糖广泛应用于食品和医药工业。
(2)核糖与脱氧核糖分别是生物体的遗传物质核糖核酸(RNA)与脱氧核糖核酸(DNA)的重要组成部分。
三、二糖
1.蔗糖和麦芽糖
类别 蔗糖 麦芽糖
分子式 _______________ ______________
物理性质 色晶体, 溶于水, 甜味 有甜味(不及蔗糖)
化学性质 水解反应,化学方程式: 水解反应,化学方程式:
C12H22O11
C12H22O11
无
易
有
2.乳糖
乳糖是一种常见的 ,主要存在于哺乳动物的乳汁中,经发酵产生 。
二糖
乳酸
四、多糖
1.组成和结构
名称 淀粉 纤维素
分子式 ____________________ __________________
n值大小 大 更大
类别 都属于
结构特点 ① —CHO,②有—OH
是否互为同分异构体 ___________
(C6H10O5)n
(C6H10O5)n
高分子化合物
无
否
2.物理性质
(1)淀粉: 物质, 甜味, 溶于冷水,热水中部分溶解,形成胶状的淀粉糊。
(2)纤维素: 物质, 甜味, 溶于水,也________ 一般的有机溶剂。
白色粉末状
没有
不
白色纤维状
没有
不
不溶于
3.化学性质
物质 淀粉 纤维素
相同点 水解反应 水解的化学方程式分别为: ;
氧化反应 都属于 糖, 被银氨溶液和新制的氢氧化铜等弱氧化剂氧化
酯化反应 由于分子中葡萄糖单元醇羟基的存在,故都能发生酯化反应
不同点 与碘作用 呈 无明显现象
非还原
不能
蓝色
深度思考1
葡萄糖、果糖、核糖和脱氧核糖分子分别有几个手性碳原子
提示 葡萄糖分子有4个,果糖分子有3个,核糖分子有3个,脱氧核糖分子有
2个。
图例展示
葡萄糖分子球棍模型
教材拓展1
糖尿病患者的尿液中含有的糖分(葡萄糖)较多,怎样检验一个病人是否患有糖尿病
提示 可用葡萄糖的特征反应进行检验。在患者的尿液中加入新制的氢氧化铜并加热,观察是否有砖红色沉淀生成。一般不用银镜反应,因为银氨溶液在配制、使用以及试管洗涤等方面均有不便。
易错辨析1
(1)糖类最早被称为“碳水化合物”,是因为糖的分子中含有水分子。( )
(2)糖类不一定都有甜味。( )
(3)葡萄糖和果糖分子式相同,结构不同,互为同分异构体;核糖与脱氧核糖分子式不同,不是同分异构体。( )
(4)能发生银镜反应,该化合物不一定属于醛。( )
(5)果糖为多羟基酮,能发生加成和酯化反应。( )
×
提示 不是;糖分子中的氢、氧原子并不是以水的形式存在,只是大多数糖类化合物中氢、氧原子的个数比是2∶1。
√
√
√
提示 葡萄糖、核糖、脱氧核糖不属于醛,也能发生银镜反应。
√
深度思考2
试分析如何利用实验方法区分蔗糖和麦芽糖
提示 蔗糖无醛基,麦芽糖有醛基,可以利用与银氨溶液或新制的氢氧化铜反应区分。
教材拓展2
中学阶段能发生银镜反应的物质:醛类、甲酸、甲酸酯类、甲酸盐、葡萄糖、麦芽糖等。
思考:能发生银镜反应的物质一定含有醛基吗
提示 不是。
教材拓展3
由淀粉制乙醇的多步反应
易错辨析2
(1)蔗糖是一种二糖,它的相对分子质量是葡萄糖的两倍。( )
(2)蔗糖、麦芽糖、淀粉水解的最终产物不相同。( )
(3)蔗糖和麦芽糖互为同分异构体,淀粉和纤维素也互为同分异构体。( )
(4)淀粉和纤维素在人体内最终都水解为葡萄糖。( )
(5)淀粉和纤维素的化学式都可以用(C6H10O5)n表示,二者是混合物。( )
×
提示 蔗糖的分子式为C12H22O11,而葡萄糖的分子式为C6H12O6。
√
提示 蔗糖水解的最终产物为葡萄糖和果糖,麦芽糖和淀粉水解的最终产物均为葡萄糖。
×
提示 淀粉和纤维素分子中n取值不同,不互为同分异构体。
×
提示 纤维素在人体内不能水解。
√
重难探究·能力素养全提升
情境探究
探究一 葡萄糖的结构与性质
按下图所示完成葡萄糖性质的两个探究实验:
实验2
请思考并回答以下问题。
1.总结反应现象,写出化学方程式。
提示
名称 实验现象 化学方程式
实验 1 试管壁上有银镜生成 CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
实验 2 试管中出现砖红色沉淀 CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH CH2OH(CHOH)4COONa+Cu2O↓+3H2O
2.根据上述实验现象得出什么结论
提示 葡萄糖中含有醛基。
3.已知葡萄糖的结构简式为 ,与乙酸反应生成酯,从理论上讲1 mol葡萄糖完全酯化需要多少乙酸
提示 1个葡萄糖分子中含有5个羟基,从理论上讲,1 mol葡萄糖完全酯化时需5 mol乙酸。
方法突破
1.葡萄糖的结构特点
2.葡萄糖的性质
反应类型 试剂或条件 表现性质的官能团
加成反应 H2/Ni 醛基
氧化反应 银氨溶液
新制的Cu(OH)2
使溴水、酸性高锰酸钾溶液褪色
生理氧化 —
酯化反应 乙酸等 羟基
应用体验
视角1糖类的组成与结构
1.对于糖类化合物的概念叙述正确的是( )
A.含有碳、氢、氧三种元素的有机化合物
B.是碳和水的化合物,又称碳水化合物
C.有甜味的物质
D.一般是多羟基醛或多羟基酮及它们的脱水缩合物
D
解析 含有C、H、O三种元素的有机物不一定是糖类,A项错误;糖类不是碳和水的化合物,B项错误;有甜味的物质不一定是糖类,C项错误。
2.葡萄糖是单糖的主要原因是( )
A.在糖类物质中含碳原子数最少
B.不能水解成更简单的糖
C.分子中有一个醛基( )
D.分子结构最简单
B
解析 从分类来看,不能再水解的糖是单糖,故答案为B。
3.下列关于核糖和脱氧核糖的说法正确的是( )
A.二者含有的官能团相同,互为同系物
B.二者分子式相同,互为同分异构体
C.核糖为五碳醛糖,脱氧核糖为五碳酮糖
D.二者均为生物体遗传物质的重要组成部分
D
解析
核糖是组成核糖核酸的成分,脱氧核糖是组成脱氧核糖核酸的成分,D项正确。
易错提醒 糖类判断的误区
(1)大多数糖类的组成可以用通式Cm(H2O)n表示;少数糖类不符合通式,如脱氧核糖(C5H10O4)、鼠李糖(C6H12O5);少数符合糖类通式的物质不是糖类,如乙酸(CH3COOH)、甲酸甲酯(HCOOCH3)。
(2)判断某物质是否属于糖类,要根据其结构特点,只有含有多羟基醛或多羟基酮以及能水解生成多羟基醛或多羟基酮的物质才属于糖类。
(3)葡萄糖和果糖属于单糖不是因为它们分子中碳原子数最少,而是因为不能水解。
4.葡萄糖作为维持生命的基础物质,下列叙述错误的是( )
A.加热条件下,葡萄糖遇到新制的氢氧化铜产生砖红色沉淀
B.工业上用葡萄糖的银镜反应生产镜子
C.葡萄糖与H2发生反应生成六羟基多元醇
D.1 mol葡萄糖最多与6 mol乙酸反应
D
解析 葡萄糖中含有醛基,加热时遇到新制的氢氧化铜会生成砖红色沉淀,故A正确;葡萄糖含有醛基,可以与银氨溶液发生银镜反应,可用于生产镜子,故B正确;葡萄糖的结构简式为CH2OH(CHOH)4CHO,醛基可以与氢气发生加成反应生成羟基,所以葡萄糖与H2发生反应生成六羟基多元醇,故C正确;1 mol葡萄糖含有5 mol羟基,最多与5 mol乙酸反应,故D错误。
【变式设问】
(1)B项中,葡萄糖发生银镜反应的实验操作是什么
(2)1 mol葡萄糖与足量的钠反应,产生标准状况下气体的体积是
L。
提示 在一支洁净的试管中配制2 mL的银氨溶液,加入1 mL 10%的葡萄糖溶液,振荡,在水浴中加热3~5 min。
提示 56 一个葡萄糖分子中含有5个羟基,1 mol葡萄糖与足量的钠反应,产生2.5 mol氢气,故在标准状况下气体的体积是56 L。
视角2单糖的性质
5.下列关于葡萄糖和果糖的说法错误的是( )
A.葡萄糖中含有醛基是还原糖,而果糖没有醛基是非还原糖
B.葡萄糖和果糖都能与H2在一定条件下作用生成己六醇
C.葡萄糖与乙酸作用生成葡萄糖五乙酸酯
D.葡萄糖和果糖都是单糖,互为同分异构体
A
解析 虽然果糖中不含有醛基,但是果糖在碱性条件下可以转化为醛糖,与葡萄糖一样也是还原糖,A错误;葡萄糖分子中含有5个—OH和1个—CHO,
果糖分子中含有5个—OH和1个 ,醛基和酮羰基都能与H2发生加成
反应,B正确;葡萄糖分子中含有5个—OH,与乙酸作用生成葡萄糖五乙酸酯,C正确;葡萄糖和果糖分子式相同,结构不同,互为同分异构体,D正确。
6.乙醇、乙酸和葡萄糖三种溶液,只用一种试剂就能将它们区别开来,该试剂是( )
A.金属钠
B.石蕊溶液
C.新制的Cu(OH)2
D.NaHCO3溶液
C
解析 新制的Cu(OH)2与乙醇不反应,可与葡萄糖溶液加热到沸腾有砖红色沉淀生成,新制的Cu(OH)2能溶于乙酸,溶液显蓝色,故能区分三种溶液。
情境探究
探究二 糖类的水解及水解产物的检验
实验1:按下表所示完成蔗糖和麦芽糖性质的探究实验
实验步骤 实验现象 实验结论
试管内无
明显现象
蔗糖分子中无醛基,是非还原糖;
实验步骤 实验现象 实验结论
试管内产生砖红色沉淀
麦芽糖分子中含有醛基,是还原糖
实验步骤 实验现象 实验结论
加入银氨溶液的试管中产生银镜;加入新制的Cu(OH)2的试管中出现砖红色沉淀
蔗糖能发生水解反应,其水解产物分子中含有醛基,具有还原性
实验2:完成如下有关淀粉水解的探究实验
(1)实验原理
判断淀粉水解的程度时,要注意检验产物中是否生成葡萄糖,同时还要确认淀粉是否水解完全。用银氨溶液或新制的Cu(OH)2和碘水来检验淀粉是否发生了水解及水解是否完全。
(2)实验步骤
请思考并回答以下问题:
1.总结实验1的实验现象及实验结论。
2.根据实验2的不同实验现象得出结论。
实验 现象A 现象B 结论
① 未出现银镜 溶液变蓝色
② 出现银镜 溶液变蓝色
③ 出现银镜 溶液不变蓝色
淀粉尚未水解
淀粉部分水解
淀粉完全水解
3.二糖水解用稀硫酸作催化剂还是用浓硫酸作催化剂
4.在检验两个实验的水解产物时,为什么不能向水解液中直接加入新制的氢氧化铜
5.实验2中,水解液中加入NaOH溶液的作用是什么 若在中和液中加入碘水,溶液不呈蓝色,能否说明淀粉已完全水解
提示 二糖水解用稀硫酸作催化剂,若用浓硫酸作催化剂,蔗糖易脱水炭化。
提示 用新制的氢氧化铜检验淀粉水解产物葡萄糖时,需在碱性条件下进行,所以需先加入过量的NaOH溶液中和掉催化剂稀硫酸后,才能加入新制的氢氧化铜进行后续实验。
提示 中和水解液中的稀硫酸,为醛基的检验创造碱性环境;中和液呈碱性, I2与NaOH可发生反应I2+2NaOH===NaI+NaIO+H2O,无法检验淀粉是否存在。
方法突破
1.糖类还原性的检验方法
2.水解产物中葡萄糖的检验
(1)水解条件
①蔗糖:稀硫酸作催化剂,水浴加热。
②纤维素:90%的浓硫酸作催化剂,小火微热。
③淀粉:稀硫酸或酶催化,水浴加热。
(2)水解产物中葡萄糖的检验:要检验糖类水解产物中的葡萄糖,必须先加入NaOH溶液中和其中的硫酸,再加入银氨溶液或新制的Cu(OH)2进行检验。
3.淀粉水解程度的判断
(1)实验原理
用银氨溶液或新制的Cu(OH)2和碘水来检验淀粉在水溶液中是否发生了水解及水解是否已进行完全。
(2)实验步骤
(3)实验现象及结论
实验 现象A 现象B 结论
1 未出现银镜 溶液变蓝色 淀粉尚未水解
2 出现银镜 溶液变蓝色 淀粉部分水解
3 出现银镜 溶液不变蓝色 淀粉完全水解
微点拨 (1)检验水解产物时需先中和再检验的:卤代烃中卤族元素的检验;糖类水解产物的检验。
(2)要检验淀粉是否水解,可以通过检验葡萄糖的存在来证明;要检验淀粉是否完全水解,除要检验葡萄糖存在外,还要检验淀粉是否还存在来证明。
应用体验
视角1二糖的结构与性质
1.下列关于蔗糖和麦芽糖的说法中,不正确的是( )
A.蔗糖与麦芽糖互为同分异构体
B.蔗糖与麦芽糖的分子式都是C12H22O11
C.蔗糖的水解产物是葡萄糖
D.麦芽糖能发生银镜反应,蔗糖不能发生银镜反应
C
解析 蔗糖与麦芽糖的分子式都是C12H22O11,二者互为同分异构体;麦芽糖是还原糖,而蔗糖是非还原糖;蔗糖的水解产物是果糖和葡萄糖。
2.下列关于蔗糖属于非还原糖而其水解产物具有还原性的实验方案的说法中正确的是( )
A.验证蔗糖属于非还原糖的操作顺序:④③
B.验证蔗糖属于非还原糖的操作顺序:③⑤
C.验证蔗糖水解产物具有还原性的操作顺序:①④⑤
D.验证蔗糖水解产物具有还原性的操作顺序:①⑤②④⑤
D
解析 在碱性条件下加银氨溶液,加热后产生光亮的银镜,可说明水解产物具有还原性,则水解后先加NaOH溶液至碱性,再加银氨溶液,验证蔗糖水解产物具有还原性的操作顺序为①⑤②④⑤,蔗糖属于非还原糖,不能发生银镜反应,则验证蔗糖属于非还原糖的操作顺序为④⑤。
视角2多糖的结构与应用
3.关于淀粉和纤维素两种物质,下列说法正确的是( )
A.二者都能水解,且水解的最终产物不相同
B.二者含C、H、O三种元素的质量分数相同,且互为同分异构体
C.它们都属于糖类,且都是有机高分子
D.都可用(C6H10O5)n表示,但淀粉能发生银镜反应,而纤维素不能
C
解析 淀粉和纤维素都是由葡萄糖单元相互连接组成的,因此水解的最终产物都是葡萄糖,A项错误;由于二者的n值都很大且不同,所以它们是有机高分子,但不互为同分异构体,B项错误、C项正确;二者都是非还原糖,D项错误。
4.生活中的一些问题常涉及化学知识,下列叙述正确的是( )
A.棉花的主要成分是纤维素
B.过多食用糖类物质如淀粉等不会导致人体发胖
C.淀粉在人体内直接水解生成葡萄糖,为人体组织提供营养
D.纤维素在人体消化过程中起重要作用,纤维素可以作为人类的营养物质
A
解析 人体中没有水解纤维素的酶,纤维素在人体中主要是加强胃肠蠕动,具有通便功能。
视角3二糖和多糖的水解实验
5.下列实验能获得成功的是( )
A.蔗糖溶液中加入稀硫酸,加热,然后加入银氨溶液,水浴加热,有银镜生成
B.在硫酸铜溶液中加入几滴稀NaOH溶液后,加入葡萄糖溶液,煮沸后,有砖红色沉淀析出
C.在淀粉溶液中加入唾液(含淀粉酶),水浴加热(36 ℃左右),冷却后加入银氨溶液,再水浴加热,有银镜生成
D.在淀粉溶液中加入稀硫酸,微热后,再加入新制的Cu(OH)2,无明显现象,说明淀粉没有水解
C
解析 A项银镜反应应在碱性环境下进行,应先加碱中和稀硫酸,再进行银镜实验;葡萄糖能与新制的Cu(OH)2反应,产生砖红色沉淀,B项NaOH用量太少;D项在加新制的Cu(OH)2之前应先加NaOH溶液,中和稀硫酸。
【变式设问】
(1)淀粉发生水解时的产物中会有蔗糖、麦芽糖吗
(2)选项D中微热后加入碘水后变蓝,能否说明淀粉没有水解
提示 有麦芽糖、没有蔗糖。根据淀粉水解的程度,其水解产物可能为麦芽糖或葡萄糖,不会生成蔗糖。
提示 不能。加入碘水后变蓝,说明还有淀粉,可能没有水解,也可能是部分水解。
6.某同学称取9 g淀粉溶于水,测定淀粉水解的百分率,其操作步骤如图所示。
提示:少量溶液计算时忽略不计。
试回答下列问题:
(1)所加试剂A是 ,B是 。只加A,不加B是否可以
(填“可以”或“不可以”),理由是 。
(2)当析出2.16 g Ag时,淀粉的水解百分率是 。
稀硫酸
NaOH溶液
不可以
银镜反应必须在碱性条件下进行
18%
解析 (1)淀粉在酸性条件下发生水解反应,故A可为稀硫酸;淀粉水解的最终产物是葡萄糖,葡萄糖分子中含有醛基,可与银氨溶液发生银镜反应,但银镜反应必须在碱性条件下进行,故B为NaOH溶液。
本 课 结 束
