6.1金刚石、石墨和C60 第2课时 碳的化学性质 课件(共23张PPT内嵌视频) -2023-2024学年九年级化学上册同步(人教版)
文档属性
| 名称 | 6.1金刚石、石墨和C60 第2课时 碳的化学性质 课件(共23张PPT内嵌视频) -2023-2024学年九年级化学上册同步(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 56.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-14 00:00:00 | ||
图片预览







文档简介
(共23张PPT)
汇报:阿拉丁
金刚石、石墨和C60(第二课时)
第六单元 课题1
新课导入
古代字画历经几百年甚至几千年而依然不褪色,你知道其中的原因吗?
探究新知
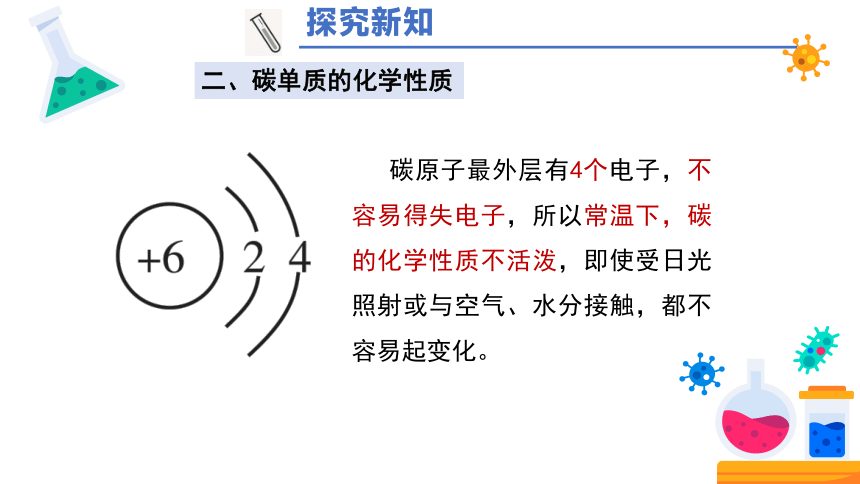
碳原子最外层有4个电子,不容易得失电子,所以常温下,碳的化学性质不活泼,即使受日光照射或与空气、水分接触,都不容易起变化。
二、碳单质的化学性质
探究新知
问题1:古代字画历经几百年甚至几千年而依然不褪色,你知道其中的原因吗?
碳在常温下化学性质不活泼,所以用墨书写或绘制的古代字画能长久保存而不褪色。
问题2:把木制的电线杆在埋入地下前,
为什么要将其表面烧焦呢?
其目的就是为了让电线杆不易腐烂,可以保存久一些
二、碳单质的化学性质
探究新知
1.碳与氧气的反应(可燃性)
现象:
发出白光,放出热量,生成一种能使澄清石灰水变浑浊的气体。
氧气充足:
C+O2 CO2
点燃
在温度升高的情况下,碳能跟很多物质发生化学反应。
思考:在高温下,碳的化学性质如何呢?
二、碳单质的化学性质
探究新知
木炭在氧气中不充分燃烧时,生成一氧化碳。
2C+O2 2CO
点燃
冬天在密闭的空间燃烧木炭烤火,容易发生CO中毒事件,Why?
氧气不足:
CO中毒原理:CO与血液中的血红蛋白结合,使血红蛋白失去携氧的能力,人因缺氧窒息而死
探究新知
氧气充足、燃烧充分时,碳燃烧生成二氧化碳
氧气不充足、燃烧不充分时,碳燃烧生成一氧化碳
CO2
C+O2
点燃
2CO
2C+O2
点燃
1.碳与氧气的反应(可燃性)
二、碳单质的化学性质
探究新知
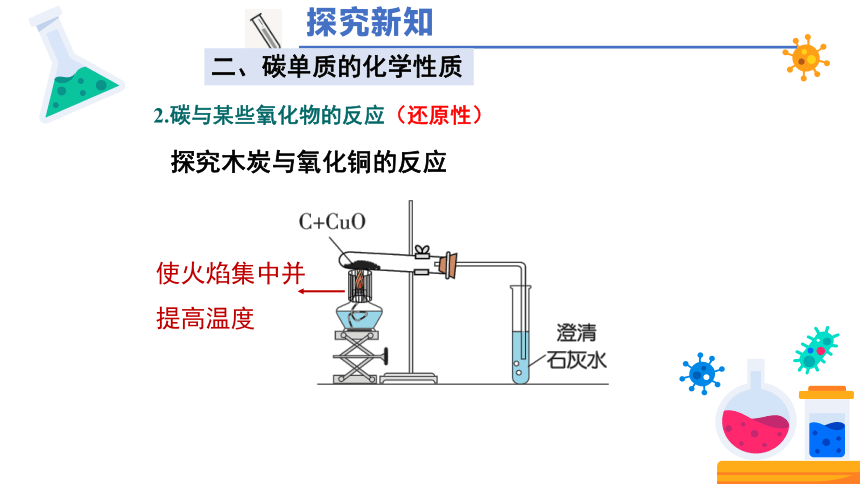
探究木炭与氧化铜的反应
使火焰集中并提高温度
2.碳与某些氧化物的反应(还原性)
二、碳单质的化学性质
探究新知
2.碳与某些氧化物的反应(还原性)
P110 实验6-2 木炭与氧化铜的反应
探究新知
2.碳与某些氧化物的反应(还原性)
P110 实验6-2 木炭与氧化铜的反应
现 象:
黑色粉末逐渐变成光亮的红色,澄清石灰水变浑浊
反应原理:
2CuO+C 2Cu+CO2
高温
二、碳单质的化学性质
澄清石灰水变浑浊
有CO2生成
黑色粉末变红色
有Cu生成
实验现象:
实验结论:
探究新知
探究新知
2.实验结束时,先撤出导气管,然后再熄灭酒精灯!
防止澄清石灰水倒流入热的试管致使试管破裂。
3.冷却后再倒出试管中的粉末,防止热的Cu被氧化为CuO
1.木炭粉末要烘干,目的是排除水蒸气的干扰,使实验现象更明显;
2.碳与某些氧化物的反应(还原性)
二、碳单质的化学性质
探究新知
金属的冶炼
3C + 2Fe2O3 4Fe + 3CO2↑
高温
探究新知
还原反应
含氧化合物里的氧被夺去的反应,叫做还原反应。
C + 2CuO 2Cu + CO2↑
高温
CuO Cu
失氧
氧化铜具有氧化性,作氧化剂
氧化铜在反应中被还原,发生还原反应
探究新知
C + 2CuO 2Cu + CO2↑
高温
C CO2
得氧
碳具有还原性,作还原剂
碳在反应中被氧化,发生氧化反应
还原反应和氧化反应在一个反应中是同时进行的,且都不属于基本反应类型。
还原反应
探究新知
应用1:碳的还原性可用于冶金工业。
应用2:在高温条件下,碳能使二氧化碳转变成一氧化碳。
如:焦炭可以把铁从它的氧化物矿石里还原出来。
3C + 2Fe2O3 3CO2↑ + 4Fe
高温
C + CO2 2CO
高温
1.下列说法错误的是( )
A.木炭燃烧可放出大量的热,能用作燃料
B.碳和氧气反应生成物一定是二氧化碳
C.碳的几种单质具有相似的化学性质
D.可利用焦炭的还原性冶炼金属
B
解析:碳和氧气反应,氧气充足时生成物是二氧化碳,氧气不足时生成物是一氧化碳。
2 如图是木炭与氧化铜反应的实验装置图,下列说法错误的是 ( )
A.该实验需要较高温度
B.木炭发生了还原反应
C.实验前应把木炭粉充分烘干
D.该实验中的木炭粉可以换成活性炭
B
氧化反应
3 如图是木炭还原氧化铜反应的实验装置图,下列说法正确的是( )
A.给酒精灯加网罩,目的是使火焰集中并提高温度
B.实验过程中,可观察到红棕色粉末逐渐变黑
C.木炭是使氧化铜还原为铜的物质,它具有氧化性
D.实验结束后,应先停止加热,
再将导气管从澄清石灰水中撤出
A
4、下列对一些事实的解释错误的是( )
C
5.用木炭还原氧化铜的实验如图所示。
(1)酒精灯加灯罩的目的是 。
(2)加热一段时间后,可观察到的现象是 。
(3)请写出实验中C发生反应的化学方程式: 。
使火焰集中,提高温度
黑色固体变为红色,澄清石灰水变浑浊
C+2CuO——2Cu+CO2↑
——
高温
课堂小结
碳的化学性质
可燃性
还原反应:含氧化合物里的氧被夺去的反应
完全燃烧生成CO2,
不完全燃烧生成CO
2CuO+C 2Cu+CO2 ↑
高温
化学性质不活泼
常温下
还原性
汇报:阿拉丁
金刚石、石墨和C60(第二课时)
第六单元 课题1
新课导入
古代字画历经几百年甚至几千年而依然不褪色,你知道其中的原因吗?
探究新知
碳原子最外层有4个电子,不容易得失电子,所以常温下,碳的化学性质不活泼,即使受日光照射或与空气、水分接触,都不容易起变化。
二、碳单质的化学性质
探究新知
问题1:古代字画历经几百年甚至几千年而依然不褪色,你知道其中的原因吗?
碳在常温下化学性质不活泼,所以用墨书写或绘制的古代字画能长久保存而不褪色。
问题2:把木制的电线杆在埋入地下前,
为什么要将其表面烧焦呢?
其目的就是为了让电线杆不易腐烂,可以保存久一些
二、碳单质的化学性质
探究新知
1.碳与氧气的反应(可燃性)
现象:
发出白光,放出热量,生成一种能使澄清石灰水变浑浊的气体。
氧气充足:
C+O2 CO2
点燃
在温度升高的情况下,碳能跟很多物质发生化学反应。
思考:在高温下,碳的化学性质如何呢?
二、碳单质的化学性质
探究新知
木炭在氧气中不充分燃烧时,生成一氧化碳。
2C+O2 2CO
点燃
冬天在密闭的空间燃烧木炭烤火,容易发生CO中毒事件,Why?
氧气不足:
CO中毒原理:CO与血液中的血红蛋白结合,使血红蛋白失去携氧的能力,人因缺氧窒息而死
探究新知
氧气充足、燃烧充分时,碳燃烧生成二氧化碳
氧气不充足、燃烧不充分时,碳燃烧生成一氧化碳
CO2
C+O2
点燃
2CO
2C+O2
点燃
1.碳与氧气的反应(可燃性)
二、碳单质的化学性质
探究新知
探究木炭与氧化铜的反应
使火焰集中并提高温度
2.碳与某些氧化物的反应(还原性)
二、碳单质的化学性质
探究新知
2.碳与某些氧化物的反应(还原性)
P110 实验6-2 木炭与氧化铜的反应
探究新知
2.碳与某些氧化物的反应(还原性)
P110 实验6-2 木炭与氧化铜的反应
现 象:
黑色粉末逐渐变成光亮的红色,澄清石灰水变浑浊
反应原理:
2CuO+C 2Cu+CO2
高温
二、碳单质的化学性质
澄清石灰水变浑浊
有CO2生成
黑色粉末变红色
有Cu生成
实验现象:
实验结论:
探究新知
探究新知
2.实验结束时,先撤出导气管,然后再熄灭酒精灯!
防止澄清石灰水倒流入热的试管致使试管破裂。
3.冷却后再倒出试管中的粉末,防止热的Cu被氧化为CuO
1.木炭粉末要烘干,目的是排除水蒸气的干扰,使实验现象更明显;
2.碳与某些氧化物的反应(还原性)
二、碳单质的化学性质
探究新知
金属的冶炼
3C + 2Fe2O3 4Fe + 3CO2↑
高温
探究新知
还原反应
含氧化合物里的氧被夺去的反应,叫做还原反应。
C + 2CuO 2Cu + CO2↑
高温
CuO Cu
失氧
氧化铜具有氧化性,作氧化剂
氧化铜在反应中被还原,发生还原反应
探究新知
C + 2CuO 2Cu + CO2↑
高温
C CO2
得氧
碳具有还原性,作还原剂
碳在反应中被氧化,发生氧化反应
还原反应和氧化反应在一个反应中是同时进行的,且都不属于基本反应类型。
还原反应
探究新知
应用1:碳的还原性可用于冶金工业。
应用2:在高温条件下,碳能使二氧化碳转变成一氧化碳。
如:焦炭可以把铁从它的氧化物矿石里还原出来。
3C + 2Fe2O3 3CO2↑ + 4Fe
高温
C + CO2 2CO
高温
1.下列说法错误的是( )
A.木炭燃烧可放出大量的热,能用作燃料
B.碳和氧气反应生成物一定是二氧化碳
C.碳的几种单质具有相似的化学性质
D.可利用焦炭的还原性冶炼金属
B
解析:碳和氧气反应,氧气充足时生成物是二氧化碳,氧气不足时生成物是一氧化碳。
2 如图是木炭与氧化铜反应的实验装置图,下列说法错误的是 ( )
A.该实验需要较高温度
B.木炭发生了还原反应
C.实验前应把木炭粉充分烘干
D.该实验中的木炭粉可以换成活性炭
B
氧化反应
3 如图是木炭还原氧化铜反应的实验装置图,下列说法正确的是( )
A.给酒精灯加网罩,目的是使火焰集中并提高温度
B.实验过程中,可观察到红棕色粉末逐渐变黑
C.木炭是使氧化铜还原为铜的物质,它具有氧化性
D.实验结束后,应先停止加热,
再将导气管从澄清石灰水中撤出
A
4、下列对一些事实的解释错误的是( )
C
5.用木炭还原氧化铜的实验如图所示。
(1)酒精灯加灯罩的目的是 。
(2)加热一段时间后,可观察到的现象是 。
(3)请写出实验中C发生反应的化学方程式: 。
使火焰集中,提高温度
黑色固体变为红色,澄清石灰水变浑浊
C+2CuO——2Cu+CO2↑
——
高温
课堂小结
碳的化学性质
可燃性
还原反应:含氧化合物里的氧被夺去的反应
完全燃烧生成CO2,
不完全燃烧生成CO
2CuO+C 2Cu+CO2 ↑
高温
化学性质不活泼
常温下
还原性
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
