2024年高考化学第一轮复习:烃
图片预览



文档简介
中小学教育资源及组卷应用平台
2024年高考化学第一轮复习:烃
一、选择题
1.下列有机物类别划分正确的是( )
A.属于苯的同系物
B.含有碳碳双键,属于烯烃
C.属于链状化合物
D.属于脂环化合物
2.下列物质或微粒之间的相互关系错误的是( )
A.和互为同分异构体
B.干冰和冰为同一种物质
C.和互为同系物
D.和互为同位素
3.烷烃及卤代烃是重要的有机化工原料,下列有关说法正确的是( )
A.一氯丁烷有3种不同的结构
B.甲烷可与氯水在光照条件下发生取代反应
C. 和 互为同分异构体
D.乙烷分子中最多有4个原子共平面
4.下列关于乙烯的说法正确的是( )
A.与溴单质或酸性高锰酸钾反应都与碳碳双键有关,但是两者原理不相同
B.CH3CH2Br不可能是乙烯的加成产物,只能是CH3CH3的一卤取代产物
C.乙烯和聚乙烯二者都能使溴水褪色,性质相似
D.乙烯与氢气发生加成反应生成乙烷,所以除去乙烷中混有少量乙烯,可以在一定条件下通入过量氢气
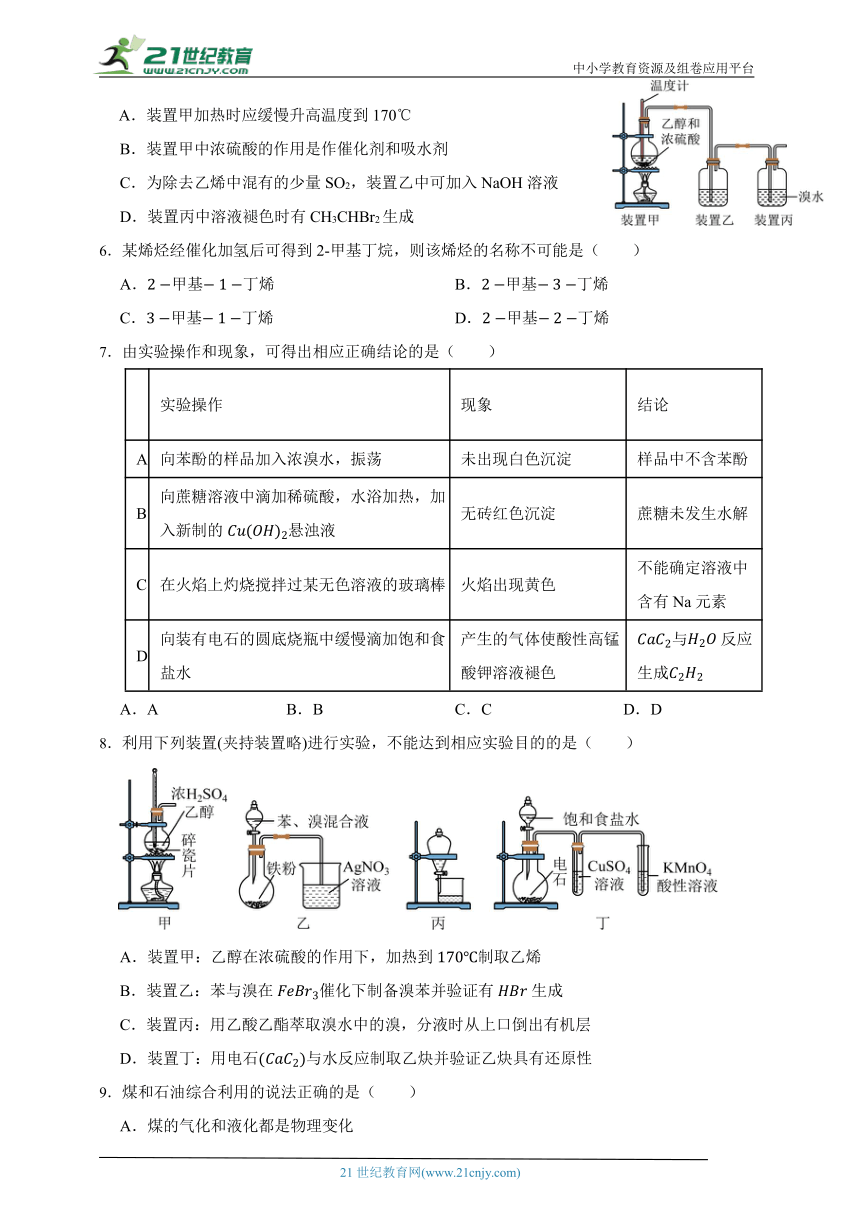
5.实验室通过如图所示装置制取乙烯并验证其性质。下列说法正确的是( )
A.装置甲加热时应缓慢升高温度到170℃
B.装置甲中浓硫酸的作用是作催化剂和吸水剂
C.为除去乙烯中混有的少量SO2,装置乙中可加入NaOH溶液
D.装置丙中溶液褪色时有CH3CHBr2生成
6.某烯烃经催化加氢后可得到2-甲基丁烷,则该烯烃的名称不可能是( )
A.甲基丁烯 B.甲基丁烯
C.甲基丁烯 D.甲基丁烯
7.由实验操作和现象,可得出相应正确结论的是( )
实验操作 现象 结论
A 向苯酚的样品加入浓溴水,振荡 未出现白色沉淀 样品中不含苯酚
B 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的悬浊液 无砖红色沉淀 蔗糖未发生水解
C 在火焰上灼烧搅拌过某无色溶液的玻璃棒 火焰出现黄色 不能确定溶液中含有Na元素
D 向装有电石的圆底烧瓶中缓慢滴加饱和食盐水 产生的气体使酸性高锰酸钾溶液褪色 与反应生成
A.A B.B C.C D.D
8.利用下列装置(夹持装置略)进行实验,不能达到相应实验目的的是( )
A.装置甲:乙醇在浓硫酸的作用下,加热到制取乙烯
B.装置乙:苯与溴在催化下制备溴苯并验证有生成
C.装置丙:用乙酸乙酯萃取溴水中的溴,分液时从上口倒出有机层
D.装置丁:用电石与水反应制取乙炔并验证乙炔具有还原性
9.煤和石油综合利用的说法正确的是( )
A.煤的气化和液化都是物理变化
B.生石灰和煤混合燃烧可减少SO2排放,CaSO3是最终产物
C.石油通过分馏和裂化都能获得汽油
D.石油分馏产品包括汽油、沥青、焦炭等
10.美好生活离不开化学知识的运用。下列有关叙述错误的是( )
A.糖类、蛋白质都是人体必需的基本营养物质
B.石油经过分馏可得到乙烯、丙烯等化工原料
C.灾后重建时常用明矾净化饮用水
D.生活中可定期用84消毒液对居住环境消毒
11.煤、石油、天然气是人类使用的主要能源,同时也是重要的化工原料。下列关于它们的综合利用的叙述错误的是( )
A.以煤、石油和天然气为原料,可以合成高分子材料
B.煤的气化是工业上获得芳香烃的一种重要来源
C.石油的裂解和裂化都是化学变化
D.天然气是一种清洁燃料,属于不可再生资源
12.劳动创造幸福,实干成就伟业,下列劳动项目所涉及的化学知识叙述正确的是( )
选项 劳动项目 化学知识
A 电池研发人员研发用于汽车的氢气燃料电池 电动汽车中的能量转化是将化学能直接转化为动能
B 营养师进行膳食指导:是否需要多补充 纤维素与蔗糖互为同分异构体
C 食品采用真空包装 减慢食品氧化速率
D 面包师用奶油给糕点裱花 奶油是高分子化合物
A.A B.B C.C D.D
13.下列物质中不能与发生化学反应的是( )
①
②
③Na
④
A.①② B.①④ C.② D.③④
14.以2-溴丙烷为原料制取1,2-丙二醇,需要经过的反应是( )
A.加成-消去-取代 B.消去-加成-取代
C.消去-取代-加成 D.取代-消去-加成
15.下列说法不正确的是( )
A.聚乳酸是一种可降解的医用高分子材料
B.饱和溶液能使蛋白质发生盐析
C.油脂发生皂化反应生成甘油和高级脂肪酸
D.纤维素水解的最终产物可用新制检验
二、多选题
16.下列有机物中,属于芳香烃的是( )
A. B.
C. D.
17.下列过程中所发生的化学反应属于取代反应的是( )
A.苯与氢气在镍作催化剂的条件下反应
B.甲烷与氯气的混合其他用强光照射
C.乙醇与乙酸混合液在浓硫酸作用下加热
D.乙烯使酸性高锰酸钾溶液褪色
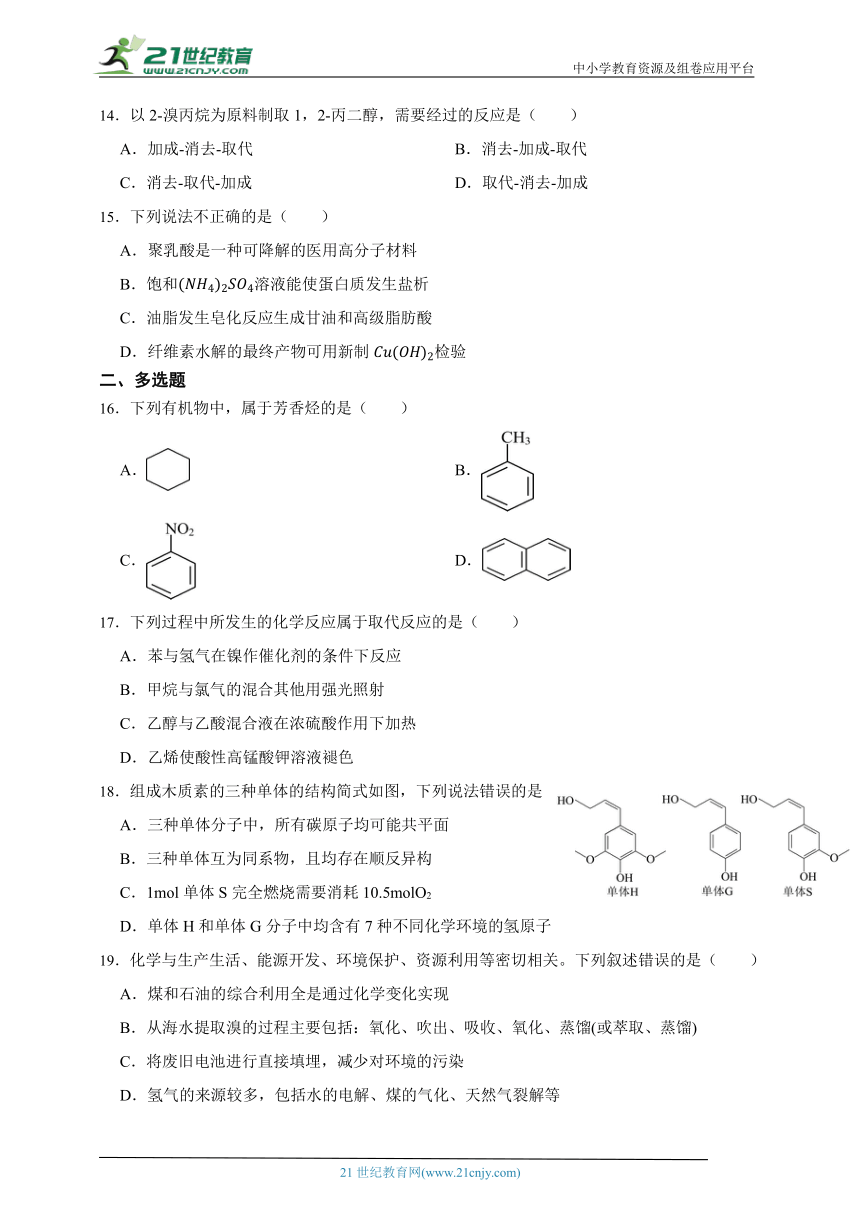
18.组成木质素的三种单体的结构简式如图,下列说法错误的是
A.三种单体分子中,所有碳原子均可能共平面
B.三种单体互为同系物,且均存在顺反异构
C.1mol单体S完全燃烧需要消耗10.5molO2
D.单体H和单体G分子中均含有7种不同化学环境的氢原子
19.化学与生产生活、能源开发、环境保护、资源利用等密切相关。下列叙述错误的是( )
A.煤和石油的综合利用全是通过化学变化实现
B.从海水提取溴的过程主要包括:氧化、吹出、吸收、氧化、蒸馏(或萃取、蒸馏)
C.将废旧电池进行直接填埋,减少对环境的污染
D.氢气的来源较多,包括水的电解、煤的气化、天然气裂解等
20.根据乙烯的性质,推测异戊二烯()的性质,下列说法正确的是( )
A.分子式为C5H8
B.不能使酸性KMnO4溶液褪色
C.含有碳碳双键,是乙烯的同系物
D.能使溴的四氯化碳溶液褪色
21.石油裂解是一个复杂的过程,其产物为混合物。例如:
下列说法中不正确的是( )
A.M为H2,N的分子式为C5H10
B.等物质的量的和完全燃烧时耗氧量相同
C.C4H6可以是烯烃
D.可用溴水区别和
22.下列设计的实验方案能达到实验目的的是( )
实验目的 实验方案
A 配制0.0100 mol·L-1的NaOH溶液 称取0.4 g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至1000mL容量瓶中定容
B 制取并纯化乙烯 将体积比为1∶3的乙醇与浓硫酸混合液(加沸石)加热至170℃,产生的气体依次通过NaOH溶液、碱石灰
C 比较Cl2与H2SO4氧化性强弱 向漂白粉中加入8mol·L-1硫酸,观察有无黄绿色气体
D 探究温度对化学反应速率的影响 向2支试管中均分别加入2mL0.01mol·L-1KMnO4溶液,再分别加入2mL0.1mol·L-1H2C2O4溶液,一支放入80℃热水中,另一支置于室温下,观察现象
A.A B.B C.C D.D
23.下图表示某高分子化合物的结构片段。关于该高分子化合物的推断正确的是( )
A.3种单体通过缩聚反应聚合
B.形成该化合物的单体只有2种
C.其中一种单体为
D.其中一种单体为1,5-二甲基苯酚
三、非选择题
24.现有K、M、N三种烃,其球棍模型如图所示,请回答下列问题。
(1)三种烃中互为同系物的是 (填对应字母,下同)
(2)等质量的三种烃完全燃烧时消耗最多的是 ,生成最多的是 。
(3)1mol K与发生取代反应,待反应完成后测得4种取代物物质的量相等,则消耗的物质的量为 。
(4)以M为基本原料可以合成多种有机物,合成路线如下:
已知:(R代表烃基,X代表卤素原子)
①A与CuO在加热条件下反应的化学方程式为 ,反应类型为 。
②B与D以物质的量之比生成E的化学方程式为 ,反应类型为 。
25.已知A是石油化学工业重要的基本原料,相对分子量为28,在一定条件下能发生如下图的转化关系,已知F是一种高分子化合物。
请回答:
(1)有机物B的结构简式是 。
(2)有机物D中的官能团名称是 。
(3)有机物A与D在一定条件下发生加成反应生成E的化学方程式 。
(4)下列说法正确的是____。
A.F能使溴的四氯化碳溶液褪色
B.B可以直接与酸性高锰酸钾溶液反应生成D
C.A生成B与C生成D的反应类型相同
D.D能使石蕊试液变红
26.有机化合物不仅数量多,而且分布广,与生产、生活密切相关。根据要求回答下列问题:
I.
(1)下列物质中,属于同一物质的是 (填序号,下同),互为同系物的为 ,互为同素异形体的为 。
A.正丁烷与2-甲基丁烷 B.金刚石和石墨 C.和D.苯与溴苯E.和
(2)II.聚甲基丙烯酸甲酯(PMMA)俗称有机玻璃,其结构简式为:。合成有机玻璃的路线如图所示:
含有的官能团的名称是 ,反应②的类型是 。
(3)A的结构简式为 。
(4)关于X的说法正确的是____
A.能与发生加成反应 B.不能使酸性高锰酸钾溶液褪色
C.能与NaOH溶液反应 D.该物质易溶于水
(5)与甲基丙烯酸()含有相同官能团的同分异构体的结构简式 (任写一种)。
27.某化合物Ⅰ可通过如图合成路线合成:
已知:
回答下列问题:
(1)中,属于烃的是 (填标号)。
(2)的反应类型属于 (填“加成”或“加成”)。
(3)F在氢氧化钠的水溶液中加热,发生反应的化学方程式为 。
(4)完全燃烧消耗 。
(5)最多可与 反应,所得产物为 。
(6)中浓硫酸的作用是 。
28.按要求回答下列问题。
(1)用系统命名法对,命名: 。
(2)已知乙酸和乙酸乙酯的混合物中含H质量分数为7.8%,则其中含氧质量分数是 。
(3)熔点比较:2-甲基丁烷 正戊烷(选填>、<、=)。
(4)在加热条件下与足量NaOH溶液完全反应的化学方程式 。
(5)甲烷与氯气在光照条件下反应,得到的产物中含有二氯甲烷、三氯甲烷和四氯化碳,分离它们的方法是 。
(6)写出苯甲醛与银氨溶液反应的化学方程式 。
(7)写出对苯二甲酸与乙二醇在催化剂作用下发生缩聚反应的化学方程式 。
(8)的同分异构体有多种,满足下列2个条件的同分异构体有 种(不考虑顺反异构),其中核磁共振氢谱有4组峰的结构简式为 (任写一种)。
①具有相同的官能团 ②苯环上有两个取代基。
(9)中的中心离子是 ,配体是 ,中含有键的物质的量为 mol。
29.以乙炔为原料制备乙酸和聚丙烯酸甲酯的合成路线如下(部分反应条件已省略)。回答下列问题:
(1)写出聚甲基丙烯酸甲酯链节的结构简式: 。
(2)写出①~⑤中原子利用率为100%的化学反应的序号: 。
(3)写出下列两个反应的化学方程式(注意标明反应条件):
反应②: ;
反应⑤: 。
(4)写出由乙炔经一步反应生成乙醛的方程式: 。
(5)可以用新制的鉴别乙醛和乙酸,请写出相关化学方程式: ; 。
30.化合物G是合成一种杀虫剂的重要中间体,其合成路线如图:
回答下列问题
(1)B中官能团的名称为 ,A生成B的反应类型为 。
(2)写出B生成C的反应方程式 。
(3)W的分子式为,其结构简式为 。
(4)满足下列条件所有的A的同分异构体有 种。
①属于芳香族化合物; ②能发生银镜反应;
写出其中核磁共振氢谱有3组峰的所有结构简式 。
(5)请以和为原料设计合成的路线(无机试剂任选) 。
31.用于制造隐形眼镜的功能高分子材料HEMA的合成路线如图所示,其中G可用于生产汽车防冻液,K是六元环状化合物,E在一定条件下可发生缩聚反应生成L。
已知:
回答下列问题:
(1)A分子中可以共平面的原子数最多有 个;①的反应类型是 。
(2)B→C的反应试剂及条件为 。
(3)写出下列反应的化学方程式:
反应④ ;
反应⑤ 。
(4)W是F与足量氢气加成后的产物,则W的一溴取代物同分异构体中符合下列条件的数目有 种(考虑立体异构)。
①能发生银镜反应和水解反应②不含环状结构③只含有两种官能团
(5)制造隐形眼镜的材料应该具有良好的亲水性,请从HEMA的结构上分析它可以作为隐形眼镜材料的可能原因 。
(6)以甲苯为原料合成 的流程图如下:
①反应条件1是 。
②K的名称是 。
32.丙烯酸乙酯天然存在于菠萝等水果中,是一种食品用合成香料。一种合成方法如下:
已知:有机物A是一种植物生长调节剂。
(1)有机物A的电子式为 。
(2)丙烯酸乙酯中含有的官能团名称为 。
(3)有机物C的结构简式为 。
(4)反应Ⅰ的化学方程式为 。
(5)反应Ⅰ、Ⅱ、Ⅲ中,原子利用率为100%的是 。
(6)46 g有机物B与36 g有机物C在一定条件下发生反应Ⅲ,如果实际产率是72%,则可得到丙烯酸乙酯的质量为 g。
(7)某实验小组用以下装置制备丙烯酸乙酯:
①球形干燥管c除起冷凝作用外,它的另一重要作用是 。
②待收集到一定量产物后停止加热,取下试管b并振荡、静置,可观察到 (填实验现象)。
③分离试管b中的液体混合物,采用的方法为 。
33.丙酸苯甲酯为无色液体,有鲜花的甜香气味,常用于配制食品、香烟、香皂、日用化妆香精,其合成路线如图所示。
回答下列问题:
(1)D的结构简式为 ,其名称为 。
(2)反应①的化学方程式为 ,反应②的反应类型为 。
(3)E中含有 种不同化学环境的氢,其与NaOH溶液反应的化学方程式为 。
(4)能与FeCl3溶液发生显色反应的D的同分异构体有 种,其中核磁共振氢谱有4组峰的同分异构体的结构简式为 。
答案解析部分
1.【答案】C
【知识点】有机物的结构和性质;饱和烃与不饱和烃;芳香烃;苯的同系物及其性质
【解析】【解答】A、 为苯乙烯,与苯结构不相似,不属于苯的同系物,故A错误;
B、 CH2=CH-COOH中除了C、H外,还含O元素,不属于烯烃,故B错误;
C、 中不存在碳环,碳原子成链状,属于链状化合物,故C正确;
D、 含有苯环,不属于脂环化合物,故D错误;
故答案为:C。
【分析】A、结构相似,在分子组成上相差一个或n个CH2的化合物互为同系物;
B、 烃是只含碳氢两种元素的有机化合物;
C、 分子中碳原子相互链接成链状的有机化合物为链状化合物;
D、含有由碳原子组成的环状结构,但不含有苯环的有机化合物为脂环化合物。
2.【答案】B
【知识点】同分异构现象和同分异构体;同系物;同位素及其应用
【解析】【解答】A.二者分子式相同,但是结构不同,所以互为同分异构体,A项正确;
B.干冰为二氧化碳,冰为水,不属于同种物质,B项错误;
C.二者结构相似,分子相差1个CH2,属于同系物,C项正确;
D. 和 质子数相同,中子数不同,互为同位素,D项正确;
故答案为:B。
【分析】A.同分异构概念:分子式相同,结构不同的两种有机物;
C.同系物概念:1.结构必须相似,2.分子相差若干CH2;
D.同位素概念:质子数相同,中子数不同的同种元素不同原子。
3.【答案】D
【知识点】卤代烃简介;烷烃
【解析】【解答】A.已知丁基有4种不同的结构,则一氯丁烷有4种不同的结构,故A错误;
B.甲烷可与氯气在光照条件下发生取代反应,不能和氯水反应,故B错误;
C.依据甲烷是正四面体型结构可知,和同一种物质,故C错误;
D.乙烷分子中单键可以旋转,可以使得两个碳原子及每个碳上的1个氢原子共面,故最多有4个原子共平面,故D正确;
故选D。
【分析】A.依据丁基有4种不同的结构判断;
B.注意反应物质的状态;
C.依据甲烷是正四面体型结构分析;
D.烷烃分子中单键可以旋转分析。
4.【答案】A
【知识点】乙烯的化学性质
【解析】【解答】A、乙烯与溴发生加成反应,与酸性高锰酸钾发生氧化还原反应,故A正确;
B、乙烯和HBr发生加成反应生成CH3CH2Br,故B错误;
C、聚乙烯不含碳碳双键,不能使溴水褪色,故C错误;
D、通入过量氢气会引入新杂质,故D错误;
故答案为:A。
【分析】乙烯中含有碳碳双键,所有原子共平面,能发生加成反应、氧化反应。
5.【答案】C
【知识点】乙烯的化学性质;乙烯的实验室制法
【解析】【解答】A、为了防止副反应的发生,装置甲加热时应迅速升高温度到170℃,故A错误;
B、装置甲中浓硫酸作催化剂和脱水剂,故B错误;
C、二氧化硫能与NaOH溶液反应,乙烯不与NaOH溶液反应,装置乙是为了除去二氧化硫,因此装置乙中可加入NaOH溶液,故C正确;
D、装置丙中,乙烯与溴水发生加成反应生成CH2BrCH2Br,故D错误;
故答案为:C。
【分析】装置甲中,乙醇和浓硫酸发生消去反应生成乙烯,装置乙可除去乙烯中混有的二氧化硫,丙装置中的溴水可检验乙烯。
6.【答案】B
【知识点】烯烃;加成反应
【解析】【解答】2-甲基丁烷相邻碳原子之间各去掉1个氢原子形成双键,从而得到烯烃,根据2-甲基丁烷的碳链结构,可知相邻碳原子之间去掉1个氢原子形成双键有3种情况,分别得到:2-甲基-1-丁烯,3-甲基-1-丁烯,2-甲基-2-丁烯,不可能是2-甲基-3-丁烯,故选B;
故答案为:B。
【分析】相邻碳原子之间各消去1个氢原子形成碳碳双键,即得到烯烃。
7.【答案】C
【知识点】焰色反应;乙炔炔烃;苯酚的性质及用途;二糖的性质和用途;化学实验方案的评价
【解析】【解答】 A.依据相似相溶原理,向苯酚的样品加入浓溴水,振荡未出现白色沉淀,可能是溴水量不足,生成的三溴苯酚溶解在过量的苯酚中,不能说明样品中不含苯酚,A错误;
B.注意反应的环境,向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的Cu(OH)2悬浊液之前应先加NaOH溶液将溶液调为碱性,B错误;
C.玻璃中含有Na2SiO3,因此火焰出现黄色不能确定溶液中含有Na元素,C正确;
D.电石与水反应的产物除了C2H2,还有H2S等具有还原性的气体生成、它们能使高锰酸钾溶液褪色,生成的气体未经除杂直接通入酸性高锰酸钾溶液中,溶液褪色不能说明CaC2与H2O反应生成C2H2,D错误;
故选C。
【分析】 A.依据相似相溶原理分析,注意反应物量的大小;
B.注意反应的环境;
C.玻璃中含有Na元素;
D.电石中含有H2S等具有还原性的气体。
8.【答案】B
【知识点】乙炔炔烃;苯的结构与性质;乙醇的消去反应;乙酸乙酯的制取;化学实验方案的评价
【解析】【解答】A、乙醇在浓硫酸的作用下加热到170℃时发生消去反应生成乙烯,该装置能达到实验目的,故A不符合题意;
B、溴易挥发,挥发的溴与硝酸银反应生成淡黄色沉淀,不能证明苯与液溴发生取代反应,故B符合题意;
C、溴不溶于水,易溶于有机溶剂,且乙酸乙酯不溶于水、其密度小于水的密度,则用乙酸乙酯萃取溴水中的溴,分液时从上口倒出有机层,该装置能达到实验目的,故C不符合题意;
D、电石和水反应生成乙炔,同时会产生还原性杂质,利用硫酸铜除去杂质气体,乙炔能被酸性高锰酸钾氧化使酸性高锰酸钾褪色,可检测乙炔,该装置能达到实验目的,故D不符合题意;
故答案为:B。
【分析】A、乙醇在170℃时发生消去反应生成乙烯;
B、溴易挥发,挥发的溴也能与硝酸银反应;
C、乙酸乙酯的密度小于水;
D、乙炔能被酸性高锰酸钾氧化。
9.【答案】C
【知识点】石油副产品的综合应用;石油的分馏产品和用途;煤的干馏和综合利用
【解析】【解答】A.煤的气化和液化均产生新物质,是化学变化,故A不符合题意;
B.亚硫酸钙在空气中变为硫酸钙,故B不符合题意;
C.石油的分馏和裂化均可得到汽油,故C符合题意;
D.石油分馏的的产品是汽油、沥青、煤油和柴油等,焦炭是煤干馏得到的,故D不符合题意;
故答案为:C
【分析】A.煤的气化和液化是化学变化
B.生石灰除去煤混合物中的硫元素,产物是硫酸钙
C.石油的分馏得到汽油,石油的裂解可得到汽油
D.焦炭是煤的干馏产物
10.【答案】B
【知识点】石油的裂化和裂解;水的净化
【解析】【解答】A、糖类、蛋白质均为人体必须的基本营养物质,故A正确;
B、石油经过裂解得到乙烯、丙烯等化工原料,故B错误;
C、明矾中含有铝离子,水解生成氢氧化铝胶体,能吸附水中的悬浮杂质,可用于净水,故C正确;
D、84消毒液的主要成分次氯酸钠具有强氧化性,能使蛋白质变性,因此可定期用84消毒液对居住环境消毒,故D正确;
故答案为:B。
【分析】A、糖类、油脂、蛋白质、水、无机盐等是人体必需的营养物质;
B、石油裂解得到乙烯、丙烯等短链烃;
C、明矾水解生成氢氧化铝胶体;
D、84消毒液的主要成分为次氯酸钠,次氯酸钠具有强氧化性。
11.【答案】B
【知识点】使用化石燃料的利弊及新能源的开发;化石燃料与基本化工原料
【解析】【解答】A.以石油、煤和天然气为主要原料生产的材料属于有机合成材料,A正确;
B、煤的干馏是工业上获得芳香烃的一种重要来源,故B错误;
C、石油的分馏是物理变化,裂化、裂解,催化重整都是化学变化,故C正确;
D.天然气的主要成分是甲烷,属于不可再生资源,故D正确;
故答案为:B。
【分析】本题主要考查化石燃料的应用。
A、合成材料又称人造材料,是人为地把不同物质经化学方法或聚合作用加工而成的材料;以石油、煤和天然气为主要原料生产的材料属于有机合成材料,如:塑料、合成橡胶、合成纤维;
B、煤干馏可以获得煤焦油,其中含有芳香烃;
C、裂化的目的是为了得到更多的10个碳原子左右的汽油,裂解的目的是为了得到碳原子数更少的烯烃,主要为了生产乙烯。可见裂解的程度比裂化更大,也成为裂解是深度裂化,由于都分解生成了新物质,所以都是化学变化;
D.天然气的主要成分是甲烷,产物只有二氧化碳和水,属于不可再生资源。
12.【答案】C
【知识点】化学反应速率;生活中的有机化合物;有机高分子化合物的结构和性质;原电池工作原理及应用
【解析】【解答】A.燃料电池,是将化学能转化为电能,A错误;
B.纤维素属于多糖,蔗糖属于二糖,不是同分异构体,B错误;
C.真空包装,去除氧气,防止食物被氧化,C正确;
D.奶油不属于有机高分子化合物,奶油属于油脂,D错误。
故答案为:C。
【分析】本题主要考查生活生产中的化学性质和用途。
13.【答案】C
【知识点】取代反应;酯化反应
【解析】【解答】根据有机物结构可知,含有羟基和羧基,既可以与酸发生酯化反应,也可以与醇发生酯化反应,同时还可以与金属钠反应置换出氢气;所以不能反映的物质为②;
故答案为:C。
【分析】根据有机物的结构和官能团来判断有机物的性质,进而判断能够与那些物质进行反应。
14.【答案】B
【知识点】有机物的结构和性质;取代反应;加成反应;消去反应
【解析】【解答】 2-溴丙烷先发生消去反应得到丙烯,丙烯再与溴单质发生加成反应,得到1,2-二溴丙烷,再发生取代反应,用-OH取代Br,得到产物1,2-丙二醇 。B选项符合题意。
故答案为:B。
【分析】消除反应,又称脱去反应或是消去反应,是指一种有机化合物分子和其他物质反应,失去部分原子或官能基(称为离去基)的有机反应。反应后分子会产生多键,为不饱和有机化合物;
加成反应是反应物分子中以重键结合的或共轭不饱和体系末端的两个原子,在反应中分别与由试剂提供的基团或原子以σ键相结合,得到一种饱和的或比较饱和的加成产物。这个加成产物可以是稳定的;也可以是不稳定的中间体,随即发生进一步变化而形成稳定产物。
取代反应是指化合物或有机物分子中任何一个原子或原子团被试剂中同类型的其它原子或原子团所替代的反应,用通式表示为:R-L(反应基质)+A-B(进攻试剂)→R-A(取代产物)+L-B(离去基团)属于化学反应的一类。
15.【答案】C
【知识点】高分子材料;盐析;水解反应
【解析】【解答】A.聚乳酸是一种可降解的医用高分子材料,故A不符合题意;
B.饱和硫酸铵中有移动的阴阳离子可使蛋白质发生盐析,故B不符合题意;
C.油脂发生皂化反应时生成甘油和高级脂肪酸钠,故C不符合题意;
D.纤维素水解为葡萄糖,可以用新制的氢氧化铜进行检验,故D不符合题意;
故答案为:C
【分析】A.聚乳酸可以发生降解;
B.盐溶液可以使蛋白质发生盐析;
C.油脂皂化反应得到的是甘油和高级脂肪酸钠;
D.醛基的检验可以用新制的氢氧化铜悬浊液。
16.【答案】B,D
【知识点】芳香烃
【解析】【解答】芳香烃即含有苯环,且有C、H两种元素组成的化合物;
A、该分子为环己烷,属于环烷烃,A错误;
B、该分子为甲苯,属于芳香烃,B正确;
C、该分子为硝基苯,含有苯环和O元素,属于芳香烃的衍生物,C错误;
D、该分子为萘,属于芳香烃,D正确;
故答案为:BD
【分析】烃只含C。H两种元素,芳香烃即含有苯环的烃类。
17.【答案】B,C
【知识点】甲烷的化学性质;乙烯的化学性质;苯的结构与性质;乙醇的化学性质;取代反应
【解析】【解答】A. 苯与氢气在镍和加热条件下反应生成环己烷,是加成反应,A错误;
B.甲烷和氯气在光照条件下,发生取代反应,B正确;
C.乙醇和乙酸在浓硫酸作用下发生反应,生成乙酸乙酯和水,是酯化反应,酯化反应也属于取代反应,C正确;
D.乙烯是酸性高锰酸钾褪色,属于氧化反应,D错误。
故答案为:B、C。
【分析】本题主要考查常见有机物的化学性质,掌握相关性质便可解题。
苯化学性质:a.氧化反应:与氧气反应,不与酸性高锰酸钾反应;b.取代反应;c.硝化反应;d.加成反应:与氢气;
甲烷化学性质:a.稳定性:不与强酸强碱,酸性高锰酸钾反应;
b.氧化反应:与O2反应生成二氧化碳和水;
c.取代反应:与卤素在光照条件下发生取代反应。
乙烯化学性质:a.氧化反应:与氧气反应,使酸性高锰酸钾褪色;b.加成反应:与氢气,溴水,水,氯化氢等; c.加聚反应。
18.【答案】B,C
【知识点】苯的同系物及其性质
【解析】【解答】A.三种单体分子中,存在苯环、碳碳双键,所有碳原子均可能共平面,A不符合题意;
B.三种单体中,官能团种类不同,不是同系物,B符合题意;
C.1mol单体S完全燃烧需要消耗11.5molO2,C符合题意;
D. 单体H和单体G分子中均含有7种不同化学环境的氢原子,D不符合题意;
故答案为:BC
【分析】A.存在苯环、碳碳双键,所有碳原子均可能共平面;
B.官能团种类不同,不是同系物;
C.1mol单体S完全燃烧需要消耗11.5molO2;
D. 单体H和单体G分子中均含有7种不同化学环境的氢原子。
19.【答案】A,C
【知识点】海水资源及其综合利用;常见的生活环境的污染及治理;石油副产品的综合应用;煤的干馏和综合利用
【解析】【解答】A.蒸馏是利用混合物中各组分熔沸点不同而分离物质的方法,没有新物质生成,则石油蒸馏过程中没有新物质生成,所以是通过物理变化实现,故A符合题意;
B.酸化的海水中通入氯气发生Cl2+2Br-=Br2+2Cl-,吹出塔中通入热空气吹出溴单质,在吸收塔中用二氧化硫和水吸收发生SO2+Br2+2H2O=2HBr+H2SO4,再通入氯气和水蒸气,发生Cl2+2Br-=Br2+2Cl-,达到富集溴的目的,冷凝精馏分离出产品溴,所以从海水提取溴的过程主要包括:氧化、吹出、吸收、氧化、蒸馏,故B符合题意;
C.废旧电池中含有重金属汞、镉、铅,进行直接填埋,对土壤、地下水污染特别严重,应回收利用可以减少污染,故C符合题意;
D.电解水生成氢气和氧气,煤的气化可得到氢气和CO,天然气中低碳烷烃在高温下吸收大量能量而分解为低碳不饱和烃和氢,所以氢气的来源较多,包括水的电解、煤的气化、天然气裂解等,故D不符合题意;
故答案为:AC。
【分析】A、石油的分馏是物理变化;
B、海水提溴包括溴离子的氧化,空气吹出,二氧化硫吸收,溴离子的氧化和溴的蒸馏;
C、废旧电池填埋会污染土壤;
D、氢气可以来自于水的电解、煤的气化、天然气裂解 。
20.【答案】A,D
【知识点】乙烯的化学性质;同系物;分子式
【解析】【解答】A.分子式为C5H8,A符合题意;
B.异戊二烯有碳碳双键,能被高锰酸钾氧化,溶液褪色,B不符合题意;
C.乙烯有1个碳碳双键,异戊二烯有2个碳碳双键,官能团数目不同,不是同系物,C不符合题意;
D.异戊二烯有碳碳双键,能与溴反应,溶液褪色,D符合题意;
故答案为:AD
【分析】A.分子式为C5H8;
B.碳碳双键能被高锰酸钾氧化;
C.官能团数目不同,不是同系物;
D.碳碳双键能与溴反应。
21.【答案】A,B
【知识点】有机物中的官能团;有机物的推断;烯烃;取代反应;加成反应
【解析】【解答】A.由图可知,甲基环戊烷加热分解时,生成物有碳碳双键,所以产物M为两个氢原子结合,即为H2。根据质量守恒定律可知,甲基环戊烷加热生成甲烷和N,则N为C5H8,A错误;
B.等物质的量的 和,碳原子相同但是氢原子数量不相同,所以完全燃烧时耗氧量不同,B错误;
C. C4H6中可以存在两个碳碳双键,也可以存在一个碳碳三键,所以 C4H6可以是烯烃,C正确;
D.因为中有不饱和碳碳双键可以使溴水褪色,所以可以可用溴水区别和 ,D正确;
故答案为:A、B。
【分析】本题主要考查有机物质的性质及应用,需要掌握基础的官能团的性质,质量守恒定量,可以解答此题。需要注意的点:不饱和烃有烯烃和炔烃,CnH2n-2(n>2)可能是烯烃或者炔烃。
A.根据质量守恒定律计算;
B.消耗氧的量,需要碳原子和氢原子的耗氧量相加;
C.C4H6中可以存在两个碳碳双键,也可以存在一个碳碳三键;
D.含有碳碳双键的物质可以使溴水褪色,烷烃不能使溴水褪色。
22.【答案】B,D
【知识点】氯气的化学性质;乙烯的实验室制法;配制一定物质的量浓度的溶液;探究影响化学反应速率的因素;化学实验方案的评价
【解析】【解答】A.0.4gNaOH固体的物质的量,由于NaOH溶解过程放热,因此需等溶液冷却至室温后再转移至容量瓶,A不符合题意;
B.产生的乙烯中混有乙醇和水蒸气,可通过NaOH溶液吸收乙醇,再通过碱石灰除去水蒸气,即可得到纯净的乙烯,B符合题意;
C.可通过反应Cl2+SO2+2H2O=2HCl+H2SO4说明氧化性Cl2>H2SO4,C不符合题意;
D.由于浓度、温度都会影响反应速率,因此探究温度对反应速率的影响,应控制反应浓度相同,D符合题意;
故答案为:BD
【分析】A.NaOH溶解过程放热,需冷却至室温后再转移至容量瓶;
B.反应生成的乙烯中混有乙醇和水蒸气;
C.根据氧化剂的氧化性强于氧化产物分析;
D.结合反应速率的影响因素分析;
23.【答案】A,C
【知识点】有机物的结构和性质;同分异构现象和同分异构体
【解析】【解答】A、縮宿聚反应的单体是:苯酚、甲醛和氨基苯,A项正确
B、縮聚反应的单体是:苯酚、甲醛和氨基苯,B项错误;
C、其中一种单体为 ,C项正确;
D、单体是:苯酚、甲醛和氨基苯,D项错误;
故答案为:AC
【分析】找高分子单体的方法:半键缩回来,临碳快牵上,单变双,双变单,若无双变单,单键就断掉。
24.【答案】(1)K、N
(2)K;M
(3)2.5mol
(4)CH3CH2OH+CuOCH3CHO+H2O+Cu;氧化反应;2CH3COOH+HOCH2CH2OHCH3COOCH2CH2OOCCH3+2H2O;酯化反应或取代反应
【知识点】甲烷的化学性质;乙烯的化学性质;烃类的燃烧;同系物;酯化反应
【解析】【解答】(1)K为CH4,M为CH2=CH2,N为CH3CH3,其中CH4和CH3CH3都属于烷烃,二者的结构相似,分子组成上相差一个CH2,因此二者互为同系物。所以三种烃中互为同系物的是K和N。
(2)三种烃的最简式分别为CH4、CH2、CH3,其中氢元素质量分数最大的是K(CH4),碳元素质量分数最大的是M(C2H4)。等质量的三种烃完全燃烧,所含氢元素的质量分数越大, 其燃烧过程中消耗O2的量越多,因此消耗O2最多的是K。所含碳元素的质量分数越大,则其燃烧生成CO2的量越多,因此生成CO2最多的是M。
(3)K为CH4,与Cl2在光照条件下发生取代反应,生成CH3Cl、CH2Cl2、CHCl3、CCl4。完全反应后,生成的四种取代产物的物质的量相等,根据碳元素守恒可得,各种取代产物的物质的量都为0.25mol。因此反应消耗Cl2的物质的量为0.25mol×1+0.25mol×2+0.25mol×3+0.25mol×4=2.5mol。
(4)①由分析可知,A为C2H5OH,C2H5OH与CuO在加热条件下发生氧化反应,生成CH3CHO和H2O,该反应的化学方程式为:C2H5OH+CuOCH3CHO+H2O+Cu。该反应的反应类型为氧化反应。
②由分析可知,B为CH3COOH,D为HOCH2CH2OH,二者按2:1反应,其反应原理为酯化反应,生成E的结构简式为CH3COOCH2CH2OOCCH3,该反应的化学方程式为:2CH3COOH+HOCH2CH2OH CH3COOCH2CH2oOCCH3+2H2O。该反应的反应类型为酯化反应(或取代反应)。
【分析】(1)同系物是指结构相似,分子组成上相差一个或多个CH2的有机物。
(2)等质量的烃完全燃烧,烃中氢元素的质量分数越大,则其燃烧所需要O2的量越多。含碳元素的质量分数越大,则燃烧生成的CO2越多。
(3)K为CH4,结合CH4与Cl2的取代反应分析。
(4)M为CH2=CH2,与H2O在催化剂条件下反应生成A,因此A为C2H5OH,与Br2的CCl4溶液发生加成反应,生成C,因此C的结构简式为BrCH2CH2Br。C2H5OH在酸性KMnO4溶液的氧化作用下,生成B,因此B的结构简式为CH3COOH。C与NaOH溶液发生水解反应,其中Br原子被-OH取代,生成醇,因此D的结构简式为HOCH2CH2OH。B与D在浓硫酸/加热条件下发生酯化反应, 生成E,因此E的结构简式为CH3COOCH2CH2OOCCH3。
25.【答案】(1)
(2)羧基
(3)
(4)B;D
【知识点】乙烯的化学性质;乙烯的用途;乙醇的化学性质;乙酸的化学性质;取代反应
【解析】【解答】乙烯是石油化学工业重要的基本原料, 且相对分子量为28 ,故A为乙烯,乙烯在催化剂的条件下发生加聚反应生成聚乙烯,即F;乙烯与水反应生成乙醇,乙醇氧化生成乙酮,乙酮氧化生成乙酸,乙酸和乙醇发生酯化反应生成乙酸乙酯。
(1)有机物B为乙醇,结构简式为 。
(2)有机物D为乙酸,含有的官能团名称是羧基。
(3)乙烯与乙酸在催化剂作用下生成乙酸乙酯,反应前有碳碳双键,反应后无碳碳双键,则反应为加成反应。 化学方程式为 。
(4)A:聚乙烯分子内无碳碳双键,不能与溴发生加成反应,不能使溴的四氯化碳溶液褪色,故A不符合题意;
B:乙醇可以被酸性高锰酸钾溶液直接氧化为乙酸,故B符合题意;
C:乙烯转化为乙醇的反应是加成反应,乙酮转化为乙酸的反应是氧化反应,反应类型不同,故C不符合题意;
D:乙酸显酸性,能使石蕊试液变红,故D符合题意;
故答案为:BD
【分析】解题关键是推断出A为乙烯,乙烯由于含有碳碳双键,可以发生加成反应和加聚反应,推断出B为乙醇,F为一种高分子化合物,F为聚乙烯;乙醇可以分步氧化成乙酮、乙酸,也可以直接被酸性高锰酸钾溶液氧化为乙酸,乙醇与乙酸在浓硫酸加热的条件下发生酯化反应生成乙酸乙酯。
26.【答案】(1)E;A;B
(2)羟基;加聚反应
(3)
(4)B;C
(5)或
【知识点】同素异形体;同分异构现象和同分异构体;同系物;聚合反应;酯化反应
【解析】【解答】(1)A、正丁烷的结构简式为CH3CH2CH2CH3,2-甲基丁烷的结构简式为,二者的结构相似,分子组成上相差一个-CH2-,因此互为同系物。
B、金刚石和石墨都是由碳元素组成的单质,互为同素异形体。
C、二者的分子式都是C3H6,但结构不同,因此互为同分异构体.
D、溴苯是苯的一溴代物。
E、二者的分子式和结构都相同,属于同一种物质。
综上,上述物质中属于同一物质的是E;互为同系物的是A;互为同素异形体的是B。
(2)CH3OH中含有官能团羟基。反应①为酯化反应,所得产物A中含有碳碳双键;反应②得到高分子化合物X,发生加聚反应。
(3)A是由与CH3OH发生酯化反应所得的产物,酯化反应的原理为“酸脱羟基,醇脱氢”,因此A的结构简式为。
(4)A、高分子化合物X中不含有碳碳双键,因此不能与Br2/CCl4发生加成反应,A不符合题意。
B、该高分子化合物X中不含有碳碳双键,其所含的酯基也不能使酸性KMnO4溶液褪色,B符合题意。
C、该高分子化合物X中含有酯基,能与NaOH溶液发生水解反应,C符合题意。
D、该高分子有机物中含有的碳原子数很多,因此不溶于水,D不符合题意。
故答案为:BC
(5)与具有相同的官能团,即含有碳碳双键、羧基;因此其同分异构体存在的是碳碳双键的位置异构,满足条件的同分异构体的结构简式为CH2=CH-CH2-COOH、CH3-CH=CH-COOH。
【分析】(1)分子式相同,结构相同的为同一种物质;同系物是指结构相似,分子组成上相差一个活多个CH2的有机物;同素异形体是指由同种元素组成的不同单质。
(2)CH3OH所含的官能团为羟基。物质A经反应②后得到高分子化合物X,据此判断反应类型。
(3)根据反应物的结构特点确定其反应原理,从而得出A的结构简式。
(4)根据X的结构简式以及具有的官能团分析选项。
(5)含有相同的官能团的同分异构体存在碳链异构和官能团位置异构,据此书写其同分异构体的结构简式。
27.【答案】(1)ACE
(2)加成
(3)+2NaOH+2NaBr
(4)1.7
(5)2;、
(6)作催化剂和吸水剂
【知识点】有机物的结构和性质;加成反应;酯化反应;物质的简单分类
【解析】【解答】(1)烃指的是C、H化合物:ACE;
(2)根据合成路线知: E到F是环己二烯与HBr发生加成反应;
(3) F在氢氧化钠的水溶液中加热, 发生的是卤代烃的水解反应,利用-OH取代溴原子: +2NaOH+2NaBr ;
(4)C是环己烯,1mol环己烯与足量氧气反应时,消耗的氧气的物质的量为8.5molO2,则 完全燃烧消耗 1.7mol氧气;所得的产物为对环己二醇、乙酸钠和水;
(5)I中含有两个酯基,1mol酯基在碱性环境下水解需要的NaOH为2mol;
(6) 的反应是酯化反应,在酯化反应中,浓硫酸的作用是催化剂和吸水剂;
【分析】(1)烃的构成元素包括:C和H,分类包括饱和烃和不饱和烃;芳香烃和脂肪烃等;
(2)环己二烯含有2个碳碳双键,与1molBr2发生1,4-加成可以得到F;
(3)卤代烃水解反应是指卤代烃与水在酸性或碱性条件下发生反应,生成相应的醇和相应的卤化物离子的过程;
(4)环己烯燃烧的方程式为:2C6H10+17O2=12CO2+10H2O;
(5)酯类在碱性条件下水解得到的产物是羧酸盐、水和醇;
(6)酯化反应需要在碱性环境下进行,选择浓硫酸的作用是催化剂,且可以作吸水剂,将水从反应中脱离,可以促进可逆反应正向进行,提高酯的产率。
28.【答案】(1)2,3-二甲基戊烷
(2)45.4%
(3)<
(4)+3NaOH+NaCl+CH3OH+H2O
(5)蒸馏
(6)+2[Ag(NH3)2]OH+2Ag↓+3NH3+H2O
(7)n +nHOCH2CH2OH+(2n-1)H2O
(8)15;、、、、
(9)Cu2+;NH3;16
【知识点】配合物的成键情况;有机化合物的命名;同分异构现象和同分异构体;醛的化学性质;缩聚反应
【解析】【解答】(1)该有机物的最长碳链含有5个碳原子,为戊烷。其中第二个、第三个碳原子上都含有一个-CH3,因此该有机物的命名为:2,3-二甲基戊烷。
(2)乙酸的分子式为C2H4O2,乙酸乙酯的分子式为C4H8O2,其中碳氢元素的质量比相同,都是1:6,所以混合物中碳元素的质量分数为7.8%×6=46.8%,因此混合物中氧元素的质量分数为1-7.8%-46.8%=45.4%。
(3)2-甲基丁烷的结构简式为,正戊烷的结构简式为CH3-CH2-CH2-CH2-CH3,二者的分子式相同,结构不同,互为同分异构体。烷烃的同分异构体中,支链越多,熔点越低,因此熔点:2-甲基丁烷<正戊烷。
(4)碳卤键、酯基都能与NaOH溶液发生水解反应,其水解产生的酚羟基、羧基能进一步与NaOH反应,因此反应的化学方程式为:+3NaOH+NaCl+CH3OH+H2O。
(5)CH2Cl2、CHCl3、CCl4为互溶的液体,但沸点不同,可用蒸馏的方法进行分离。
(6)苯甲醛能被银氨溶液氧化成-COOH,进一步与NH3反应生成-COONH4,同时生成Ag。该反应的化学方程式为:+2[Ag(NH3)2]OH+2Ag↓+3NH3+H2O。
(7)对苯二甲酸与乙二醇发生缩聚反应,生成聚对苯二甲酸乙二酯和水,该反应的化学方程式为:n +nHOCH2CH2OH+(2n-1)H2O。
(8)具有相同的官能团,则分子结构中含有C=C、氯原子、-COOH。苯环上只有两个取代基,则具有“邻间对”三种结构。因此两个取代基可分别为-Cl和-CCl=CHCOOH、-Cl和-CH=CClCOOH、-COOH和-CH=CCl2、-COOH和-CCl=CHCl、-Cl和-C(COOH)=CHCl,共五种,所以满足条件的同分异构体共有5×3=15种。其中核磁共振氢谱有4组峰的结构具有对称性,两个取代基位于对位,其结构简式为、、、、。
(9)[Cu(NH3)4]2+的中心离子为Cu2+,配体为NH3,配位原子为N原子。[Cu(NH3)4]2+中NH3分子中含有3个N-H化学键,即含有3个σ键;N原子与Cu2+形成四个配位键,即含有4个σ键。因此1mol[Cu(NH3)4]2+所含的σ键的个数为1mol×(4+3×4)=16mol。
【分析】(1)选取碳原子数最多的碳链作为主链,从靠近支链的一端开始编号,对烷烃进行命名。
(2)根据元素质量比进行计算。
(3)同分异构体中,支链越多,熔沸点越低。
(4)分子结构中含有碳卤键、直接,都能与NaOH溶液发生水解反应,结合水解产物结构进一步确定与NaOH的反应。
(5)互溶但沸点不同的液体的分离用蒸馏。
(6)银氨溶液具有氧化性,能将-CHO氧化成-COOH,-COOH进一步与NH3反应,生成-COONH4,据此写出反应的化学方程式。
(7)对苯二甲酸与乙二醇发生缩聚反应的过程中,生成聚酯结构,生成高分子的同时,生成小分子H2O,据此写出反应的化学方程式。
(8)根据限定条件确定同分异构体的结构和个数。
(9)[Cu(NH3)4]2+的中心离子为Cu2+,配体为NH3,配位原子为N原子。配位键也属于σ键。
29.【答案】(1)
(2)①③④
(3);
(4)
(5);
【知识点】有机物的合成;有机化学反应的综合应用;乙炔炔烃;醛与Cu(OH)2的反应;加成反应
【解析】【解答】(1)根据聚丙烯酸甲酯的结构简式可知,其链节为 ,故答案为: ;
(2)加成反应中原子原理为100%,①~⑤属于加成反应的是①③④,则原子利用率为100%的化学反应的序号:①③④,故答案为:①③④;
(3)反应②为丙烯酸和甲醇发生酯化反应生成CH2=CHCOOCH3,反应的化学方程式为: ;反应⑤为乙醇催化氧化生成乙醛,反应的化学方程式为 ,故答案为:;;
(4)乙炔和水发生加成反应生成乙醛,反应的化学方程式为: ,故答案为: ;
(5) 新制的 与乙醛反应生成氧化亚铁砖红色沉淀,反应的化学方程式为 ;新制的 与乙酸发生中和反应,反应的化学方程式为: ,故答案为:;。
【分析】丙烯酸和甲醇反应生成X,则X的结构简式为CH2=CHCOOCH3,CH2=CHCOOCH3发生加聚反应生成聚丙烯酸甲酯。
30.【答案】(1)酮羰基、碳氯键;加成反应
(2)+HCl
(3)
(4)6;
(5)
【知识点】有机物的合成;有机物的结构和性质;同分异构现象和同分异构体
【解析】【解答】(1)根据B的结构简式可知,B中含有的官能团为酮羰基、碳氯键;根据A、B的结构简式可知,A与乙烯发生加成反应生成B,则A生成B的反应类型为加成反应,故答案为:酮羰基、碳氯键;加成反应;
(2)根据B、C的结构简式可知,B生成C的化学方程式为: +HCl ,故答案为: +HCl ;
(3)由分析可知,W的结构简式为,故答案为:;
(4)A的同分异构体满足:①属于芳香族化合物,说明含有苯环,②能发生银镜反应,说明含有醛基则其结构简式中应含有2个氯原子和1个醛基,两个氯原子在苯环上有邻、间、对3种位置,再将醛基放上去,分别有2种、3种、1种位置关系,则符合条件的同分异构体共有:2+3+1=6种;其中核磁共振氢谱有3组峰的所有结构简式为 ,故答案为:6; ;
(5)根据逆合成分析法, 可由与发生取代反应得到, 发生类似D→E的反应得到,可由 催化氧化得到,则合成路线为: ,故答案为: 。
【分析】E和W反应生成G,结合W的分子式可知,W的结构简式为 。
31.【答案】(1)7;消去反应
(2)NaOH水溶液、加热
(3)2(CH3)2C(OH)COOH +2H2O;n(CH3)2C(OH)COOH + nH2O
(4)5
(5)HEMA结构中的羟基不仅增大了材料的亲水性和吸水性,而且不同聚合物分子中的羟基与水之间产生氢键等作用,形成网状结构的凝胶,使隐形眼镜更柔软。
(6)光照;苯甲醛
【知识点】有机物的推断;有机物的合成;有机物的结构和性质;同分异构现象和同分异构体;烯烃
【解析】【解答】(1)由分析可知,A为CH2=CHCH3,碳碳双键为平面结构,单键可旋转,则A分子中可以共平面的原子数最多有7个;反应①为E发生消去反应生成F,则①的反应类型为消去反应,故答案为:7;消去反应;
(2)B→C为卤代烃的水解反应,反应试剂及条件为NaOH水溶液、加热,故答案为:NaOH水溶液、加热;
(3)反应④为两分子E发生酯化反应生成K,反应的化学方程式为:2(CH3)2C(OH)COOH +2H2O ;反应⑤为E发生缩聚反应生成L,反应的化学方程式为: n(CH3)2C(OH)COOH + nH2O ,故答案为: 2(CH3)2C(OH)COOH +2H2O ; n(CH3)2C(OH)COOH + nH2O ;
(4) F为CH2=C(CH3)COOH,F与足量氢气加成后得到(CH3)2CHCOOH,W的一溴取代物同分异构体中符合:①能发生银镜反应和水解反应,说明含有溴原子、酯基、醛基;②不含环状结构;③只含有两种官能团,说明含有溴原子和HCOO-,符合条件的结构相当于丙烷中的2个氢原子被-Br、HCOO-取代,如果-Br、HCOO-位于同一个碳原子上,有2种位置,如果-Br、HCOO-位于两个碳原子上,有3种位置,所以符合条件的同分异构体有5种,故答案为:5;
(5)HEMA可以作为隐形眼镜材料的可能原因为:EMA结构中的羟基不仅增大了材料的亲水性和吸水性,而且不同聚合物分子中的羟基与水之间产生氢键等作用,形成网状结构的凝胶,使隐形眼镜更柔软,故答案为:EMA结构中的羟基不仅增大了材料的亲水性和吸水性,而且不同聚合物分子中的羟基与水之间产生氢键等作用,形成网状结构的凝胶,使隐形眼镜更柔软;
(6)①甲苯和氯气在光照条件下发生取代反应生成氯甲基苯,则反应条件1是光照,故答案为:光照;
②氯甲基苯发生水解反应生成苯甲醇,苯甲醇发生氧化反应生成K,K和HCN发生已知反应得到产品,则K为,名称为苯甲醛,故答案为:苯甲醛。
【分析】D和HCN发生已知反应生成E,则D为CH3COCH3,C能转化为D,结合C的分子式可知,C为CH3CH(OH)CH3,B水解生成C,结合B的分子式可知,B为CH3CHBrCH3,A发生加成反应生成B,则A为CH2=CHCH3,G可用于生产汽车防冻液,则G为HOCH2CH2OH,I和溴发生加成反应生成J,J发生水解反应生成G,则I为CH2=CH2、J为BrCH2CH2Br,H发生加聚反应生成HEMA,H为CH2=C(CH3)COOCH2CH2OH,E发生消去反应生成F,则F为CH2=C(CH3)COOH,K是六元环状化合物,则K为,在一定条件下可发生缩聚反应生成L,则L为。
32.【答案】(1)
(2)酯基、碳碳双键
(3)
(4)
(5)反应Ⅰ
(6)36
(7)防倒吸;液体分层,上层为无色油层,下层为无色水层;分液
【知识点】有机物的推断;乙烯的化学性质;乙酸乙酯的制取;电子式、化学式或化学符号及名称的综合
【解析】【解答】(1)有机物A的结构简式为CH2=CH2,其电子式为。
(2)丙烯酸乙酯的结构简式为CH2=CHCOOCH2CH3,其中所含的官能团有碳碳双键、酯基。
(3)有机物C的结构简式为CH2=CHCOOH。
(4)反应ⅠCH2=CH2与H2O发生加成反应,生成CH3CH2OH,该反应的化学方程式为:CH2=CH2+H2O CH3CH2OH。
(5)反应Ⅰ为加成反应,其产物只有一种,原子利用率达到100%;反应Ⅱ为氧化反应,在生成有机物C的同时生成H2O,原子利用率小于100%;反应Ⅲ中有机物B和C发生酯化反应,生成丙烯酸乙酯的同时,生成H2O,原子利用率小于100%。因此上述三个反应中,原子利用率为100%的是反应Ⅰ。
(6)由反应的化学方程式可知,每46份质量的有机物B与72份质量的有机物C反应生成100份质量的丙烯酸乙酯,因此46g有机物B与36g有机物C反应时,36g有机物C完全反应,理论上可生成50g丙烯酸乙酯。由于实际产率为72%,所以反应过程中丙烯酸乙酯的实际产量为50g×72%=36g。
(7)①球形干燥管可以起到冷凝和防倒吸作用。
②反应后生成的乙酸乙酯不溶于饱和Na2CO3溶液,因此可观察到分层现象。由于乙酸乙酯的密度比水小,所以油层在上层。故可观察到的现象为:液体分层,上层为无色油层,下层为无色水层。
③试管b中的液体混合物为两种不互溶的液体,可采用分液的方法进行分离。
【分析】有机物A是一种植物生长调节剂,因此A为CH2=CH2。CH2=CHCH3与O2反应生成有机物C,有机物B和有机物C反应生成CH2=CHCOOCH2CH3,因此有机物C为CH2=CHCOOH,有机物B为CH3CH2OH。CH3CH2OH可由CH2=CH2与H2O发生加成反应生成,因此无机物M为H2O。
33.【答案】(1);苯甲醇
(2);氧化反应
(3)6;
(4)3;
【知识点】有机物的结构式;有机物的合成;有机物的结构和性质;同分异构现象和同分异构体;苯酚的化学性质
【解析】【解答】(1) 根据合成路线知D是苯甲醇;
(2)反应①是丙醇发生催化氧化: ;反应②是丙醛被氧化为丙酸,属于氧化反应;
(3)E有一个对称轴,因此苯环上存在对称结构,有等效氢,所以整个分子中等效氢的种类数为:6种;酯类在碱性环境下的水解方程式为: ;
(4)D是苯甲醛,与 FeCl3溶液发生显色反应 应该有酚羟基,其同分异构体有3种; 其中核磁共振氢谱有4组峰的同分异构体的结构简式为。
【分析】根据合成路线可知:A为丙醛,B为丙酸,C为1-氯甲苯,D为苯甲醇。
试题分析部分
1、试卷总体分布分析
总分:127分
分值分布 客观题(占比) 46.0(36.2%)
主观题(占比) 81.0(63.8%)
题量分布 客观题(占比) 23(69.7%)
主观题(占比) 10(30.3%)
2、试卷题量分布分析
大题题型 题目量(占比) 分值(占比)
选择题 15(45.5%) 30.0(23.6%)
非选择题 10(30.3%) 81.0(63.8%)
多选题 8(24.2%) 16.0(12.6%)
3、试卷难度结构分析
序号 难易度 占比
1 普通 (48.5%)
2 容易 (21.2%)
3 困难 (30.3%)
4、试卷知识点分析
序号 知识点(认知水平) 分值(占比) 对应题号
1 甲烷的化学性质 10.0(7.9%) 17,24
2 乙醇的消去反应 2.0(1.6%) 8
3 化石燃料与基本化工原料 2.0(1.6%) 11
4 有机物中的官能团 2.0(1.6%) 21
5 乙烯的化学性质 30.0(23.6%) 4,5,17,20,24,25,32
6 苯的同系物及其性质 4.0(3.1%) 1,18
7 乙酸乙酯的制取 11.0(8.7%) 8,32
8 乙醇的化学性质 7.0(5.5%) 17,25
9 醛与Cu(OH)2的反应 7.0(5.5%) 29
10 同系物 21.0(16.5%) 2,20,24,26
11 探究影响化学反应速率的因素 2.0(1.6%) 22
12 烃类的燃烧 8.0(6.3%) 24
13 乙炔炔烃 11.0(8.7%) 7,8,29
14 苯酚的化学性质 8.0(6.3%) 33
15 石油副产品的综合应用 4.0(3.1%) 9,19
16 高分子材料 2.0(1.6%) 15
17 烷烃 2.0(1.6%) 3
18 配制一定物质的量浓度的溶液 2.0(1.6%) 22
19 有机物的推断 20.0(15.7%) 21,31,32
20 有机物的合成 31.0(24.4%) 29,30,31,33
21 饱和烃与不饱和烃 2.0(1.6%) 1
22 石油的裂化和裂解 2.0(1.6%) 10
23 物质的简单分类 7.0(5.5%) 27
24 常见的生活环境的污染及治理 2.0(1.6%) 19
25 同素异形体 9.0(7.1%) 26
26 使用化石燃料的利弊及新能源的开发 2.0(1.6%) 11
27 有机化学反应的综合应用 7.0(5.5%) 29
28 化学反应速率 2.0(1.6%) 12
29 生活中的有机化合物 2.0(1.6%) 12
30 苯酚的性质及用途 2.0(1.6%) 7
31 化学实验方案的评价 6.0(4.7%) 7,8,22
32 烯烃 13.0(10.2%) 6,21,31
33 取代反应 13.0(10.2%) 13,14,17,21,25
34 芳香烃 4.0(3.1%) 1,16
35 有机化合物的命名 12.0(9.4%) 28
36 二糖的性质和用途 2.0(1.6%) 7
37 缩聚反应 12.0(9.4%) 28
38 乙酸的化学性质 5.0(3.9%) 25
39 醛的化学性质 12.0(9.4%) 28
40 有机物的结构式 8.0(6.3%) 33
41 乙烯的用途 5.0(3.9%) 25
42 聚合反应 9.0(7.1%) 26
43 焰色反应 2.0(1.6%) 7
44 盐析 2.0(1.6%) 15
45 水的净化 2.0(1.6%) 10
46 配合物的成键情况 12.0(9.4%) 28
47 原电池工作原理及应用 2.0(1.6%) 12
48 消去反应 2.0(1.6%) 14
49 氯气的化学性质 2.0(1.6%) 22
50 同分异构现象和同分异构体 49.0(38.6%) 2,23,26,28,30,31,33
51 乙烯的实验室制法 4.0(3.1%) 5,22
52 卤代烃简介 2.0(1.6%) 3
53 加成反应 20.0(15.7%) 6,14,21,27,29
54 石油的分馏产品和用途 2.0(1.6%) 9
55 海水资源及其综合利用 2.0(1.6%) 19
56 有机物的结构和性质 37.0(29.1%) 1,14,23,27,30,31,33
57 苯的结构与性质 4.0(3.1%) 8,17
58 煤的干馏和综合利用 4.0(3.1%) 9,19
59 水解反应 2.0(1.6%) 15
60 电子式、化学式或化学符号及名称的综合 9.0(7.1%) 32
61 有机高分子化合物的结构和性质 2.0(1.6%) 12
62 酯化反应 26.0(20.5%) 13,24,26,27
63 同位素及其应用 2.0(1.6%) 2
64 分子式 2.0(1.6%) 20
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024年高考化学第一轮复习:烃
一、选择题
1.下列有机物类别划分正确的是( )
A.属于苯的同系物
B.含有碳碳双键,属于烯烃
C.属于链状化合物
D.属于脂环化合物
2.下列物质或微粒之间的相互关系错误的是( )
A.和互为同分异构体
B.干冰和冰为同一种物质
C.和互为同系物
D.和互为同位素
3.烷烃及卤代烃是重要的有机化工原料,下列有关说法正确的是( )
A.一氯丁烷有3种不同的结构
B.甲烷可与氯水在光照条件下发生取代反应
C. 和 互为同分异构体
D.乙烷分子中最多有4个原子共平面
4.下列关于乙烯的说法正确的是( )
A.与溴单质或酸性高锰酸钾反应都与碳碳双键有关,但是两者原理不相同
B.CH3CH2Br不可能是乙烯的加成产物,只能是CH3CH3的一卤取代产物
C.乙烯和聚乙烯二者都能使溴水褪色,性质相似
D.乙烯与氢气发生加成反应生成乙烷,所以除去乙烷中混有少量乙烯,可以在一定条件下通入过量氢气
5.实验室通过如图所示装置制取乙烯并验证其性质。下列说法正确的是( )
A.装置甲加热时应缓慢升高温度到170℃
B.装置甲中浓硫酸的作用是作催化剂和吸水剂
C.为除去乙烯中混有的少量SO2,装置乙中可加入NaOH溶液
D.装置丙中溶液褪色时有CH3CHBr2生成
6.某烯烃经催化加氢后可得到2-甲基丁烷,则该烯烃的名称不可能是( )
A.甲基丁烯 B.甲基丁烯
C.甲基丁烯 D.甲基丁烯
7.由实验操作和现象,可得出相应正确结论的是( )
实验操作 现象 结论
A 向苯酚的样品加入浓溴水,振荡 未出现白色沉淀 样品中不含苯酚
B 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的悬浊液 无砖红色沉淀 蔗糖未发生水解
C 在火焰上灼烧搅拌过某无色溶液的玻璃棒 火焰出现黄色 不能确定溶液中含有Na元素
D 向装有电石的圆底烧瓶中缓慢滴加饱和食盐水 产生的气体使酸性高锰酸钾溶液褪色 与反应生成
A.A B.B C.C D.D
8.利用下列装置(夹持装置略)进行实验,不能达到相应实验目的的是( )
A.装置甲:乙醇在浓硫酸的作用下,加热到制取乙烯
B.装置乙:苯与溴在催化下制备溴苯并验证有生成
C.装置丙:用乙酸乙酯萃取溴水中的溴,分液时从上口倒出有机层
D.装置丁:用电石与水反应制取乙炔并验证乙炔具有还原性
9.煤和石油综合利用的说法正确的是( )
A.煤的气化和液化都是物理变化
B.生石灰和煤混合燃烧可减少SO2排放,CaSO3是最终产物
C.石油通过分馏和裂化都能获得汽油
D.石油分馏产品包括汽油、沥青、焦炭等
10.美好生活离不开化学知识的运用。下列有关叙述错误的是( )
A.糖类、蛋白质都是人体必需的基本营养物质
B.石油经过分馏可得到乙烯、丙烯等化工原料
C.灾后重建时常用明矾净化饮用水
D.生活中可定期用84消毒液对居住环境消毒
11.煤、石油、天然气是人类使用的主要能源,同时也是重要的化工原料。下列关于它们的综合利用的叙述错误的是( )
A.以煤、石油和天然气为原料,可以合成高分子材料
B.煤的气化是工业上获得芳香烃的一种重要来源
C.石油的裂解和裂化都是化学变化
D.天然气是一种清洁燃料,属于不可再生资源
12.劳动创造幸福,实干成就伟业,下列劳动项目所涉及的化学知识叙述正确的是( )
选项 劳动项目 化学知识
A 电池研发人员研发用于汽车的氢气燃料电池 电动汽车中的能量转化是将化学能直接转化为动能
B 营养师进行膳食指导:是否需要多补充 纤维素与蔗糖互为同分异构体
C 食品采用真空包装 减慢食品氧化速率
D 面包师用奶油给糕点裱花 奶油是高分子化合物
A.A B.B C.C D.D
13.下列物质中不能与发生化学反应的是( )
①
②
③Na
④
A.①② B.①④ C.② D.③④
14.以2-溴丙烷为原料制取1,2-丙二醇,需要经过的反应是( )
A.加成-消去-取代 B.消去-加成-取代
C.消去-取代-加成 D.取代-消去-加成
15.下列说法不正确的是( )
A.聚乳酸是一种可降解的医用高分子材料
B.饱和溶液能使蛋白质发生盐析
C.油脂发生皂化反应生成甘油和高级脂肪酸
D.纤维素水解的最终产物可用新制检验
二、多选题
16.下列有机物中,属于芳香烃的是( )
A. B.
C. D.
17.下列过程中所发生的化学反应属于取代反应的是( )
A.苯与氢气在镍作催化剂的条件下反应
B.甲烷与氯气的混合其他用强光照射
C.乙醇与乙酸混合液在浓硫酸作用下加热
D.乙烯使酸性高锰酸钾溶液褪色
18.组成木质素的三种单体的结构简式如图,下列说法错误的是
A.三种单体分子中,所有碳原子均可能共平面
B.三种单体互为同系物,且均存在顺反异构
C.1mol单体S完全燃烧需要消耗10.5molO2
D.单体H和单体G分子中均含有7种不同化学环境的氢原子
19.化学与生产生活、能源开发、环境保护、资源利用等密切相关。下列叙述错误的是( )
A.煤和石油的综合利用全是通过化学变化实现
B.从海水提取溴的过程主要包括:氧化、吹出、吸收、氧化、蒸馏(或萃取、蒸馏)
C.将废旧电池进行直接填埋,减少对环境的污染
D.氢气的来源较多,包括水的电解、煤的气化、天然气裂解等
20.根据乙烯的性质,推测异戊二烯()的性质,下列说法正确的是( )
A.分子式为C5H8
B.不能使酸性KMnO4溶液褪色
C.含有碳碳双键,是乙烯的同系物
D.能使溴的四氯化碳溶液褪色
21.石油裂解是一个复杂的过程,其产物为混合物。例如:
下列说法中不正确的是( )
A.M为H2,N的分子式为C5H10
B.等物质的量的和完全燃烧时耗氧量相同
C.C4H6可以是烯烃
D.可用溴水区别和
22.下列设计的实验方案能达到实验目的的是( )
实验目的 实验方案
A 配制0.0100 mol·L-1的NaOH溶液 称取0.4 g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至1000mL容量瓶中定容
B 制取并纯化乙烯 将体积比为1∶3的乙醇与浓硫酸混合液(加沸石)加热至170℃,产生的气体依次通过NaOH溶液、碱石灰
C 比较Cl2与H2SO4氧化性强弱 向漂白粉中加入8mol·L-1硫酸,观察有无黄绿色气体
D 探究温度对化学反应速率的影响 向2支试管中均分别加入2mL0.01mol·L-1KMnO4溶液,再分别加入2mL0.1mol·L-1H2C2O4溶液,一支放入80℃热水中,另一支置于室温下,观察现象
A.A B.B C.C D.D
23.下图表示某高分子化合物的结构片段。关于该高分子化合物的推断正确的是( )
A.3种单体通过缩聚反应聚合
B.形成该化合物的单体只有2种
C.其中一种单体为
D.其中一种单体为1,5-二甲基苯酚
三、非选择题
24.现有K、M、N三种烃,其球棍模型如图所示,请回答下列问题。
(1)三种烃中互为同系物的是 (填对应字母,下同)
(2)等质量的三种烃完全燃烧时消耗最多的是 ,生成最多的是 。
(3)1mol K与发生取代反应,待反应完成后测得4种取代物物质的量相等,则消耗的物质的量为 。
(4)以M为基本原料可以合成多种有机物,合成路线如下:
已知:(R代表烃基,X代表卤素原子)
①A与CuO在加热条件下反应的化学方程式为 ,反应类型为 。
②B与D以物质的量之比生成E的化学方程式为 ,反应类型为 。
25.已知A是石油化学工业重要的基本原料,相对分子量为28,在一定条件下能发生如下图的转化关系,已知F是一种高分子化合物。
请回答:
(1)有机物B的结构简式是 。
(2)有机物D中的官能团名称是 。
(3)有机物A与D在一定条件下发生加成反应生成E的化学方程式 。
(4)下列说法正确的是____。
A.F能使溴的四氯化碳溶液褪色
B.B可以直接与酸性高锰酸钾溶液反应生成D
C.A生成B与C生成D的反应类型相同
D.D能使石蕊试液变红
26.有机化合物不仅数量多,而且分布广,与生产、生活密切相关。根据要求回答下列问题:
I.
(1)下列物质中,属于同一物质的是 (填序号,下同),互为同系物的为 ,互为同素异形体的为 。
A.正丁烷与2-甲基丁烷 B.金刚石和石墨 C.和D.苯与溴苯E.和
(2)II.聚甲基丙烯酸甲酯(PMMA)俗称有机玻璃,其结构简式为:。合成有机玻璃的路线如图所示:
含有的官能团的名称是 ,反应②的类型是 。
(3)A的结构简式为 。
(4)关于X的说法正确的是____
A.能与发生加成反应 B.不能使酸性高锰酸钾溶液褪色
C.能与NaOH溶液反应 D.该物质易溶于水
(5)与甲基丙烯酸()含有相同官能团的同分异构体的结构简式 (任写一种)。
27.某化合物Ⅰ可通过如图合成路线合成:
已知:
回答下列问题:
(1)中,属于烃的是 (填标号)。
(2)的反应类型属于 (填“加成”或“加成”)。
(3)F在氢氧化钠的水溶液中加热,发生反应的化学方程式为 。
(4)完全燃烧消耗 。
(5)最多可与 反应,所得产物为 。
(6)中浓硫酸的作用是 。
28.按要求回答下列问题。
(1)用系统命名法对,命名: 。
(2)已知乙酸和乙酸乙酯的混合物中含H质量分数为7.8%,则其中含氧质量分数是 。
(3)熔点比较:2-甲基丁烷 正戊烷(选填>、<、=)。
(4)在加热条件下与足量NaOH溶液完全反应的化学方程式 。
(5)甲烷与氯气在光照条件下反应,得到的产物中含有二氯甲烷、三氯甲烷和四氯化碳,分离它们的方法是 。
(6)写出苯甲醛与银氨溶液反应的化学方程式 。
(7)写出对苯二甲酸与乙二醇在催化剂作用下发生缩聚反应的化学方程式 。
(8)的同分异构体有多种,满足下列2个条件的同分异构体有 种(不考虑顺反异构),其中核磁共振氢谱有4组峰的结构简式为 (任写一种)。
①具有相同的官能团 ②苯环上有两个取代基。
(9)中的中心离子是 ,配体是 ,中含有键的物质的量为 mol。
29.以乙炔为原料制备乙酸和聚丙烯酸甲酯的合成路线如下(部分反应条件已省略)。回答下列问题:
(1)写出聚甲基丙烯酸甲酯链节的结构简式: 。
(2)写出①~⑤中原子利用率为100%的化学反应的序号: 。
(3)写出下列两个反应的化学方程式(注意标明反应条件):
反应②: ;
反应⑤: 。
(4)写出由乙炔经一步反应生成乙醛的方程式: 。
(5)可以用新制的鉴别乙醛和乙酸,请写出相关化学方程式: ; 。
30.化合物G是合成一种杀虫剂的重要中间体,其合成路线如图:
回答下列问题
(1)B中官能团的名称为 ,A生成B的反应类型为 。
(2)写出B生成C的反应方程式 。
(3)W的分子式为,其结构简式为 。
(4)满足下列条件所有的A的同分异构体有 种。
①属于芳香族化合物; ②能发生银镜反应;
写出其中核磁共振氢谱有3组峰的所有结构简式 。
(5)请以和为原料设计合成的路线(无机试剂任选) 。
31.用于制造隐形眼镜的功能高分子材料HEMA的合成路线如图所示,其中G可用于生产汽车防冻液,K是六元环状化合物,E在一定条件下可发生缩聚反应生成L。
已知:
回答下列问题:
(1)A分子中可以共平面的原子数最多有 个;①的反应类型是 。
(2)B→C的反应试剂及条件为 。
(3)写出下列反应的化学方程式:
反应④ ;
反应⑤ 。
(4)W是F与足量氢气加成后的产物,则W的一溴取代物同分异构体中符合下列条件的数目有 种(考虑立体异构)。
①能发生银镜反应和水解反应②不含环状结构③只含有两种官能团
(5)制造隐形眼镜的材料应该具有良好的亲水性,请从HEMA的结构上分析它可以作为隐形眼镜材料的可能原因 。
(6)以甲苯为原料合成 的流程图如下:
①反应条件1是 。
②K的名称是 。
32.丙烯酸乙酯天然存在于菠萝等水果中,是一种食品用合成香料。一种合成方法如下:
已知:有机物A是一种植物生长调节剂。
(1)有机物A的电子式为 。
(2)丙烯酸乙酯中含有的官能团名称为 。
(3)有机物C的结构简式为 。
(4)反应Ⅰ的化学方程式为 。
(5)反应Ⅰ、Ⅱ、Ⅲ中,原子利用率为100%的是 。
(6)46 g有机物B与36 g有机物C在一定条件下发生反应Ⅲ,如果实际产率是72%,则可得到丙烯酸乙酯的质量为 g。
(7)某实验小组用以下装置制备丙烯酸乙酯:
①球形干燥管c除起冷凝作用外,它的另一重要作用是 。
②待收集到一定量产物后停止加热,取下试管b并振荡、静置,可观察到 (填实验现象)。
③分离试管b中的液体混合物,采用的方法为 。
33.丙酸苯甲酯为无色液体,有鲜花的甜香气味,常用于配制食品、香烟、香皂、日用化妆香精,其合成路线如图所示。
回答下列问题:
(1)D的结构简式为 ,其名称为 。
(2)反应①的化学方程式为 ,反应②的反应类型为 。
(3)E中含有 种不同化学环境的氢,其与NaOH溶液反应的化学方程式为 。
(4)能与FeCl3溶液发生显色反应的D的同分异构体有 种,其中核磁共振氢谱有4组峰的同分异构体的结构简式为 。
答案解析部分
1.【答案】C
【知识点】有机物的结构和性质;饱和烃与不饱和烃;芳香烃;苯的同系物及其性质
【解析】【解答】A、 为苯乙烯,与苯结构不相似,不属于苯的同系物,故A错误;
B、 CH2=CH-COOH中除了C、H外,还含O元素,不属于烯烃,故B错误;
C、 中不存在碳环,碳原子成链状,属于链状化合物,故C正确;
D、 含有苯环,不属于脂环化合物,故D错误;
故答案为:C。
【分析】A、结构相似,在分子组成上相差一个或n个CH2的化合物互为同系物;
B、 烃是只含碳氢两种元素的有机化合物;
C、 分子中碳原子相互链接成链状的有机化合物为链状化合物;
D、含有由碳原子组成的环状结构,但不含有苯环的有机化合物为脂环化合物。
2.【答案】B
【知识点】同分异构现象和同分异构体;同系物;同位素及其应用
【解析】【解答】A.二者分子式相同,但是结构不同,所以互为同分异构体,A项正确;
B.干冰为二氧化碳,冰为水,不属于同种物质,B项错误;
C.二者结构相似,分子相差1个CH2,属于同系物,C项正确;
D. 和 质子数相同,中子数不同,互为同位素,D项正确;
故答案为:B。
【分析】A.同分异构概念:分子式相同,结构不同的两种有机物;
C.同系物概念:1.结构必须相似,2.分子相差若干CH2;
D.同位素概念:质子数相同,中子数不同的同种元素不同原子。
3.【答案】D
【知识点】卤代烃简介;烷烃
【解析】【解答】A.已知丁基有4种不同的结构,则一氯丁烷有4种不同的结构,故A错误;
B.甲烷可与氯气在光照条件下发生取代反应,不能和氯水反应,故B错误;
C.依据甲烷是正四面体型结构可知,和同一种物质,故C错误;
D.乙烷分子中单键可以旋转,可以使得两个碳原子及每个碳上的1个氢原子共面,故最多有4个原子共平面,故D正确;
故选D。
【分析】A.依据丁基有4种不同的结构判断;
B.注意反应物质的状态;
C.依据甲烷是正四面体型结构分析;
D.烷烃分子中单键可以旋转分析。
4.【答案】A
【知识点】乙烯的化学性质
【解析】【解答】A、乙烯与溴发生加成反应,与酸性高锰酸钾发生氧化还原反应,故A正确;
B、乙烯和HBr发生加成反应生成CH3CH2Br,故B错误;
C、聚乙烯不含碳碳双键,不能使溴水褪色,故C错误;
D、通入过量氢气会引入新杂质,故D错误;
故答案为:A。
【分析】乙烯中含有碳碳双键,所有原子共平面,能发生加成反应、氧化反应。
5.【答案】C
【知识点】乙烯的化学性质;乙烯的实验室制法
【解析】【解答】A、为了防止副反应的发生,装置甲加热时应迅速升高温度到170℃,故A错误;
B、装置甲中浓硫酸作催化剂和脱水剂,故B错误;
C、二氧化硫能与NaOH溶液反应,乙烯不与NaOH溶液反应,装置乙是为了除去二氧化硫,因此装置乙中可加入NaOH溶液,故C正确;
D、装置丙中,乙烯与溴水发生加成反应生成CH2BrCH2Br,故D错误;
故答案为:C。
【分析】装置甲中,乙醇和浓硫酸发生消去反应生成乙烯,装置乙可除去乙烯中混有的二氧化硫,丙装置中的溴水可检验乙烯。
6.【答案】B
【知识点】烯烃;加成反应
【解析】【解答】2-甲基丁烷相邻碳原子之间各去掉1个氢原子形成双键,从而得到烯烃,根据2-甲基丁烷的碳链结构,可知相邻碳原子之间去掉1个氢原子形成双键有3种情况,分别得到:2-甲基-1-丁烯,3-甲基-1-丁烯,2-甲基-2-丁烯,不可能是2-甲基-3-丁烯,故选B;
故答案为:B。
【分析】相邻碳原子之间各消去1个氢原子形成碳碳双键,即得到烯烃。
7.【答案】C
【知识点】焰色反应;乙炔炔烃;苯酚的性质及用途;二糖的性质和用途;化学实验方案的评价
【解析】【解答】 A.依据相似相溶原理,向苯酚的样品加入浓溴水,振荡未出现白色沉淀,可能是溴水量不足,生成的三溴苯酚溶解在过量的苯酚中,不能说明样品中不含苯酚,A错误;
B.注意反应的环境,向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的Cu(OH)2悬浊液之前应先加NaOH溶液将溶液调为碱性,B错误;
C.玻璃中含有Na2SiO3,因此火焰出现黄色不能确定溶液中含有Na元素,C正确;
D.电石与水反应的产物除了C2H2,还有H2S等具有还原性的气体生成、它们能使高锰酸钾溶液褪色,生成的气体未经除杂直接通入酸性高锰酸钾溶液中,溶液褪色不能说明CaC2与H2O反应生成C2H2,D错误;
故选C。
【分析】 A.依据相似相溶原理分析,注意反应物量的大小;
B.注意反应的环境;
C.玻璃中含有Na元素;
D.电石中含有H2S等具有还原性的气体。
8.【答案】B
【知识点】乙炔炔烃;苯的结构与性质;乙醇的消去反应;乙酸乙酯的制取;化学实验方案的评价
【解析】【解答】A、乙醇在浓硫酸的作用下加热到170℃时发生消去反应生成乙烯,该装置能达到实验目的,故A不符合题意;
B、溴易挥发,挥发的溴与硝酸银反应生成淡黄色沉淀,不能证明苯与液溴发生取代反应,故B符合题意;
C、溴不溶于水,易溶于有机溶剂,且乙酸乙酯不溶于水、其密度小于水的密度,则用乙酸乙酯萃取溴水中的溴,分液时从上口倒出有机层,该装置能达到实验目的,故C不符合题意;
D、电石和水反应生成乙炔,同时会产生还原性杂质,利用硫酸铜除去杂质气体,乙炔能被酸性高锰酸钾氧化使酸性高锰酸钾褪色,可检测乙炔,该装置能达到实验目的,故D不符合题意;
故答案为:B。
【分析】A、乙醇在170℃时发生消去反应生成乙烯;
B、溴易挥发,挥发的溴也能与硝酸银反应;
C、乙酸乙酯的密度小于水;
D、乙炔能被酸性高锰酸钾氧化。
9.【答案】C
【知识点】石油副产品的综合应用;石油的分馏产品和用途;煤的干馏和综合利用
【解析】【解答】A.煤的气化和液化均产生新物质,是化学变化,故A不符合题意;
B.亚硫酸钙在空气中变为硫酸钙,故B不符合题意;
C.石油的分馏和裂化均可得到汽油,故C符合题意;
D.石油分馏的的产品是汽油、沥青、煤油和柴油等,焦炭是煤干馏得到的,故D不符合题意;
故答案为:C
【分析】A.煤的气化和液化是化学变化
B.生石灰除去煤混合物中的硫元素,产物是硫酸钙
C.石油的分馏得到汽油,石油的裂解可得到汽油
D.焦炭是煤的干馏产物
10.【答案】B
【知识点】石油的裂化和裂解;水的净化
【解析】【解答】A、糖类、蛋白质均为人体必须的基本营养物质,故A正确;
B、石油经过裂解得到乙烯、丙烯等化工原料,故B错误;
C、明矾中含有铝离子,水解生成氢氧化铝胶体,能吸附水中的悬浮杂质,可用于净水,故C正确;
D、84消毒液的主要成分次氯酸钠具有强氧化性,能使蛋白质变性,因此可定期用84消毒液对居住环境消毒,故D正确;
故答案为:B。
【分析】A、糖类、油脂、蛋白质、水、无机盐等是人体必需的营养物质;
B、石油裂解得到乙烯、丙烯等短链烃;
C、明矾水解生成氢氧化铝胶体;
D、84消毒液的主要成分为次氯酸钠,次氯酸钠具有强氧化性。
11.【答案】B
【知识点】使用化石燃料的利弊及新能源的开发;化石燃料与基本化工原料
【解析】【解答】A.以石油、煤和天然气为主要原料生产的材料属于有机合成材料,A正确;
B、煤的干馏是工业上获得芳香烃的一种重要来源,故B错误;
C、石油的分馏是物理变化,裂化、裂解,催化重整都是化学变化,故C正确;
D.天然气的主要成分是甲烷,属于不可再生资源,故D正确;
故答案为:B。
【分析】本题主要考查化石燃料的应用。
A、合成材料又称人造材料,是人为地把不同物质经化学方法或聚合作用加工而成的材料;以石油、煤和天然气为主要原料生产的材料属于有机合成材料,如:塑料、合成橡胶、合成纤维;
B、煤干馏可以获得煤焦油,其中含有芳香烃;
C、裂化的目的是为了得到更多的10个碳原子左右的汽油,裂解的目的是为了得到碳原子数更少的烯烃,主要为了生产乙烯。可见裂解的程度比裂化更大,也成为裂解是深度裂化,由于都分解生成了新物质,所以都是化学变化;
D.天然气的主要成分是甲烷,产物只有二氧化碳和水,属于不可再生资源。
12.【答案】C
【知识点】化学反应速率;生活中的有机化合物;有机高分子化合物的结构和性质;原电池工作原理及应用
【解析】【解答】A.燃料电池,是将化学能转化为电能,A错误;
B.纤维素属于多糖,蔗糖属于二糖,不是同分异构体,B错误;
C.真空包装,去除氧气,防止食物被氧化,C正确;
D.奶油不属于有机高分子化合物,奶油属于油脂,D错误。
故答案为:C。
【分析】本题主要考查生活生产中的化学性质和用途。
13.【答案】C
【知识点】取代反应;酯化反应
【解析】【解答】根据有机物结构可知,含有羟基和羧基,既可以与酸发生酯化反应,也可以与醇发生酯化反应,同时还可以与金属钠反应置换出氢气;所以不能反映的物质为②;
故答案为:C。
【分析】根据有机物的结构和官能团来判断有机物的性质,进而判断能够与那些物质进行反应。
14.【答案】B
【知识点】有机物的结构和性质;取代反应;加成反应;消去反应
【解析】【解答】 2-溴丙烷先发生消去反应得到丙烯,丙烯再与溴单质发生加成反应,得到1,2-二溴丙烷,再发生取代反应,用-OH取代Br,得到产物1,2-丙二醇 。B选项符合题意。
故答案为:B。
【分析】消除反应,又称脱去反应或是消去反应,是指一种有机化合物分子和其他物质反应,失去部分原子或官能基(称为离去基)的有机反应。反应后分子会产生多键,为不饱和有机化合物;
加成反应是反应物分子中以重键结合的或共轭不饱和体系末端的两个原子,在反应中分别与由试剂提供的基团或原子以σ键相结合,得到一种饱和的或比较饱和的加成产物。这个加成产物可以是稳定的;也可以是不稳定的中间体,随即发生进一步变化而形成稳定产物。
取代反应是指化合物或有机物分子中任何一个原子或原子团被试剂中同类型的其它原子或原子团所替代的反应,用通式表示为:R-L(反应基质)+A-B(进攻试剂)→R-A(取代产物)+L-B(离去基团)属于化学反应的一类。
15.【答案】C
【知识点】高分子材料;盐析;水解反应
【解析】【解答】A.聚乳酸是一种可降解的医用高分子材料,故A不符合题意;
B.饱和硫酸铵中有移动的阴阳离子可使蛋白质发生盐析,故B不符合题意;
C.油脂发生皂化反应时生成甘油和高级脂肪酸钠,故C不符合题意;
D.纤维素水解为葡萄糖,可以用新制的氢氧化铜进行检验,故D不符合题意;
故答案为:C
【分析】A.聚乳酸可以发生降解;
B.盐溶液可以使蛋白质发生盐析;
C.油脂皂化反应得到的是甘油和高级脂肪酸钠;
D.醛基的检验可以用新制的氢氧化铜悬浊液。
16.【答案】B,D
【知识点】芳香烃
【解析】【解答】芳香烃即含有苯环,且有C、H两种元素组成的化合物;
A、该分子为环己烷,属于环烷烃,A错误;
B、该分子为甲苯,属于芳香烃,B正确;
C、该分子为硝基苯,含有苯环和O元素,属于芳香烃的衍生物,C错误;
D、该分子为萘,属于芳香烃,D正确;
故答案为:BD
【分析】烃只含C。H两种元素,芳香烃即含有苯环的烃类。
17.【答案】B,C
【知识点】甲烷的化学性质;乙烯的化学性质;苯的结构与性质;乙醇的化学性质;取代反应
【解析】【解答】A. 苯与氢气在镍和加热条件下反应生成环己烷,是加成反应,A错误;
B.甲烷和氯气在光照条件下,发生取代反应,B正确;
C.乙醇和乙酸在浓硫酸作用下发生反应,生成乙酸乙酯和水,是酯化反应,酯化反应也属于取代反应,C正确;
D.乙烯是酸性高锰酸钾褪色,属于氧化反应,D错误。
故答案为:B、C。
【分析】本题主要考查常见有机物的化学性质,掌握相关性质便可解题。
苯化学性质:a.氧化反应:与氧气反应,不与酸性高锰酸钾反应;b.取代反应;c.硝化反应;d.加成反应:与氢气;
甲烷化学性质:a.稳定性:不与强酸强碱,酸性高锰酸钾反应;
b.氧化反应:与O2反应生成二氧化碳和水;
c.取代反应:与卤素在光照条件下发生取代反应。
乙烯化学性质:a.氧化反应:与氧气反应,使酸性高锰酸钾褪色;b.加成反应:与氢气,溴水,水,氯化氢等; c.加聚反应。
18.【答案】B,C
【知识点】苯的同系物及其性质
【解析】【解答】A.三种单体分子中,存在苯环、碳碳双键,所有碳原子均可能共平面,A不符合题意;
B.三种单体中,官能团种类不同,不是同系物,B符合题意;
C.1mol单体S完全燃烧需要消耗11.5molO2,C符合题意;
D. 单体H和单体G分子中均含有7种不同化学环境的氢原子,D不符合题意;
故答案为:BC
【分析】A.存在苯环、碳碳双键,所有碳原子均可能共平面;
B.官能团种类不同,不是同系物;
C.1mol单体S完全燃烧需要消耗11.5molO2;
D. 单体H和单体G分子中均含有7种不同化学环境的氢原子。
19.【答案】A,C
【知识点】海水资源及其综合利用;常见的生活环境的污染及治理;石油副产品的综合应用;煤的干馏和综合利用
【解析】【解答】A.蒸馏是利用混合物中各组分熔沸点不同而分离物质的方法,没有新物质生成,则石油蒸馏过程中没有新物质生成,所以是通过物理变化实现,故A符合题意;
B.酸化的海水中通入氯气发生Cl2+2Br-=Br2+2Cl-,吹出塔中通入热空气吹出溴单质,在吸收塔中用二氧化硫和水吸收发生SO2+Br2+2H2O=2HBr+H2SO4,再通入氯气和水蒸气,发生Cl2+2Br-=Br2+2Cl-,达到富集溴的目的,冷凝精馏分离出产品溴,所以从海水提取溴的过程主要包括:氧化、吹出、吸收、氧化、蒸馏,故B符合题意;
C.废旧电池中含有重金属汞、镉、铅,进行直接填埋,对土壤、地下水污染特别严重,应回收利用可以减少污染,故C符合题意;
D.电解水生成氢气和氧气,煤的气化可得到氢气和CO,天然气中低碳烷烃在高温下吸收大量能量而分解为低碳不饱和烃和氢,所以氢气的来源较多,包括水的电解、煤的气化、天然气裂解等,故D不符合题意;
故答案为:AC。
【分析】A、石油的分馏是物理变化;
B、海水提溴包括溴离子的氧化,空气吹出,二氧化硫吸收,溴离子的氧化和溴的蒸馏;
C、废旧电池填埋会污染土壤;
D、氢气可以来自于水的电解、煤的气化、天然气裂解 。
20.【答案】A,D
【知识点】乙烯的化学性质;同系物;分子式
【解析】【解答】A.分子式为C5H8,A符合题意;
B.异戊二烯有碳碳双键,能被高锰酸钾氧化,溶液褪色,B不符合题意;
C.乙烯有1个碳碳双键,异戊二烯有2个碳碳双键,官能团数目不同,不是同系物,C不符合题意;
D.异戊二烯有碳碳双键,能与溴反应,溶液褪色,D符合题意;
故答案为:AD
【分析】A.分子式为C5H8;
B.碳碳双键能被高锰酸钾氧化;
C.官能团数目不同,不是同系物;
D.碳碳双键能与溴反应。
21.【答案】A,B
【知识点】有机物中的官能团;有机物的推断;烯烃;取代反应;加成反应
【解析】【解答】A.由图可知,甲基环戊烷加热分解时,生成物有碳碳双键,所以产物M为两个氢原子结合,即为H2。根据质量守恒定律可知,甲基环戊烷加热生成甲烷和N,则N为C5H8,A错误;
B.等物质的量的 和,碳原子相同但是氢原子数量不相同,所以完全燃烧时耗氧量不同,B错误;
C. C4H6中可以存在两个碳碳双键,也可以存在一个碳碳三键,所以 C4H6可以是烯烃,C正确;
D.因为中有不饱和碳碳双键可以使溴水褪色,所以可以可用溴水区别和 ,D正确;
故答案为:A、B。
【分析】本题主要考查有机物质的性质及应用,需要掌握基础的官能团的性质,质量守恒定量,可以解答此题。需要注意的点:不饱和烃有烯烃和炔烃,CnH2n-2(n>2)可能是烯烃或者炔烃。
A.根据质量守恒定律计算;
B.消耗氧的量,需要碳原子和氢原子的耗氧量相加;
C.C4H6中可以存在两个碳碳双键,也可以存在一个碳碳三键;
D.含有碳碳双键的物质可以使溴水褪色,烷烃不能使溴水褪色。
22.【答案】B,D
【知识点】氯气的化学性质;乙烯的实验室制法;配制一定物质的量浓度的溶液;探究影响化学反应速率的因素;化学实验方案的评价
【解析】【解答】A.0.4gNaOH固体的物质的量,由于NaOH溶解过程放热,因此需等溶液冷却至室温后再转移至容量瓶,A不符合题意;
B.产生的乙烯中混有乙醇和水蒸气,可通过NaOH溶液吸收乙醇,再通过碱石灰除去水蒸气,即可得到纯净的乙烯,B符合题意;
C.可通过反应Cl2+SO2+2H2O=2HCl+H2SO4说明氧化性Cl2>H2SO4,C不符合题意;
D.由于浓度、温度都会影响反应速率,因此探究温度对反应速率的影响,应控制反应浓度相同,D符合题意;
故答案为:BD
【分析】A.NaOH溶解过程放热,需冷却至室温后再转移至容量瓶;
B.反应生成的乙烯中混有乙醇和水蒸气;
C.根据氧化剂的氧化性强于氧化产物分析;
D.结合反应速率的影响因素分析;
23.【答案】A,C
【知识点】有机物的结构和性质;同分异构现象和同分异构体
【解析】【解答】A、縮宿聚反应的单体是:苯酚、甲醛和氨基苯,A项正确
B、縮聚反应的单体是:苯酚、甲醛和氨基苯,B项错误;
C、其中一种单体为 ,C项正确;
D、单体是:苯酚、甲醛和氨基苯,D项错误;
故答案为:AC
【分析】找高分子单体的方法:半键缩回来,临碳快牵上,单变双,双变单,若无双变单,单键就断掉。
24.【答案】(1)K、N
(2)K;M
(3)2.5mol
(4)CH3CH2OH+CuOCH3CHO+H2O+Cu;氧化反应;2CH3COOH+HOCH2CH2OHCH3COOCH2CH2OOCCH3+2H2O;酯化反应或取代反应
【知识点】甲烷的化学性质;乙烯的化学性质;烃类的燃烧;同系物;酯化反应
【解析】【解答】(1)K为CH4,M为CH2=CH2,N为CH3CH3,其中CH4和CH3CH3都属于烷烃,二者的结构相似,分子组成上相差一个CH2,因此二者互为同系物。所以三种烃中互为同系物的是K和N。
(2)三种烃的最简式分别为CH4、CH2、CH3,其中氢元素质量分数最大的是K(CH4),碳元素质量分数最大的是M(C2H4)。等质量的三种烃完全燃烧,所含氢元素的质量分数越大, 其燃烧过程中消耗O2的量越多,因此消耗O2最多的是K。所含碳元素的质量分数越大,则其燃烧生成CO2的量越多,因此生成CO2最多的是M。
(3)K为CH4,与Cl2在光照条件下发生取代反应,生成CH3Cl、CH2Cl2、CHCl3、CCl4。完全反应后,生成的四种取代产物的物质的量相等,根据碳元素守恒可得,各种取代产物的物质的量都为0.25mol。因此反应消耗Cl2的物质的量为0.25mol×1+0.25mol×2+0.25mol×3+0.25mol×4=2.5mol。
(4)①由分析可知,A为C2H5OH,C2H5OH与CuO在加热条件下发生氧化反应,生成CH3CHO和H2O,该反应的化学方程式为:C2H5OH+CuOCH3CHO+H2O+Cu。该反应的反应类型为氧化反应。
②由分析可知,B为CH3COOH,D为HOCH2CH2OH,二者按2:1反应,其反应原理为酯化反应,生成E的结构简式为CH3COOCH2CH2OOCCH3,该反应的化学方程式为:2CH3COOH+HOCH2CH2OH CH3COOCH2CH2oOCCH3+2H2O。该反应的反应类型为酯化反应(或取代反应)。
【分析】(1)同系物是指结构相似,分子组成上相差一个或多个CH2的有机物。
(2)等质量的烃完全燃烧,烃中氢元素的质量分数越大,则其燃烧所需要O2的量越多。含碳元素的质量分数越大,则燃烧生成的CO2越多。
(3)K为CH4,结合CH4与Cl2的取代反应分析。
(4)M为CH2=CH2,与H2O在催化剂条件下反应生成A,因此A为C2H5OH,与Br2的CCl4溶液发生加成反应,生成C,因此C的结构简式为BrCH2CH2Br。C2H5OH在酸性KMnO4溶液的氧化作用下,生成B,因此B的结构简式为CH3COOH。C与NaOH溶液发生水解反应,其中Br原子被-OH取代,生成醇,因此D的结构简式为HOCH2CH2OH。B与D在浓硫酸/加热条件下发生酯化反应, 生成E,因此E的结构简式为CH3COOCH2CH2OOCCH3。
25.【答案】(1)
(2)羧基
(3)
(4)B;D
【知识点】乙烯的化学性质;乙烯的用途;乙醇的化学性质;乙酸的化学性质;取代反应
【解析】【解答】乙烯是石油化学工业重要的基本原料, 且相对分子量为28 ,故A为乙烯,乙烯在催化剂的条件下发生加聚反应生成聚乙烯,即F;乙烯与水反应生成乙醇,乙醇氧化生成乙酮,乙酮氧化生成乙酸,乙酸和乙醇发生酯化反应生成乙酸乙酯。
(1)有机物B为乙醇,结构简式为 。
(2)有机物D为乙酸,含有的官能团名称是羧基。
(3)乙烯与乙酸在催化剂作用下生成乙酸乙酯,反应前有碳碳双键,反应后无碳碳双键,则反应为加成反应。 化学方程式为 。
(4)A:聚乙烯分子内无碳碳双键,不能与溴发生加成反应,不能使溴的四氯化碳溶液褪色,故A不符合题意;
B:乙醇可以被酸性高锰酸钾溶液直接氧化为乙酸,故B符合题意;
C:乙烯转化为乙醇的反应是加成反应,乙酮转化为乙酸的反应是氧化反应,反应类型不同,故C不符合题意;
D:乙酸显酸性,能使石蕊试液变红,故D符合题意;
故答案为:BD
【分析】解题关键是推断出A为乙烯,乙烯由于含有碳碳双键,可以发生加成反应和加聚反应,推断出B为乙醇,F为一种高分子化合物,F为聚乙烯;乙醇可以分步氧化成乙酮、乙酸,也可以直接被酸性高锰酸钾溶液氧化为乙酸,乙醇与乙酸在浓硫酸加热的条件下发生酯化反应生成乙酸乙酯。
26.【答案】(1)E;A;B
(2)羟基;加聚反应
(3)
(4)B;C
(5)或
【知识点】同素异形体;同分异构现象和同分异构体;同系物;聚合反应;酯化反应
【解析】【解答】(1)A、正丁烷的结构简式为CH3CH2CH2CH3,2-甲基丁烷的结构简式为,二者的结构相似,分子组成上相差一个-CH2-,因此互为同系物。
B、金刚石和石墨都是由碳元素组成的单质,互为同素异形体。
C、二者的分子式都是C3H6,但结构不同,因此互为同分异构体.
D、溴苯是苯的一溴代物。
E、二者的分子式和结构都相同,属于同一种物质。
综上,上述物质中属于同一物质的是E;互为同系物的是A;互为同素异形体的是B。
(2)CH3OH中含有官能团羟基。反应①为酯化反应,所得产物A中含有碳碳双键;反应②得到高分子化合物X,发生加聚反应。
(3)A是由与CH3OH发生酯化反应所得的产物,酯化反应的原理为“酸脱羟基,醇脱氢”,因此A的结构简式为。
(4)A、高分子化合物X中不含有碳碳双键,因此不能与Br2/CCl4发生加成反应,A不符合题意。
B、该高分子化合物X中不含有碳碳双键,其所含的酯基也不能使酸性KMnO4溶液褪色,B符合题意。
C、该高分子化合物X中含有酯基,能与NaOH溶液发生水解反应,C符合题意。
D、该高分子有机物中含有的碳原子数很多,因此不溶于水,D不符合题意。
故答案为:BC
(5)与具有相同的官能团,即含有碳碳双键、羧基;因此其同分异构体存在的是碳碳双键的位置异构,满足条件的同分异构体的结构简式为CH2=CH-CH2-COOH、CH3-CH=CH-COOH。
【分析】(1)分子式相同,结构相同的为同一种物质;同系物是指结构相似,分子组成上相差一个活多个CH2的有机物;同素异形体是指由同种元素组成的不同单质。
(2)CH3OH所含的官能团为羟基。物质A经反应②后得到高分子化合物X,据此判断反应类型。
(3)根据反应物的结构特点确定其反应原理,从而得出A的结构简式。
(4)根据X的结构简式以及具有的官能团分析选项。
(5)含有相同的官能团的同分异构体存在碳链异构和官能团位置异构,据此书写其同分异构体的结构简式。
27.【答案】(1)ACE
(2)加成
(3)+2NaOH+2NaBr
(4)1.7
(5)2;、
(6)作催化剂和吸水剂
【知识点】有机物的结构和性质;加成反应;酯化反应;物质的简单分类
【解析】【解答】(1)烃指的是C、H化合物:ACE;
(2)根据合成路线知: E到F是环己二烯与HBr发生加成反应;
(3) F在氢氧化钠的水溶液中加热, 发生的是卤代烃的水解反应,利用-OH取代溴原子: +2NaOH+2NaBr ;
(4)C是环己烯,1mol环己烯与足量氧气反应时,消耗的氧气的物质的量为8.5molO2,则 完全燃烧消耗 1.7mol氧气;所得的产物为对环己二醇、乙酸钠和水;
(5)I中含有两个酯基,1mol酯基在碱性环境下水解需要的NaOH为2mol;
(6) 的反应是酯化反应,在酯化反应中,浓硫酸的作用是催化剂和吸水剂;
【分析】(1)烃的构成元素包括:C和H,分类包括饱和烃和不饱和烃;芳香烃和脂肪烃等;
(2)环己二烯含有2个碳碳双键,与1molBr2发生1,4-加成可以得到F;
(3)卤代烃水解反应是指卤代烃与水在酸性或碱性条件下发生反应,生成相应的醇和相应的卤化物离子的过程;
(4)环己烯燃烧的方程式为:2C6H10+17O2=12CO2+10H2O;
(5)酯类在碱性条件下水解得到的产物是羧酸盐、水和醇;
(6)酯化反应需要在碱性环境下进行,选择浓硫酸的作用是催化剂,且可以作吸水剂,将水从反应中脱离,可以促进可逆反应正向进行,提高酯的产率。
28.【答案】(1)2,3-二甲基戊烷
(2)45.4%
(3)<
(4)+3NaOH+NaCl+CH3OH+H2O
(5)蒸馏
(6)+2[Ag(NH3)2]OH+2Ag↓+3NH3+H2O
(7)n +nHOCH2CH2OH+(2n-1)H2O
(8)15;、、、、
(9)Cu2+;NH3;16
【知识点】配合物的成键情况;有机化合物的命名;同分异构现象和同分异构体;醛的化学性质;缩聚反应
【解析】【解答】(1)该有机物的最长碳链含有5个碳原子,为戊烷。其中第二个、第三个碳原子上都含有一个-CH3,因此该有机物的命名为:2,3-二甲基戊烷。
(2)乙酸的分子式为C2H4O2,乙酸乙酯的分子式为C4H8O2,其中碳氢元素的质量比相同,都是1:6,所以混合物中碳元素的质量分数为7.8%×6=46.8%,因此混合物中氧元素的质量分数为1-7.8%-46.8%=45.4%。
(3)2-甲基丁烷的结构简式为,正戊烷的结构简式为CH3-CH2-CH2-CH2-CH3,二者的分子式相同,结构不同,互为同分异构体。烷烃的同分异构体中,支链越多,熔点越低,因此熔点:2-甲基丁烷<正戊烷。
(4)碳卤键、酯基都能与NaOH溶液发生水解反应,其水解产生的酚羟基、羧基能进一步与NaOH反应,因此反应的化学方程式为:+3NaOH+NaCl+CH3OH+H2O。
(5)CH2Cl2、CHCl3、CCl4为互溶的液体,但沸点不同,可用蒸馏的方法进行分离。
(6)苯甲醛能被银氨溶液氧化成-COOH,进一步与NH3反应生成-COONH4,同时生成Ag。该反应的化学方程式为:+2[Ag(NH3)2]OH+2Ag↓+3NH3+H2O。
(7)对苯二甲酸与乙二醇发生缩聚反应,生成聚对苯二甲酸乙二酯和水,该反应的化学方程式为:n +nHOCH2CH2OH+(2n-1)H2O。
(8)具有相同的官能团,则分子结构中含有C=C、氯原子、-COOH。苯环上只有两个取代基,则具有“邻间对”三种结构。因此两个取代基可分别为-Cl和-CCl=CHCOOH、-Cl和-CH=CClCOOH、-COOH和-CH=CCl2、-COOH和-CCl=CHCl、-Cl和-C(COOH)=CHCl,共五种,所以满足条件的同分异构体共有5×3=15种。其中核磁共振氢谱有4组峰的结构具有对称性,两个取代基位于对位,其结构简式为、、、、。
(9)[Cu(NH3)4]2+的中心离子为Cu2+,配体为NH3,配位原子为N原子。[Cu(NH3)4]2+中NH3分子中含有3个N-H化学键,即含有3个σ键;N原子与Cu2+形成四个配位键,即含有4个σ键。因此1mol[Cu(NH3)4]2+所含的σ键的个数为1mol×(4+3×4)=16mol。
【分析】(1)选取碳原子数最多的碳链作为主链,从靠近支链的一端开始编号,对烷烃进行命名。
(2)根据元素质量比进行计算。
(3)同分异构体中,支链越多,熔沸点越低。
(4)分子结构中含有碳卤键、直接,都能与NaOH溶液发生水解反应,结合水解产物结构进一步确定与NaOH的反应。
(5)互溶但沸点不同的液体的分离用蒸馏。
(6)银氨溶液具有氧化性,能将-CHO氧化成-COOH,-COOH进一步与NH3反应,生成-COONH4,据此写出反应的化学方程式。
(7)对苯二甲酸与乙二醇发生缩聚反应的过程中,生成聚酯结构,生成高分子的同时,生成小分子H2O,据此写出反应的化学方程式。
(8)根据限定条件确定同分异构体的结构和个数。
(9)[Cu(NH3)4]2+的中心离子为Cu2+,配体为NH3,配位原子为N原子。配位键也属于σ键。
29.【答案】(1)
(2)①③④
(3);
(4)
(5);
【知识点】有机物的合成;有机化学反应的综合应用;乙炔炔烃;醛与Cu(OH)2的反应;加成反应
【解析】【解答】(1)根据聚丙烯酸甲酯的结构简式可知,其链节为 ,故答案为: ;
(2)加成反应中原子原理为100%,①~⑤属于加成反应的是①③④,则原子利用率为100%的化学反应的序号:①③④,故答案为:①③④;
(3)反应②为丙烯酸和甲醇发生酯化反应生成CH2=CHCOOCH3,反应的化学方程式为: ;反应⑤为乙醇催化氧化生成乙醛,反应的化学方程式为 ,故答案为:;;
(4)乙炔和水发生加成反应生成乙醛,反应的化学方程式为: ,故答案为: ;
(5) 新制的 与乙醛反应生成氧化亚铁砖红色沉淀,反应的化学方程式为 ;新制的 与乙酸发生中和反应,反应的化学方程式为: ,故答案为:;。
【分析】丙烯酸和甲醇反应生成X,则X的结构简式为CH2=CHCOOCH3,CH2=CHCOOCH3发生加聚反应生成聚丙烯酸甲酯。
30.【答案】(1)酮羰基、碳氯键;加成反应
(2)+HCl
(3)
(4)6;
(5)
【知识点】有机物的合成;有机物的结构和性质;同分异构现象和同分异构体
【解析】【解答】(1)根据B的结构简式可知,B中含有的官能团为酮羰基、碳氯键;根据A、B的结构简式可知,A与乙烯发生加成反应生成B,则A生成B的反应类型为加成反应,故答案为:酮羰基、碳氯键;加成反应;
(2)根据B、C的结构简式可知,B生成C的化学方程式为: +HCl ,故答案为: +HCl ;
(3)由分析可知,W的结构简式为,故答案为:;
(4)A的同分异构体满足:①属于芳香族化合物,说明含有苯环,②能发生银镜反应,说明含有醛基则其结构简式中应含有2个氯原子和1个醛基,两个氯原子在苯环上有邻、间、对3种位置,再将醛基放上去,分别有2种、3种、1种位置关系,则符合条件的同分异构体共有:2+3+1=6种;其中核磁共振氢谱有3组峰的所有结构简式为 ,故答案为:6; ;
(5)根据逆合成分析法, 可由与发生取代反应得到, 发生类似D→E的反应得到,可由 催化氧化得到,则合成路线为: ,故答案为: 。
【分析】E和W反应生成G,结合W的分子式可知,W的结构简式为 。
31.【答案】(1)7;消去反应
(2)NaOH水溶液、加热
(3)2(CH3)2C(OH)COOH +2H2O;n(CH3)2C(OH)COOH + nH2O
(4)5
(5)HEMA结构中的羟基不仅增大了材料的亲水性和吸水性,而且不同聚合物分子中的羟基与水之间产生氢键等作用,形成网状结构的凝胶,使隐形眼镜更柔软。
(6)光照;苯甲醛
【知识点】有机物的推断;有机物的合成;有机物的结构和性质;同分异构现象和同分异构体;烯烃
【解析】【解答】(1)由分析可知,A为CH2=CHCH3,碳碳双键为平面结构,单键可旋转,则A分子中可以共平面的原子数最多有7个;反应①为E发生消去反应生成F,则①的反应类型为消去反应,故答案为:7;消去反应;
(2)B→C为卤代烃的水解反应,反应试剂及条件为NaOH水溶液、加热,故答案为:NaOH水溶液、加热;
(3)反应④为两分子E发生酯化反应生成K,反应的化学方程式为:2(CH3)2C(OH)COOH +2H2O ;反应⑤为E发生缩聚反应生成L,反应的化学方程式为: n(CH3)2C(OH)COOH + nH2O ,故答案为: 2(CH3)2C(OH)COOH +2H2O ; n(CH3)2C(OH)COOH + nH2O ;
(4) F为CH2=C(CH3)COOH,F与足量氢气加成后得到(CH3)2CHCOOH,W的一溴取代物同分异构体中符合:①能发生银镜反应和水解反应,说明含有溴原子、酯基、醛基;②不含环状结构;③只含有两种官能团,说明含有溴原子和HCOO-,符合条件的结构相当于丙烷中的2个氢原子被-Br、HCOO-取代,如果-Br、HCOO-位于同一个碳原子上,有2种位置,如果-Br、HCOO-位于两个碳原子上,有3种位置,所以符合条件的同分异构体有5种,故答案为:5;
(5)HEMA可以作为隐形眼镜材料的可能原因为:EMA结构中的羟基不仅增大了材料的亲水性和吸水性,而且不同聚合物分子中的羟基与水之间产生氢键等作用,形成网状结构的凝胶,使隐形眼镜更柔软,故答案为:EMA结构中的羟基不仅增大了材料的亲水性和吸水性,而且不同聚合物分子中的羟基与水之间产生氢键等作用,形成网状结构的凝胶,使隐形眼镜更柔软;
(6)①甲苯和氯气在光照条件下发生取代反应生成氯甲基苯,则反应条件1是光照,故答案为:光照;
②氯甲基苯发生水解反应生成苯甲醇,苯甲醇发生氧化反应生成K,K和HCN发生已知反应得到产品,则K为,名称为苯甲醛,故答案为:苯甲醛。
【分析】D和HCN发生已知反应生成E,则D为CH3COCH3,C能转化为D,结合C的分子式可知,C为CH3CH(OH)CH3,B水解生成C,结合B的分子式可知,B为CH3CHBrCH3,A发生加成反应生成B,则A为CH2=CHCH3,G可用于生产汽车防冻液,则G为HOCH2CH2OH,I和溴发生加成反应生成J,J发生水解反应生成G,则I为CH2=CH2、J为BrCH2CH2Br,H发生加聚反应生成HEMA,H为CH2=C(CH3)COOCH2CH2OH,E发生消去反应生成F,则F为CH2=C(CH3)COOH,K是六元环状化合物,则K为,在一定条件下可发生缩聚反应生成L,则L为。
32.【答案】(1)
(2)酯基、碳碳双键
(3)
(4)
(5)反应Ⅰ
(6)36
(7)防倒吸;液体分层,上层为无色油层,下层为无色水层;分液
【知识点】有机物的推断;乙烯的化学性质;乙酸乙酯的制取;电子式、化学式或化学符号及名称的综合
【解析】【解答】(1)有机物A的结构简式为CH2=CH2,其电子式为。
(2)丙烯酸乙酯的结构简式为CH2=CHCOOCH2CH3,其中所含的官能团有碳碳双键、酯基。
(3)有机物C的结构简式为CH2=CHCOOH。
(4)反应ⅠCH2=CH2与H2O发生加成反应,生成CH3CH2OH,该反应的化学方程式为:CH2=CH2+H2O CH3CH2OH。
(5)反应Ⅰ为加成反应,其产物只有一种,原子利用率达到100%;反应Ⅱ为氧化反应,在生成有机物C的同时生成H2O,原子利用率小于100%;反应Ⅲ中有机物B和C发生酯化反应,生成丙烯酸乙酯的同时,生成H2O,原子利用率小于100%。因此上述三个反应中,原子利用率为100%的是反应Ⅰ。
(6)由反应的化学方程式可知,每46份质量的有机物B与72份质量的有机物C反应生成100份质量的丙烯酸乙酯,因此46g有机物B与36g有机物C反应时,36g有机物C完全反应,理论上可生成50g丙烯酸乙酯。由于实际产率为72%,所以反应过程中丙烯酸乙酯的实际产量为50g×72%=36g。
(7)①球形干燥管可以起到冷凝和防倒吸作用。
②反应后生成的乙酸乙酯不溶于饱和Na2CO3溶液,因此可观察到分层现象。由于乙酸乙酯的密度比水小,所以油层在上层。故可观察到的现象为:液体分层,上层为无色油层,下层为无色水层。
③试管b中的液体混合物为两种不互溶的液体,可采用分液的方法进行分离。
【分析】有机物A是一种植物生长调节剂,因此A为CH2=CH2。CH2=CHCH3与O2反应生成有机物C,有机物B和有机物C反应生成CH2=CHCOOCH2CH3,因此有机物C为CH2=CHCOOH,有机物B为CH3CH2OH。CH3CH2OH可由CH2=CH2与H2O发生加成反应生成,因此无机物M为H2O。
33.【答案】(1);苯甲醇
(2);氧化反应
(3)6;
(4)3;
【知识点】有机物的结构式;有机物的合成;有机物的结构和性质;同分异构现象和同分异构体;苯酚的化学性质
【解析】【解答】(1) 根据合成路线知D是苯甲醇;
(2)反应①是丙醇发生催化氧化: ;反应②是丙醛被氧化为丙酸,属于氧化反应;
(3)E有一个对称轴,因此苯环上存在对称结构,有等效氢,所以整个分子中等效氢的种类数为:6种;酯类在碱性环境下的水解方程式为: ;
(4)D是苯甲醛,与 FeCl3溶液发生显色反应 应该有酚羟基,其同分异构体有3种; 其中核磁共振氢谱有4组峰的同分异构体的结构简式为。
【分析】根据合成路线可知:A为丙醛,B为丙酸,C为1-氯甲苯,D为苯甲醇。
试题分析部分
1、试卷总体分布分析
总分:127分
分值分布 客观题(占比) 46.0(36.2%)
主观题(占比) 81.0(63.8%)
题量分布 客观题(占比) 23(69.7%)
主观题(占比) 10(30.3%)
2、试卷题量分布分析
大题题型 题目量(占比) 分值(占比)
选择题 15(45.5%) 30.0(23.6%)
非选择题 10(30.3%) 81.0(63.8%)
多选题 8(24.2%) 16.0(12.6%)
3、试卷难度结构分析
序号 难易度 占比
1 普通 (48.5%)
2 容易 (21.2%)
3 困难 (30.3%)
4、试卷知识点分析
序号 知识点(认知水平) 分值(占比) 对应题号
1 甲烷的化学性质 10.0(7.9%) 17,24
2 乙醇的消去反应 2.0(1.6%) 8
3 化石燃料与基本化工原料 2.0(1.6%) 11
4 有机物中的官能团 2.0(1.6%) 21
5 乙烯的化学性质 30.0(23.6%) 4,5,17,20,24,25,32
6 苯的同系物及其性质 4.0(3.1%) 1,18
7 乙酸乙酯的制取 11.0(8.7%) 8,32
8 乙醇的化学性质 7.0(5.5%) 17,25
9 醛与Cu(OH)2的反应 7.0(5.5%) 29
10 同系物 21.0(16.5%) 2,20,24,26
11 探究影响化学反应速率的因素 2.0(1.6%) 22
12 烃类的燃烧 8.0(6.3%) 24
13 乙炔炔烃 11.0(8.7%) 7,8,29
14 苯酚的化学性质 8.0(6.3%) 33
15 石油副产品的综合应用 4.0(3.1%) 9,19
16 高分子材料 2.0(1.6%) 15
17 烷烃 2.0(1.6%) 3
18 配制一定物质的量浓度的溶液 2.0(1.6%) 22
19 有机物的推断 20.0(15.7%) 21,31,32
20 有机物的合成 31.0(24.4%) 29,30,31,33
21 饱和烃与不饱和烃 2.0(1.6%) 1
22 石油的裂化和裂解 2.0(1.6%) 10
23 物质的简单分类 7.0(5.5%) 27
24 常见的生活环境的污染及治理 2.0(1.6%) 19
25 同素异形体 9.0(7.1%) 26
26 使用化石燃料的利弊及新能源的开发 2.0(1.6%) 11
27 有机化学反应的综合应用 7.0(5.5%) 29
28 化学反应速率 2.0(1.6%) 12
29 生活中的有机化合物 2.0(1.6%) 12
30 苯酚的性质及用途 2.0(1.6%) 7
31 化学实验方案的评价 6.0(4.7%) 7,8,22
32 烯烃 13.0(10.2%) 6,21,31
33 取代反应 13.0(10.2%) 13,14,17,21,25
34 芳香烃 4.0(3.1%) 1,16
35 有机化合物的命名 12.0(9.4%) 28
36 二糖的性质和用途 2.0(1.6%) 7
37 缩聚反应 12.0(9.4%) 28
38 乙酸的化学性质 5.0(3.9%) 25
39 醛的化学性质 12.0(9.4%) 28
40 有机物的结构式 8.0(6.3%) 33
41 乙烯的用途 5.0(3.9%) 25
42 聚合反应 9.0(7.1%) 26
43 焰色反应 2.0(1.6%) 7
44 盐析 2.0(1.6%) 15
45 水的净化 2.0(1.6%) 10
46 配合物的成键情况 12.0(9.4%) 28
47 原电池工作原理及应用 2.0(1.6%) 12
48 消去反应 2.0(1.6%) 14
49 氯气的化学性质 2.0(1.6%) 22
50 同分异构现象和同分异构体 49.0(38.6%) 2,23,26,28,30,31,33
51 乙烯的实验室制法 4.0(3.1%) 5,22
52 卤代烃简介 2.0(1.6%) 3
53 加成反应 20.0(15.7%) 6,14,21,27,29
54 石油的分馏产品和用途 2.0(1.6%) 9
55 海水资源及其综合利用 2.0(1.6%) 19
56 有机物的结构和性质 37.0(29.1%) 1,14,23,27,30,31,33
57 苯的结构与性质 4.0(3.1%) 8,17
58 煤的干馏和综合利用 4.0(3.1%) 9,19
59 水解反应 2.0(1.6%) 15
60 电子式、化学式或化学符号及名称的综合 9.0(7.1%) 32
61 有机高分子化合物的结构和性质 2.0(1.6%) 12
62 酯化反应 26.0(20.5%) 13,24,26,27
63 同位素及其应用 2.0(1.6%) 2
64 分子式 2.0(1.6%) 20
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
