2.2 氯及其化合物 (含解析)同步练习题 2023-2024学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 2.2 氯及其化合物 (含解析)同步练习题 2023-2024学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 347.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-17 00:00:00 | ||
图片预览


文档简介
2.2 氯及其化合物 同步练习题
一、选择题
1.室温下,下列各组离子在指定溶液中能大量共存的是
A.溶液:
B.溶液:
C.溶液:
D.氨水溶液:
2.下列物质间的转化不能一步实现的是
A.NaCl →NaHCO3 B.Fe→FeCl3
C.Na→Na2O2 D.CaCO3→Ca(OH)2
3.氯及其化合物广泛应用于日常生活中,例如常用的含氯消毒剂“84”消毒液(含有NaClO)、清洁剂“洁厕灵”(含有盐酸)等。“84”消毒液与“洁厕灵”不能混合使用。氯气是制备含氯化合物的重要原料。下列有关氯气的实验装置或操作能达到实验目的的是
A B C D
产生Cl2 除去Cl2中的HCl 将溶液中的Br-氧化为Br2 测氯水的pH
A.A B.B C.C D.D
4.下列化合物中,不能由单质之间直接化合生成的是
A.Na2O B.Na2O2 C.CuCl2 D.FeCl2
5.数字化实验将传感器、数据采集器和计算机相连,可利用信息技术对化学实验进行数据的采集和分析。如图是数字化实验得到的光照过程中氯水中的溶液pH、氯离子浓度、氧气体积的变化情况。下列有关说法正确的是
A.若在光照开始时,向氯水中滴入几滴紫色石蕊试液,随着实验的进行,溶液红色逐渐加深,最终颜色深度不再改变
B.图丙中浓度增大的原因是在光照条件下分解产生了
C.从图中相关曲线变化可知在光照过程中溶液的导电能力逐渐增强
D.在饱和氯水中滴加溶液,无明显现象
6.下列物质中,不能由单质直接化合生成的是
A.HCl B.FeCl3 C.CuCl D.NaCl
7.新型冠状病毒肺炎疫情在全球多地爆发,“84”消毒液是大规模环境消毒剂。已知:“84”消毒液由Cl2和NaOH反应制得。下列说法不正确的是( )
A.“84”消毒液的有效成分是NaClO和NaCl
B.“84”消毒液储能杀菌消毒外,还可做漂白剂
C.检验该消毒液中是否含有Cl-的方程式为Ag++Cl-=AgCl↓
D.不能用pH试纸来测该溶液的pH
8.化学与生活息息相关。下列关于各“剂”在生活中的应用说法错误的是
A.活性炭包常用作冰箱的“除味剂” B.氧化钠可用作潜艇的“供氧剂”
C.活性铁粉在食品袋中作“去氧剂” D.可用作自来水的“消毒剂”
二、非选择题
9.新冠病毒的消毒剂有很多种,如84消毒液、H2O2溶液和酸性KMnO4溶液等。请回答下列问题:
(1)将H2O2加入浸泡铜片的稀硫酸中可以使铜片溶解,该反应的离子方程式为_____。
(2)高锰酸钾与盐酸在常温下反应可以制得氯气,此时MnO转化为Mn2+。
①上述反应的化学方程式为_____,其中盐酸表现出的性质是_____。
②有同学猜测铁与氯气反应可能还会生成氯化亚铁(假设铁已完全反应),该同学根据能否使酸性高锰酸钾溶液褪色来检验生成物中是否含氯化亚铁,你认为该同学的依据能否达到目的,并说明理由:_____。
③将8.7gMnO2与100g36.5%的盐酸充分反应后,再向溶液中加入足量的AgNO3溶液。若不考虑盐酸的挥发和氯气的溶解,则上述可制得的氯气是_____g,会得到_____g白色沉淀。
10.(1)请写出指定物质对应的化学式。消毒剂碘伏中含有碘分子_____________,胶卷中必不可少的感光材料_____________,加碘盐中含有碘酸钾_____________,发酵粉含有小苏打_____________。
(2)化工厂镁着火,不能用二氧化碳灭火,用化学方程式解释__________________________。
(3)电解饱和食盐水是氯碱工业的基础,写出化学方程式__________________________。
(4)稀醋酸处理热水瓶中水垢(主要成分为碳酸钙)的离子方程式__________________________。
11.现有失去标签的A、B、C、D、E五个集气瓶,分别充满H2、O2、Cl2、HCl、HBr五种气体中的一种,其中C是黄绿色,A、C混和见光爆炸,C、D混合在瓶壁上出现橙红色小液滴,E遇到潮湿空气出现白雾,则这五个集气瓶中装的气体分别是:A_______B_______C_______D_______E_______。
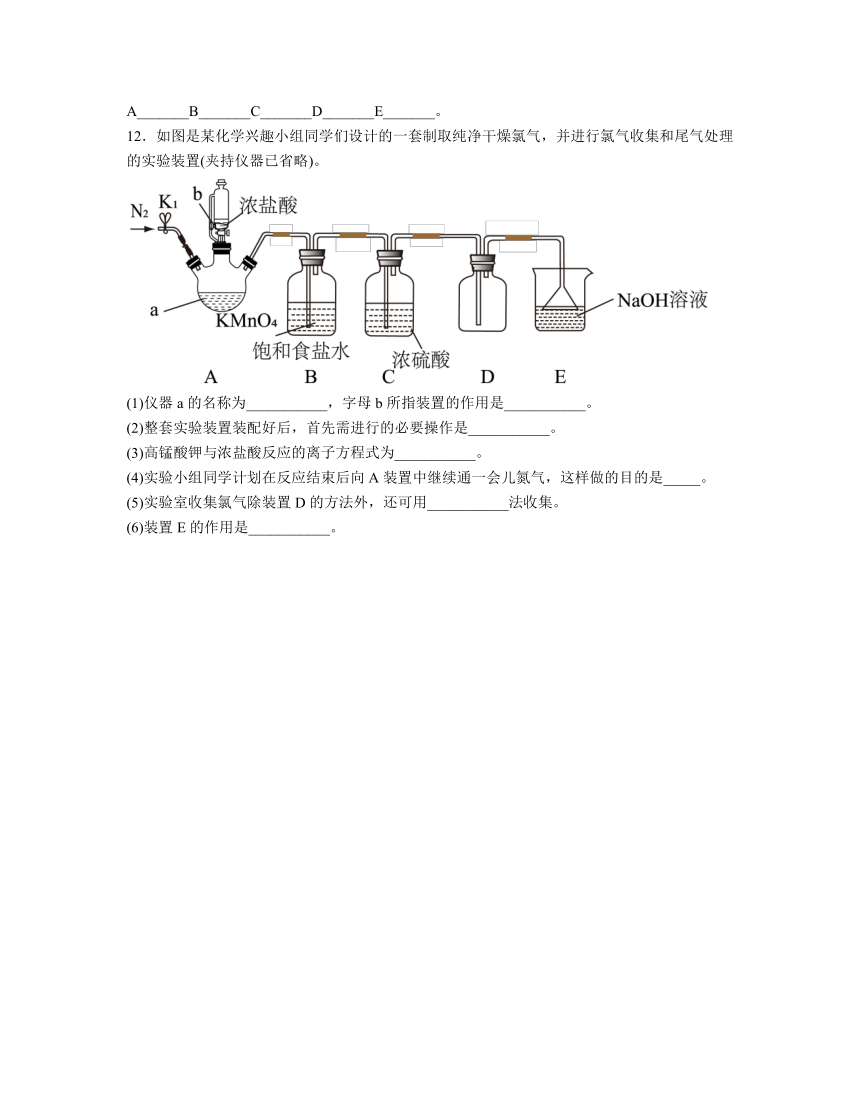
12.如图是某化学兴趣小组同学们设计的一套制取纯净干燥氯气,并进行氯气收集和尾气处理的实验装置(夹持仪器已省略)。
(1)仪器a的名称为___________,字母b所指装置的作用是___________。
(2)整套实验装置装配好后,首先需进行的必要操作是___________。
(3)高锰酸钾与浓盐酸反应的离子方程式为___________。
(4)实验小组同学计划在反应结束后向A装置中继续通一会儿氮气,这样做的目的是_____。
(5)实验室收集氯气除装置D的方法外,还可用___________法收集。
(6)装置E的作用是___________。
【参考答案】
一、选择题
1.A
解析:A.溶液中四种离子之间不发生反应,可以大量共存,故A选;
B.溶液中和I-发生氧化还原反应,不能大量共存,故B不选;
C.溶液中H+和形成弱酸,不能大量共存,故C不选;
D.氨水溶液呈碱性,Mg2+在碱性溶液中会形成氢氧化镁沉淀,故D不选;
故选A。
2.D
解析:A.向氨化的氯化钠溶液中通入二氧化碳,氯化钠溶液与氨气、二氧化碳反应生成碳酸氢钠和氯化铵,则氯化钠能一步转化为碳酸氢钠,故A不符合题意;
B.铁与氯气加热生成氯化铁,故B不符合题意;
C.钠和氧气在共热条件下反应生成过氧化钠,则钠能一步转化为过氧化钠,故C不符合题意;
D.碳酸钙不溶于水,不能一步反应生成氢氧化钙,碳酸钙转化为氢氧化钙的步骤为碳酸钙先高温分解生成氧化钙,氧化钙与水发生化合反应生成氢氧化钙,故D符合题意;
故选D。
3.C
解析:A.浓盐酸和二氧化锰在加热条件下反应生成Cl2,故A错误;
B.HCl和NaHCO3反应生成二氧化碳引入了新的杂质,应该用饱和食盐水除去Cl2中的HCl,故B错误;
C.Cl2的氧化性强于Br2,将Cl2通入含Br-的溶液中,可以将溶液中的Br-氧化为Br2,故C正确;
D.氯水具有漂白性,不能用pH试纸测氯水的pH,故D错误;
故选C。
4.D
解析:A.钠和氧气常温反应生成Na2O,A不合题意;
B.钠和氧气加热或点燃条件下反应生成Na2O2,B不合题意;
C.铜在氯气中燃烧生成CuCl2,C不合题意;
D.铁在氯气中燃烧生成FeCl3,D符合题意;
故选D。
5.C
解析:A.次氯酸具有强氧化性,能使有色物质褪色且不可逆;若在光照开始时,向氯水中滴入几滴紫色石蕊试液,溶液变红色又褪色,A错误;
B.图丙中浓度增大的原因是次氯酸在光照条件下分解产生了,B错误;
C.在光照过程中溶液中离子浓度增大,可知在光照过程中溶液的导电能力逐渐增强,C正确;
D.饱和氯水中存在氯离子,在饱和氯水中滴加溶液,生成白色氯化银沉淀,D错误;
故选C。
6.C
解析:A.H2与Cl2反应可直接化合得到HCl,A不符合题意;
B.Fe与Cl2直接化合得到FeCl3,B不符合题意;
C.Cu与Cl2直接化合得到CuCl2, 不能得到CuCl,C符合题意;
D.Cl2与Na反应可直接化合得到NaCl,D不符合题意;
故答案为:C。
7.A
解析:“84”消毒液由Cl2和NaOH反应制得,该反应方程式为Cl2+2NaOH=NaCl+NaClO+H2O。
A.“84”消毒液的有效成分是具有漂白性的NaClO,故A项错误;
B.“84”消毒液中NaClO有强氧化性,能用作日常消毒,另外NaClO具有漂白性,故B项正确;
C.氯离子能和银离子结合生成白色的AgCl沉淀,该反应可以用来检验氯离子,故C项正确;
D.NaClO具有漂白性,能将pH试纸漂白,因此不能用pH试纸来测试该溶液的pH值,故D项正确;
综上所述,答案选A项。
8.B
解析:A.活性炭可吸附异味,所以常用作冰箱的“除味剂”,A正确;
B.过氧化钠可与人呼出的二氧化碳或水蒸气发生反应产生氧气,可用作潜艇的“供氧剂”,B错误;
C.铁粉具有强还原性,所以在食品袋中可作“去氧剂”,C正确;
D.具有一定的氧化性,可进行杀菌消毒,所以可用作自来水的“消毒剂”,D正确;
故选B。
二、非选择题
9.(1)
(2) 还原性和酸性; 不能,因为高锰酸钾可以氧化Cl-,自身颜色褪色; 7.1 28.6
解析:(1)将H2O2加入浸泡铜片的稀硫酸中可以使铜片溶解,反应的离子方程式为;故答案为;
(2)①高锰酸钾与盐酸在常温下反应可以制得氯气,离子方程式为,盐酸表现出还原性和酸性;故答案为;还原性和酸性;
②由题可知,高锰酸钾可以氧化Cl-,也会使高锰酸钾颜色褪色;故答案为不能,因为高锰酸钾可以氧化Cl-,自身颜色褪色;
③,,,说明盐酸过量,可认为MnO2完全反应,所以,;,所以,;故答案为7.1;28.6。
10. I2 AgBr KIO3 NaHCO3 2Mg+CO2 2MgO+C
解析:(1)碘分子为:I2;胶卷中必不可少的感光材料是AgBr;碘酸钾的化学式为KIO3;发酵粉含有的小苏打是碳酸氢钠,化学式为NaHCO3;
(2)二氧化碳会和镁发生反应,方程式为:2Mg+CO22MgO+C;
(3)电解饱和食盐水化学方程式为:;
(4)稀醋酸处理热水瓶中水垢(主要成分为碳酸钙)的离子方程式为:;
11. H2 O2 Cl2 HBr HCl
【分析】由“C是黄绿色”知C是氯气,由“A、C混和见光爆炸”知A是氢气,由“C、D混合在瓶壁上出现橙红色小液滴”知D是溴化氢,由“E遇到潮湿空气出现白雾”知E是氯化氢,剩下的B便是氧气。
解析:据分析可知,A为H2,B为O2,C为Cl2,D为HBr,E为HCl;
故答案为H2,O2,Cl2,HBr,HCl。
12.(1) 三颈烧瓶 平衡压强,便于浓盐酸顺利流下
(2)检查装置的气密性
(3)
(4)将氯气充分排出,以便被NaOH溶液充分吸收,防止污染空气
(5)排饱和食盐水
(6)吸收氯气,防止污染空气:防止倒吸
【分析】利用高锰酸钾和浓盐酸反应生成氯气,用饱和食盐水除去氯气中的氯化氢气体,浓硫酸除去氯气中的水,在装置D中收集氯气,最后用氢氧化钠溶液吸收多余氯气,防止污染。据此解答。
解析:(1)仪器a为三颈烧瓶,b可以平衡压强,便于浓盐酸顺利滴下;
(2)首先进行的操作是检查装置的气密性;
(3)高锰酸钾和浓盐酸反应生成氯气,反应的离子方程式为:;
(4)实验后持续通氮气,是为了将装置中的氯气全部排出,被氢氧化钠溶液吸收,防止污染空气;
(5)氯气在饱和食盐水中的溶解度很小,故可以用排饱和食盐水的方法收集氯气;
(6)装置E为吸收氯气,防止污染,倒置漏斗是为了防止倒吸
一、选择题
1.室温下,下列各组离子在指定溶液中能大量共存的是
A.溶液:
B.溶液:
C.溶液:
D.氨水溶液:
2.下列物质间的转化不能一步实现的是
A.NaCl →NaHCO3 B.Fe→FeCl3
C.Na→Na2O2 D.CaCO3→Ca(OH)2
3.氯及其化合物广泛应用于日常生活中,例如常用的含氯消毒剂“84”消毒液(含有NaClO)、清洁剂“洁厕灵”(含有盐酸)等。“84”消毒液与“洁厕灵”不能混合使用。氯气是制备含氯化合物的重要原料。下列有关氯气的实验装置或操作能达到实验目的的是
A B C D
产生Cl2 除去Cl2中的HCl 将溶液中的Br-氧化为Br2 测氯水的pH
A.A B.B C.C D.D
4.下列化合物中,不能由单质之间直接化合生成的是
A.Na2O B.Na2O2 C.CuCl2 D.FeCl2
5.数字化实验将传感器、数据采集器和计算机相连,可利用信息技术对化学实验进行数据的采集和分析。如图是数字化实验得到的光照过程中氯水中的溶液pH、氯离子浓度、氧气体积的变化情况。下列有关说法正确的是
A.若在光照开始时,向氯水中滴入几滴紫色石蕊试液,随着实验的进行,溶液红色逐渐加深,最终颜色深度不再改变
B.图丙中浓度增大的原因是在光照条件下分解产生了
C.从图中相关曲线变化可知在光照过程中溶液的导电能力逐渐增强
D.在饱和氯水中滴加溶液,无明显现象
6.下列物质中,不能由单质直接化合生成的是
A.HCl B.FeCl3 C.CuCl D.NaCl
7.新型冠状病毒肺炎疫情在全球多地爆发,“84”消毒液是大规模环境消毒剂。已知:“84”消毒液由Cl2和NaOH反应制得。下列说法不正确的是( )
A.“84”消毒液的有效成分是NaClO和NaCl
B.“84”消毒液储能杀菌消毒外,还可做漂白剂
C.检验该消毒液中是否含有Cl-的方程式为Ag++Cl-=AgCl↓
D.不能用pH试纸来测该溶液的pH
8.化学与生活息息相关。下列关于各“剂”在生活中的应用说法错误的是
A.活性炭包常用作冰箱的“除味剂” B.氧化钠可用作潜艇的“供氧剂”
C.活性铁粉在食品袋中作“去氧剂” D.可用作自来水的“消毒剂”
二、非选择题
9.新冠病毒的消毒剂有很多种,如84消毒液、H2O2溶液和酸性KMnO4溶液等。请回答下列问题:
(1)将H2O2加入浸泡铜片的稀硫酸中可以使铜片溶解,该反应的离子方程式为_____。
(2)高锰酸钾与盐酸在常温下反应可以制得氯气,此时MnO转化为Mn2+。
①上述反应的化学方程式为_____,其中盐酸表现出的性质是_____。
②有同学猜测铁与氯气反应可能还会生成氯化亚铁(假设铁已完全反应),该同学根据能否使酸性高锰酸钾溶液褪色来检验生成物中是否含氯化亚铁,你认为该同学的依据能否达到目的,并说明理由:_____。
③将8.7gMnO2与100g36.5%的盐酸充分反应后,再向溶液中加入足量的AgNO3溶液。若不考虑盐酸的挥发和氯气的溶解,则上述可制得的氯气是_____g,会得到_____g白色沉淀。
10.(1)请写出指定物质对应的化学式。消毒剂碘伏中含有碘分子_____________,胶卷中必不可少的感光材料_____________,加碘盐中含有碘酸钾_____________,发酵粉含有小苏打_____________。
(2)化工厂镁着火,不能用二氧化碳灭火,用化学方程式解释__________________________。
(3)电解饱和食盐水是氯碱工业的基础,写出化学方程式__________________________。
(4)稀醋酸处理热水瓶中水垢(主要成分为碳酸钙)的离子方程式__________________________。
11.现有失去标签的A、B、C、D、E五个集气瓶,分别充满H2、O2、Cl2、HCl、HBr五种气体中的一种,其中C是黄绿色,A、C混和见光爆炸,C、D混合在瓶壁上出现橙红色小液滴,E遇到潮湿空气出现白雾,则这五个集气瓶中装的气体分别是:A_______B_______C_______D_______E_______。
12.如图是某化学兴趣小组同学们设计的一套制取纯净干燥氯气,并进行氯气收集和尾气处理的实验装置(夹持仪器已省略)。
(1)仪器a的名称为___________,字母b所指装置的作用是___________。
(2)整套实验装置装配好后,首先需进行的必要操作是___________。
(3)高锰酸钾与浓盐酸反应的离子方程式为___________。
(4)实验小组同学计划在反应结束后向A装置中继续通一会儿氮气,这样做的目的是_____。
(5)实验室收集氯气除装置D的方法外,还可用___________法收集。
(6)装置E的作用是___________。
【参考答案】
一、选择题
1.A
解析:A.溶液中四种离子之间不发生反应,可以大量共存,故A选;
B.溶液中和I-发生氧化还原反应,不能大量共存,故B不选;
C.溶液中H+和形成弱酸,不能大量共存,故C不选;
D.氨水溶液呈碱性,Mg2+在碱性溶液中会形成氢氧化镁沉淀,故D不选;
故选A。
2.D
解析:A.向氨化的氯化钠溶液中通入二氧化碳,氯化钠溶液与氨气、二氧化碳反应生成碳酸氢钠和氯化铵,则氯化钠能一步转化为碳酸氢钠,故A不符合题意;
B.铁与氯气加热生成氯化铁,故B不符合题意;
C.钠和氧气在共热条件下反应生成过氧化钠,则钠能一步转化为过氧化钠,故C不符合题意;
D.碳酸钙不溶于水,不能一步反应生成氢氧化钙,碳酸钙转化为氢氧化钙的步骤为碳酸钙先高温分解生成氧化钙,氧化钙与水发生化合反应生成氢氧化钙,故D符合题意;
故选D。
3.C
解析:A.浓盐酸和二氧化锰在加热条件下反应生成Cl2,故A错误;
B.HCl和NaHCO3反应生成二氧化碳引入了新的杂质,应该用饱和食盐水除去Cl2中的HCl,故B错误;
C.Cl2的氧化性强于Br2,将Cl2通入含Br-的溶液中,可以将溶液中的Br-氧化为Br2,故C正确;
D.氯水具有漂白性,不能用pH试纸测氯水的pH,故D错误;
故选C。
4.D
解析:A.钠和氧气常温反应生成Na2O,A不合题意;
B.钠和氧气加热或点燃条件下反应生成Na2O2,B不合题意;
C.铜在氯气中燃烧生成CuCl2,C不合题意;
D.铁在氯气中燃烧生成FeCl3,D符合题意;
故选D。
5.C
解析:A.次氯酸具有强氧化性,能使有色物质褪色且不可逆;若在光照开始时,向氯水中滴入几滴紫色石蕊试液,溶液变红色又褪色,A错误;
B.图丙中浓度增大的原因是次氯酸在光照条件下分解产生了,B错误;
C.在光照过程中溶液中离子浓度增大,可知在光照过程中溶液的导电能力逐渐增强,C正确;
D.饱和氯水中存在氯离子,在饱和氯水中滴加溶液,生成白色氯化银沉淀,D错误;
故选C。
6.C
解析:A.H2与Cl2反应可直接化合得到HCl,A不符合题意;
B.Fe与Cl2直接化合得到FeCl3,B不符合题意;
C.Cu与Cl2直接化合得到CuCl2, 不能得到CuCl,C符合题意;
D.Cl2与Na反应可直接化合得到NaCl,D不符合题意;
故答案为:C。
7.A
解析:“84”消毒液由Cl2和NaOH反应制得,该反应方程式为Cl2+2NaOH=NaCl+NaClO+H2O。
A.“84”消毒液的有效成分是具有漂白性的NaClO,故A项错误;
B.“84”消毒液中NaClO有强氧化性,能用作日常消毒,另外NaClO具有漂白性,故B项正确;
C.氯离子能和银离子结合生成白色的AgCl沉淀,该反应可以用来检验氯离子,故C项正确;
D.NaClO具有漂白性,能将pH试纸漂白,因此不能用pH试纸来测试该溶液的pH值,故D项正确;
综上所述,答案选A项。
8.B
解析:A.活性炭可吸附异味,所以常用作冰箱的“除味剂”,A正确;
B.过氧化钠可与人呼出的二氧化碳或水蒸气发生反应产生氧气,可用作潜艇的“供氧剂”,B错误;
C.铁粉具有强还原性,所以在食品袋中可作“去氧剂”,C正确;
D.具有一定的氧化性,可进行杀菌消毒,所以可用作自来水的“消毒剂”,D正确;
故选B。
二、非选择题
9.(1)
(2) 还原性和酸性; 不能,因为高锰酸钾可以氧化Cl-,自身颜色褪色; 7.1 28.6
解析:(1)将H2O2加入浸泡铜片的稀硫酸中可以使铜片溶解,反应的离子方程式为;故答案为;
(2)①高锰酸钾与盐酸在常温下反应可以制得氯气,离子方程式为,盐酸表现出还原性和酸性;故答案为;还原性和酸性;
②由题可知,高锰酸钾可以氧化Cl-,也会使高锰酸钾颜色褪色;故答案为不能,因为高锰酸钾可以氧化Cl-,自身颜色褪色;
③,,,说明盐酸过量,可认为MnO2完全反应,所以,;,所以,;故答案为7.1;28.6。
10. I2 AgBr KIO3 NaHCO3 2Mg+CO2 2MgO+C
解析:(1)碘分子为:I2;胶卷中必不可少的感光材料是AgBr;碘酸钾的化学式为KIO3;发酵粉含有的小苏打是碳酸氢钠,化学式为NaHCO3;
(2)二氧化碳会和镁发生反应,方程式为:2Mg+CO22MgO+C;
(3)电解饱和食盐水化学方程式为:;
(4)稀醋酸处理热水瓶中水垢(主要成分为碳酸钙)的离子方程式为:;
11. H2 O2 Cl2 HBr HCl
【分析】由“C是黄绿色”知C是氯气,由“A、C混和见光爆炸”知A是氢气,由“C、D混合在瓶壁上出现橙红色小液滴”知D是溴化氢,由“E遇到潮湿空气出现白雾”知E是氯化氢,剩下的B便是氧气。
解析:据分析可知,A为H2,B为O2,C为Cl2,D为HBr,E为HCl;
故答案为H2,O2,Cl2,HBr,HCl。
12.(1) 三颈烧瓶 平衡压强,便于浓盐酸顺利流下
(2)检查装置的气密性
(3)
(4)将氯气充分排出,以便被NaOH溶液充分吸收,防止污染空气
(5)排饱和食盐水
(6)吸收氯气,防止污染空气:防止倒吸
【分析】利用高锰酸钾和浓盐酸反应生成氯气,用饱和食盐水除去氯气中的氯化氢气体,浓硫酸除去氯气中的水,在装置D中收集氯气,最后用氢氧化钠溶液吸收多余氯气,防止污染。据此解答。
解析:(1)仪器a为三颈烧瓶,b可以平衡压强,便于浓盐酸顺利滴下;
(2)首先进行的操作是检查装置的气密性;
(3)高锰酸钾和浓盐酸反应生成氯气,反应的离子方程式为:;
(4)实验后持续通氮气,是为了将装置中的氯气全部排出,被氢氧化钠溶液吸收,防止污染空气;
(5)氯气在饱和食盐水中的溶解度很小,故可以用排饱和食盐水的方法收集氯气;
(6)装置E为吸收氯气,防止污染,倒置漏斗是为了防止倒吸
