【备考2024】高考生物总复习知识讲解课件 :专题4 酶与ATP(共40张PPT)
文档属性
| 名称 | 【备考2024】高考生物总复习知识讲解课件 :专题4 酶与ATP(共40张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 生物学 | ||
| 更新时间 | 2023-11-19 00:00:00 | ||
图片预览







文档简介
(共40张PPT)
专题四 酶与ATP
高考生物总复习知识讲解
基础篇
考点一 酶
一、酶的概念剖析与作用机理
1.酶的概念剖析与拓展
化学本质 绝大多数是 蛋白质 少数是RNA
合成原料 氨基酸 核糖核苷酸
合成场所 核糖体 主要是细胞核
来源 一般来说,活细胞都能产生酶 生理功能 具有 催化 作用
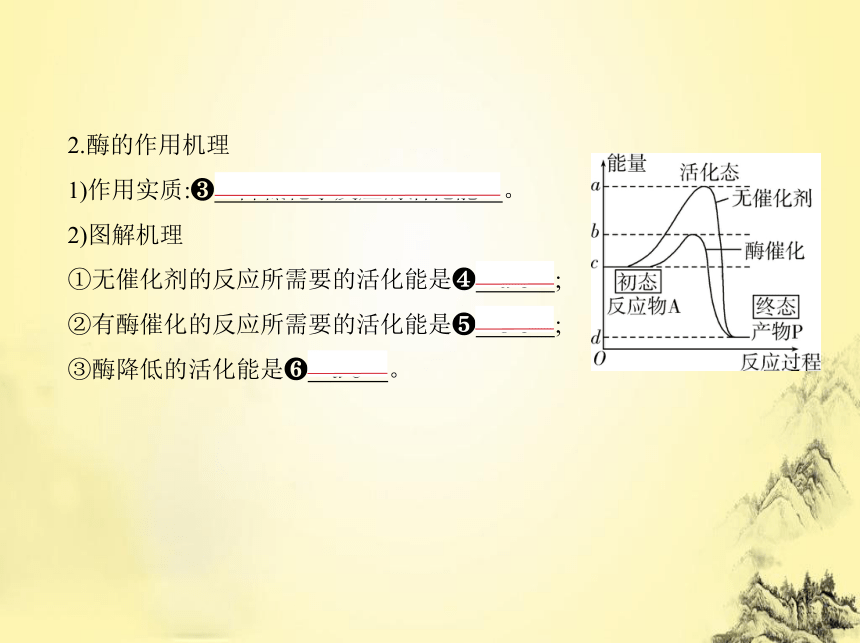
2.酶的作用机理
1)作用实质: 降低化学反应的活化能 。
2)图解机理
①无催化剂的反应所需要的活化能是 a-c ;
②有酶催化的反应所需要的活化能是 b-c ;
③酶降低的活化能是 a-b 。
二、酶的特性
1.酶具有高效性
1)原因:与无机催化剂相比,酶降低活化能的作用更显著。
2)特点:酶能缩短达到化学平衡点的时间,但不改变平衡点,因而酶不会改
变最终 生成物 的量。且反应前后酶的数量和性质不变。
易混易错
(1)加酶与不加催化剂相比,体现了酶具有催化作用。(2)加酶与加无机催
化剂相比,体现了酶具有高效性。
2.酶具有专一性
1)含义:每一种酶只能催化一种或一类化学反应。
2)图中显示,酶A能催化反应物发生化学反应,而酶
B不能,说明酶A具有 专一性 。
3)除上述情况外,像DNA连接酶、RNA聚合酶等酶类分别可催化一类化
学反应。
知识归纳
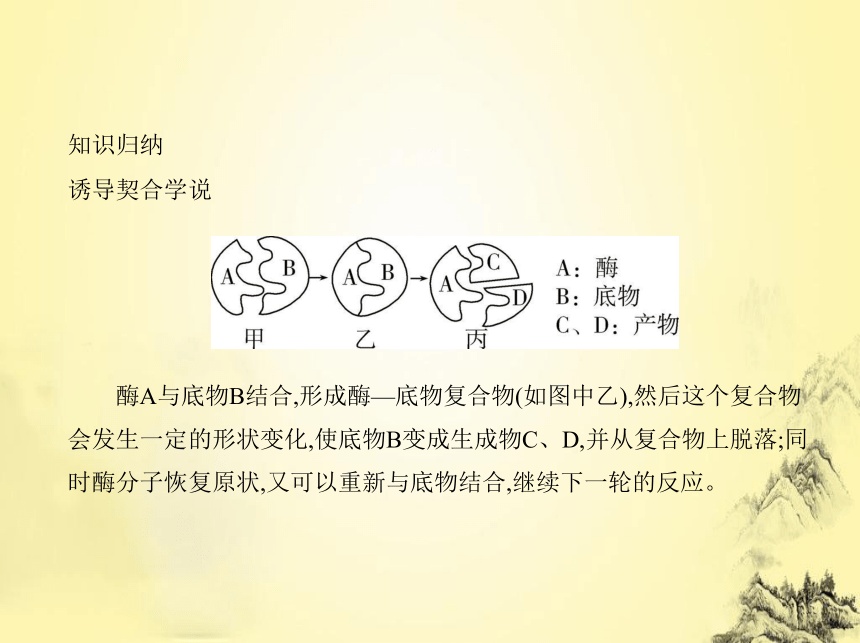
诱导契合学说
酶A与底物B结合,形成酶—底物复合物(如图中乙),然后这个复合物
会发生一定的形状变化,使底物B变成生成物C、D,并从复合物上脱落;同
时酶分子恢复原状,又可以重新与底物结合,继续下一轮的反应。
3.酶的作用条件较温和
1)特点:在最适宜的温度和pH条件下,酶的活性最高。
2)酶活性
①实质:酶催化特定化学反应的能力。
②表示方法:酶促反应速率(可用单位时间内产物的生成量或反应物的消
耗量表示)。
三、影响酶促反应速率的因素
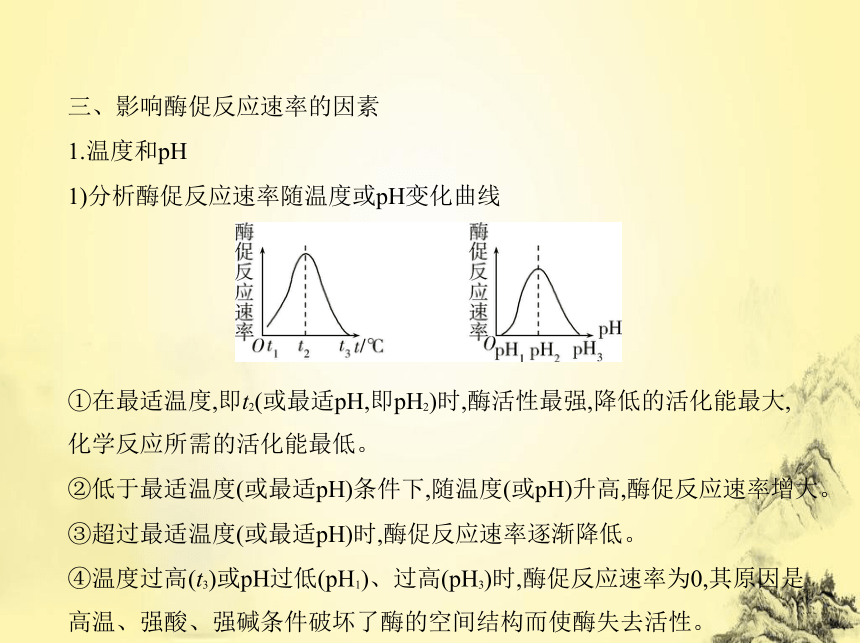
1.温度和pH
1)分析酶促反应速率随温度或pH变化曲线
①在最适温度,即t2(或最适pH,即pH2)时,酶活性最强,降低的活化能最大,
化学反应所需的活化能最低。
②低于最适温度(或最适pH)条件下,随温度(或pH)升高,酶促反应速率增大。
③超过最适温度(或最适pH)时,酶促反应速率逐渐降低。
④温度过高(t3)或pH过低(pH1)、过高(pH3)时,酶促反应速率为0,其原因是
高温、强酸、强碱条件破坏了酶的空间结构而使酶失去活性。
易混易错
(1)低温条件下(t1时),酶的活性低的原因不是低温破坏了酶的空间结构,而
是低温抑制了酶的活性,当温度由t1上升到t2时,酶的活性可以恢复为最高
活性,因此酶需在低温(pH最适)条件下保存。
(2)即使将导致酶失去活性的条件恢复至最适条件(如温度由t3降低至t2),
酶活性也不能恢复。
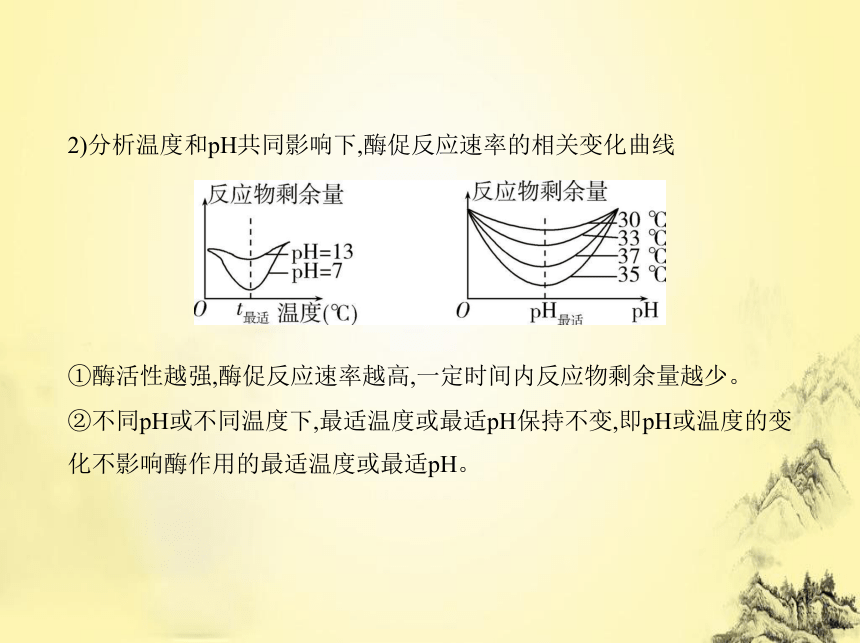
2)分析温度和pH共同影响下,酶促反应速率的相关变化曲线
①酶活性越强,酶促反应速率越高,一定时间内反应物剩余量越少。
②不同pH或不同温度下,最适温度或最适pH保持不变,即pH或温度的变
化不影响酶作用的最适温度或最适pH。
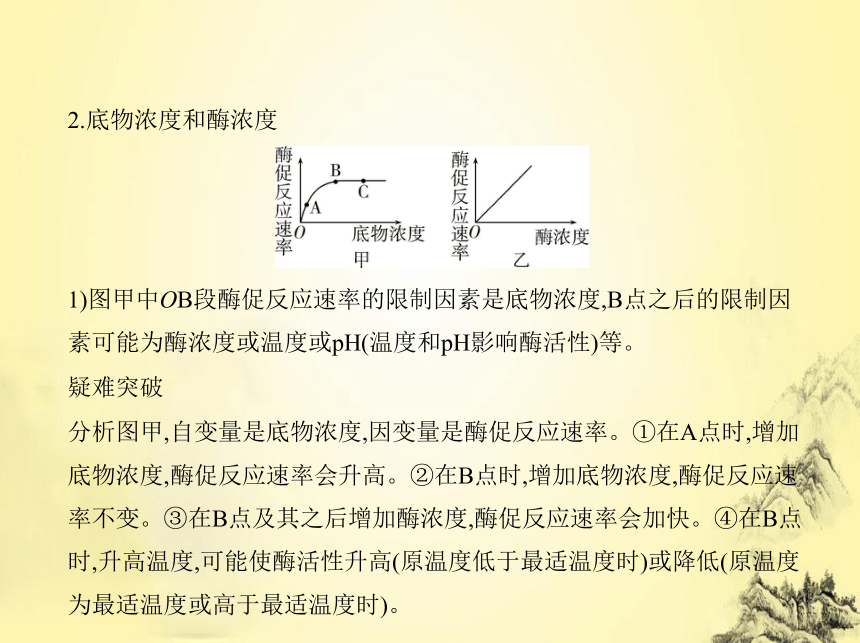
2.底物浓度和酶浓度
1)图甲中OB段酶促反应速率的限制因素是底物浓度,B点之后的限制因
素可能为酶浓度或温度或pH(温度和pH影响酶活性)等。
疑难突破
分析图甲,自变量是底物浓度,因变量是酶促反应速率。①在A点时,增加
底物浓度,酶促反应速率会升高。②在B点时,增加底物浓度,酶促反应速
率不变。③在B点及其之后增加酶浓度,酶促反应速率会加快。④在B点
时,升高温度,可能使酶活性升高(原温度低于最适温度时)或降低(原温度
为最适温度或高于最适温度时)。
2)图乙表示在底物充足时,酶促反应速率与酶浓度成正比。
注意:底物浓度和酶浓度不影响酶活性,其通过影响酶与底物的接触影响
酶促反应速率。
知识拓展
抑制剂
酶的抑制剂有竞争性抑制剂和非竞争性抑制剂
竞争性抑制剂与底物具有类似的结构,能与底物竞争酶的活性部位,当抑
制剂结合到酶活性部位后,底物被排斥在酶活性部位以外,导致酶促反应
被抑制;非竞争性抑制剂与底物结构不同,与酶结合的位点也不同,非竞争
性抑制剂与酶结合后,可引起酶构象改变并导致酶无法与底物结合,或者
虽然可以与底物结合但是无法得到产物等,这些都会导致酶活性降低或
丧失,如图。
竞争性抑制剂抑制酶与底物的结合,若增加底物浓度,抑制剂与酶活
性部位结合的概率变小,抑制程度减小。
考点训练(请判断下列说法是否正确)
1.酶是由活细胞产生的,一般在细胞内、外均具有催化作用。 ( )
2.酶分子在催化反应完成后立即被降解成氨基酸或核糖核苷酸。 ( )
3.萨姆纳从刀豆种子提取液中分离出的脲酶是蛋白质。 ( )
4.具有生物催化功能的RNA称为核酶,具有生物催化功能的蛋白质称为
蛋白酶。 ( )
5.酶能为化学反应提供能量。 ( )
6.温度过高或过低都会破坏酶的空间结构,而使酶失去活性。 ( )
答案
1.√
2. 在反应前后,酶的数量和性质都不变。
3.√
4. 蛋白酶是催化蛋白质水解的酶,而绝大多数酶都为蛋白质,因此蛋白质类的酶不能称为蛋白酶。
5. 酶能降低化学反应的活化能,但不能为化学反应提供能量。
6. 温度过低会抑制酶的活性,但不会破坏酶的空间结构。
考点二 ATP
一、ATP的结构与功能
1.ATP的全称: 腺苷三磷酸 。
2.
知识归纳
(1)利用关系图理解腺苷、AMP、ADP、ATP之间的关系
注意:AMP即腺嘌呤核糖核苷酸,为RNA的基本组成单位之一。
(2)辨析不同“A”的含义
上述结构中所圈的A的含义:①腺苷 ②腺嘌呤 ③腺嘌呤脱氧核苷酸
④腺嘌呤核糖核苷酸
(3)ATP在酶的作用下水解使脱离下来的末端磷酸基团挟能量与其他分
子结合,从而使后者发生变化。1 mol ATP水解释放的能量高达30.54 kJ,
故ATP是一种高能磷酸化合物。
3.ATP的功能:细胞生命活动的直接能源物质。
注意:ATP是提供能量的物质,不是能量。
二、ATP和ADP的相互转化
1.过程
易混易错
(1)ATP与ADP的相互转化不是可逆反应,因为转化过程中所需的酶及反
应场所等不完全相同。
(2)吸能反应如蛋白质的合成吸收能量,放能反应如葡萄糖的氧化分解释
放能量。ATP的合成伴随着放能反应(即放能反应释放的能量可用于
ATP的合成),ATP的水解伴随着吸能反应(即吸能反应所需的能量可来自
ATP水解释放的能量)。
(3)ATP与ADP相互转化时,物质(如Pi)可重复利用,能量不可重复利用。
2.特点:ATP在细胞内含量很少,代谢旺盛的细胞内ATP含量也不会明显
增加,但ATP与ADP之间的转化速度会明显加快,以满足细胞对能量的需
求。
知识拓展
ATP的产生量与O2供给量的关系
甲图 乙图
(1)甲图中A点表示细胞通过无氧呼吸产生少量ATP。
(2)甲图中AB段表示随O2供给量增多,有氧呼吸加强,ATP的产生量随之增加。
(3)甲图中BC段限制因素可能是酶、ADP、Pi等的量。
(4)乙图中ATP产生量与O2供给量无关,可发生在哺乳动物成熟红细胞中。
三、ATP的利用
1.ATP:绝大多数生命活动的直接能源物质
疑难突破
思考 细胞中除ATP外,还有其他高能磷酸化合物,如CTP、GTP、
UTP、dATP、dTTP、dCTP、dGTP等,也可以为细胞的生命活动提供能
量。结合图分析,说说它们与ATP在结构组成上有什么不同
提示 ①分析图可发现,GTP与ATP中含有的碱基不同,它们分别是鸟嘌
呤和腺嘌呤,其他结构都相同。②dATP与ATP中含有的五碳糖不同,它们
分别是脱氧核糖和核糖,其他结构都相同。③综合分析,CTP、GTP、
UTP与ATP在结构组成上仅碱基不同;dTTP、dCTP、dGTP与ATP在结构
组成上不仅碱基不同,而且五碳糖也不同。
2.ATP与分子磷酸化
1)含义:ATP水解释放的磷酸基团使蛋白质等分子磷酸化。
2)意义:蛋白质分子被磷酸化后,空间结构发生变化,活性也被改变,因而可
以参与各种化学反应。
3)实例:Ca2+经主动运输转运到细胞外的过程。
Ca2+与载体蛋白结合,ATP水解酶被激活→ATP末端磷酸基团转移到载体
蛋白上→载体蛋白空间结构发生变化,使Ca2+的结合位点转向膜外侧,将
Ca2+释放到膜外。
考点训练(请判断下列说法是否正确)
1.组成ATP、RNA、DNA的元素相同,且都含有腺苷。 ( )
2.细胞质基质、线粒体、叶绿体都是合成ATP的场所。 ( )
3.细胞中所有需能部位都有ATP的水解。 ( )
4.ATP是驱动生命活动的直接能源物质,但它在细胞中含量很少。 ( )
5.人体内淀粉水解成葡萄糖时,伴随有ATP的生成。 ( )
6.运动时,细胞内ATP含量会大大增加。( )
答案
1. 腺苷由腺嘌呤和核糖组成,而DNA中不含核糖。
2.√
3. 细胞中并非所有需能部位都利用ATP释放的能量,也可能利用其他高能磷酸化合物,如GTP、CTP等。
4.√
5. 淀粉的水解在消化道内进行,该过程会释放能量,但消化道内不存在ATP合成酶,无法生成ATP。
6. 运动时,细胞内ATP与ADP的转化速度会加快,但ATP含量保持相对
稳定。
综合篇
提升 酶的特性相关实验设计
1.探究酶的高效性
1)实验变量:自变量——催化剂种类(酶和无机催化剂);因变量——酶促
反应速率。
2)实验思路
对照组:反应物+无机催化剂→反应速率慢;
实验组:反应物+等量酶溶液→反应速率快。
3)示例:与FeCl3溶液相比,过氧化氢酶催化H2O2分解产生O2的效率高。
2.探究酶的专一性
1)设计思路一:不同底物相同酶(换底物不换酶)
①实验变量:自变量——不同底物;因变量——底物是否被分解。
②实验思路
实验组:底物甲+酶A溶液→底物甲被分解;
对照组:底物乙+酶A溶液→底物乙未分解。
③示例
2)设计思路二:相同底物不同酶(换酶不换底物)
①实验变量:自变量——不同酶(酶的种类);因变量——底物是否被分
解。
②实验思路
实验组:底物甲+酶A溶液→底物甲被分解;
对照组:底物甲+酶B溶液→底物甲未分解。
③示例
3.探究温度或pH对酶活性的影响实验
1)探究温度对酶活性的影响(以淀粉酶为例)
2)探究酶的最适温度(也可探究温度对酶活性的影响)
易混易错
反应物与酶液应在相应温度下分别保存后再混合,不能先混合再在相应
温度下保存,原因是反应物与酶液混合后可能会立刻发生反应,影响实验
的观察或检测。
3)探究pH对酶活性的影响(以H2O2酶为例)
4)探究酶的最适pH(也可探究pH对酶活性的影响)
易混易错
酶活性实验探究中的“五不宜”
(1)试剂的选择
①研究温度对酶活性影响的实验时,鉴定淀粉是否分解用碘液,不宜选用
斐林试剂,因为斐林试剂需水浴加热,而该实验中需严格控制温度。②若
反应物与生成物均能与试剂发生反应,如麦芽糖及其水解后形成的葡萄
糖均能与斐林试剂反应,再如蛋白质及其水解后形成的多肽均能与双缩
脲试剂反应,此类试剂不宜选用。③若反应物与生成物均不能与试剂反
应,如蔗糖及其水解后的单糖均不能与碘液反应,此类试剂也不宜选用。
(2)反应物和酶的选择
①研究酶的适宜温度实验时,不宜选用H2O2酶催化H2O2的分解,因为H2O2在加热的条件下会分解。②研究酶的适宜pH实验时,由于酸对淀粉有分解作用,因此不宜选用淀粉和淀粉酶作为实验材料,常选用H2O2和H2O2酶。
应用篇
应用 自变量、因变量的判断及二者关系的探究
解题思路
确定自变量 人为控制的对实验对象进行处理的因素为自变量。其判断
可依据如下方式:
1)可依据实验目的判断,如“探究温度对酶活性的影响”,需要人为控制
温度来探究对酶活性的影响,则温度是自变量。
2)可依据对照实验中的单一变量原则判断,如“在室温条件下,分别向装
有2 mL相同浓度的H2O2溶液试管中分别加入2滴H2O2酶溶液和FeCl3溶液,
观察气泡产生速率”,则温度、H2O2溶液量、催化剂滴数都相同(为无关
变量,一般需保持相同且适宜),催化剂种类不同,故自变量为催化剂种类。
3)可依据坐标图判断,通常横坐标可代表自变量(横坐标为时间时,一般不
为自变量,需从图中其他信息中来寻找)。
确定因变量 因自变量改变而变化的变量为因变量,如“H2O2酶和FeCl3
催化H2O2分解实验”中,随催化剂种类(自变量)改变而变化的H2O2分解速
率(或氧气产生速率)为因变量。因变量可以直接或间接观察、检测。通
常,纵坐标可代表因变量。
分析自变量与因变量的关系 自变量是“因”,因变量是“果”,二者有
因果关系。
答题模式
通过自变量变化推测因变量变化(实验结果);也可通过因变量的变化
逆推自变量变化。
例题讲解
例 已知酶X能催化二糖A(非还原糖)水解为单糖,请回答下列问题。
该图是在最适温度和pH下,探究二糖A的水解条件得出的结果。该实验
中,自变量为 ,根据图示结果可以得出的实验结论是酶X的
催化作用具有 。
解题思路
确定自变量 根据坐标图分析可知,实验中人为加入不同的催化剂来探
究单糖生成速率,则催化剂的种类为自变量。反应的时间也会对实验结
果造成影响,其为无关变量。
确定因变量 图中纵坐标可代表因变量,即随催化剂的种类改变而变化
的单糖生成量为因变量。
分析自变量与因变量的关系 一定时间范围内,加酶组单糖生成量比加无
机催化剂组高,说明酶具有高效性。
答案 催化剂种类 高效性
专题四 酶与ATP
高考生物总复习知识讲解
基础篇
考点一 酶
一、酶的概念剖析与作用机理
1.酶的概念剖析与拓展
化学本质 绝大多数是 蛋白质 少数是RNA
合成原料 氨基酸 核糖核苷酸
合成场所 核糖体 主要是细胞核
来源 一般来说,活细胞都能产生酶 生理功能 具有 催化 作用
2.酶的作用机理
1)作用实质: 降低化学反应的活化能 。
2)图解机理
①无催化剂的反应所需要的活化能是 a-c ;
②有酶催化的反应所需要的活化能是 b-c ;
③酶降低的活化能是 a-b 。
二、酶的特性
1.酶具有高效性
1)原因:与无机催化剂相比,酶降低活化能的作用更显著。
2)特点:酶能缩短达到化学平衡点的时间,但不改变平衡点,因而酶不会改
变最终 生成物 的量。且反应前后酶的数量和性质不变。
易混易错
(1)加酶与不加催化剂相比,体现了酶具有催化作用。(2)加酶与加无机催
化剂相比,体现了酶具有高效性。
2.酶具有专一性
1)含义:每一种酶只能催化一种或一类化学反应。
2)图中显示,酶A能催化反应物发生化学反应,而酶
B不能,说明酶A具有 专一性 。
3)除上述情况外,像DNA连接酶、RNA聚合酶等酶类分别可催化一类化
学反应。
知识归纳
诱导契合学说
酶A与底物B结合,形成酶—底物复合物(如图中乙),然后这个复合物
会发生一定的形状变化,使底物B变成生成物C、D,并从复合物上脱落;同
时酶分子恢复原状,又可以重新与底物结合,继续下一轮的反应。
3.酶的作用条件较温和
1)特点:在最适宜的温度和pH条件下,酶的活性最高。
2)酶活性
①实质:酶催化特定化学反应的能力。
②表示方法:酶促反应速率(可用单位时间内产物的生成量或反应物的消
耗量表示)。
三、影响酶促反应速率的因素
1.温度和pH
1)分析酶促反应速率随温度或pH变化曲线
①在最适温度,即t2(或最适pH,即pH2)时,酶活性最强,降低的活化能最大,
化学反应所需的活化能最低。
②低于最适温度(或最适pH)条件下,随温度(或pH)升高,酶促反应速率增大。
③超过最适温度(或最适pH)时,酶促反应速率逐渐降低。
④温度过高(t3)或pH过低(pH1)、过高(pH3)时,酶促反应速率为0,其原因是
高温、强酸、强碱条件破坏了酶的空间结构而使酶失去活性。
易混易错
(1)低温条件下(t1时),酶的活性低的原因不是低温破坏了酶的空间结构,而
是低温抑制了酶的活性,当温度由t1上升到t2时,酶的活性可以恢复为最高
活性,因此酶需在低温(pH最适)条件下保存。
(2)即使将导致酶失去活性的条件恢复至最适条件(如温度由t3降低至t2),
酶活性也不能恢复。
2)分析温度和pH共同影响下,酶促反应速率的相关变化曲线
①酶活性越强,酶促反应速率越高,一定时间内反应物剩余量越少。
②不同pH或不同温度下,最适温度或最适pH保持不变,即pH或温度的变
化不影响酶作用的最适温度或最适pH。
2.底物浓度和酶浓度
1)图甲中OB段酶促反应速率的限制因素是底物浓度,B点之后的限制因
素可能为酶浓度或温度或pH(温度和pH影响酶活性)等。
疑难突破
分析图甲,自变量是底物浓度,因变量是酶促反应速率。①在A点时,增加
底物浓度,酶促反应速率会升高。②在B点时,增加底物浓度,酶促反应速
率不变。③在B点及其之后增加酶浓度,酶促反应速率会加快。④在B点
时,升高温度,可能使酶活性升高(原温度低于最适温度时)或降低(原温度
为最适温度或高于最适温度时)。
2)图乙表示在底物充足时,酶促反应速率与酶浓度成正比。
注意:底物浓度和酶浓度不影响酶活性,其通过影响酶与底物的接触影响
酶促反应速率。
知识拓展
抑制剂
酶的抑制剂有竞争性抑制剂和非竞争性抑制剂
竞争性抑制剂与底物具有类似的结构,能与底物竞争酶的活性部位,当抑
制剂结合到酶活性部位后,底物被排斥在酶活性部位以外,导致酶促反应
被抑制;非竞争性抑制剂与底物结构不同,与酶结合的位点也不同,非竞争
性抑制剂与酶结合后,可引起酶构象改变并导致酶无法与底物结合,或者
虽然可以与底物结合但是无法得到产物等,这些都会导致酶活性降低或
丧失,如图。
竞争性抑制剂抑制酶与底物的结合,若增加底物浓度,抑制剂与酶活
性部位结合的概率变小,抑制程度减小。
考点训练(请判断下列说法是否正确)
1.酶是由活细胞产生的,一般在细胞内、外均具有催化作用。 ( )
2.酶分子在催化反应完成后立即被降解成氨基酸或核糖核苷酸。 ( )
3.萨姆纳从刀豆种子提取液中分离出的脲酶是蛋白质。 ( )
4.具有生物催化功能的RNA称为核酶,具有生物催化功能的蛋白质称为
蛋白酶。 ( )
5.酶能为化学反应提供能量。 ( )
6.温度过高或过低都会破坏酶的空间结构,而使酶失去活性。 ( )
答案
1.√
2. 在反应前后,酶的数量和性质都不变。
3.√
4. 蛋白酶是催化蛋白质水解的酶,而绝大多数酶都为蛋白质,因此蛋白质类的酶不能称为蛋白酶。
5. 酶能降低化学反应的活化能,但不能为化学反应提供能量。
6. 温度过低会抑制酶的活性,但不会破坏酶的空间结构。
考点二 ATP
一、ATP的结构与功能
1.ATP的全称: 腺苷三磷酸 。
2.
知识归纳
(1)利用关系图理解腺苷、AMP、ADP、ATP之间的关系
注意:AMP即腺嘌呤核糖核苷酸,为RNA的基本组成单位之一。
(2)辨析不同“A”的含义
上述结构中所圈的A的含义:①腺苷 ②腺嘌呤 ③腺嘌呤脱氧核苷酸
④腺嘌呤核糖核苷酸
(3)ATP在酶的作用下水解使脱离下来的末端磷酸基团挟能量与其他分
子结合,从而使后者发生变化。1 mol ATP水解释放的能量高达30.54 kJ,
故ATP是一种高能磷酸化合物。
3.ATP的功能:细胞生命活动的直接能源物质。
注意:ATP是提供能量的物质,不是能量。
二、ATP和ADP的相互转化
1.过程
易混易错
(1)ATP与ADP的相互转化不是可逆反应,因为转化过程中所需的酶及反
应场所等不完全相同。
(2)吸能反应如蛋白质的合成吸收能量,放能反应如葡萄糖的氧化分解释
放能量。ATP的合成伴随着放能反应(即放能反应释放的能量可用于
ATP的合成),ATP的水解伴随着吸能反应(即吸能反应所需的能量可来自
ATP水解释放的能量)。
(3)ATP与ADP相互转化时,物质(如Pi)可重复利用,能量不可重复利用。
2.特点:ATP在细胞内含量很少,代谢旺盛的细胞内ATP含量也不会明显
增加,但ATP与ADP之间的转化速度会明显加快,以满足细胞对能量的需
求。
知识拓展
ATP的产生量与O2供给量的关系
甲图 乙图
(1)甲图中A点表示细胞通过无氧呼吸产生少量ATP。
(2)甲图中AB段表示随O2供给量增多,有氧呼吸加强,ATP的产生量随之增加。
(3)甲图中BC段限制因素可能是酶、ADP、Pi等的量。
(4)乙图中ATP产生量与O2供给量无关,可发生在哺乳动物成熟红细胞中。
三、ATP的利用
1.ATP:绝大多数生命活动的直接能源物质
疑难突破
思考 细胞中除ATP外,还有其他高能磷酸化合物,如CTP、GTP、
UTP、dATP、dTTP、dCTP、dGTP等,也可以为细胞的生命活动提供能
量。结合图分析,说说它们与ATP在结构组成上有什么不同
提示 ①分析图可发现,GTP与ATP中含有的碱基不同,它们分别是鸟嘌
呤和腺嘌呤,其他结构都相同。②dATP与ATP中含有的五碳糖不同,它们
分别是脱氧核糖和核糖,其他结构都相同。③综合分析,CTP、GTP、
UTP与ATP在结构组成上仅碱基不同;dTTP、dCTP、dGTP与ATP在结构
组成上不仅碱基不同,而且五碳糖也不同。
2.ATP与分子磷酸化
1)含义:ATP水解释放的磷酸基团使蛋白质等分子磷酸化。
2)意义:蛋白质分子被磷酸化后,空间结构发生变化,活性也被改变,因而可
以参与各种化学反应。
3)实例:Ca2+经主动运输转运到细胞外的过程。
Ca2+与载体蛋白结合,ATP水解酶被激活→ATP末端磷酸基团转移到载体
蛋白上→载体蛋白空间结构发生变化,使Ca2+的结合位点转向膜外侧,将
Ca2+释放到膜外。
考点训练(请判断下列说法是否正确)
1.组成ATP、RNA、DNA的元素相同,且都含有腺苷。 ( )
2.细胞质基质、线粒体、叶绿体都是合成ATP的场所。 ( )
3.细胞中所有需能部位都有ATP的水解。 ( )
4.ATP是驱动生命活动的直接能源物质,但它在细胞中含量很少。 ( )
5.人体内淀粉水解成葡萄糖时,伴随有ATP的生成。 ( )
6.运动时,细胞内ATP含量会大大增加。( )
答案
1. 腺苷由腺嘌呤和核糖组成,而DNA中不含核糖。
2.√
3. 细胞中并非所有需能部位都利用ATP释放的能量,也可能利用其他高能磷酸化合物,如GTP、CTP等。
4.√
5. 淀粉的水解在消化道内进行,该过程会释放能量,但消化道内不存在ATP合成酶,无法生成ATP。
6. 运动时,细胞内ATP与ADP的转化速度会加快,但ATP含量保持相对
稳定。
综合篇
提升 酶的特性相关实验设计
1.探究酶的高效性
1)实验变量:自变量——催化剂种类(酶和无机催化剂);因变量——酶促
反应速率。
2)实验思路
对照组:反应物+无机催化剂→反应速率慢;
实验组:反应物+等量酶溶液→反应速率快。
3)示例:与FeCl3溶液相比,过氧化氢酶催化H2O2分解产生O2的效率高。
2.探究酶的专一性
1)设计思路一:不同底物相同酶(换底物不换酶)
①实验变量:自变量——不同底物;因变量——底物是否被分解。
②实验思路
实验组:底物甲+酶A溶液→底物甲被分解;
对照组:底物乙+酶A溶液→底物乙未分解。
③示例
2)设计思路二:相同底物不同酶(换酶不换底物)
①实验变量:自变量——不同酶(酶的种类);因变量——底物是否被分
解。
②实验思路
实验组:底物甲+酶A溶液→底物甲被分解;
对照组:底物甲+酶B溶液→底物甲未分解。
③示例
3.探究温度或pH对酶活性的影响实验
1)探究温度对酶活性的影响(以淀粉酶为例)
2)探究酶的最适温度(也可探究温度对酶活性的影响)
易混易错
反应物与酶液应在相应温度下分别保存后再混合,不能先混合再在相应
温度下保存,原因是反应物与酶液混合后可能会立刻发生反应,影响实验
的观察或检测。
3)探究pH对酶活性的影响(以H2O2酶为例)
4)探究酶的最适pH(也可探究pH对酶活性的影响)
易混易错
酶活性实验探究中的“五不宜”
(1)试剂的选择
①研究温度对酶活性影响的实验时,鉴定淀粉是否分解用碘液,不宜选用
斐林试剂,因为斐林试剂需水浴加热,而该实验中需严格控制温度。②若
反应物与生成物均能与试剂发生反应,如麦芽糖及其水解后形成的葡萄
糖均能与斐林试剂反应,再如蛋白质及其水解后形成的多肽均能与双缩
脲试剂反应,此类试剂不宜选用。③若反应物与生成物均不能与试剂反
应,如蔗糖及其水解后的单糖均不能与碘液反应,此类试剂也不宜选用。
(2)反应物和酶的选择
①研究酶的适宜温度实验时,不宜选用H2O2酶催化H2O2的分解,因为H2O2在加热的条件下会分解。②研究酶的适宜pH实验时,由于酸对淀粉有分解作用,因此不宜选用淀粉和淀粉酶作为实验材料,常选用H2O2和H2O2酶。
应用篇
应用 自变量、因变量的判断及二者关系的探究
解题思路
确定自变量 人为控制的对实验对象进行处理的因素为自变量。其判断
可依据如下方式:
1)可依据实验目的判断,如“探究温度对酶活性的影响”,需要人为控制
温度来探究对酶活性的影响,则温度是自变量。
2)可依据对照实验中的单一变量原则判断,如“在室温条件下,分别向装
有2 mL相同浓度的H2O2溶液试管中分别加入2滴H2O2酶溶液和FeCl3溶液,
观察气泡产生速率”,则温度、H2O2溶液量、催化剂滴数都相同(为无关
变量,一般需保持相同且适宜),催化剂种类不同,故自变量为催化剂种类。
3)可依据坐标图判断,通常横坐标可代表自变量(横坐标为时间时,一般不
为自变量,需从图中其他信息中来寻找)。
确定因变量 因自变量改变而变化的变量为因变量,如“H2O2酶和FeCl3
催化H2O2分解实验”中,随催化剂种类(自变量)改变而变化的H2O2分解速
率(或氧气产生速率)为因变量。因变量可以直接或间接观察、检测。通
常,纵坐标可代表因变量。
分析自变量与因变量的关系 自变量是“因”,因变量是“果”,二者有
因果关系。
答题模式
通过自变量变化推测因变量变化(实验结果);也可通过因变量的变化
逆推自变量变化。
例题讲解
例 已知酶X能催化二糖A(非还原糖)水解为单糖,请回答下列问题。
该图是在最适温度和pH下,探究二糖A的水解条件得出的结果。该实验
中,自变量为 ,根据图示结果可以得出的实验结论是酶X的
催化作用具有 。
解题思路
确定自变量 根据坐标图分析可知,实验中人为加入不同的催化剂来探
究单糖生成速率,则催化剂的种类为自变量。反应的时间也会对实验结
果造成影响,其为无关变量。
确定因变量 图中纵坐标可代表因变量,即随催化剂的种类改变而变化
的单糖生成量为因变量。
分析自变量与因变量的关系 一定时间范围内,加酶组单糖生成量比加无
机催化剂组高,说明酶具有高效性。
答案 催化剂种类 高效性
同课章节目录
