1.2.1 研究物质性质的基本方法 课件(共26张PPT) 2023-2024学年高一化学鲁科版(2029)必修第一册
文档属性
| 名称 | 1.2.1 研究物质性质的基本方法 课件(共26张PPT) 2023-2024学年高一化学鲁科版(2029)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 275.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-21 00:00:00 | ||
图片预览








文档简介
(共26张PPT)
第1章 认识化学科学
第2节 研究物质性质的方法和程序
第1课时 研究物质性质的基本方法
研究物质的性质是化学研究的一项重要内容。只有深入地研究物质的性质,才能更好地利用物质。例如,通过对叠氮化钠 (NaN3) 性质的研究,制成了一种用于汽车安全气囊的气体发生剂;通过对液态氢和液态氧性质的研究,制成了一种火箭推进剂……那么,怎样才能科学地研究物质的性质呢
已膨起的汽车安全气囊
一、研究物质性质的基本方法
研究物质的性质,常常运用观察、实验、分类、比较等方法。
观察是一种有计划、有目的地运用感官考察研究对象的方法。人们既可以直接用肉眼观察物质的颜色、状态以及用鼻子闻物质的气味等,也可以借助一些仪器来进行更为细致的观察。需要注意的是,在观察过程中,不仅要用感官去搜集信息,还要积极地动脑思考并及时储存和处理所搜集的信息;观察要有明确而具体的目的,要对观察到的现象进行分析和综合。
1.观察法
(1)含义:观察是一种有 、有 地运用感官考察研究对象的方法。
2.实验法
(1)含义:通过实验来验证对物质性质的 或探究物质未知的性质的方法。
(2)注意的问题:在进行实验时,要注意控制 、 、溶液的浓度等条件。
计划
目的
压强
预测
温度
运用观察法时的注意事项
①不能用手直接接触化学药品。
②严禁品尝化学药品的味道。
③闻气体气味时要用“扇闻法”。
3.分类法
在研究物质性质时,可以运用分类的方法总结各类物质的 ,并根据物质所属的类别对物质及其变化进行 。
4.比较法
运用比较的方法,认识各种物质性质之间的异同与内在联系。
一般性质
预测
观察·思考
观察金属钠及金属钠与水反应的现象
观察目的
1.认识金属钠的颜色、状态、硬度和密度的相对大小以及熔点的相对高低。
2.认识金属钠与水的反应。
观察内容
1.观察盛放在试剂瓶中的金属钠。用镊子将金属钠从试剂瓶中取出,用滤纸将其表面的煤油吸干,在玻璃片上用小刀切下一小块金属钠,观察钠块的切面。
2.向培养皿中加入适量的水,滴入 1~2 滴酚酞溶液,取一块绿豆粒大小的金属钠放入水中,观察现象。
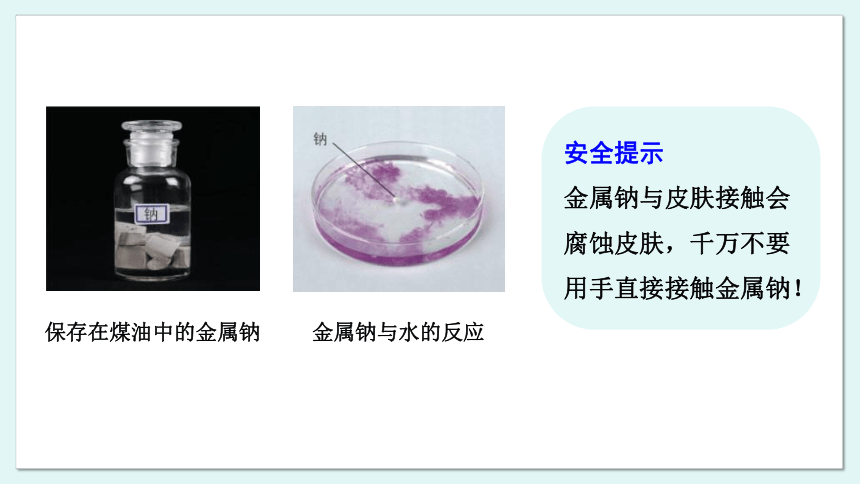
保存在煤油中的金属钠
金属钠与水的反应
安全提示
金属钠与皮肤接触会腐蚀皮肤,千万不要用手直接接触金属钠!
状态 颜色 光泽 硬度 密度 熔点
有金属光泽 ,可切割 比水的 ,比 的大 熔点较
。
观察记录:
固体
银白色
小
小
煤油
低
金属钠的物理性质
实验步骤 实验现象 现象分析
钠浮在水面上 钠的密度比水 。
钠熔化成闪亮的小球 钠的熔点 ,反应 。
小球在水面上四处游动,最后完全消失 反应产生的 推动小球运动
与水反应发出嘶嘶响声 钠与水反应产生 。
反应后溶液变为红色 反应生成 物质
小
低
放出热量
气体
气体
碱性
钠是一种银白色金属,通常保存在煤油或石蜡油中;熔点为97.8 ℃,沸点为 882.9℃;密度为0.97 g·cm-3。
金属钠能与水发生反应生成氢氧化钠和氢气。
2Na + 2H2O === 2NaOH + H2
金属钠的主要用途
金属钠可用于制造高压钠灯,这种灯因钠蒸气放电而产生的黄光射程远、透雾能力强,常用作路灯。金属钠还可用于钛、锆、铌、钽等金属的冶炼。钠和钾的合金可用作原子反应堆的导热剂。
实验是根据科学研究的目的,尽可能排除外界影响、突出主要因素,并利用一些专门的仪器设备,人为地变革、控制或模拟研究对象,使某一现象或过程发生或再现的研究方法。在研究物质性质的过程中,可通过实验来验证对物质性质的预测或探究物质未知的性质。
利用实验方法研究物质性质时,实验前要明确实验目的、实验用品和实验方案等;实验中要仔细观察实验现象,并做好实验记录;实验后要对实验结果进行分析,并写好实验报告。实验过程中,要注意控制温度、压强、溶液的浓度等条件,这是因为同样的反应物在不同的条件下可能会发生不同的反应。
活动·探究
金属钠与氧气的反应
实验目的
1.探究金属钠与氧气的反应
2.认识条件控制对于实验研究的意义。
实验用品
金属钠;
酒精灯,坩埚,三脚架,泥三角,坩埚钳,镊子,小刀,玻璃片,滤纸,火柴。
实验方案
1.将切好的金属钠放置在空气中,观察现象。
2.将一小块金属钠放入坩埚中加热,观察现象。
反应条件 空气 加热或点燃
实验步骤
实验现象 新切开的钠具有 色的金属光泽,在空气中很快变 。 钠先熔化成 ,然后剧烈燃烧,火焰呈 色,生成 色固体
化学方程式 缓慢氧化: 4Na+O2===2Na2O 剧烈燃烧:
2Na+O2===Na2O2
结论 钠是非常活泼的金属,与O2反应条件不同时,现象不同,产物也不同
银白
暗
小球
黄
淡黄
金属钠的切面在空气中的变化
在空气中加热金属钠所发生的变化
思考
1.通过这组实验,你对金属钠与氧气的反应有了哪些认识?
2.金属钠除了能与氧气、水发生反应外,还能与哪些物质发生反应 请比较金属钠与其他金属在化学性质上的相同点和不同点。
3.在研究金属钠性质的过程中,你用到了哪些研究方法
金属钠放置在空气中会迅速被氧化,失去金属光泽,生成白色的氧化钠 (Na2O);金属钠在空气中加热会生成过氧化钠 (Na2O2)。
4Na+O2===2Na2O
2Na+O2===Na2O2
过氧化钠
过氧化钠是一种淡黄色的固体粉末。它与水或二氧化碳反应皆可产生氧气,所发生的反应常用于呼吸面具和潜水艇里的氧气供给。
2Na2O2+ 2H2O === 4NaOH + O2
2Na2O2+ CO2 === 2Na2CO3 + O2
除了观察和实验外,分类和比较也是研究物质性质时的常用方法。在研究物质的性质时,可以运用分类的方法总结各类物质的一般性质,并根据物质所属的类别对物质及其变化进行预测;可以运用比较的方法,认识各种物质性质之间的异同与内在联系。
除了研究物质性质的基本方法外,在进行化学研究时还会用到假说和模型的方法。在已有事实和科学理论的基础上,科学工作者往往通过提出假说对有关现象或规律的本质以及未知物质或现象进行推测性说明,通过建构模型对物质或物质的变化进行简化模拟。假说和模型具有解释性功能和预见性功能,但是所做的预测或说明是否正确还需要通过实验来验证。在科学研究中,随着研究的深入,往往是旧的假说或模型被推翻而建立起新的假说或模型。
完成课后相关练习
谢谢观看
谢谢观看
第1章 认识化学科学
第2节 研究物质性质的方法和程序
第1课时 研究物质性质的基本方法
研究物质的性质是化学研究的一项重要内容。只有深入地研究物质的性质,才能更好地利用物质。例如,通过对叠氮化钠 (NaN3) 性质的研究,制成了一种用于汽车安全气囊的气体发生剂;通过对液态氢和液态氧性质的研究,制成了一种火箭推进剂……那么,怎样才能科学地研究物质的性质呢
已膨起的汽车安全气囊
一、研究物质性质的基本方法
研究物质的性质,常常运用观察、实验、分类、比较等方法。
观察是一种有计划、有目的地运用感官考察研究对象的方法。人们既可以直接用肉眼观察物质的颜色、状态以及用鼻子闻物质的气味等,也可以借助一些仪器来进行更为细致的观察。需要注意的是,在观察过程中,不仅要用感官去搜集信息,还要积极地动脑思考并及时储存和处理所搜集的信息;观察要有明确而具体的目的,要对观察到的现象进行分析和综合。
1.观察法
(1)含义:观察是一种有 、有 地运用感官考察研究对象的方法。
2.实验法
(1)含义:通过实验来验证对物质性质的 或探究物质未知的性质的方法。
(2)注意的问题:在进行实验时,要注意控制 、 、溶液的浓度等条件。
计划
目的
压强
预测
温度
运用观察法时的注意事项
①不能用手直接接触化学药品。
②严禁品尝化学药品的味道。
③闻气体气味时要用“扇闻法”。
3.分类法
在研究物质性质时,可以运用分类的方法总结各类物质的 ,并根据物质所属的类别对物质及其变化进行 。
4.比较法
运用比较的方法,认识各种物质性质之间的异同与内在联系。
一般性质
预测
观察·思考
观察金属钠及金属钠与水反应的现象
观察目的
1.认识金属钠的颜色、状态、硬度和密度的相对大小以及熔点的相对高低。
2.认识金属钠与水的反应。
观察内容
1.观察盛放在试剂瓶中的金属钠。用镊子将金属钠从试剂瓶中取出,用滤纸将其表面的煤油吸干,在玻璃片上用小刀切下一小块金属钠,观察钠块的切面。
2.向培养皿中加入适量的水,滴入 1~2 滴酚酞溶液,取一块绿豆粒大小的金属钠放入水中,观察现象。
保存在煤油中的金属钠
金属钠与水的反应
安全提示
金属钠与皮肤接触会腐蚀皮肤,千万不要用手直接接触金属钠!
状态 颜色 光泽 硬度 密度 熔点
有金属光泽 ,可切割 比水的 ,比 的大 熔点较
。
观察记录:
固体
银白色
小
小
煤油
低
金属钠的物理性质
实验步骤 实验现象 现象分析
钠浮在水面上 钠的密度比水 。
钠熔化成闪亮的小球 钠的熔点 ,反应 。
小球在水面上四处游动,最后完全消失 反应产生的 推动小球运动
与水反应发出嘶嘶响声 钠与水反应产生 。
反应后溶液变为红色 反应生成 物质
小
低
放出热量
气体
气体
碱性
钠是一种银白色金属,通常保存在煤油或石蜡油中;熔点为97.8 ℃,沸点为 882.9℃;密度为0.97 g·cm-3。
金属钠能与水发生反应生成氢氧化钠和氢气。
2Na + 2H2O === 2NaOH + H2
金属钠的主要用途
金属钠可用于制造高压钠灯,这种灯因钠蒸气放电而产生的黄光射程远、透雾能力强,常用作路灯。金属钠还可用于钛、锆、铌、钽等金属的冶炼。钠和钾的合金可用作原子反应堆的导热剂。
实验是根据科学研究的目的,尽可能排除外界影响、突出主要因素,并利用一些专门的仪器设备,人为地变革、控制或模拟研究对象,使某一现象或过程发生或再现的研究方法。在研究物质性质的过程中,可通过实验来验证对物质性质的预测或探究物质未知的性质。
利用实验方法研究物质性质时,实验前要明确实验目的、实验用品和实验方案等;实验中要仔细观察实验现象,并做好实验记录;实验后要对实验结果进行分析,并写好实验报告。实验过程中,要注意控制温度、压强、溶液的浓度等条件,这是因为同样的反应物在不同的条件下可能会发生不同的反应。
活动·探究
金属钠与氧气的反应
实验目的
1.探究金属钠与氧气的反应
2.认识条件控制对于实验研究的意义。
实验用品
金属钠;
酒精灯,坩埚,三脚架,泥三角,坩埚钳,镊子,小刀,玻璃片,滤纸,火柴。
实验方案
1.将切好的金属钠放置在空气中,观察现象。
2.将一小块金属钠放入坩埚中加热,观察现象。
反应条件 空气 加热或点燃
实验步骤
实验现象 新切开的钠具有 色的金属光泽,在空气中很快变 。 钠先熔化成 ,然后剧烈燃烧,火焰呈 色,生成 色固体
化学方程式 缓慢氧化: 4Na+O2===2Na2O 剧烈燃烧:
2Na+O2===Na2O2
结论 钠是非常活泼的金属,与O2反应条件不同时,现象不同,产物也不同
银白
暗
小球
黄
淡黄
金属钠的切面在空气中的变化
在空气中加热金属钠所发生的变化
思考
1.通过这组实验,你对金属钠与氧气的反应有了哪些认识?
2.金属钠除了能与氧气、水发生反应外,还能与哪些物质发生反应 请比较金属钠与其他金属在化学性质上的相同点和不同点。
3.在研究金属钠性质的过程中,你用到了哪些研究方法
金属钠放置在空气中会迅速被氧化,失去金属光泽,生成白色的氧化钠 (Na2O);金属钠在空气中加热会生成过氧化钠 (Na2O2)。
4Na+O2===2Na2O
2Na+O2===Na2O2
过氧化钠
过氧化钠是一种淡黄色的固体粉末。它与水或二氧化碳反应皆可产生氧气,所发生的反应常用于呼吸面具和潜水艇里的氧气供给。
2Na2O2+ 2H2O === 4NaOH + O2
2Na2O2+ CO2 === 2Na2CO3 + O2
除了观察和实验外,分类和比较也是研究物质性质时的常用方法。在研究物质的性质时,可以运用分类的方法总结各类物质的一般性质,并根据物质所属的类别对物质及其变化进行预测;可以运用比较的方法,认识各种物质性质之间的异同与内在联系。
除了研究物质性质的基本方法外,在进行化学研究时还会用到假说和模型的方法。在已有事实和科学理论的基础上,科学工作者往往通过提出假说对有关现象或规律的本质以及未知物质或现象进行推测性说明,通过建构模型对物质或物质的变化进行简化模拟。假说和模型具有解释性功能和预见性功能,但是所做的预测或说明是否正确还需要通过实验来验证。在科学研究中,随着研究的深入,往往是旧的假说或模型被推翻而建立起新的假说或模型。
完成课后相关练习
谢谢观看
谢谢观看
