1.2.1 物质的量 课件(共38张PPT) 2023-2024学年高一化学苏教版(2029)必修第一册
文档属性
| 名称 | 1.2.1 物质的量 课件(共38张PPT) 2023-2024学年高一化学苏教版(2029)必修第一册 |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-21 00:00:00 | ||
图片预览








文档简介
(共38张PPT)
必 修 一
学
化
J
S
第二单元 物质的化学计量
课时 1 2.1 物质的量
说一说
微粒数
物质质量
物质的量
化学方程式:C + O2 == CO2表示什么意义?
点燃
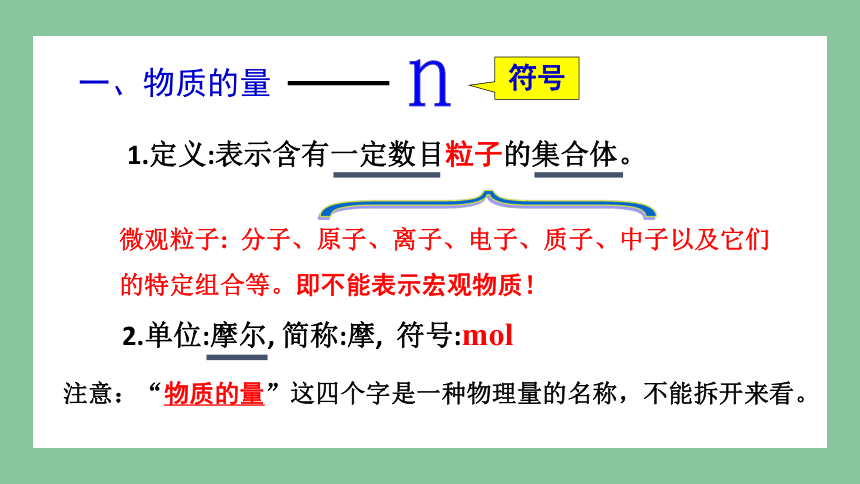
1.定义:表示含有一定数目粒子的集合体。
2.单位:摩尔, 简称:摩, 符号:mol
微观粒子: 分子、原子、离子、电子、质子、中子以及它们的特定组合等。即不能表示宏观物质!
符号
注意:“物质的量”这四个字是一种物理量的名称,不能拆开来看。
一、物质的量
下列叙述是否正确
1、摩尔是七个基本物理量之一
2、摩尔是物质的质量单位
3、摩尔是物质的数量单位
摩尔是物质的量的单位。
物质的量是七个基本物理量之一。
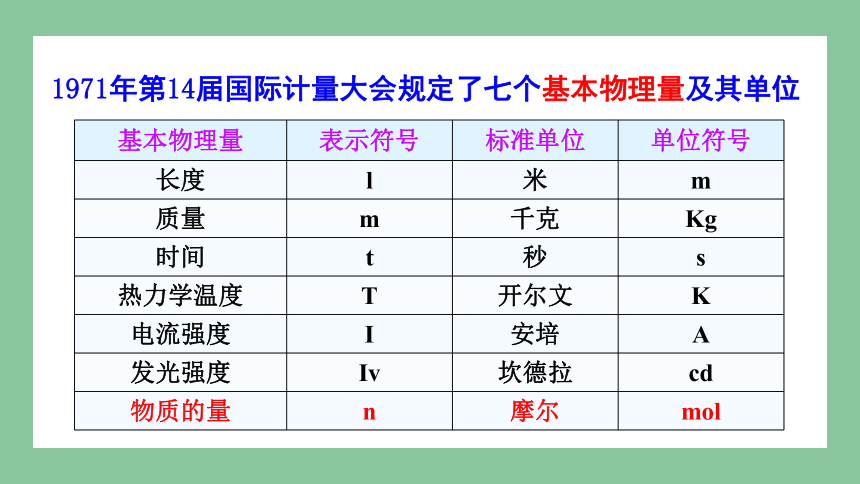
基本物理量 表示符号 标准单位 单位符号
长度 l 米 m
质量 m 千克 Kg
时间 t 秒 s
热力学温度 T 开尔文 K
电流强度 I 安培 A
发光强度 Iv 坎德拉 cd
物质的量 n 摩尔 mol
1971年第14届国际计量大会规定了七个基本物理量及其单位
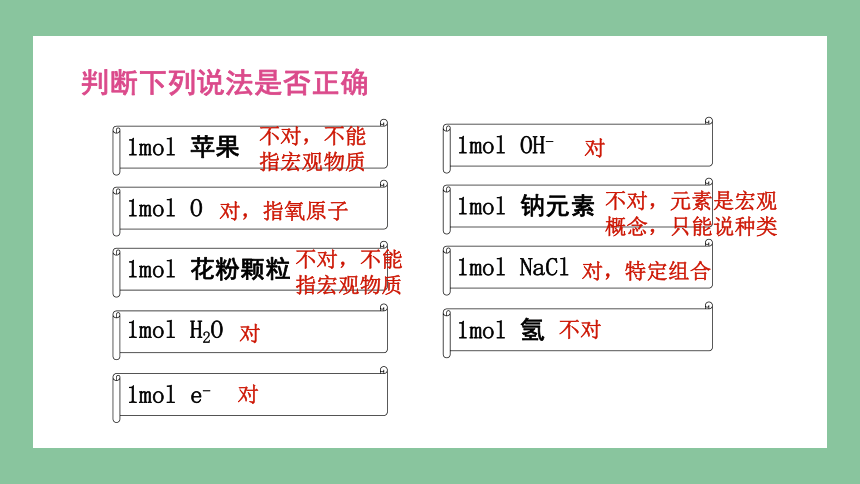
1mol 苹果
1mol O
1mol 花粉颗粒
判断下列说法是否正确
1mol H2O
1mol e-
1mol OH-
1mol 钠元素
1mol NaCl
不对,不能指宏观物质
对,指氧原子
不对,不能指宏观物质
对
对
对
不对,元素是宏观概念,只能说种类
对,特定组合
1mol 氢
不对
1、物质的量表示的是微观粒子的集合体,不表示宏观物质的数目
2、物质由不同的微粒构成,因此,我们在使用摩尔表示物质的量时,一般用化学式指明粒子的种类
3、粒子的种类可以是分子、原子、离子;也可以是质子、中子、电子等
使用物质的量和摩尔时的注意事项
1mol粒子
?个
一打鸡蛋12个
一副扑克54张
一令白纸500张
……
看一看课本
2、阿伏加德罗常数: 0.012Kg 12C中所含有的碳原子数,符号为NA,单位mol-1。约为 6.02×1023mol-1。
1、1 mol粒子的数目与 0.012 kg 12C中所含的碳原子数目相同。
3、1 mol任何微粒都含有阿伏加德罗常数个微粒,约为 6.02×1023个。
阿伏加德罗是意大利化学家。他在化学上的重大贡献是建立分子学说。为了纪念阿伏加德罗的伟大功绩,将 0.012kg 12C中所含的C原子数目称为阿伏加德罗常数,它是自然科学中的基本常数之一。
阿伏加德罗
Avogadro
1776~1856
因此我们可以这样说
1mol C中约含有 6.02×1023 个碳原子
1mol O2中约含有 6.02×1023 个氧分子
1mol H2O中约含有 6.02×1023 个H2O
1mol H+中约含有 6.02×1023 个H+
1mol 任何粒子集合体都约含有6.02×1023个这种粒子.
xmol 某种微粒集合体中所含微粒数为x×6.02×1023.
物质的量(n)、阿伏加德罗常数(NA)、粒子数(N)之间有何关系?
想一想关系
xmol 某种微粒集合体中所含微粒数为x×6.02×1023.
n
NA
N
阿伏加德罗常数
物质的量
微粒个数
(约6.02×1023mol-1)
N
=
NA
×
n
微粒
1摩尔: 阿伏加德罗常数
物质的量
个数(N)
1堆的量(NA)
堆数(n)
认识本质
化繁为简,易于表达
在0.5mol O2中含有的O2的分子数目是多少?
解:O2的分子数为
N = n(O2) × NA
= 0.5 mol × 6.02 ×1023mol -1
= 3.01 × 1023 个
答:O2的分子数为 3.01 × 1023 个。
例题1
在0.5mol O2中含有的O的原子数目是多少?
解:O2的O原子数为
N = n(O2) × NA × 2
= 0.5 mol × 6.02 ×1023mol -1 × 2
= 6.02 × 1023 个
答:O2的O原子为 6.02 × 1023 个。
例题2
例题3
在0.5mol O2中含有的电子数目是多少?
解:O2的电子数为
N = n(O2) × NA × 16
= 0.5 mol × 6.02 ×1023mol -1 × 16
= 4.816 × 1024 个
答:含有的电子数为 4.816 × 1024 个。
0.5mol H2中的氢分子数____________
1mol NaCl中的氯离子数____________
1mol H2SO4中的氧原子数____________
1.204X1024 个水分子的物质的量___________
9.03X1023 个铁原子的物质的量____________
6.02 ×1023
3.01 ×1023
2.408 ×1024
2 mol
1.5 mol
【问题解决】
物质的量 (n)
基准:NA
1、表示含有一定数目粒子的集合体
2、专有名词,不能随意拆开
3、对象为微观粒子
单位:摩尔(mol)
1、基本物理量的单位
2、量度对象:具体微观粒子及其特定组合
3、使用时用化学式指明粒子的种类
1、准确值:12g12C所含原子数
近似值: 6.02 1023
n=
NA
N
2、
基本物理量
课堂小结
1、下列数量的各物质中,含原子个数最多的是( )
A、1mol HCl B、3.01 x 1023 个碘分子
C、12g 12C D、0.5mol CH4
D
2、与 0.3mol H2O 含有相同氢原子数的是( )
A、0.3 mol HNO3 B、3.01 X 1023个 HNO3分子
C、0.2 mol H3PO4 D、0.1mol NH3
C
课堂练习
课后思考
微观粒子
一个C原子
一个O原子
一个Fe原子
宏观质量
扩大6.02 ×1023
1molC原子
12g
相对原子质量
12
1molO原子
16g
16
1molFe原子
56g
56
规律一:1mol任何原子的质量如果以克为单位,在数值上等于该原子的相对原子质量。
1 mol任何粒子的数目与 0.012 kg 12C中所含的碳原子数目相同。
1)1molNa的质量为 。
2molH的质量为 。
3molO的质量为 。
2)1molH2的质量为 。
1molH2O的质量为 。
2molH2SO4的质量为 。
1molMg2+的质量为 。
23g
2g
48g
24g
196g
18g
2g
【问题解决】
规律二:1mol任何分子的质量如果以克为单位,在数值上等于该分子的相对分子质量。
规律三:1mol任何离子的质量如果以克为单位,在数值上等于该离子的相对离子质量。
结论:1mol任何物质的质量,以克为单位,在数值上等于该物质的相对原子量或相对分子量。
符号
1.定义:单位物质的量的物质所具有的质量。
2.单位:克·摩-1或克/摩。符号: g·mol-1或 g/mol
3.数值:等于该物质的相对原子量或相对分子量。
二、摩尔质量
物质的量(n)、物质的质量(m)、物质的摩尔质量(M)之间有何关系?
想一想关系
物质的量(mol)=
物质的质量(g)
摩尔质量(g/mol)
1 mol C的质量为 12g,
2 mol C的质量为 24g,
3 mol C的质量为 36g,
......
1molCa2+的质量为 ,Ca2+的摩尔质量为 。Na2O2的摩尔质量为 。0.5molSO42-的质量为 。1molH2O的摩尔质量为 ,2molH2O的摩尔质量为 。0.5molO2约含有 个氧原子,质量为 ,O原子的摩尔质量为 。
40g
40g·mol-1
48g
78g·mol-1
18g·mol-1
18g·mol-1
6.02×1023
16g
16g·mol-1
注意:摩尔质量只与物质的种类有关,与物质的量、物质的质量无关
【问题解决】
483g Na2SO4·10H2O中所含的Na+和SO42-的物质的量各是多少?所含H2O分子的数目是多少?
解:Na2SO4·10H2O的相对分子质量为322,摩尔质量为322 g·mol-1。
则Na+的物质的量为3.00mol,SO42-的物质的量为1.50mol,H2O的物质的量为15.0mol。
例题1
答:483 g Na2SO4·10H2O中所含的Na+的物质的量为3.00 mol,SO42-的物质的量为1.50mol,H2O分子的数目约为9.03×1024。
2 1 2
4 32 36
知识拓展
2 1 2
物质的量在化学反应方程式中的应用
2 H2 + O2 == 2 H2O
化学计量数(系数): 2 1 2
粒子数(N/个):
质量(m/g):
物质的量(n/mol):
点燃
2 mol H2 和 1 mol O2 完全反应可以生成 2 mol H2O
例题2
1.氢氧化钠溶液与盐酸反应。
2.氧化铁在高温下与一氧化碳反应。
3.氯酸钾受热分解生成氧气和氯化钾。
4.过氧化氢分解生成氧气和水。
NaOH + HCl == NaCl + H2O
Fe2O3 + 3CO == 2Fe + 3CO2
高温
2KClO3 == 3O2↑ + 2KCl
▲
MnO2
2H2O2 == O2↑ + 2H2O
MnO2
1、下列说法正确的是( )
A、6.02 ×1023个12C原子的质量为 1g
B、H的摩尔质量为 1g
C、H2SO4的摩尔质量等于 6.02×1023 个H2SO4分子的质量
D、NaOH的摩尔质量为 40g·mol-1
D
课堂练习
2、1molH2含有 molH,含有 mole-, 个质子; 1molNa中约含 Na, mole-,含质子的物质的量为 。
2
1.204×1024
6.02×1023
11
11mol
2
3、2.5mol铜原子的质量是多少克
解: 铜的相对原子质量是 63.5,
铜的摩尔质量是 63.5 g/mol。
m(Cu)=63.5g/mol×2.5 mol=158.8g
答:2.5mol 铜原子的质量等于158.8g。
课后思考
看
观
谢
谢
必 修 一
学
化
J
S
第二单元 物质的化学计量
课时 1 2.1 物质的量
说一说
微粒数
物质质量
物质的量
化学方程式:C + O2 == CO2表示什么意义?
点燃
1.定义:表示含有一定数目粒子的集合体。
2.单位:摩尔, 简称:摩, 符号:mol
微观粒子: 分子、原子、离子、电子、质子、中子以及它们的特定组合等。即不能表示宏观物质!
符号
注意:“物质的量”这四个字是一种物理量的名称,不能拆开来看。
一、物质的量
下列叙述是否正确
1、摩尔是七个基本物理量之一
2、摩尔是物质的质量单位
3、摩尔是物质的数量单位
摩尔是物质的量的单位。
物质的量是七个基本物理量之一。
基本物理量 表示符号 标准单位 单位符号
长度 l 米 m
质量 m 千克 Kg
时间 t 秒 s
热力学温度 T 开尔文 K
电流强度 I 安培 A
发光强度 Iv 坎德拉 cd
物质的量 n 摩尔 mol
1971年第14届国际计量大会规定了七个基本物理量及其单位
1mol 苹果
1mol O
1mol 花粉颗粒
判断下列说法是否正确
1mol H2O
1mol e-
1mol OH-
1mol 钠元素
1mol NaCl
不对,不能指宏观物质
对,指氧原子
不对,不能指宏观物质
对
对
对
不对,元素是宏观概念,只能说种类
对,特定组合
1mol 氢
不对
1、物质的量表示的是微观粒子的集合体,不表示宏观物质的数目
2、物质由不同的微粒构成,因此,我们在使用摩尔表示物质的量时,一般用化学式指明粒子的种类
3、粒子的种类可以是分子、原子、离子;也可以是质子、中子、电子等
使用物质的量和摩尔时的注意事项
1mol粒子
?个
一打鸡蛋12个
一副扑克54张
一令白纸500张
……
看一看课本
2、阿伏加德罗常数: 0.012Kg 12C中所含有的碳原子数,符号为NA,单位mol-1。约为 6.02×1023mol-1。
1、1 mol粒子的数目与 0.012 kg 12C中所含的碳原子数目相同。
3、1 mol任何微粒都含有阿伏加德罗常数个微粒,约为 6.02×1023个。
阿伏加德罗是意大利化学家。他在化学上的重大贡献是建立分子学说。为了纪念阿伏加德罗的伟大功绩,将 0.012kg 12C中所含的C原子数目称为阿伏加德罗常数,它是自然科学中的基本常数之一。
阿伏加德罗
Avogadro
1776~1856
因此我们可以这样说
1mol C中约含有 6.02×1023 个碳原子
1mol O2中约含有 6.02×1023 个氧分子
1mol H2O中约含有 6.02×1023 个H2O
1mol H+中约含有 6.02×1023 个H+
1mol 任何粒子集合体都约含有6.02×1023个这种粒子.
xmol 某种微粒集合体中所含微粒数为x×6.02×1023.
物质的量(n)、阿伏加德罗常数(NA)、粒子数(N)之间有何关系?
想一想关系
xmol 某种微粒集合体中所含微粒数为x×6.02×1023.
n
NA
N
阿伏加德罗常数
物质的量
微粒个数
(约6.02×1023mol-1)
N
=
NA
×
n
微粒
1摩尔: 阿伏加德罗常数
物质的量
个数(N)
1堆的量(NA)
堆数(n)
认识本质
化繁为简,易于表达
在0.5mol O2中含有的O2的分子数目是多少?
解:O2的分子数为
N = n(O2) × NA
= 0.5 mol × 6.02 ×1023mol -1
= 3.01 × 1023 个
答:O2的分子数为 3.01 × 1023 个。
例题1
在0.5mol O2中含有的O的原子数目是多少?
解:O2的O原子数为
N = n(O2) × NA × 2
= 0.5 mol × 6.02 ×1023mol -1 × 2
= 6.02 × 1023 个
答:O2的O原子为 6.02 × 1023 个。
例题2
例题3
在0.5mol O2中含有的电子数目是多少?
解:O2的电子数为
N = n(O2) × NA × 16
= 0.5 mol × 6.02 ×1023mol -1 × 16
= 4.816 × 1024 个
答:含有的电子数为 4.816 × 1024 个。
0.5mol H2中的氢分子数____________
1mol NaCl中的氯离子数____________
1mol H2SO4中的氧原子数____________
1.204X1024 个水分子的物质的量___________
9.03X1023 个铁原子的物质的量____________
6.02 ×1023
3.01 ×1023
2.408 ×1024
2 mol
1.5 mol
【问题解决】
物质的量 (n)
基准:NA
1、表示含有一定数目粒子的集合体
2、专有名词,不能随意拆开
3、对象为微观粒子
单位:摩尔(mol)
1、基本物理量的单位
2、量度对象:具体微观粒子及其特定组合
3、使用时用化学式指明粒子的种类
1、准确值:12g12C所含原子数
近似值: 6.02 1023
n=
NA
N
2、
基本物理量
课堂小结
1、下列数量的各物质中,含原子个数最多的是( )
A、1mol HCl B、3.01 x 1023 个碘分子
C、12g 12C D、0.5mol CH4
D
2、与 0.3mol H2O 含有相同氢原子数的是( )
A、0.3 mol HNO3 B、3.01 X 1023个 HNO3分子
C、0.2 mol H3PO4 D、0.1mol NH3
C
课堂练习
课后思考
微观粒子
一个C原子
一个O原子
一个Fe原子
宏观质量
扩大6.02 ×1023
1molC原子
12g
相对原子质量
12
1molO原子
16g
16
1molFe原子
56g
56
规律一:1mol任何原子的质量如果以克为单位,在数值上等于该原子的相对原子质量。
1 mol任何粒子的数目与 0.012 kg 12C中所含的碳原子数目相同。
1)1molNa的质量为 。
2molH的质量为 。
3molO的质量为 。
2)1molH2的质量为 。
1molH2O的质量为 。
2molH2SO4的质量为 。
1molMg2+的质量为 。
23g
2g
48g
24g
196g
18g
2g
【问题解决】
规律二:1mol任何分子的质量如果以克为单位,在数值上等于该分子的相对分子质量。
规律三:1mol任何离子的质量如果以克为单位,在数值上等于该离子的相对离子质量。
结论:1mol任何物质的质量,以克为单位,在数值上等于该物质的相对原子量或相对分子量。
符号
1.定义:单位物质的量的物质所具有的质量。
2.单位:克·摩-1或克/摩。符号: g·mol-1或 g/mol
3.数值:等于该物质的相对原子量或相对分子量。
二、摩尔质量
物质的量(n)、物质的质量(m)、物质的摩尔质量(M)之间有何关系?
想一想关系
物质的量(mol)=
物质的质量(g)
摩尔质量(g/mol)
1 mol C的质量为 12g,
2 mol C的质量为 24g,
3 mol C的质量为 36g,
......
1molCa2+的质量为 ,Ca2+的摩尔质量为 。Na2O2的摩尔质量为 。0.5molSO42-的质量为 。1molH2O的摩尔质量为 ,2molH2O的摩尔质量为 。0.5molO2约含有 个氧原子,质量为 ,O原子的摩尔质量为 。
40g
40g·mol-1
48g
78g·mol-1
18g·mol-1
18g·mol-1
6.02×1023
16g
16g·mol-1
注意:摩尔质量只与物质的种类有关,与物质的量、物质的质量无关
【问题解决】
483g Na2SO4·10H2O中所含的Na+和SO42-的物质的量各是多少?所含H2O分子的数目是多少?
解:Na2SO4·10H2O的相对分子质量为322,摩尔质量为322 g·mol-1。
则Na+的物质的量为3.00mol,SO42-的物质的量为1.50mol,H2O的物质的量为15.0mol。
例题1
答:483 g Na2SO4·10H2O中所含的Na+的物质的量为3.00 mol,SO42-的物质的量为1.50mol,H2O分子的数目约为9.03×1024。
2 1 2
4 32 36
知识拓展
2 1 2
物质的量在化学反应方程式中的应用
2 H2 + O2 == 2 H2O
化学计量数(系数): 2 1 2
粒子数(N/个):
质量(m/g):
物质的量(n/mol):
点燃
2 mol H2 和 1 mol O2 完全反应可以生成 2 mol H2O
例题2
1.氢氧化钠溶液与盐酸反应。
2.氧化铁在高温下与一氧化碳反应。
3.氯酸钾受热分解生成氧气和氯化钾。
4.过氧化氢分解生成氧气和水。
NaOH + HCl == NaCl + H2O
Fe2O3 + 3CO == 2Fe + 3CO2
高温
2KClO3 == 3O2↑ + 2KCl
▲
MnO2
2H2O2 == O2↑ + 2H2O
MnO2
1、下列说法正确的是( )
A、6.02 ×1023个12C原子的质量为 1g
B、H的摩尔质量为 1g
C、H2SO4的摩尔质量等于 6.02×1023 个H2SO4分子的质量
D、NaOH的摩尔质量为 40g·mol-1
D
课堂练习
2、1molH2含有 molH,含有 mole-, 个质子; 1molNa中约含 Na, mole-,含质子的物质的量为 。
2
1.204×1024
6.02×1023
11
11mol
2
3、2.5mol铜原子的质量是多少克
解: 铜的相对原子质量是 63.5,
铜的摩尔质量是 63.5 g/mol。
m(Cu)=63.5g/mol×2.5 mol=158.8g
答:2.5mol 铜原子的质量等于158.8g。
课后思考
看
观
谢
谢
