3.3.1 溴和碘的提取 课件(共34张PPT) 2023-2024学年高一化学苏教版(2029)必修第一册
文档属性
| 名称 | 3.3.1 溴和碘的提取 课件(共34张PPT) 2023-2024学年高一化学苏教版(2029)必修第一册 |

|
|
| 格式 | ppt | ||
| 文件大小 | 3.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-21 00:00:00 | ||
图片预览











文档简介
(共34张PPT)
必 修 一
学
化
J
S
专题3 从海水中获得的化学物质
1935 年方志敏在狱中用米汤在白纸上写下密信,通过地下工作的同志送给鲁迅。
鲁迅先生接到密信后,用干净的碗盛上一碗清水,滴入少量碘酒,并将密信浸入碘水中,白纸上马上呈现出淡蓝色的字迹。
化学密信
碘遇淀粉变蓝——用于检验碘
海水中部分元素含量图
海洋中溴元素约为100万亿吨,碘元素约为800亿吨。溴0.00083mol/L;碘0.00000047mol/L。
海洋中含量较高的元素钠镁氯等,提取已经成为产业。
溴碘等元素在陆地含量极少,只能从海洋提取。
Brˉ
Brˉ
Brˉ
Iˉ
Iˉ
Iˉ
Br2
?
I2
?
问题思考
海洋中溴元素和碘元素都是以Br-、I-形式存在,该如何从海水中提取溴单质(Br2)和碘单质(I2)?
溴(Br2):深红棕色液体;密度比水大;易挥发;在水中溶解度很小;易溶于酒精、四氯化碳等有机溶剂;有极强烈的毒害性与腐蚀性。
溴的保存:密闭保存,常往盛溴的试剂瓶中加入一些水——水封
1、溴的物理性质
Br2是常温下唯一呈液态状的非金属单质
一、溴、碘的性质
溴蒸气
溴和溴水
液溴Br2
橙黄色
2、碘的物理性质
碘(I2):紫黑色固体;密度比水大;易升华;在水中溶解度很小;易溶于酒精、四氯化碳等有机溶剂。
特性:I2能使淀粉变蓝
碘(I2)单质
碘蒸气
碘水:黄色溶液
碘的有机溶液:紫红色溶液
『实验1』在一支试管中加入2ml-3ml KBr 溶液,滴加少量新制氯水
现象:
溶液的颜色逐渐加深,最后变成了橙黄色
二、溴、碘的提取原理
观察与思考
『实验1 』 再往原溶液滴加CCl4,振荡、静置
现象:
溶液分层,上层无色,下层橙红色
化学方程式:
Cl2 + 2KBr = Br2 + 2KCl
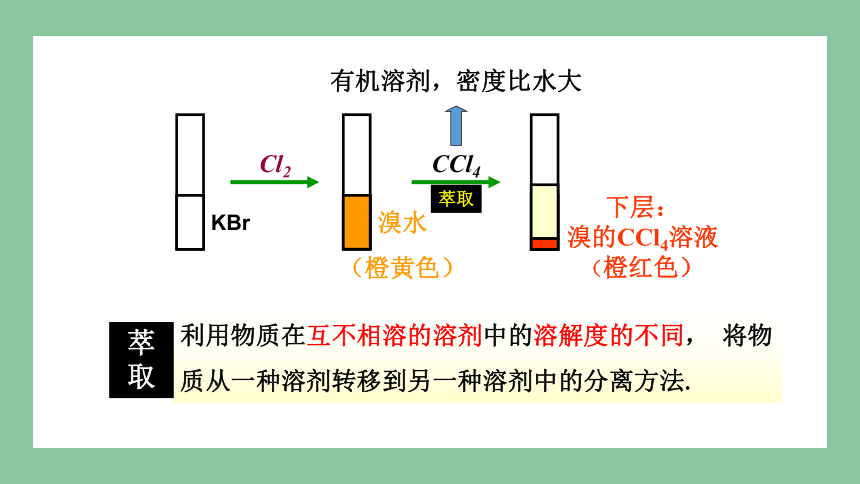
CCl4
Cl2
KBr
溴水
下层:
溴的CCl4溶液
(橙黄色)
(橙红色)
有机溶剂,密度比水大
萃取
利用物质在互不相溶的溶剂中的溶解度的不同, 将物质从一种溶剂转移到另一种溶剂中的分离方法.
萃取
『实验2』在一支试管中加入2mlKI溶液,滴加少量
新制氯水
现象:
溶液的颜色逐渐加深,最后变成了棕黄色
『实验2 』 再往原溶液滴加CCl4,振荡、静置
现象:
溶液分层,上层无色,下层紫红色
化学方程式:
Cl2 + 2KI = I2 + 2KCl
CCl4
Cl2
KI
碘水
下层:
碘的CCl4溶液
(棕黄色)
(紫红色)
萃取
实验体系 氯水+KBr溶液 氯水+KI溶液
现象
结论
无色→橙黄色.加入CCl4上层变浅,下层变橙红色
无色→棕黄色.加入CCl4上层变浅,下层变紫红色
氯可以置换出溴
氯可以置换出碘
溴、碘的提取实验
在不同溶剂中的颜色 物理特性
水 四氯化碳
溴Br2
碘I2
橙黄色
橙红色
棕黄色
紫红色
易挥发
易升华
溴、碘的溶解性及特性
溴、碘在水中溶解度很小,易溶于酒精、CCl4等有机溶剂
湿润的淀粉KI试纸遇到Cl2为什么会变蓝?用于检验Cl2
请写出化学反应方程式
Cl2 + 2KI = I2 + 2KCl
问题思考
三、溴、碘的提取流程
常见氧化剂 价格(万元/吨)
Cl2 0.155
O2 0.13
KMnO4 3.4
K2Cr2O7(重铬酸钾) 3.76
KClO3 2.7
H2O2 1.4
Na2O2(过氧化钠) 17
氧化剂选择
不能将Br-氧化
√
1.溴的提取
溴易挥发,鼓入热空气使其全部挥发出来,冷凝得到粗溴。
思考:为什么要鼓入热空气?
粗盐
母液
通入Cl2
Br2蒸汽跑出来
粗Br2
Br2水
海水
鼓入热空气
冷凝
提纯
液溴
知识拓展
方法1: SO2吸收富集, 氯气氧化;
SO2+Br2+2H2O=2HBr+H2SO4
2HBr+Cl2=2HCl+Br2
粗溴的提纯方法
方法2: Na2CO3溶液吸收富集, H2SO4酸化;
3Na2CO3+3Br2=NaBrO3+5NaBr+3CO2
NaBrO3+5NaBr+3H2SO4=3Br2+3Na2SO4+3H2O
碘的含量 海水 海带
浓度(mg/kg) 0.06 3000~5000
含碘元素丰富的海带
海藻森林
海带森林
2.碘的提取
①灼烧
②浸泡
含I-溶液
③过滤
含碘悬浊液
①升华
②凝华
干海带
粗碘
氯气
过滤
碘单质
滤渣
AgNO3溶液
KCl溶液
KI溶液
AgNO3溶液
NaBr溶液
AgNO3溶液
实验室常用硝酸银溶液和稀硝酸来检验
四、Cl-、Br-、I-的鉴别
实验现象和化学方程式
NaCl溶液
NaBr溶液
NaI溶液
生成不溶于稀硝酸的白色沉淀
生成不溶于稀硝酸的淡黄色沉淀
生成不溶于稀硝酸的黄色沉淀
NaCl + AgNO3 = AgCl↓ + NaNO3
NaBr + AgNO3 = AgBr↓ + NaNO3
NaI + AgNO3 = AgI↓ + NaNO3
AgBr
溴:熏蒸剂、杀虫剂、抗爆剂
AgBr 感光材料
碘:药品、食品
AgI人工降雨
AgI
五、溴、碘及其化合物的用途
抗爆剂
AgBr
KIO3
远离海洋的内陆山区的土壤和水中碘含量较少,该地区食物中含碘量也不高,居民较易发生甲状腺肿大,因此称为地方性甲状腺肿大。
碘缺乏严重影响儿童的正常发育,表现为智力低下、聋哑、矮小、生长停渧等。
C
B
1. 下列能使淀粉变蓝的物质是( )
A. KI B. KCI C. I2 D. Br2
2. 要除去液溴中溶解的少量Cl2,可采的方法是( )
A. 加入NaCl B. 加入适量的NaBr
C. 加入适量的Cl2 D. 加入适量的Br2
课堂练习
4. 鉴别Cl-、Br-、I-可以选用的试剂是( )
A. 碘水、淀粉溶液 B. 氯水、CCl4
C. 淀粉KI溶液 D. AgNO3溶液、稀硝酸
BD
C
3. 下列物质中,不能使湿润的淀粉碘化钾试纸变蓝的是( )
A. 碘水 B. 溴水 C. 氯化钾溶液 D. 氯气
1. 溴、碘的物理性质
2. Cl2制取Br2、I2及Br2制取I2的化学方程式
3. 溴水、溴的四氯化碳溶液的颜色
碘水、碘的四氯化碳溶液的颜色
课堂练习
4. 工业上提取溴、碘的流程
5. Cl-、Br-、I-的鉴别方法
AgCl、AgBr、AgI颜色的区别
6. 溴、碘及其化合物的用途
Cl2 + 2KBr = 2KCl + Br2
Cl2 + 2KI = 2KCl + I2
Br2 + 2KI = 2KBr + I2
0 -1 -1 0
失去2×e-
得到2×e-
氧化剂
还原剂
还原
产物
氧化
产物
氧化性:Cl2 > Br2 > I2
看
观
谢
谢
必 修 一
学
化
J
S
专题3 从海水中获得的化学物质
1935 年方志敏在狱中用米汤在白纸上写下密信,通过地下工作的同志送给鲁迅。
鲁迅先生接到密信后,用干净的碗盛上一碗清水,滴入少量碘酒,并将密信浸入碘水中,白纸上马上呈现出淡蓝色的字迹。
化学密信
碘遇淀粉变蓝——用于检验碘
海水中部分元素含量图
海洋中溴元素约为100万亿吨,碘元素约为800亿吨。溴0.00083mol/L;碘0.00000047mol/L。
海洋中含量较高的元素钠镁氯等,提取已经成为产业。
溴碘等元素在陆地含量极少,只能从海洋提取。
Brˉ
Brˉ
Brˉ
Iˉ
Iˉ
Iˉ
Br2
?
I2
?
问题思考
海洋中溴元素和碘元素都是以Br-、I-形式存在,该如何从海水中提取溴单质(Br2)和碘单质(I2)?
溴(Br2):深红棕色液体;密度比水大;易挥发;在水中溶解度很小;易溶于酒精、四氯化碳等有机溶剂;有极强烈的毒害性与腐蚀性。
溴的保存:密闭保存,常往盛溴的试剂瓶中加入一些水——水封
1、溴的物理性质
Br2是常温下唯一呈液态状的非金属单质
一、溴、碘的性质
溴蒸气
溴和溴水
液溴Br2
橙黄色
2、碘的物理性质
碘(I2):紫黑色固体;密度比水大;易升华;在水中溶解度很小;易溶于酒精、四氯化碳等有机溶剂。
特性:I2能使淀粉变蓝
碘(I2)单质
碘蒸气
碘水:黄色溶液
碘的有机溶液:紫红色溶液
『实验1』在一支试管中加入2ml-3ml KBr 溶液,滴加少量新制氯水
现象:
溶液的颜色逐渐加深,最后变成了橙黄色
二、溴、碘的提取原理
观察与思考
『实验1 』 再往原溶液滴加CCl4,振荡、静置
现象:
溶液分层,上层无色,下层橙红色
化学方程式:
Cl2 + 2KBr = Br2 + 2KCl
CCl4
Cl2
KBr
溴水
下层:
溴的CCl4溶液
(橙黄色)
(橙红色)
有机溶剂,密度比水大
萃取
利用物质在互不相溶的溶剂中的溶解度的不同, 将物质从一种溶剂转移到另一种溶剂中的分离方法.
萃取
『实验2』在一支试管中加入2mlKI溶液,滴加少量
新制氯水
现象:
溶液的颜色逐渐加深,最后变成了棕黄色
『实验2 』 再往原溶液滴加CCl4,振荡、静置
现象:
溶液分层,上层无色,下层紫红色
化学方程式:
Cl2 + 2KI = I2 + 2KCl
CCl4
Cl2
KI
碘水
下层:
碘的CCl4溶液
(棕黄色)
(紫红色)
萃取
实验体系 氯水+KBr溶液 氯水+KI溶液
现象
结论
无色→橙黄色.加入CCl4上层变浅,下层变橙红色
无色→棕黄色.加入CCl4上层变浅,下层变紫红色
氯可以置换出溴
氯可以置换出碘
溴、碘的提取实验
在不同溶剂中的颜色 物理特性
水 四氯化碳
溴Br2
碘I2
橙黄色
橙红色
棕黄色
紫红色
易挥发
易升华
溴、碘的溶解性及特性
溴、碘在水中溶解度很小,易溶于酒精、CCl4等有机溶剂
湿润的淀粉KI试纸遇到Cl2为什么会变蓝?用于检验Cl2
请写出化学反应方程式
Cl2 + 2KI = I2 + 2KCl
问题思考
三、溴、碘的提取流程
常见氧化剂 价格(万元/吨)
Cl2 0.155
O2 0.13
KMnO4 3.4
K2Cr2O7(重铬酸钾) 3.76
KClO3 2.7
H2O2 1.4
Na2O2(过氧化钠) 17
氧化剂选择
不能将Br-氧化
√
1.溴的提取
溴易挥发,鼓入热空气使其全部挥发出来,冷凝得到粗溴。
思考:为什么要鼓入热空气?
粗盐
母液
通入Cl2
Br2蒸汽跑出来
粗Br2
Br2水
海水
鼓入热空气
冷凝
提纯
液溴
知识拓展
方法1: SO2吸收富集, 氯气氧化;
SO2+Br2+2H2O=2HBr+H2SO4
2HBr+Cl2=2HCl+Br2
粗溴的提纯方法
方法2: Na2CO3溶液吸收富集, H2SO4酸化;
3Na2CO3+3Br2=NaBrO3+5NaBr+3CO2
NaBrO3+5NaBr+3H2SO4=3Br2+3Na2SO4+3H2O
碘的含量 海水 海带
浓度(mg/kg) 0.06 3000~5000
含碘元素丰富的海带
海藻森林
海带森林
2.碘的提取
①灼烧
②浸泡
含I-溶液
③过滤
含碘悬浊液
①升华
②凝华
干海带
粗碘
氯气
过滤
碘单质
滤渣
AgNO3溶液
KCl溶液
KI溶液
AgNO3溶液
NaBr溶液
AgNO3溶液
实验室常用硝酸银溶液和稀硝酸来检验
四、Cl-、Br-、I-的鉴别
实验现象和化学方程式
NaCl溶液
NaBr溶液
NaI溶液
生成不溶于稀硝酸的白色沉淀
生成不溶于稀硝酸的淡黄色沉淀
生成不溶于稀硝酸的黄色沉淀
NaCl + AgNO3 = AgCl↓ + NaNO3
NaBr + AgNO3 = AgBr↓ + NaNO3
NaI + AgNO3 = AgI↓ + NaNO3
AgBr
溴:熏蒸剂、杀虫剂、抗爆剂
AgBr 感光材料
碘:药品、食品
AgI人工降雨
AgI
五、溴、碘及其化合物的用途
抗爆剂
AgBr
KIO3
远离海洋的内陆山区的土壤和水中碘含量较少,该地区食物中含碘量也不高,居民较易发生甲状腺肿大,因此称为地方性甲状腺肿大。
碘缺乏严重影响儿童的正常发育,表现为智力低下、聋哑、矮小、生长停渧等。
C
B
1. 下列能使淀粉变蓝的物质是( )
A. KI B. KCI C. I2 D. Br2
2. 要除去液溴中溶解的少量Cl2,可采的方法是( )
A. 加入NaCl B. 加入适量的NaBr
C. 加入适量的Cl2 D. 加入适量的Br2
课堂练习
4. 鉴别Cl-、Br-、I-可以选用的试剂是( )
A. 碘水、淀粉溶液 B. 氯水、CCl4
C. 淀粉KI溶液 D. AgNO3溶液、稀硝酸
BD
C
3. 下列物质中,不能使湿润的淀粉碘化钾试纸变蓝的是( )
A. 碘水 B. 溴水 C. 氯化钾溶液 D. 氯气
1. 溴、碘的物理性质
2. Cl2制取Br2、I2及Br2制取I2的化学方程式
3. 溴水、溴的四氯化碳溶液的颜色
碘水、碘的四氯化碳溶液的颜色
课堂练习
4. 工业上提取溴、碘的流程
5. Cl-、Br-、I-的鉴别方法
AgCl、AgBr、AgI颜色的区别
6. 溴、碘及其化合物的用途
Cl2 + 2KBr = 2KCl + Br2
Cl2 + 2KI = 2KCl + I2
Br2 + 2KI = 2KBr + I2
0 -1 -1 0
失去2×e-
得到2×e-
氧化剂
还原剂
还原
产物
氧化
产物
氧化性:Cl2 > Br2 > I2
看
观
谢
谢
