人教版 高中化学 选择性必修2 2.3.2 分子结构与物质的性质(共30张PPT)
文档属性
| 名称 | 人教版 高中化学 选择性必修2 2.3.2 分子结构与物质的性质(共30张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 6.6MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-22 08:33:56 | ||
图片预览










文档简介
(共30张PPT)
汇报人:XXX
XX月XX日
分子结构与物质的性质
人教版高中化学选择必修二
H2O (l)
H2O (g)
水的沸腾
活动1 观察水的沸腾过程,思考以下问题
是否为化学变化
有没有破坏化学键?
是否需要吸收能量?
结论:水分子间存在分子间的作用力
水的沸腾
分子间的作用力
医用酒精消毒
分子间普遍存在相互作用力,
这类分子间的作用力称为范德华力。
范德华(1837-1923)
荷兰物理学家,提出了范德华方程,研究了毛细作用,对附着力进行了计算,推导出物体气、液、固三相相互转化条件下的临界点计算公式。1910年因研究气态和液态方程获诺贝尔物理学奖。
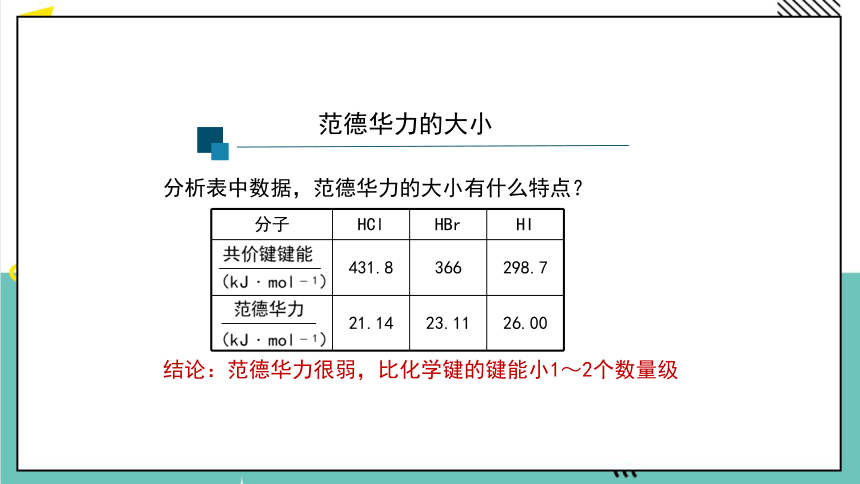
范德华力
分析表中数据,范德华力的大小有什么特点?
结论:范德华力很弱,比化学键的键能小1~2个数量级
分子 HCl HBr HI
431.8 366 298.7
21.14 23.11 26.00
力
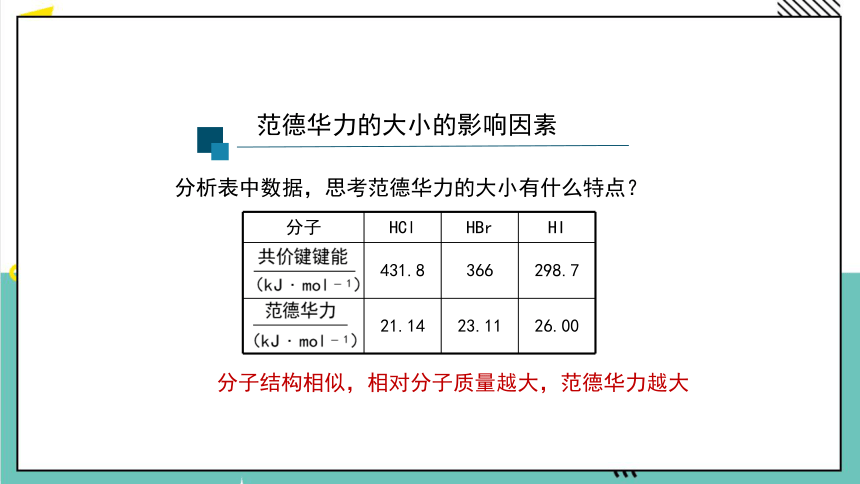
范德华力的大小
分析表中数据,思考范德华力的大小有什么特点?
分子结构相似,相对分子质量越大,范德华力越大
分子 HCl HBr HI
431.8 366 298.7
21.14 23.11 26.00
力
范德华力的大小的影响因素
分析表中数据,思考范德华力的大小有什么特点?
范德华力的大小的影响因素
相对分子质量相同或相近时,
分子的极性越大,范德华力越大
分子 HCl HBr HI Ar CO
431.8 366 298.7 无 745
21.14 23.11 26.00 8.50 8.75
力
活动2 分析表中数据,思考范德华力的大小有什么特点?
相对分子质量相同或相近时,
分子的极性越大,范德华力越大
范德华力的大小的影响因素
相对分子质量相同或相近时,分子极性越大,范德华力越大
分子结构相似,相对分子质量越大,范德华力越大
范德华力的大小的影响因素
观看加热过程中物质的状态变化的微观模拟过程
资料
范德华力对物质性质的影响
观看加热过程中物质的状态变化的微观模拟过程
范德华力对物质性质的影响
加热
加热
分子间的范德华力越大,物质的熔、沸点越高
思考 范德华力与物质性质之间的关系
分子间的范德华力越大,物质的熔、沸点越高
分子 HCl HBr HI Ar CO
21.14 23.11 26.00 8.50 8.75
熔点/℃ -114.2 -86 -50.8 -189.2 -205
沸点/℃ -85 -67 -35.1 -185.9 -191.5
力
范德华力对物质性质的影响
小结:
分子的极性越大
相对分子质量越大
范德华力
越大
物质的熔、沸点
越高
范德华力对物质性质的影响
Br2
I2
气态
液态
固态
熔、沸点依次升高
常温下
范德华力依次增大
Cl2
Cl2、Br2 、I2的相对分子质量依次增大,
想一想
第IVA族:
与预测结果相符
预测第IVA族、第VIA族元素的氢化物的沸点相对大小
应用
为什么H2O的相对分子质量比H2S的小,而沸点比H2S的高得多
预测第IVA族、第VIA族元素的氢化物的沸点相对大小
应用
在水分子的O-H中,共用电子对强烈的偏向O,使得H几乎成为“裸露”的质子,其显正电性,它能与另一个水分子中相对显负电性的O的孤电子对产生静电作用,这种静电作用就是氢键。
- - - - - -
氢键
沸点/℃
周期
氢键的形成条件
O—H
…
O
N—H
…
N
F—H
…
F
沸点/℃
周期
氢键的形成条件
X—H
Y—
…
共价键
氢键
氢键的大小
467 11 18.8
氢键比化学键的键能小,不属于化学键,
是除范德华力外的另一种分子间的作用力。
力
以冰晶体为例:
想一想
邻羟基苯甲醛(熔点-7 ℃)
对羟基苯甲醛(熔点115 ℃)
解释为什么邻羟基苯甲醛和对羟基苯甲醛熔、沸点不同?请将氢键表示出来说明。
想一想
邻羟基苯甲醛(熔点-7 ℃)
对羟基苯甲醛(熔点115 ℃)
分
子
内
氢
键
分
子
间氢
键
解释为什么邻羟基苯甲醛和对羟基苯甲醛熔、沸点不同?请将氢键表示出来说明
总结
化学键 范德华力 氢键
存在范围 分子内,原子间 分子之间 分子之间
作用力 强弱 较强 比化学键的键能小1~2个数量级 比化学键的键能小1~2个数量级
对物质性质的影响 主要影响 化学性质 主要影响物理性质(如熔、沸点) 主要影响物理性质
(如熔、沸点)
氢键对物质性质的影响
蛋白质中的氢键
DNA中的氢键
氢键对物质性质的影响
练一练
下列事实可用氢键解释的是( )
氯气易液化 B. 氨气极易溶于水
C.HF的酸性比HI的弱 D.水加热到很高的温度都难以分解
练一练
下列事实可用氢键解释的是( )
氯气易液化 B. 氨气极易溶于水
C.HF的酸性比HI的弱 D.水加热到很高的温度都难以分解
B
练一练
关于氢键的说法正确的是 ( )
A.每一个水分子内含有两个氢键
B.冰、水中都存在氢键
C.分子间形成的氢键使物质的熔点和沸点降低
D.邻羟基苯甲醛的沸点比对羟基苯甲醛的沸点高
B
练一练
一个水分子最多能形成几个氢键?
汇报人:XXX
XX月XX日
分子结构与物质的性质
人教版高中化学选择必修二
H2O (l)
H2O (g)
水的沸腾
活动1 观察水的沸腾过程,思考以下问题
是否为化学变化
有没有破坏化学键?
是否需要吸收能量?
结论:水分子间存在分子间的作用力
水的沸腾
分子间的作用力
医用酒精消毒
分子间普遍存在相互作用力,
这类分子间的作用力称为范德华力。
范德华(1837-1923)
荷兰物理学家,提出了范德华方程,研究了毛细作用,对附着力进行了计算,推导出物体气、液、固三相相互转化条件下的临界点计算公式。1910年因研究气态和液态方程获诺贝尔物理学奖。
范德华力
分析表中数据,范德华力的大小有什么特点?
结论:范德华力很弱,比化学键的键能小1~2个数量级
分子 HCl HBr HI
431.8 366 298.7
21.14 23.11 26.00
力
范德华力的大小
分析表中数据,思考范德华力的大小有什么特点?
分子结构相似,相对分子质量越大,范德华力越大
分子 HCl HBr HI
431.8 366 298.7
21.14 23.11 26.00
力
范德华力的大小的影响因素
分析表中数据,思考范德华力的大小有什么特点?
范德华力的大小的影响因素
相对分子质量相同或相近时,
分子的极性越大,范德华力越大
分子 HCl HBr HI Ar CO
431.8 366 298.7 无 745
21.14 23.11 26.00 8.50 8.75
力
活动2 分析表中数据,思考范德华力的大小有什么特点?
相对分子质量相同或相近时,
分子的极性越大,范德华力越大
范德华力的大小的影响因素
相对分子质量相同或相近时,分子极性越大,范德华力越大
分子结构相似,相对分子质量越大,范德华力越大
范德华力的大小的影响因素
观看加热过程中物质的状态变化的微观模拟过程
资料
范德华力对物质性质的影响
观看加热过程中物质的状态变化的微观模拟过程
范德华力对物质性质的影响
加热
加热
分子间的范德华力越大,物质的熔、沸点越高
思考 范德华力与物质性质之间的关系
分子间的范德华力越大,物质的熔、沸点越高
分子 HCl HBr HI Ar CO
21.14 23.11 26.00 8.50 8.75
熔点/℃ -114.2 -86 -50.8 -189.2 -205
沸点/℃ -85 -67 -35.1 -185.9 -191.5
力
范德华力对物质性质的影响
小结:
分子的极性越大
相对分子质量越大
范德华力
越大
物质的熔、沸点
越高
范德华力对物质性质的影响
Br2
I2
气态
液态
固态
熔、沸点依次升高
常温下
范德华力依次增大
Cl2
Cl2、Br2 、I2的相对分子质量依次增大,
想一想
第IVA族:
与预测结果相符
预测第IVA族、第VIA族元素的氢化物的沸点相对大小
应用
为什么H2O的相对分子质量比H2S的小,而沸点比H2S的高得多
预测第IVA族、第VIA族元素的氢化物的沸点相对大小
应用
在水分子的O-H中,共用电子对强烈的偏向O,使得H几乎成为“裸露”的质子,其显正电性,它能与另一个水分子中相对显负电性的O的孤电子对产生静电作用,这种静电作用就是氢键。
- - - - - -
氢键
沸点/℃
周期
氢键的形成条件
O—H
…
O
N—H
…
N
F—H
…
F
沸点/℃
周期
氢键的形成条件
X—H
Y—
…
共价键
氢键
氢键的大小
467 11 18.8
氢键比化学键的键能小,不属于化学键,
是除范德华力外的另一种分子间的作用力。
力
以冰晶体为例:
想一想
邻羟基苯甲醛(熔点-7 ℃)
对羟基苯甲醛(熔点115 ℃)
解释为什么邻羟基苯甲醛和对羟基苯甲醛熔、沸点不同?请将氢键表示出来说明。
想一想
邻羟基苯甲醛(熔点-7 ℃)
对羟基苯甲醛(熔点115 ℃)
分
子
内
氢
键
分
子
间氢
键
解释为什么邻羟基苯甲醛和对羟基苯甲醛熔、沸点不同?请将氢键表示出来说明
总结
化学键 范德华力 氢键
存在范围 分子内,原子间 分子之间 分子之间
作用力 强弱 较强 比化学键的键能小1~2个数量级 比化学键的键能小1~2个数量级
对物质性质的影响 主要影响 化学性质 主要影响物理性质(如熔、沸点) 主要影响物理性质
(如熔、沸点)
氢键对物质性质的影响
蛋白质中的氢键
DNA中的氢键
氢键对物质性质的影响
练一练
下列事实可用氢键解释的是( )
氯气易液化 B. 氨气极易溶于水
C.HF的酸性比HI的弱 D.水加热到很高的温度都难以分解
练一练
下列事实可用氢键解释的是( )
氯气易液化 B. 氨气极易溶于水
C.HF的酸性比HI的弱 D.水加热到很高的温度都难以分解
B
练一练
关于氢键的说法正确的是 ( )
A.每一个水分子内含有两个氢键
B.冰、水中都存在氢键
C.分子间形成的氢键使物质的熔点和沸点降低
D.邻羟基苯甲醛的沸点比对羟基苯甲醛的沸点高
B
练一练
一个水分子最多能形成几个氢键?
