第9讲 配制一定物质的量浓度的溶液(含解析)-2024年江苏省普通高中学业水平合格性考试复习
文档属性
| 名称 | 第9讲 配制一定物质的量浓度的溶液(含解析)-2024年江苏省普通高中学业水平合格性考试复习 |  | |
| 格式 | doc | ||
| 文件大小 | 750.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-21 20:48:08 | ||
图片预览

文档简介
第9讲 配制一定物质的量浓度的溶液
一定物质的量浓度溶液的配制
1.所需仪器:天平(或量筒)、烧杯、玻璃棒、 、 等。
2.容量瓶的使用
①容量瓶上标有 、 、 ,常见的容量瓶规格有 等。
②容量瓶使用前要 。
③容量瓶 用来溶解或稀释物质, 用作反应容器或长时间存放溶液。容量瓶容积是在瓶身所标温度下确定的,不能将 转移入容量瓶。
3.配制步骤:① ;② ;③ 后冷却;④ ;⑤ ;⑥ ;⑦摇匀;⑧装液。
4.配制一定物质的量浓度溶液操作注意事项
①根据所配溶液的体积选取合适规格的容量瓶。如配制950 mL 0.1 mol·L-1 Na2CO3溶液,应选用 mL的容量瓶。
②托盘天平只能精确到 g。
③转移后一定要用水洗涤烧杯和玻璃棒2~3次,洗涤液 。
④定容时,视线应平视刻度线,与 相切。
⑤定容后,经振荡、摇匀、静置后出现液面低于刻度线, 。
⑥定容时,若加水超过刻度线,则应 。
5.配制一定物质的量浓度溶液误差分析(根据公式c=)。
操作 c
天平的砝码沾有其他物质或已生锈
称量易潮解的物质(如氢氧化钠)时间过长
搅拌时有部分液体溅出
未洗涤烧杯和玻璃棒
烧杯中的液体未冷却到室温就转移入容量瓶
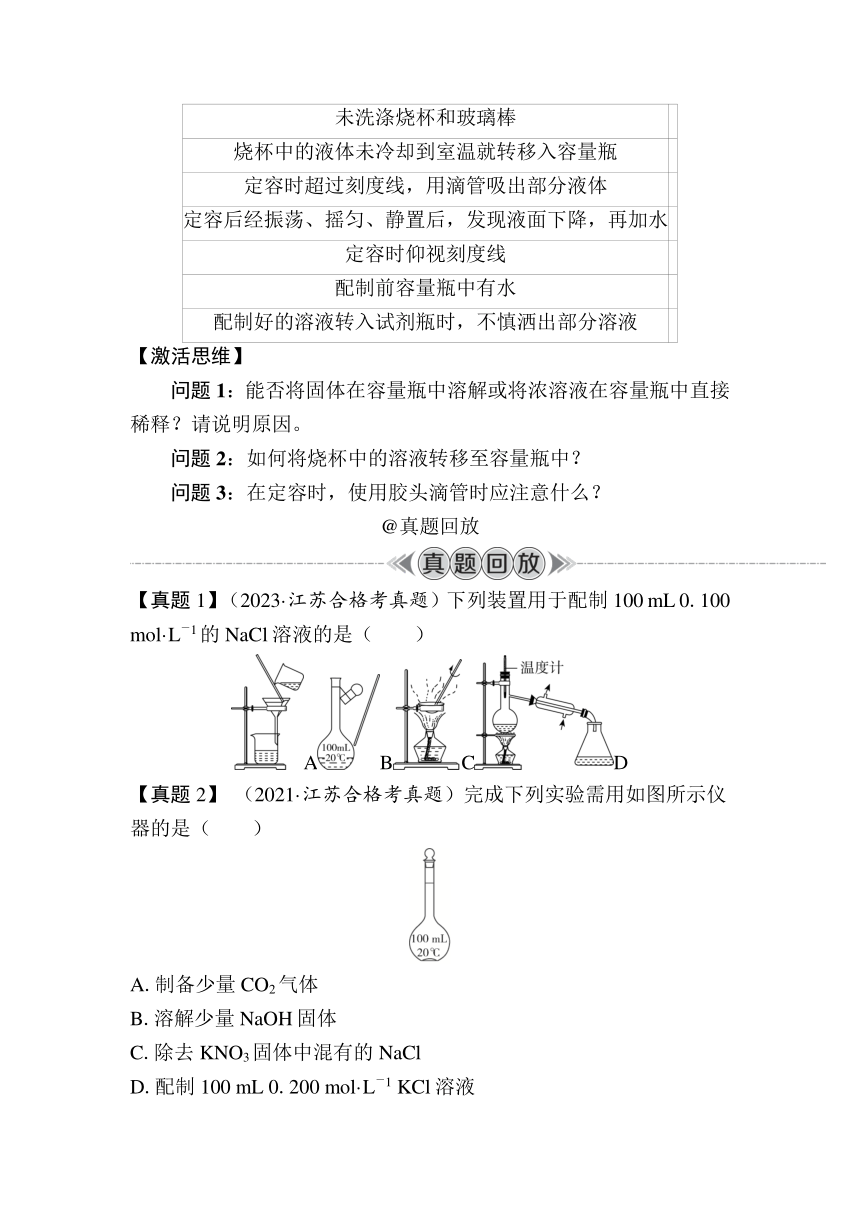
定容时超过刻度线,用滴管吸出部分液体
定容后经振荡、摇匀、静置后,发现液面下降,再加水
定容时仰视刻度线
配制前容量瓶中有水
配制好的溶液转入试剂瓶时,不慎洒出部分溶液
【激活思维】
问题1:能否将固体在容量瓶中溶解或将浓溶液在容量瓶中直接稀释?请说明原因。
问题2:如何将烧杯中的溶液转移至容量瓶中?
问题3:在定容时,使用胶头滴管时应注意什么?
@真题回放
【真题1】(2023·江苏合格考真题)下列装置用于配制100 mL 0.100 mol·L-1的NaCl溶液的是( )
ABCD
【真题2】 (2021·江苏合格考真题)完成下列实验需用如图所示仪器的是( )
A.制备少量CO2气体
B.溶解少量NaOH固体
C.除去KNO3固体中混有的NaCl
D.配制100 mL 0.200 mol·L-1 KCl溶液
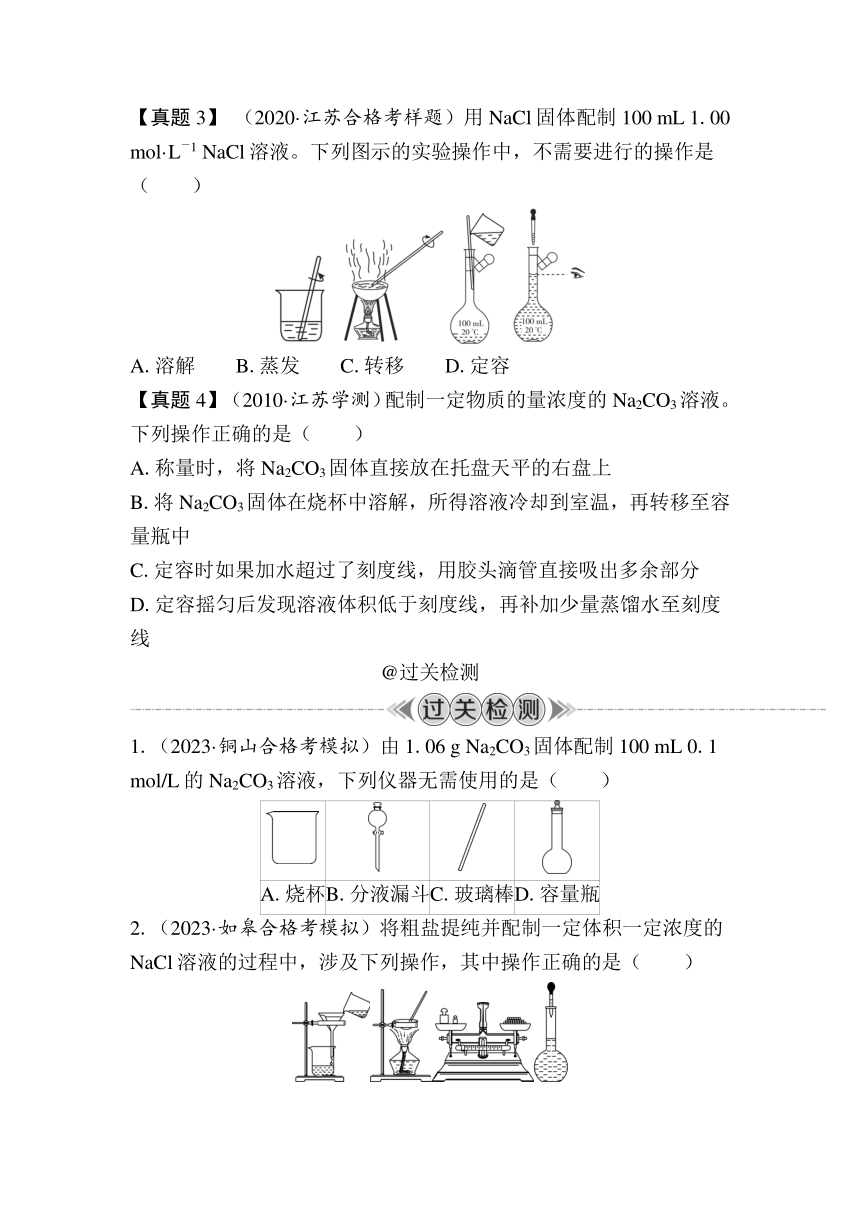
【真题3】 (2020·江苏合格考样题)用NaCl固体配制100 mL 1.00 mol·L-1 NaCl溶液。下列图示的实验操作中,不需要进行的操作是( )
A.溶解 B.蒸发 C.转移 D.定容
【真题4】 (2010·江苏学测)配制一定物质的量浓度的Na2CO3溶液。下列操作正确的是( )
A.称量时,将Na2CO3固体直接放在托盘天平的右盘上
B.将Na2CO3固体在烧杯中溶解,所得溶液冷却到室温,再转移至容量瓶中
C.定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分
D.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
@过关检测
1.(2023·铜山合格考模拟)由1.06 g Na2CO3固体配制100 mL 0.1 mol/L的Na2CO3溶液,下列仪器无需使用的是( )
A.烧杯 B.分液漏斗 C.玻璃棒 D.容量瓶
2.(2023·如皋合格考模拟)将粗盐提纯并配制一定体积一定浓度的NaCl溶液的过程中,涉及下列操作,其中操作正确的是( )
A.过滤 B.蒸发 C.称量 D.定容
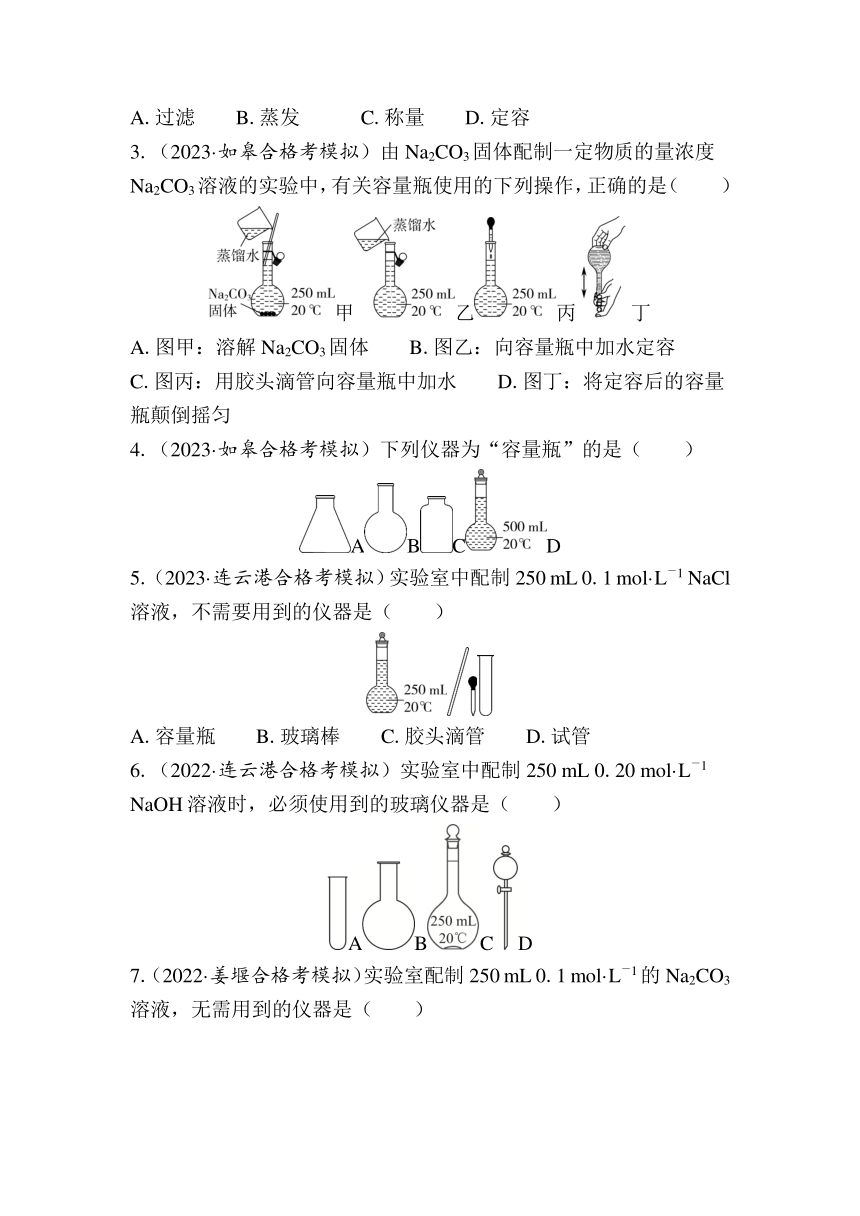
3.(2023·如皋合格考模拟)由Na2CO3固体配制一定物质的量浓度Na2CO3溶液的实验中,有关容量瓶使用的下列操作,正确的是( )
甲乙丙丁
A.图甲:溶解Na2CO3固体 B.图乙:向容量瓶中加水定容
C.图丙:用胶头滴管向容量瓶中加水 D.图丁:将定容后的容量瓶颠倒摇匀
4.(2023·如皋合格考模拟)下列仪器为“容量瓶”的是( )
ABCD
5.(2023·连云港合格考模拟)实验室中配制250 mL 0.1 mol·L-1 NaCl溶液,不需要用到的仪器是( )
A.容量瓶 B.玻璃棒 C.胶头滴管 D.试管
6.(2022·连云港合格考模拟)实验室中配制250 mL 0.20 mol·L-1 NaOH溶液时,必须使用到的玻璃仪器是( )
ABCD
7.(2022·姜堰合格考模拟)实验室配制250 mL 0.1 mol·L-1的Na2CO3溶液,无需用到的仪器是( )
ABCD
8.(2022·盐城合格考模拟)配制一定物质的量浓度的溶液是一个重要的定量实验,下列有关说法正确的是( )
A.容量瓶用蒸馏水洗净后,不需要干燥
B.配制一定物质的量浓度的稀盐酸时,用量筒量取9.82 mL浓盐酸
C.配制1 L 0.1 mol·L-1的NaCl溶液时,将NaCl固体放入容量瓶中溶解
D.定容时,为防止液滴飞溅,胶头滴管紧贴容量瓶内壁
9.(2022·丹阳合格考模拟)配制100 mL 1.00 mol/L的NaCl溶液时,下列说法正确的是( )
A.选用250 mL容量瓶
B.俯视容量瓶刻度线定容
C.溶解搅拌时有液体溅出,会使所配制溶液浓度偏低
D.定容后摇匀,发现液面低于刻度线,再加蒸馏水至刻度线
10.(2020·南京合格考模拟)用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列操作规范的是( )
A.称量 B.溶解
C.转移溶液 D.定容
11.(2021·苏州合格考模拟)用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是( )
A.干燥的 B.瓶塞不漏水的
C.用欲配制的溶液润洗过的 D.以上三项均须要求的
12.(2021·扬州合格考模拟)某学生配制0.10 mol· NaOH溶液100 mL,下列操作会造成实际浓度偏高的是( )
A.用蒸馏水洗涤容量瓶后,用烧碱溶液润洗 B.把烧碱放在滤纸上称量
C.定容时仰视刻度线 D.使用在空气中部分变质的烧碱
第9讲 配制一定物质的量浓度的溶液
【考点填空】
1.一定规格的容量瓶 胶头滴管
2.①刻度线 温度 规格 50 mL、100 mL、250 mL、500 mL
②检查是否漏水
③不能 不能 热溶液
3.①计算 ②称量(或量取) ③溶解或稀释 ④转移
⑤洗涤 ⑥定容
4.①1 000 ② 0.1 ③要注入容量瓶 ④ 凹液面最低处 ⑤ 不能再加水 ⑥重新配制
5.偏大 偏小 偏小 偏小 偏大 偏小 偏小 偏小 无影响 无影响
问题1:不能。因为在溶解或稀释时,会有热量的变化,对容量瓶的容积会造成影响。所以应在烧杯中溶解或稀释,冷却至室温后才能将溶液转移至容量瓶中。
问题2:应用玻璃棒引流。
问题3:胶头滴管不能碰到容量瓶内壁,应将胶头滴管垂直于容量瓶上方。
【真题回放】
1.B 解析:配制溶液需要用到容量瓶,B项正确。
2.D 解析:图示仪器为容量瓶,用于配制一定物质的量浓度的溶液,D项正确。A项,应用分液漏斗和试管等制备CO2;B项,溶解固体要用玻璃棒和烧杯;C项,采用冷却结晶分离,需要用烧杯等。
3.B 解析:A项,固体需要先溶解;C项,将溶解后的液体转移至容量瓶中;D项,加水定容至刻度线。
4.B 解析:A项,称量Na2CO3固体需用称量纸,且遵循“左物右码”原则,错误;B项,溶液温度需恢复至室温后方可转移到容量瓶中,正确;C项,定容时如果加水超过了刻度线,必须重新配制,错误;D项,定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线将导致所配溶液的浓度偏低,错误。
【过关检测】
1.B 解析:用Na2CO3固体配制一定物质的量浓度的Na2CO3溶液时,需要使用的玻璃仪器是容量瓶、烧杯、玻璃棒、胶头滴管,不使用分液漏斗,故B符合题意。
2.B 解析:A项,缺少玻璃棒引流,错误;C项,“左物右码”,位置放反了,错误;D项,胶头滴管不可插入容量瓶内,错误。
3.D 解析:A项,不能直接在容量瓶中溶解固体,错误;B项,要用玻璃棒引流,错误;C项,胶头滴管不能插入容量瓶内,错误。
4.D 解析:A为锥形瓶,B为圆底烧瓶,C为集气瓶,D为容量瓶。
5.D 解析:配制溶液需要用容量瓶定容;玻璃棒用于搅拌溶解,向容量瓶中引流溶液;胶头滴管用于定容;试管不需要用,D项正确。
6.C 解析:配制一定物质的量浓度的溶液,必须用到容量瓶,C项正确。
7.A 解析:配制一定物质的量浓度的溶液,不需要用到烧瓶。烧杯用于溶解,胶头滴管用于定容,容量瓶用于配制一定体积的溶液。
8.A 解析:A项,最后还需要加水定容至刻度线,所以开始时容量瓶中有水,不需要干燥,正确;B项,量筒的精确度为0.1 mL,错误;C项,不可将固体放入容量瓶中直接溶解,错误;D项,胶头滴管不能碰到容量瓶内壁,错误。
9.C 解析:A项,应选用100 mL容量瓶,错误;B项,眼睛要平视刻度线定容,错误;C项,液体溅出,溶质减少,则所配溶液的浓度偏低,正确;D项,摇匀后低于刻度线,不能再加蒸馏水,错误。
10.B 解析:A项,应为“左物右码”,错误;C项,应用玻璃棒引流,错误;D项,胶头滴管不能伸入容量瓶内,错误。
11.B 解析:容量瓶在使用前要检查是否漏水,B项正确。使用前无需干燥,也不必用溶液润洗,有少量水也没有关系。
12.A 解析:A项,润洗时,容量瓶中溶质会增多,浓度偏高,正确;B项,NaOH吸收CO2和H2O,溶质质量减少,浓度偏低,错误;C项,仰视定容,加水超过刻度线,浓度偏低,错误;D项,烧碱的质量减少,浓度偏低,错误。
一定物质的量浓度溶液的配制
1.所需仪器:天平(或量筒)、烧杯、玻璃棒、 、 等。
2.容量瓶的使用
①容量瓶上标有 、 、 ,常见的容量瓶规格有 等。
②容量瓶使用前要 。
③容量瓶 用来溶解或稀释物质, 用作反应容器或长时间存放溶液。容量瓶容积是在瓶身所标温度下确定的,不能将 转移入容量瓶。
3.配制步骤:① ;② ;③ 后冷却;④ ;⑤ ;⑥ ;⑦摇匀;⑧装液。
4.配制一定物质的量浓度溶液操作注意事项
①根据所配溶液的体积选取合适规格的容量瓶。如配制950 mL 0.1 mol·L-1 Na2CO3溶液,应选用 mL的容量瓶。
②托盘天平只能精确到 g。
③转移后一定要用水洗涤烧杯和玻璃棒2~3次,洗涤液 。
④定容时,视线应平视刻度线,与 相切。
⑤定容后,经振荡、摇匀、静置后出现液面低于刻度线, 。
⑥定容时,若加水超过刻度线,则应 。
5.配制一定物质的量浓度溶液误差分析(根据公式c=)。
操作 c
天平的砝码沾有其他物质或已生锈
称量易潮解的物质(如氢氧化钠)时间过长
搅拌时有部分液体溅出
未洗涤烧杯和玻璃棒
烧杯中的液体未冷却到室温就转移入容量瓶
定容时超过刻度线,用滴管吸出部分液体
定容后经振荡、摇匀、静置后,发现液面下降,再加水
定容时仰视刻度线
配制前容量瓶中有水
配制好的溶液转入试剂瓶时,不慎洒出部分溶液
【激活思维】
问题1:能否将固体在容量瓶中溶解或将浓溶液在容量瓶中直接稀释?请说明原因。
问题2:如何将烧杯中的溶液转移至容量瓶中?
问题3:在定容时,使用胶头滴管时应注意什么?
@真题回放
【真题1】(2023·江苏合格考真题)下列装置用于配制100 mL 0.100 mol·L-1的NaCl溶液的是( )
ABCD
【真题2】 (2021·江苏合格考真题)完成下列实验需用如图所示仪器的是( )
A.制备少量CO2气体
B.溶解少量NaOH固体
C.除去KNO3固体中混有的NaCl
D.配制100 mL 0.200 mol·L-1 KCl溶液
【真题3】 (2020·江苏合格考样题)用NaCl固体配制100 mL 1.00 mol·L-1 NaCl溶液。下列图示的实验操作中,不需要进行的操作是( )
A.溶解 B.蒸发 C.转移 D.定容
【真题4】 (2010·江苏学测)配制一定物质的量浓度的Na2CO3溶液。下列操作正确的是( )
A.称量时,将Na2CO3固体直接放在托盘天平的右盘上
B.将Na2CO3固体在烧杯中溶解,所得溶液冷却到室温,再转移至容量瓶中
C.定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分
D.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
@过关检测
1.(2023·铜山合格考模拟)由1.06 g Na2CO3固体配制100 mL 0.1 mol/L的Na2CO3溶液,下列仪器无需使用的是( )
A.烧杯 B.分液漏斗 C.玻璃棒 D.容量瓶
2.(2023·如皋合格考模拟)将粗盐提纯并配制一定体积一定浓度的NaCl溶液的过程中,涉及下列操作,其中操作正确的是( )
A.过滤 B.蒸发 C.称量 D.定容
3.(2023·如皋合格考模拟)由Na2CO3固体配制一定物质的量浓度Na2CO3溶液的实验中,有关容量瓶使用的下列操作,正确的是( )
甲乙丙丁
A.图甲:溶解Na2CO3固体 B.图乙:向容量瓶中加水定容
C.图丙:用胶头滴管向容量瓶中加水 D.图丁:将定容后的容量瓶颠倒摇匀
4.(2023·如皋合格考模拟)下列仪器为“容量瓶”的是( )
ABCD
5.(2023·连云港合格考模拟)实验室中配制250 mL 0.1 mol·L-1 NaCl溶液,不需要用到的仪器是( )
A.容量瓶 B.玻璃棒 C.胶头滴管 D.试管
6.(2022·连云港合格考模拟)实验室中配制250 mL 0.20 mol·L-1 NaOH溶液时,必须使用到的玻璃仪器是( )
ABCD
7.(2022·姜堰合格考模拟)实验室配制250 mL 0.1 mol·L-1的Na2CO3溶液,无需用到的仪器是( )
ABCD
8.(2022·盐城合格考模拟)配制一定物质的量浓度的溶液是一个重要的定量实验,下列有关说法正确的是( )
A.容量瓶用蒸馏水洗净后,不需要干燥
B.配制一定物质的量浓度的稀盐酸时,用量筒量取9.82 mL浓盐酸
C.配制1 L 0.1 mol·L-1的NaCl溶液时,将NaCl固体放入容量瓶中溶解
D.定容时,为防止液滴飞溅,胶头滴管紧贴容量瓶内壁
9.(2022·丹阳合格考模拟)配制100 mL 1.00 mol/L的NaCl溶液时,下列说法正确的是( )
A.选用250 mL容量瓶
B.俯视容量瓶刻度线定容
C.溶解搅拌时有液体溅出,会使所配制溶液浓度偏低
D.定容后摇匀,发现液面低于刻度线,再加蒸馏水至刻度线
10.(2020·南京合格考模拟)用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列操作规范的是( )
A.称量 B.溶解
C.转移溶液 D.定容
11.(2021·苏州合格考模拟)用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是( )
A.干燥的 B.瓶塞不漏水的
C.用欲配制的溶液润洗过的 D.以上三项均须要求的
12.(2021·扬州合格考模拟)某学生配制0.10 mol· NaOH溶液100 mL,下列操作会造成实际浓度偏高的是( )
A.用蒸馏水洗涤容量瓶后,用烧碱溶液润洗 B.把烧碱放在滤纸上称量
C.定容时仰视刻度线 D.使用在空气中部分变质的烧碱
第9讲 配制一定物质的量浓度的溶液
【考点填空】
1.一定规格的容量瓶 胶头滴管
2.①刻度线 温度 规格 50 mL、100 mL、250 mL、500 mL
②检查是否漏水
③不能 不能 热溶液
3.①计算 ②称量(或量取) ③溶解或稀释 ④转移
⑤洗涤 ⑥定容
4.①1 000 ② 0.1 ③要注入容量瓶 ④ 凹液面最低处 ⑤ 不能再加水 ⑥重新配制
5.偏大 偏小 偏小 偏小 偏大 偏小 偏小 偏小 无影响 无影响
问题1:不能。因为在溶解或稀释时,会有热量的变化,对容量瓶的容积会造成影响。所以应在烧杯中溶解或稀释,冷却至室温后才能将溶液转移至容量瓶中。
问题2:应用玻璃棒引流。
问题3:胶头滴管不能碰到容量瓶内壁,应将胶头滴管垂直于容量瓶上方。
【真题回放】
1.B 解析:配制溶液需要用到容量瓶,B项正确。
2.D 解析:图示仪器为容量瓶,用于配制一定物质的量浓度的溶液,D项正确。A项,应用分液漏斗和试管等制备CO2;B项,溶解固体要用玻璃棒和烧杯;C项,采用冷却结晶分离,需要用烧杯等。
3.B 解析:A项,固体需要先溶解;C项,将溶解后的液体转移至容量瓶中;D项,加水定容至刻度线。
4.B 解析:A项,称量Na2CO3固体需用称量纸,且遵循“左物右码”原则,错误;B项,溶液温度需恢复至室温后方可转移到容量瓶中,正确;C项,定容时如果加水超过了刻度线,必须重新配制,错误;D项,定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线将导致所配溶液的浓度偏低,错误。
【过关检测】
1.B 解析:用Na2CO3固体配制一定物质的量浓度的Na2CO3溶液时,需要使用的玻璃仪器是容量瓶、烧杯、玻璃棒、胶头滴管,不使用分液漏斗,故B符合题意。
2.B 解析:A项,缺少玻璃棒引流,错误;C项,“左物右码”,位置放反了,错误;D项,胶头滴管不可插入容量瓶内,错误。
3.D 解析:A项,不能直接在容量瓶中溶解固体,错误;B项,要用玻璃棒引流,错误;C项,胶头滴管不能插入容量瓶内,错误。
4.D 解析:A为锥形瓶,B为圆底烧瓶,C为集气瓶,D为容量瓶。
5.D 解析:配制溶液需要用容量瓶定容;玻璃棒用于搅拌溶解,向容量瓶中引流溶液;胶头滴管用于定容;试管不需要用,D项正确。
6.C 解析:配制一定物质的量浓度的溶液,必须用到容量瓶,C项正确。
7.A 解析:配制一定物质的量浓度的溶液,不需要用到烧瓶。烧杯用于溶解,胶头滴管用于定容,容量瓶用于配制一定体积的溶液。
8.A 解析:A项,最后还需要加水定容至刻度线,所以开始时容量瓶中有水,不需要干燥,正确;B项,量筒的精确度为0.1 mL,错误;C项,不可将固体放入容量瓶中直接溶解,错误;D项,胶头滴管不能碰到容量瓶内壁,错误。
9.C 解析:A项,应选用100 mL容量瓶,错误;B项,眼睛要平视刻度线定容,错误;C项,液体溅出,溶质减少,则所配溶液的浓度偏低,正确;D项,摇匀后低于刻度线,不能再加蒸馏水,错误。
10.B 解析:A项,应为“左物右码”,错误;C项,应用玻璃棒引流,错误;D项,胶头滴管不能伸入容量瓶内,错误。
11.B 解析:容量瓶在使用前要检查是否漏水,B项正确。使用前无需干燥,也不必用溶液润洗,有少量水也没有关系。
12.A 解析:A项,润洗时,容量瓶中溶质会增多,浓度偏高,正确;B项,NaOH吸收CO2和H2O,溶质质量减少,浓度偏低,错误;C项,仰视定容,加水超过刻度线,浓度偏低,错误;D项,烧碱的质量减少,浓度偏低,错误。
同课章节目录
