【核 心 素 养】3.1.2铁的重要化合物课件(共20页)2023-2024学年上学期高一化学人教版(2019)必修第一册
文档属性
| 名称 | 【核 心 素 养】3.1.2铁的重要化合物课件(共20页)2023-2024学年上学期高一化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 26.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-22 00:00:00 | ||
图片预览






文档简介
(共20张PPT)
第
三
章
铁
金
属
材
料
第一 节 铁 及 其 化 合 物
铁 的 重 要 化 合 物
化学1 必修 人民教育出版社
化学2 必修 人民教育出版社
教 学 目 标
核 心 素 养
1.了解铁的重要化合物的主要性质及应用。
2.掌握Fe2+、Fe3+的检验方法及其相互转化。
3.了解Fe(OH)2、Fe(OH)3的制备方法。
1.通过日常生活中见到的铁及铁化合物的应用对铁的氧化物的知识进行总结学习,培养学生论据推理与模型认知的化学核心素养。
2.通过FeCl2溶液和FeCl3溶液的鉴别学习铁盐及铁的氢氧化物性质,培养学生科学探究与创新意识的化学核心素养。
问题思考
砖的颜色为何有青有红?
天下江山第一楼
——黄鹤楼
苏州建筑
——粉墙黛瓦
问题思考
铁在自然界中分布极为广泛,为何人类发现和利用铁却比黄金和铜要迟?
磁铁矿
赤铁矿
氧化亚铁
褐铁矿
黄铁矿
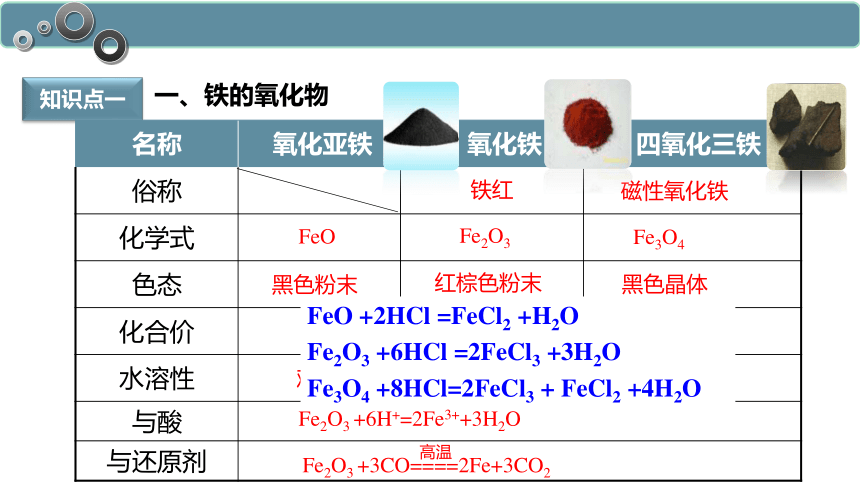
知识点一
名称 氧化亚铁 氧化铁 四氧化三铁
俗称
化学式
色态
化合价
水溶性
与酸 与还原剂 一、铁的氧化物
铁红
磁性氧化铁
FeO
Fe2O3
Fe3O4
黑色粉末
红棕色粉末
黑色晶体
+ 2
+ 3
+ 2、+ 3
难溶
难溶
难溶
Fe2O3 +6H+=2Fe3++3H2O
Fe2O3 +3CO====2Fe+3CO2
高温
FeO +2HCl =FeCl2 +H2O
Fe2O3 +6HCl =2FeCl3 +3H2O
Fe3O4 +8HCl=2FeCl3 + FeCl2 +4H2O
思考交流
铁是人体必需的微量元素中含量最多的一种(约4~5g),缺铁性贫血已成为仅次于结核病的全球患病率最高、耗资最大的公共卫生问题。那铁元素在人体中又是以什么形式存在呢?
二价铁为主要存在形式
实验探究
两瓶失去标签的FeCl2溶液和FeCl3溶液,如何进行鉴别?
1. 直接观察法
Fe3+:黄色
Fe2+:浅绿色
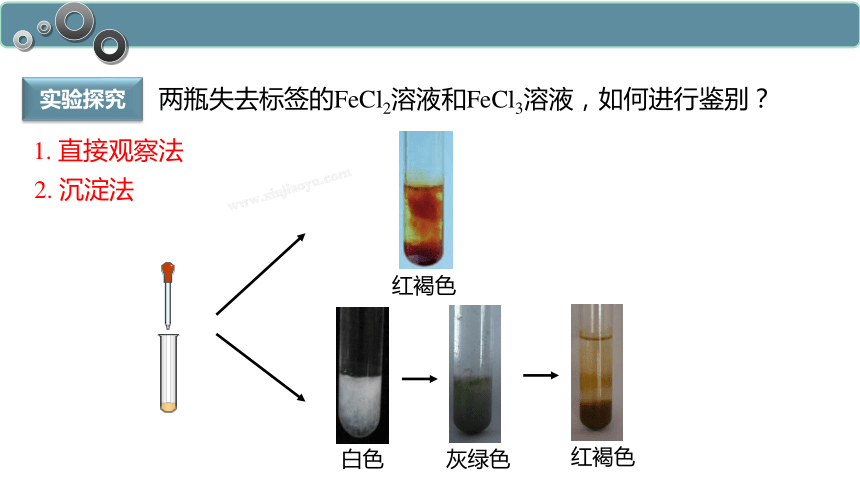
实验探究
—FeCl3 溶液
—NaOH溶液
2. 沉淀法
—FeCl2 溶液
—NaOH溶液
两瓶失去标签的FeCl2溶液和FeCl3溶液,如何进行鉴别?
1. 直接观察法
Fe(OH)3制备实验
Fe(OH)2制备实验
实验探究
白色
红褐色
灰绿色
红褐色
2. 沉淀法
两瓶失去标签的FeCl2溶液和FeCl3溶液,如何进行鉴别?
1. 直接观察法
知识点二
二、铁的氢氧化物
化学式 Fe(OH)2 Fe(OH)3
色态
溶解性
稳定性
与O2反应
与酸反应
制备
白色固体
红褐色固体
难溶
难溶
不稳定,易被空气氧化
加热易分解
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+= Fe3++3H2O
4Fe(OH)2+2H2O+O2=4Fe(OH)3
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
白色→灰绿色→红褐色
实验探究
KSCN溶液
—FeCl3溶液
—NaOH溶液
—FeCl3溶液
—KSCN溶液
3. 加入硫氰化钾法
有红褐色沉淀
溶液变为血红色
无现象
最灵敏
2. 沉淀法
两瓶失去标签的FeCl2溶液和FeCl3溶液,如何进行鉴别?
1. 直接观察法
知识点三
Fe3+ Fe2+
溶液颜色
与碱反应
氧化还原反应
检验
三、铁盐和亚铁盐
黄色
浅绿色
Fe(OH)2沉淀
Fe(OH)3沉淀
Fe ← Fe3+→ Fe2+
Fe ← Fe2+→ Fe3+
⑴观察溶液的颜色
⑵加OH-
⑶加KSCN溶液
⑴观察溶液的颜色
⑵加OH-,观察沉淀颜色变化
⑶加KSCN后再加氯水
视频导学
知识运用
设计实验,实现Fe2+和Fe3+的相互转化。
(1)FeCl2溶液、FeCl3溶液、KSCN溶液。
(2)新制氯水、酸性KMnO4溶液、H2O2溶液。
(3)铁粉、铜粉、Vc。
Fe2+
Fe3+
相互转化
?
加氧化剂
加还原剂
形成方法
认识元素及其化合物性质的视角
物质类别和元素状态,是学习元素及其化合物性质的重要认识视角。
1. 基于物质类别和元素价态,可以预测物质的性质。
2. 基于物质类别和元素价态,可以设计物质间转化的途径。
Fe2O3
金属氧化物
物质类别
性质
与酸反应
元素价态
+3价
性质
氧化性
制备FeSO4
物质类别
元素价态
单质铁与Fe3+反应
金属单质与盐的置换
形成方法
Fe2+
Fe3+
Cl2 O2 HNO3 KMnO4
Fe Cu
浅绿色
棕黄色
Fe(OH)3
Fe(OH)2
红褐色
白色
空气中放置
碱
酸
碱
酸
自我测试
1.(2022·广东东莞高一阶段检测)某兴趣小组用如图所示装置进行铁与水蒸气反应的实验,下列说法错误的是
A.烧瓶a中加入碎瓷片的作用是防止
液体暴沸
B.b中发生反应的化学方程式为2Fe+
3H2O(g) ==== Fe2O3+3H2
C.b中石棉绒的主要作用是增大铁粉与水蒸气的接触面积,使反应更加充分
D.c中试剂可以是碱石灰
√
高温
自我测试
2.打印机使用的墨粉中含有Fe3O4,下列关于Fe3O4说法正确的是
A.有磁性,是FeO与Fe2O3的混合物
B.属于两性氧化物,与酸、碱都能反应
C.Fe3O4与稀盐酸反应生成Fe2+与Fe3+物质的量之比为2∶1
D.Fe与水蒸气在高温下反应能生成Fe3O4
√
自我测试
3.如图所示装置可用来制取Fe(OH)2并观察其在空气中被氧化的颜色变化。实验时必须使用铁屑、稀硫酸和NaOH溶液。
(1)在试管Ⅰ中加入的试剂是________________。
(2)在试管Ⅱ中加入的试剂是________________。
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和试管Ⅱ中
加入试剂,塞紧塞子后的实验步骤是__________________________
__________________________________________________。
稀硫酸、铁屑
NaOH溶液
打开止水夹a,待试管Ⅰ中反应生成的氢气排尽装置中的空气后,再关闭止水夹a
自我测试
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是____________________________________________
_________________________。
(5)实验完毕,拔去试管Ⅱ中的橡胶塞,放入一部分空气,此时试管Ⅱ中发生反应的化学方程式为_______________________________。
试管Ⅰ中反应生成的H2充满了试管Ⅰ和试管Ⅱ,且外界空气不容易进入
4Fe(OH)2+2H2O+O2===4Fe(OH)3
第
三
章
铁
金
属
材
料
第一 节 铁 及 其 化 合 物
铁 的 重 要 化 合 物
化学1 必修 人民教育出版社
化学2 必修 人民教育出版社
教 学 目 标
核 心 素 养
1.了解铁的重要化合物的主要性质及应用。
2.掌握Fe2+、Fe3+的检验方法及其相互转化。
3.了解Fe(OH)2、Fe(OH)3的制备方法。
1.通过日常生活中见到的铁及铁化合物的应用对铁的氧化物的知识进行总结学习,培养学生论据推理与模型认知的化学核心素养。
2.通过FeCl2溶液和FeCl3溶液的鉴别学习铁盐及铁的氢氧化物性质,培养学生科学探究与创新意识的化学核心素养。
问题思考
砖的颜色为何有青有红?
天下江山第一楼
——黄鹤楼
苏州建筑
——粉墙黛瓦
问题思考
铁在自然界中分布极为广泛,为何人类发现和利用铁却比黄金和铜要迟?
磁铁矿
赤铁矿
氧化亚铁
褐铁矿
黄铁矿
知识点一
名称 氧化亚铁 氧化铁 四氧化三铁
俗称
化学式
色态
化合价
水溶性
与酸 与还原剂 一、铁的氧化物
铁红
磁性氧化铁
FeO
Fe2O3
Fe3O4
黑色粉末
红棕色粉末
黑色晶体
+ 2
+ 3
+ 2、+ 3
难溶
难溶
难溶
Fe2O3 +6H+=2Fe3++3H2O
Fe2O3 +3CO====2Fe+3CO2
高温
FeO +2HCl =FeCl2 +H2O
Fe2O3 +6HCl =2FeCl3 +3H2O
Fe3O4 +8HCl=2FeCl3 + FeCl2 +4H2O
思考交流
铁是人体必需的微量元素中含量最多的一种(约4~5g),缺铁性贫血已成为仅次于结核病的全球患病率最高、耗资最大的公共卫生问题。那铁元素在人体中又是以什么形式存在呢?
二价铁为主要存在形式
实验探究
两瓶失去标签的FeCl2溶液和FeCl3溶液,如何进行鉴别?
1. 直接观察法
Fe3+:黄色
Fe2+:浅绿色
实验探究
—FeCl3 溶液
—NaOH溶液
2. 沉淀法
—FeCl2 溶液
—NaOH溶液
两瓶失去标签的FeCl2溶液和FeCl3溶液,如何进行鉴别?
1. 直接观察法
Fe(OH)3制备实验
Fe(OH)2制备实验
实验探究
白色
红褐色
灰绿色
红褐色
2. 沉淀法
两瓶失去标签的FeCl2溶液和FeCl3溶液,如何进行鉴别?
1. 直接观察法
知识点二
二、铁的氢氧化物
化学式 Fe(OH)2 Fe(OH)3
色态
溶解性
稳定性
与O2反应
与酸反应
制备
白色固体
红褐色固体
难溶
难溶
不稳定,易被空气氧化
加热易分解
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+= Fe3++3H2O
4Fe(OH)2+2H2O+O2=4Fe(OH)3
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
白色→灰绿色→红褐色
实验探究
KSCN溶液
—FeCl3溶液
—NaOH溶液
—FeCl3溶液
—KSCN溶液
3. 加入硫氰化钾法
有红褐色沉淀
溶液变为血红色
无现象
最灵敏
2. 沉淀法
两瓶失去标签的FeCl2溶液和FeCl3溶液,如何进行鉴别?
1. 直接观察法
知识点三
Fe3+ Fe2+
溶液颜色
与碱反应
氧化还原反应
检验
三、铁盐和亚铁盐
黄色
浅绿色
Fe(OH)2沉淀
Fe(OH)3沉淀
Fe ← Fe3+→ Fe2+
Fe ← Fe2+→ Fe3+
⑴观察溶液的颜色
⑵加OH-
⑶加KSCN溶液
⑴观察溶液的颜色
⑵加OH-,观察沉淀颜色变化
⑶加KSCN后再加氯水
视频导学
知识运用
设计实验,实现Fe2+和Fe3+的相互转化。
(1)FeCl2溶液、FeCl3溶液、KSCN溶液。
(2)新制氯水、酸性KMnO4溶液、H2O2溶液。
(3)铁粉、铜粉、Vc。
Fe2+
Fe3+
相互转化
?
加氧化剂
加还原剂
形成方法
认识元素及其化合物性质的视角
物质类别和元素状态,是学习元素及其化合物性质的重要认识视角。
1. 基于物质类别和元素价态,可以预测物质的性质。
2. 基于物质类别和元素价态,可以设计物质间转化的途径。
Fe2O3
金属氧化物
物质类别
性质
与酸反应
元素价态
+3价
性质
氧化性
制备FeSO4
物质类别
元素价态
单质铁与Fe3+反应
金属单质与盐的置换
形成方法
Fe2+
Fe3+
Cl2 O2 HNO3 KMnO4
Fe Cu
浅绿色
棕黄色
Fe(OH)3
Fe(OH)2
红褐色
白色
空气中放置
碱
酸
碱
酸
自我测试
1.(2022·广东东莞高一阶段检测)某兴趣小组用如图所示装置进行铁与水蒸气反应的实验,下列说法错误的是
A.烧瓶a中加入碎瓷片的作用是防止
液体暴沸
B.b中发生反应的化学方程式为2Fe+
3H2O(g) ==== Fe2O3+3H2
C.b中石棉绒的主要作用是增大铁粉与水蒸气的接触面积,使反应更加充分
D.c中试剂可以是碱石灰
√
高温
自我测试
2.打印机使用的墨粉中含有Fe3O4,下列关于Fe3O4说法正确的是
A.有磁性,是FeO与Fe2O3的混合物
B.属于两性氧化物,与酸、碱都能反应
C.Fe3O4与稀盐酸反应生成Fe2+与Fe3+物质的量之比为2∶1
D.Fe与水蒸气在高温下反应能生成Fe3O4
√
自我测试
3.如图所示装置可用来制取Fe(OH)2并观察其在空气中被氧化的颜色变化。实验时必须使用铁屑、稀硫酸和NaOH溶液。
(1)在试管Ⅰ中加入的试剂是________________。
(2)在试管Ⅱ中加入的试剂是________________。
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和试管Ⅱ中
加入试剂,塞紧塞子后的实验步骤是__________________________
__________________________________________________。
稀硫酸、铁屑
NaOH溶液
打开止水夹a,待试管Ⅰ中反应生成的氢气排尽装置中的空气后,再关闭止水夹a
自我测试
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是____________________________________________
_________________________。
(5)实验完毕,拔去试管Ⅱ中的橡胶塞,放入一部分空气,此时试管Ⅱ中发生反应的化学方程式为_______________________________。
试管Ⅰ中反应生成的H2充满了试管Ⅰ和试管Ⅱ,且外界空气不容易进入
4Fe(OH)2+2H2O+O2===4Fe(OH)3
