2024鲁教版高中化学选择性必修2同步练习题--专题强化练11 “切割法”在晶胞计算中的应用(含解析)
文档属性
| 名称 | 2024鲁教版高中化学选择性必修2同步练习题--专题强化练11 “切割法”在晶胞计算中的应用(含解析) | 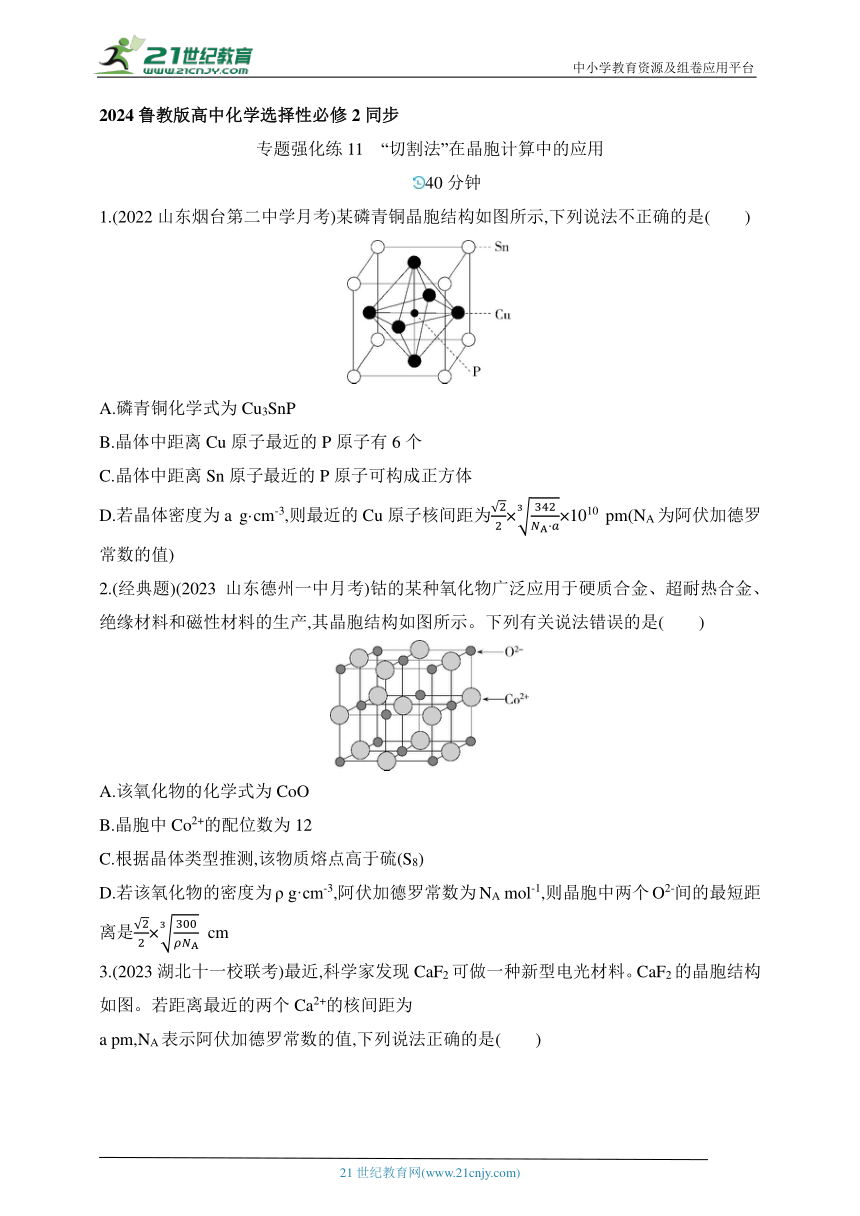 | |
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-22 19:39:23 | ||
图片预览

文档简介
中小学教育资源及组卷应用平台
2024鲁教版高中化学选择性必修2同步
专题强化练11 “切割法”在晶胞计算中的应用
40分钟
1.(2022山东烟台第二中学月考)某磷青铜晶胞结构如图所示,下列说法不正确的是( )
A.磷青铜化学式为Cu3SnP
B.晶体中距离Cu原子最近的P原子有6个
C.晶体中距离Sn原子最近的P原子可构成正方体
D.若晶体密度为a g·cm-3,则最近的Cu原子核间距为××1010 pm(NA为阿伏加德罗常数的值)
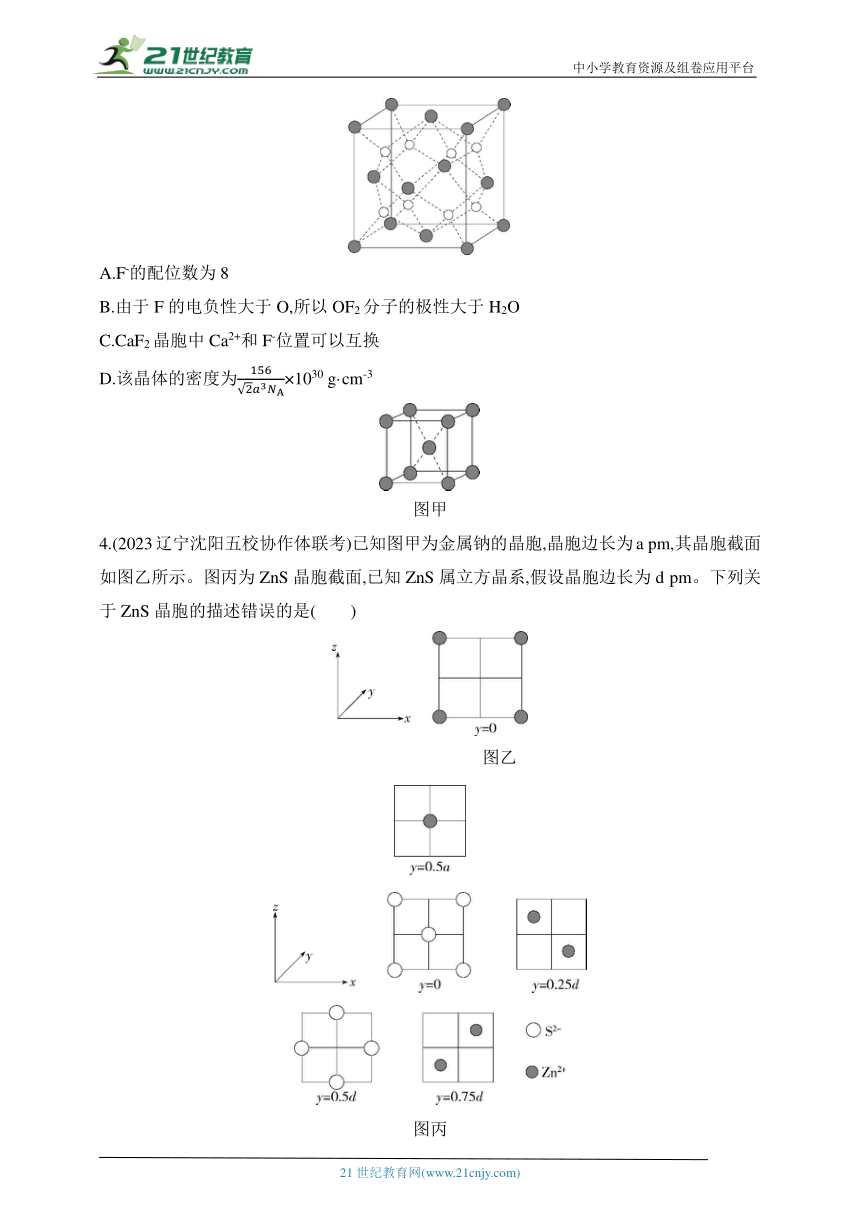
2.(经典题)(2023山东德州一中月考)钴的某种氧化物广泛应用于硬质合金、超耐热合金、绝缘材料和磁性材料的生产,其晶胞结构如图所示。下列有关说法错误的是( )
A.该氧化物的化学式为CoO
B.晶胞中Co2+的配位数为12
C.根据晶体类型推测,该物质熔点高于硫(S8)
D.若该氧化物的密度为ρ g·cm-3,阿伏加德罗常数为NA mol-1,则晶胞中两个O2-间的最短距离是× cm
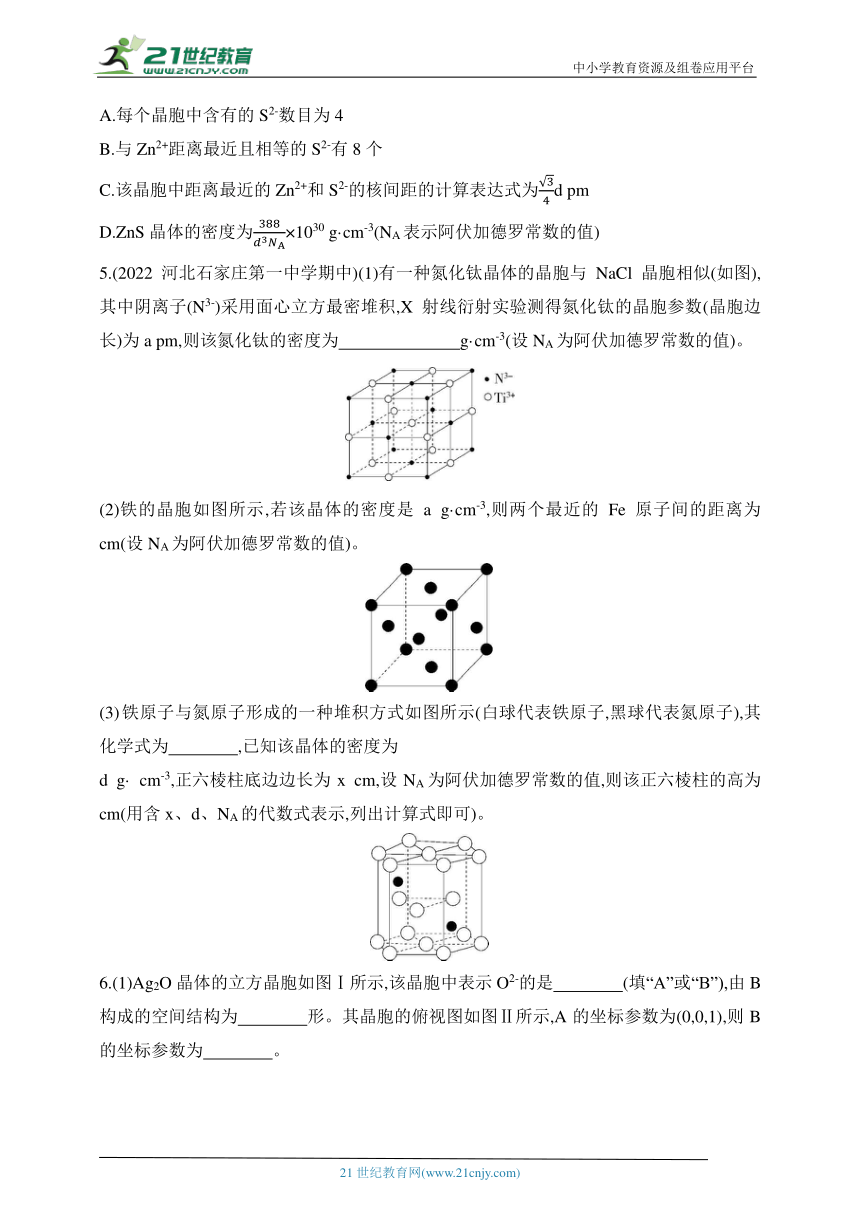
3.(2023湖北十一校联考)最近,科学家发现CaF2可做一种新型电光材料。CaF2的晶胞结构如图。若距离最近的两个Ca2+的核间距为
a pm,NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.F-的配位数为8
B.由于F的电负性大于O,所以OF2分子的极性大于H2O
C.CaF2晶胞中Ca2+和F-位置可以互换
D.该晶体的密度为×1030 g·cm-3
图甲
4.(2023辽宁沈阳五校协作体联考)已知图甲为金属钠的晶胞,晶胞边长为a pm,其晶胞截面如图乙所示。图丙为ZnS晶胞截面,已知ZnS属立方晶系,假设晶胞边长为d pm。下列关于ZnS晶胞的描述错误的是( )
图乙
图丙
A.每个晶胞中含有的S2-数目为4
B.与Zn2+距离最近且相等的S2-有8个
C.该晶胞中距离最近的Zn2+和S2-的核间距的计算表达式为d pm
D.ZnS晶体的密度为×1030 g·cm-3(NA表示阿伏加德罗常数的值)
5.(2022河北石家庄第一中学期中)(1)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如图),其中阴离子(N3-)采用面心立方最密堆积,X射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为a pm,则该氮化钛的密度为 g·cm-3(设NA为阿伏加德罗常数的值)。
(2)铁的晶胞如图所示,若该晶体的密度是a g·cm-3,则两个最近的Fe原子间的距离为 cm(设NA为阿伏加德罗常数的值)。
铁原子与氮原子形成的一种堆积方式如图所示(白球代表铁原子,黑球代表氮原子),其化学式为 ,已知该晶体的密度为
d g· cm-3,正六棱柱底边边长为x cm,设NA为阿伏加德罗常数的值,则该正六棱柱的高为 cm(用含x、d、NA的代数式表示,列出计算式即可)。
6.(1)Ag2O晶体的立方晶胞如图Ⅰ所示,该晶胞中表示O2-的是 (填“A”或“B”),由B构成的空间结构为 形。其晶胞的俯视图如图Ⅱ所示,A的坐标参数为(0,0,1),则B的坐标参数为 。
(2)某氧化物超导材料钙钛矿晶胞结构如图所示,该化合物的化学式为 ,已知正方体的边长为a pm,该晶体的密度为ρ g·cm-3,则阿伏加德罗常数的值(NA)可表示为 (用含a、ρ的式子表示)。
(3)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。
晶体中每个铁原子周围距离最近且相等的镁原子有 个,原子坐标参数可以表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0),B为(,,),C为(,,0),则D的坐标参数为 。
专题强化练11 “切割法”在晶胞计算中的应用
1.B 2.B 3.D 4.B
1.B 根据“切割法”计算可得磷青铜的化学式为Cu3SnP,A正确;晶体中距离Cu原子最近的P原子有2个,B错误;Sn原子位于晶胞顶点,被8个晶胞共用,P原子位于晶胞体心,8个P原子可构成正方体,C正确;晶胞的质量为 g,晶胞的体积为 cm3,晶胞棱长为 cm=×1010 pm,最近的两个Cu原子核间距为面对角线长的一半,为××1010 pm,D正确。
2.B 根据“切割法”可知,一个晶胞中含Co2+的个数为12×+1=4、O2-的个数为8×+6×=4,所以该氧化物的化学式为CoO,故A正确;晶胞中Co2+的配位数为6,故B错误;一般来说,分子晶体的熔点低于离子晶体,CoO为离子晶体,S8为分子晶体,则CoO的熔点高于S8的熔点,故C正确;设晶胞棱长为a cm,1个晶胞中含有4个CoO,晶体密度
ρ g·cm-3= g·cm-3= g·cm-3,则a= ,所以两个O2-间的最短距离为a cm=× cm,故D正确。
D 根据“切割法”可知,一个晶胞中含有灰球的个数为8×+6×=4,白球个数为8,则灰球为Ca2+,白球为F-,F-的配位数为4,A错误;由于O、H元素的电负性差值大于O、F元素的电负性差值,则OF2分子的电荷分布比H2O均匀,所以OF2分子的极性小于H2O,B错误;若Ca2+和F-位置互换,化学式为Ca2F,C错误;该晶胞中距离最近的两个Ca2+的核间距为面对角线长度的一半,设晶胞边长为d pm,则d=a,一个该晶胞中含有4个CaF2,故该晶体密度为×1030 g·
cm-3,D正确。
B 由图丙可知,硫离子位于晶胞的顶点和面心,一个晶胞中硫离子的个数为8×+6×=4,锌离子的个数为4,A项正确;Zn2+位于S2-的正四面体空隙内,与Zn2+距离最近且相等的S2-有4个,B项错误;晶胞中距离最近的S2-和Zn2+的核间距等于体对角线长的,故核间距的计算表达式为d pm,C项正确;ZnS晶体的密度为 g·cm-3=
×1030 g·cm-3,D项正确。
5.答案 (1)×1030
(2)·
(3)Fe3N
解析 (1)该晶胞中含有Ti3+数为12×+1=4,N3-数为8×+6×=4,晶胞边长为a pm,则该晶体的密度ρ== g·cm-3=×
1030 g·cm-3。
设晶胞的边长为x cm,则两个最近的Fe原子间的距离为x cm,根据“切割法”可知一个晶胞中含有的铁原子数为8×+6×=4,则
a g·cm-3= g·cm-3,解得x=,则两个最近的Fe原子间的距离为x cm=· cm。
(3)由题图可知,12个铁原子位于正六棱柱的顶点,2个铁原子位于上、下底面,3个铁原子位于内部,则含有Fe的个数为6,2个氮原子位于内部,则其化学式为Fe3N;正六棱柱底面的面积为x2 cm2,正六棱柱体积V=底面积×高,则该正六棱柱的高为 cm。
6.答案 (1)A 正四面体 (,,)
(2)CaTiO3
(3)8 (,,)
解析 (1)根据Ag2O晶体的立方晶胞结构可知,A的数目为8×+1=2,B的数目为4,A、B数目比为1∶2,则该晶胞中表示O2-的是A;由B构成的空间结构为正四面体形;由晶胞的俯视图可知,若A为图Ⅱ中左下角的白球,则B为图Ⅱ中右下角的黑球,其中A的坐标参数为(0,0,1),则B的坐标参数为(,,)。
(2)由题图可知,晶胞中Ti4+位于体心,数目为1,O2-位于面心,数目为6×=3,Ca2+位于顶点,数目为8×=1,则该化合物的化学式为CaTiO3。已知正方体的边长为a pm=a×10-10 cm,该晶体的密度为ρ g·cm-3,则有=ρ g·cm-3,则阿伏加德罗常数的值可表示为。
(3)由题图分析可知,每个Fe周围距离最近且相等的Mg有8个;根据晶胞结构和原子坐标参数A为(0,0,0),B为(,,),C为(,,0),可推测D的坐标参数为(,,)。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024鲁教版高中化学选择性必修2同步
专题强化练11 “切割法”在晶胞计算中的应用
40分钟
1.(2022山东烟台第二中学月考)某磷青铜晶胞结构如图所示,下列说法不正确的是( )
A.磷青铜化学式为Cu3SnP
B.晶体中距离Cu原子最近的P原子有6个
C.晶体中距离Sn原子最近的P原子可构成正方体
D.若晶体密度为a g·cm-3,则最近的Cu原子核间距为××1010 pm(NA为阿伏加德罗常数的值)
2.(经典题)(2023山东德州一中月考)钴的某种氧化物广泛应用于硬质合金、超耐热合金、绝缘材料和磁性材料的生产,其晶胞结构如图所示。下列有关说法错误的是( )
A.该氧化物的化学式为CoO
B.晶胞中Co2+的配位数为12
C.根据晶体类型推测,该物质熔点高于硫(S8)
D.若该氧化物的密度为ρ g·cm-3,阿伏加德罗常数为NA mol-1,则晶胞中两个O2-间的最短距离是× cm
3.(2023湖北十一校联考)最近,科学家发现CaF2可做一种新型电光材料。CaF2的晶胞结构如图。若距离最近的两个Ca2+的核间距为
a pm,NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.F-的配位数为8
B.由于F的电负性大于O,所以OF2分子的极性大于H2O
C.CaF2晶胞中Ca2+和F-位置可以互换
D.该晶体的密度为×1030 g·cm-3
图甲
4.(2023辽宁沈阳五校协作体联考)已知图甲为金属钠的晶胞,晶胞边长为a pm,其晶胞截面如图乙所示。图丙为ZnS晶胞截面,已知ZnS属立方晶系,假设晶胞边长为d pm。下列关于ZnS晶胞的描述错误的是( )
图乙
图丙
A.每个晶胞中含有的S2-数目为4
B.与Zn2+距离最近且相等的S2-有8个
C.该晶胞中距离最近的Zn2+和S2-的核间距的计算表达式为d pm
D.ZnS晶体的密度为×1030 g·cm-3(NA表示阿伏加德罗常数的值)
5.(2022河北石家庄第一中学期中)(1)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如图),其中阴离子(N3-)采用面心立方最密堆积,X射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为a pm,则该氮化钛的密度为 g·cm-3(设NA为阿伏加德罗常数的值)。
(2)铁的晶胞如图所示,若该晶体的密度是a g·cm-3,则两个最近的Fe原子间的距离为 cm(设NA为阿伏加德罗常数的值)。
铁原子与氮原子形成的一种堆积方式如图所示(白球代表铁原子,黑球代表氮原子),其化学式为 ,已知该晶体的密度为
d g· cm-3,正六棱柱底边边长为x cm,设NA为阿伏加德罗常数的值,则该正六棱柱的高为 cm(用含x、d、NA的代数式表示,列出计算式即可)。
6.(1)Ag2O晶体的立方晶胞如图Ⅰ所示,该晶胞中表示O2-的是 (填“A”或“B”),由B构成的空间结构为 形。其晶胞的俯视图如图Ⅱ所示,A的坐标参数为(0,0,1),则B的坐标参数为 。
(2)某氧化物超导材料钙钛矿晶胞结构如图所示,该化合物的化学式为 ,已知正方体的边长为a pm,该晶体的密度为ρ g·cm-3,则阿伏加德罗常数的值(NA)可表示为 (用含a、ρ的式子表示)。
(3)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。
晶体中每个铁原子周围距离最近且相等的镁原子有 个,原子坐标参数可以表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0),B为(,,),C为(,,0),则D的坐标参数为 。
专题强化练11 “切割法”在晶胞计算中的应用
1.B 2.B 3.D 4.B
1.B 根据“切割法”计算可得磷青铜的化学式为Cu3SnP,A正确;晶体中距离Cu原子最近的P原子有2个,B错误;Sn原子位于晶胞顶点,被8个晶胞共用,P原子位于晶胞体心,8个P原子可构成正方体,C正确;晶胞的质量为 g,晶胞的体积为 cm3,晶胞棱长为 cm=×1010 pm,最近的两个Cu原子核间距为面对角线长的一半,为××1010 pm,D正确。
2.B 根据“切割法”可知,一个晶胞中含Co2+的个数为12×+1=4、O2-的个数为8×+6×=4,所以该氧化物的化学式为CoO,故A正确;晶胞中Co2+的配位数为6,故B错误;一般来说,分子晶体的熔点低于离子晶体,CoO为离子晶体,S8为分子晶体,则CoO的熔点高于S8的熔点,故C正确;设晶胞棱长为a cm,1个晶胞中含有4个CoO,晶体密度
ρ g·cm-3= g·cm-3= g·cm-3,则a= ,所以两个O2-间的最短距离为a cm=× cm,故D正确。
D 根据“切割法”可知,一个晶胞中含有灰球的个数为8×+6×=4,白球个数为8,则灰球为Ca2+,白球为F-,F-的配位数为4,A错误;由于O、H元素的电负性差值大于O、F元素的电负性差值,则OF2分子的电荷分布比H2O均匀,所以OF2分子的极性小于H2O,B错误;若Ca2+和F-位置互换,化学式为Ca2F,C错误;该晶胞中距离最近的两个Ca2+的核间距为面对角线长度的一半,设晶胞边长为d pm,则d=a,一个该晶胞中含有4个CaF2,故该晶体密度为×1030 g·
cm-3,D正确。
B 由图丙可知,硫离子位于晶胞的顶点和面心,一个晶胞中硫离子的个数为8×+6×=4,锌离子的个数为4,A项正确;Zn2+位于S2-的正四面体空隙内,与Zn2+距离最近且相等的S2-有4个,B项错误;晶胞中距离最近的S2-和Zn2+的核间距等于体对角线长的,故核间距的计算表达式为d pm,C项正确;ZnS晶体的密度为 g·cm-3=
×1030 g·cm-3,D项正确。
5.答案 (1)×1030
(2)·
(3)Fe3N
解析 (1)该晶胞中含有Ti3+数为12×+1=4,N3-数为8×+6×=4,晶胞边长为a pm,则该晶体的密度ρ== g·cm-3=×
1030 g·cm-3。
设晶胞的边长为x cm,则两个最近的Fe原子间的距离为x cm,根据“切割法”可知一个晶胞中含有的铁原子数为8×+6×=4,则
a g·cm-3= g·cm-3,解得x=,则两个最近的Fe原子间的距离为x cm=· cm。
(3)由题图可知,12个铁原子位于正六棱柱的顶点,2个铁原子位于上、下底面,3个铁原子位于内部,则含有Fe的个数为6,2个氮原子位于内部,则其化学式为Fe3N;正六棱柱底面的面积为x2 cm2,正六棱柱体积V=底面积×高,则该正六棱柱的高为 cm。
6.答案 (1)A 正四面体 (,,)
(2)CaTiO3
(3)8 (,,)
解析 (1)根据Ag2O晶体的立方晶胞结构可知,A的数目为8×+1=2,B的数目为4,A、B数目比为1∶2,则该晶胞中表示O2-的是A;由B构成的空间结构为正四面体形;由晶胞的俯视图可知,若A为图Ⅱ中左下角的白球,则B为图Ⅱ中右下角的黑球,其中A的坐标参数为(0,0,1),则B的坐标参数为(,,)。
(2)由题图可知,晶胞中Ti4+位于体心,数目为1,O2-位于面心,数目为6×=3,Ca2+位于顶点,数目为8×=1,则该化合物的化学式为CaTiO3。已知正方体的边长为a pm=a×10-10 cm,该晶体的密度为ρ g·cm-3,则有=ρ g·cm-3,则阿伏加德罗常数的值可表示为。
(3)由题图分析可知,每个Fe周围距离最近且相等的Mg有8个;根据晶胞结构和原子坐标参数A为(0,0,0),B为(,,),C为(,,0),可推测D的坐标参数为(,,)。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
