人教版 高中化学 选择性必修3 1.1.1 有机化合物的结构特点(共39张PPT)
文档属性
| 名称 | 人教版 高中化学 选择性必修3 1.1.1 有机化合物的结构特点(共39张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 829.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-22 00:00:00 | ||
图片预览









文档简介
(共39张PPT)
汇报人:XXX
XX月XX日
有机化合物的结构特点
人教版高中化学选择必修三
一、有机化合物中碳原子的成键特点
碳原子基态时的外层电子的分布:
C:2S2 2Px1 2py1 2pz
杂化:SP3、SP2、SP
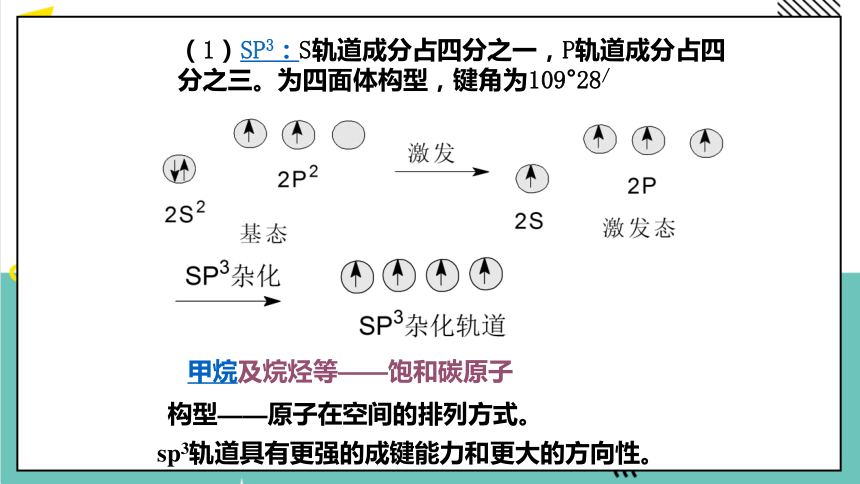
(1)SP3:S轨道成分占四分之一,P轨道成分占四分之三。为四面体构型,键角为109°28/
sp3轨道具有更强的成键能力和更大的方向性。
甲烷及烷烃等——饱和碳原子
构型——原子在空间的排列方式。
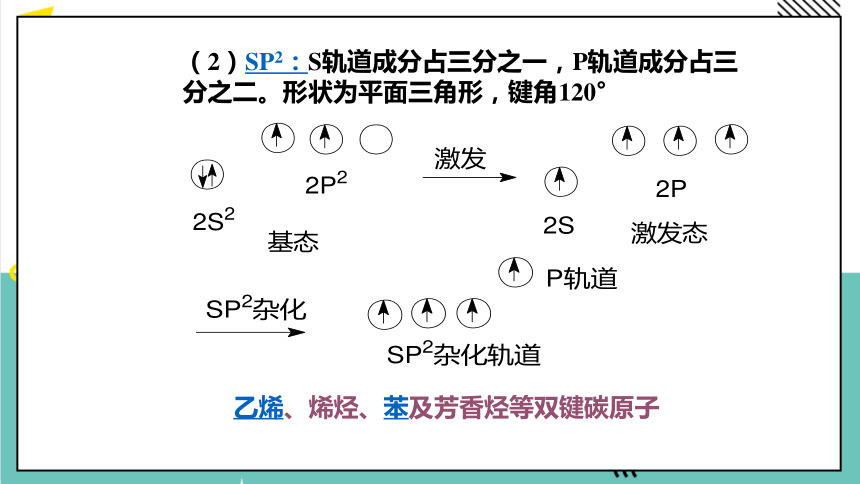
(2)SP2:S轨道成分占三分之一,P轨道成分占三分之二。形状为平面三角形,键角120°
乙烯、烯烃、苯及芳香烃等双键碳原子
(3)SP:S、P轨道成分各占二分之一。为一直线形分子。键角180°
乙炔及炔烃等三键碳原子
σ键:可以沿键轴旋转。
电子云沿键轴近似于圆柱形对称分布。 成键的两个原子可以围绕键轴旋转,而不影响电子云的分布。
π键:不能沿键轴旋转。
电子云分布在 键所在平面的上下两方,呈块 状分布
资料卡片
结构——分子中原子间的排列次序,原子相互间的立体位置、化学键的结合状态以及分子中电子的分布状况等各项内容的总和。
分子的性质不仅取决于其元素组成,更取决于分子的结构。“结构决定性质,性质反映结构”。
构造(结构)——分子中原子间相互连接的顺序叫做分子的构造。
分子式:只能反映分子中原子的种类和个数。
电子式:比较直观,但书写比较麻烦。
结构式:把电子式中的一对共用电子对用一条“-”来表示。
结构简式:把碳原子上所连接的相同原子进行合并,合并以后的个数写在该原子的右下方;省略单键。
苯的构造式
路易斯式
结构式
键线式
结构简式
2-甲基丙醇的表示方法:
路易斯式书写麻烦
结构式较麻烦
结构简式较为常用
键线式较为常用
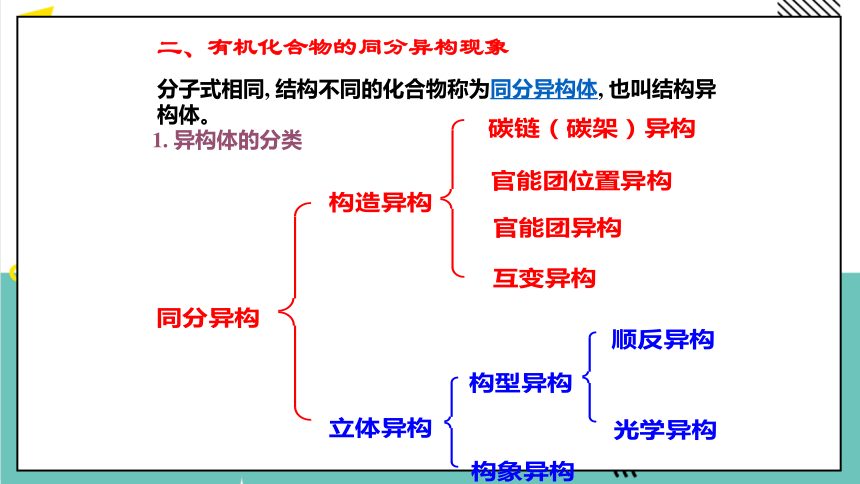
分子式相同, 结构不同的化合物称为同分异构体, 也叫结构异构体。
二、有机化合物的同分异构现象
1. 异构体的分类
包括:碳架异构、位置异构、 官能团异构
戊烷有三种同分异构体
烷烃的分子形状
正戊烷 异戊烷 新戊烷
沸点(b.p) 36.1℃ 27.9℃ 9.5℃
支链烷烃:相同C原子的烷烃,支链愈多沸点愈低。
2. 构造异构(同分异构):是指具有相同的分子式,但由于分子中原子结合的顺序不同而产生的异构。
3. 同分异构体的种类及其书写规律:
碳链异构: 指碳原子的连接次序不同引起的异构, 如:
位置异构: 官能团的位置不同引起的异构:
官能团异构: 官能团不同引起的异构, 如: 烯烃和环烷烃
书写方法: 碳链异构→位置异构→官能团异构
COOH
键线式:
结构简式:
CH3-CH-CHCH2CH2CH-COOH
CH3
CH3
CH3
骨架式:
C-C-C-C-C-C-COOH
C
C
C
练习
例1. 写出化学式C4H10O的所有可能物质的结构简式
C4H10O
类别异构
位置异构
位置异构
醇
醚
碳链异构
碳链异构
例题2: C11H16 的苯的同系物中, 只含有一个支链, 且支链上含有两个“—CH3”的结构有四种, 写出其结构简式.
伯碳:与一个C原子直接相连。
仲碳:与二个C原子直接相连。
叔碳:与三个C原子直接相连。
季碳: 与四个C原子直接相连。
1. 碳原子分类
知识回顾
①同一碳原子上的氢原子是等效的。
②同一碳原子上所连接甲基上的氢原子是等效的。
③处于同一面对称位置上的氢原子是等效的。
2. 确定一元取代物的同分异构体的基本方法与技巧
(1)等同氢
常见一元取代物只有一种的10个碳原子以内的烷烃
CH3CH3
CH4
CH3
CH3-C-CH3
CH3
例如:对称轴
CH3CH2CH2CH2CH3
① ② ③ ② ①
② ① ③ ① ②
CH3-CH2-CH-CH2-CH3
① CH2
② CH3
CH3
CH3 – C – CH2- CH3
① CH3 ② ③
a
a
b
b
b
b
a
a
(2)对称技巧
例3. 进行一氯取代后,只能生成3种沸点不同的产物的烷烃是---------------------------------( )
A. (CH3)2CHCH2CH2CH3
B. (CH3CH2)2CHCH3
C.(CH3)2CHCH(CH3)2
D.(CH3)3CCH2CH3
A. C ③ ④ ⑤
② C-C-C-C
C ①
D. C
C-C-C-C
① C ② ③
D
(3)转换技巧
例4.已知化学式为C12H12的物质A的结构简式为
A苯环上的二溴代物有9种同分异
构体,以此推断A苯环上的四溴代
物的异构体数目有 -------( )
A.9种 B. 10种
C. 11种 D. 12种
CH3
CH3
A
例5. 式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为 ( )
A.3 B.4 C.5 D.6
CH3 — CH—CH3
D
— CH2— CH2—CH3
— C3H7
CH3
— C3H7
科学史话
1874年荷兰化学家范特霍夫
(J.H.van’t Hoff,1852—1911)
和法国化学家列别尔(J.A.Le Bel,1847—1930)分别独立地提出了碳
价四面体学说,即碳原子占据四面体的中心,它的4个价键指向四面体的4个顶点。这一学说揭示了有机物旋光异构现象的原因,也奠定了有机立体化学的基础,推动了有机化学的发展。
1901年诺贝尔化学奖获得者:雅可比·亨利克·范特霍夫
送鲜奶的范特霍夫和化学家范特霍夫被人们合并传成了“牧场化学家”。
范特霍夫的父亲从这件事中得知儿子很喜欢化学,就从家里让出一间房子作为工作室,专门供儿子做化学实验。从此,范特霍夫就开始“经营”自己的小实验室。他把父母给的零用钱和从其他亲友那里得 到的“赞助”积累起来购买了各种实验器具和药品,课作时间从事自己的化学实验。立志当一名化学家,1869年,范特霍夫从鹿特丹五年制中学毕业了。选择什么样的职业呢 在当时,化学作为一 门学问已有很多人进行了研究,但是人们普遍认为化学不是一种职业,从事化学的人,还要兼做其他工作才能够维持自己的生活。父亲为了让他多增加一些知识,才支持他做化学实验。要把化学做为一种职业,做一个化学家,父亲就难以同意了。因为这样做恐怕连自己的生活都维持不了。为此,父子俩争辨了多次,但是必须有一个结论才行呀。 一天晚饭过后,父子俩又开始讨论这个老话题了。 “中学毕业了,你打算上哪个学校 ”父亲心平气和地问道。当然,选择学校也就是选择职业了。
“学习化学对我比较合适,爸爸,你说对吗 ”儿子说出了心里话。父母并不想让他成为一个化学家,而想把他培养成一名工程师。几经周折,范特霍夫进入了 荷兰的台夫特工业专科学校学习。这个学校虽然是专门学习工艺技术的,但讲授化学课的奥德曼却是一个很有水平的教授。他推理清晰,论述有序,很能激发起人们对化学的兴趣。范特霍夫在奥德曼教授的指导下进步很快。由于范特霍夫的努力,仅用了2年时间就学完了一般人3年才能学完的课程。1871年,范特霍夫毕业了,他终于说服了父母,可以全力进行化学研究了。为了打好基础,找准研究的方向,必须拜师求教。范特霍夫只身来到德国的波恩,拜当时世 界著名的有机化学家佛莱德·凯库勒为师。佛莱德·凯库勒是个传奇的化学家,他在梦中见蛇在狂舞,首尾相接,从而解决了苯环的结构。在波恩期间,范特霍夫在有机化学方面受到了良好的训练。随后,他又前往法国巴黎向医学化学家武兹请教。1874年,回到荷兰,在乌特勒支大学获得博士学位。从此他就开始了更深入的研究工作。
范特霍夫首先提出了碳的四面体结构学说。过去的有机结构理论认为有机分子中的原子都处 在一个平面内,这与很多现象是矛盾的。范特霍夫的理论纠正了过去的错误。但是这一新的理论却遭到了一些权威人士的反对,当时德国有机化学家哈曼·柯尔比就是其中一个。这位老科学家倚老卖老,根本不愿学习新的东西。在没有认真研究的情况下,就毫无根据地把范特霍夫斥责了一顿。范特霍夫对这位才先生的高论嗤之以鼻,不与其辩论。这一下可气坏了老柯尔比,他跳着脚非要与范特霍夫一比高低。范特霍夫本来就想与这些化学界的权威们争一高低,因为事实是迟早会说话的。既然柯尔比 不远千里从德国来到荷兰,那也只好以礼相见了。毕竟范特霍夫是晚辈,当柯尔比气势汹汹地冲进范特霍夫的办公室时,范特霍夫已经恭恭敬敬地等候他了。待柯尔比的火气稍稍减退之后,范特霍夫平心静气地向他陈述了自己的观点,并请柯尔比用事实来批评自己的理论。 这位老权威暗暗地吃了一惊,眼前的年轻人非同小可,讲述观点时条理清楚,论证有据,不 可不服呀。柯尔比毕竟还是要讲道理、讲事实的。
平心而论,范特霍夫的理论是正确的,他刚来时的火气完全消失了,并邀请范特霍夫去普鲁士科学院工作。
范特霍夫实事求是、谦虚谨慎的态度使很多人都能心悦诚服地接受他的理论。1901年,瑞典皇家科学院收到的20份诺贝尔化学奖候选人提案中,有11份提名范特霍夫。这一年的诺贝尔化学奖颁发给范特霍夫,他当之无愧。1901年12月10日,对于范特霍夫来说是一个值得纪念的日子,对于人类也是一个纪念的日子,这一天,首次颁发诺贝尔奖,范特霍夫是第一位诺贝尔化学奖的获奖者。非常有趣的是,范特霍夫创立的碳的四面体结构学说并不是获奖原因,而是他的另外两篇著名论文《化学动力学研究》和《气体体系或稀溶液中的化学平衡》使他获得首届诺贝尔化学奖。
1911年3月1日,范特霍夫在柏林附近的斯特利茨逝世。终年59岁
附表:烷烃的碳原子数与其对应的同分异构体数
碳原子数 1 2 3 4 5 6 7 8 9 10
同分异体数 1 1 1 2 3 5 9 18 35 75
常见的类别异构现象
序号
类别
通式
1
烯烃
环烷烃
2
炔烃
二烯烃
3
饱和一元脂肪醇
饱和醚
4
饱和一元脂肪醛
酮
5
饱和羧酸
酯
CnH2n
CnH2n-2
CnH2n+2O
CnH2nO
CnH2nO2
汇报人:XXX
XX月XX日
有机化合物的结构特点
人教版高中化学选择必修三
一、有机化合物中碳原子的成键特点
碳原子基态时的外层电子的分布:
C:2S2 2Px1 2py1 2pz
杂化:SP3、SP2、SP
(1)SP3:S轨道成分占四分之一,P轨道成分占四分之三。为四面体构型,键角为109°28/
sp3轨道具有更强的成键能力和更大的方向性。
甲烷及烷烃等——饱和碳原子
构型——原子在空间的排列方式。
(2)SP2:S轨道成分占三分之一,P轨道成分占三分之二。形状为平面三角形,键角120°
乙烯、烯烃、苯及芳香烃等双键碳原子
(3)SP:S、P轨道成分各占二分之一。为一直线形分子。键角180°
乙炔及炔烃等三键碳原子
σ键:可以沿键轴旋转。
电子云沿键轴近似于圆柱形对称分布。 成键的两个原子可以围绕键轴旋转,而不影响电子云的分布。
π键:不能沿键轴旋转。
电子云分布在 键所在平面的上下两方,呈块 状分布
资料卡片
结构——分子中原子间的排列次序,原子相互间的立体位置、化学键的结合状态以及分子中电子的分布状况等各项内容的总和。
分子的性质不仅取决于其元素组成,更取决于分子的结构。“结构决定性质,性质反映结构”。
构造(结构)——分子中原子间相互连接的顺序叫做分子的构造。
分子式:只能反映分子中原子的种类和个数。
电子式:比较直观,但书写比较麻烦。
结构式:把电子式中的一对共用电子对用一条“-”来表示。
结构简式:把碳原子上所连接的相同原子进行合并,合并以后的个数写在该原子的右下方;省略单键。
苯的构造式
路易斯式
结构式
键线式
结构简式
2-甲基丙醇的表示方法:
路易斯式书写麻烦
结构式较麻烦
结构简式较为常用
键线式较为常用
分子式相同, 结构不同的化合物称为同分异构体, 也叫结构异构体。
二、有机化合物的同分异构现象
1. 异构体的分类
包括:碳架异构、位置异构、 官能团异构
戊烷有三种同分异构体
烷烃的分子形状
正戊烷 异戊烷 新戊烷
沸点(b.p) 36.1℃ 27.9℃ 9.5℃
支链烷烃:相同C原子的烷烃,支链愈多沸点愈低。
2. 构造异构(同分异构):是指具有相同的分子式,但由于分子中原子结合的顺序不同而产生的异构。
3. 同分异构体的种类及其书写规律:
碳链异构: 指碳原子的连接次序不同引起的异构, 如:
位置异构: 官能团的位置不同引起的异构:
官能团异构: 官能团不同引起的异构, 如: 烯烃和环烷烃
书写方法: 碳链异构→位置异构→官能团异构
COOH
键线式:
结构简式:
CH3-CH-CHCH2CH2CH-COOH
CH3
CH3
CH3
骨架式:
C-C-C-C-C-C-COOH
C
C
C
练习
例1. 写出化学式C4H10O的所有可能物质的结构简式
C4H10O
类别异构
位置异构
位置异构
醇
醚
碳链异构
碳链异构
例题2: C11H16 的苯的同系物中, 只含有一个支链, 且支链上含有两个“—CH3”的结构有四种, 写出其结构简式.
伯碳:与一个C原子直接相连。
仲碳:与二个C原子直接相连。
叔碳:与三个C原子直接相连。
季碳: 与四个C原子直接相连。
1. 碳原子分类
知识回顾
①同一碳原子上的氢原子是等效的。
②同一碳原子上所连接甲基上的氢原子是等效的。
③处于同一面对称位置上的氢原子是等效的。
2. 确定一元取代物的同分异构体的基本方法与技巧
(1)等同氢
常见一元取代物只有一种的10个碳原子以内的烷烃
CH3CH3
CH4
CH3
CH3-C-CH3
CH3
例如:对称轴
CH3CH2CH2CH2CH3
① ② ③ ② ①
② ① ③ ① ②
CH3-CH2-CH-CH2-CH3
① CH2
② CH3
CH3
CH3 – C – CH2- CH3
① CH3 ② ③
a
a
b
b
b
b
a
a
(2)对称技巧
例3. 进行一氯取代后,只能生成3种沸点不同的产物的烷烃是---------------------------------( )
A. (CH3)2CHCH2CH2CH3
B. (CH3CH2)2CHCH3
C.(CH3)2CHCH(CH3)2
D.(CH3)3CCH2CH3
A. C ③ ④ ⑤
② C-C-C-C
C ①
D. C
C-C-C-C
① C ② ③
D
(3)转换技巧
例4.已知化学式为C12H12的物质A的结构简式为
A苯环上的二溴代物有9种同分异
构体,以此推断A苯环上的四溴代
物的异构体数目有 -------( )
A.9种 B. 10种
C. 11种 D. 12种
CH3
CH3
A
例5. 式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为 ( )
A.3 B.4 C.5 D.6
CH3 — CH—CH3
D
— CH2— CH2—CH3
— C3H7
CH3
— C3H7
科学史话
1874年荷兰化学家范特霍夫
(J.H.van’t Hoff,1852—1911)
和法国化学家列别尔(J.A.Le Bel,1847—1930)分别独立地提出了碳
价四面体学说,即碳原子占据四面体的中心,它的4个价键指向四面体的4个顶点。这一学说揭示了有机物旋光异构现象的原因,也奠定了有机立体化学的基础,推动了有机化学的发展。
1901年诺贝尔化学奖获得者:雅可比·亨利克·范特霍夫
送鲜奶的范特霍夫和化学家范特霍夫被人们合并传成了“牧场化学家”。
范特霍夫的父亲从这件事中得知儿子很喜欢化学,就从家里让出一间房子作为工作室,专门供儿子做化学实验。从此,范特霍夫就开始“经营”自己的小实验室。他把父母给的零用钱和从其他亲友那里得 到的“赞助”积累起来购买了各种实验器具和药品,课作时间从事自己的化学实验。立志当一名化学家,1869年,范特霍夫从鹿特丹五年制中学毕业了。选择什么样的职业呢 在当时,化学作为一 门学问已有很多人进行了研究,但是人们普遍认为化学不是一种职业,从事化学的人,还要兼做其他工作才能够维持自己的生活。父亲为了让他多增加一些知识,才支持他做化学实验。要把化学做为一种职业,做一个化学家,父亲就难以同意了。因为这样做恐怕连自己的生活都维持不了。为此,父子俩争辨了多次,但是必须有一个结论才行呀。 一天晚饭过后,父子俩又开始讨论这个老话题了。 “中学毕业了,你打算上哪个学校 ”父亲心平气和地问道。当然,选择学校也就是选择职业了。
“学习化学对我比较合适,爸爸,你说对吗 ”儿子说出了心里话。父母并不想让他成为一个化学家,而想把他培养成一名工程师。几经周折,范特霍夫进入了 荷兰的台夫特工业专科学校学习。这个学校虽然是专门学习工艺技术的,但讲授化学课的奥德曼却是一个很有水平的教授。他推理清晰,论述有序,很能激发起人们对化学的兴趣。范特霍夫在奥德曼教授的指导下进步很快。由于范特霍夫的努力,仅用了2年时间就学完了一般人3年才能学完的课程。1871年,范特霍夫毕业了,他终于说服了父母,可以全力进行化学研究了。为了打好基础,找准研究的方向,必须拜师求教。范特霍夫只身来到德国的波恩,拜当时世 界著名的有机化学家佛莱德·凯库勒为师。佛莱德·凯库勒是个传奇的化学家,他在梦中见蛇在狂舞,首尾相接,从而解决了苯环的结构。在波恩期间,范特霍夫在有机化学方面受到了良好的训练。随后,他又前往法国巴黎向医学化学家武兹请教。1874年,回到荷兰,在乌特勒支大学获得博士学位。从此他就开始了更深入的研究工作。
范特霍夫首先提出了碳的四面体结构学说。过去的有机结构理论认为有机分子中的原子都处 在一个平面内,这与很多现象是矛盾的。范特霍夫的理论纠正了过去的错误。但是这一新的理论却遭到了一些权威人士的反对,当时德国有机化学家哈曼·柯尔比就是其中一个。这位老科学家倚老卖老,根本不愿学习新的东西。在没有认真研究的情况下,就毫无根据地把范特霍夫斥责了一顿。范特霍夫对这位才先生的高论嗤之以鼻,不与其辩论。这一下可气坏了老柯尔比,他跳着脚非要与范特霍夫一比高低。范特霍夫本来就想与这些化学界的权威们争一高低,因为事实是迟早会说话的。既然柯尔比 不远千里从德国来到荷兰,那也只好以礼相见了。毕竟范特霍夫是晚辈,当柯尔比气势汹汹地冲进范特霍夫的办公室时,范特霍夫已经恭恭敬敬地等候他了。待柯尔比的火气稍稍减退之后,范特霍夫平心静气地向他陈述了自己的观点,并请柯尔比用事实来批评自己的理论。 这位老权威暗暗地吃了一惊,眼前的年轻人非同小可,讲述观点时条理清楚,论证有据,不 可不服呀。柯尔比毕竟还是要讲道理、讲事实的。
平心而论,范特霍夫的理论是正确的,他刚来时的火气完全消失了,并邀请范特霍夫去普鲁士科学院工作。
范特霍夫实事求是、谦虚谨慎的态度使很多人都能心悦诚服地接受他的理论。1901年,瑞典皇家科学院收到的20份诺贝尔化学奖候选人提案中,有11份提名范特霍夫。这一年的诺贝尔化学奖颁发给范特霍夫,他当之无愧。1901年12月10日,对于范特霍夫来说是一个值得纪念的日子,对于人类也是一个纪念的日子,这一天,首次颁发诺贝尔奖,范特霍夫是第一位诺贝尔化学奖的获奖者。非常有趣的是,范特霍夫创立的碳的四面体结构学说并不是获奖原因,而是他的另外两篇著名论文《化学动力学研究》和《气体体系或稀溶液中的化学平衡》使他获得首届诺贝尔化学奖。
1911年3月1日,范特霍夫在柏林附近的斯特利茨逝世。终年59岁
附表:烷烃的碳原子数与其对应的同分异构体数
碳原子数 1 2 3 4 5 6 7 8 9 10
同分异体数 1 1 1 2 3 5 9 18 35 75
常见的类别异构现象
序号
类别
通式
1
烯烃
环烷烃
2
炔烃
二烯烃
3
饱和一元脂肪醇
饱和醚
4
饱和一元脂肪醛
酮
5
饱和羧酸
酯
CnH2n
CnH2n-2
CnH2n+2O
CnH2nO
CnH2nO2
