专题 原电池原理和化学电源(共44张PPT)
文档属性
| 名称 | 专题 原电池原理和化学电源(共44张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 4.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-22 23:13:48 | ||
图片预览





文档简介
(共44张PPT)
专题 原电池原理和化学电源
考题统计
原电池原理和化学电源:
湖南卷(2023、2022、2021),广东卷(2023、2022),浙江卷(2022、2021),辽宁卷(2023、2022、2021),河北卷(2021),天津卷(2021、2020),山东卷(2023、2021),全国新课标卷(2023)
聚焦核心要点
要点1原电池的工作原理与应用
课标指引:1.认识化学能与电能相互转化的实际意义及其重要应用。
2.能分析、解释原电池的工作原理,能设计简单的原电池。
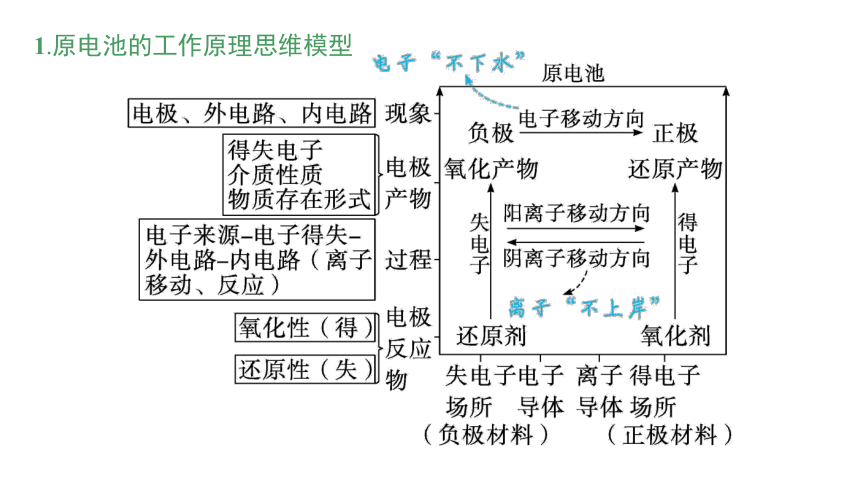
1.原电池的工作原理思维模型
2.原电池中电极反应和电池反应的书写方法
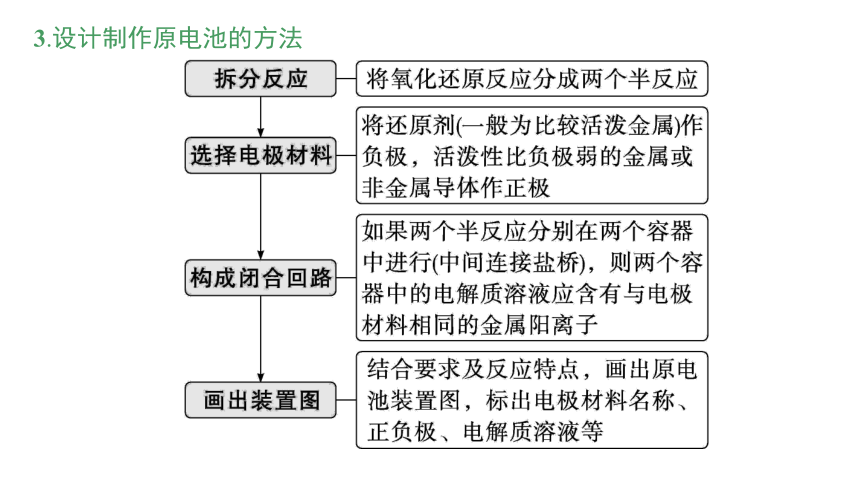
3.设计制作原电池的方法
要点2新型化学电源及分析
课标指引:1.能列举常见的化学电源,并能利用相关信息分析化学电源的工作原理。 2.能综合考虑化学变化中的物质变化和能量变化来分析、解决实际问题,如新型电池的开发等。
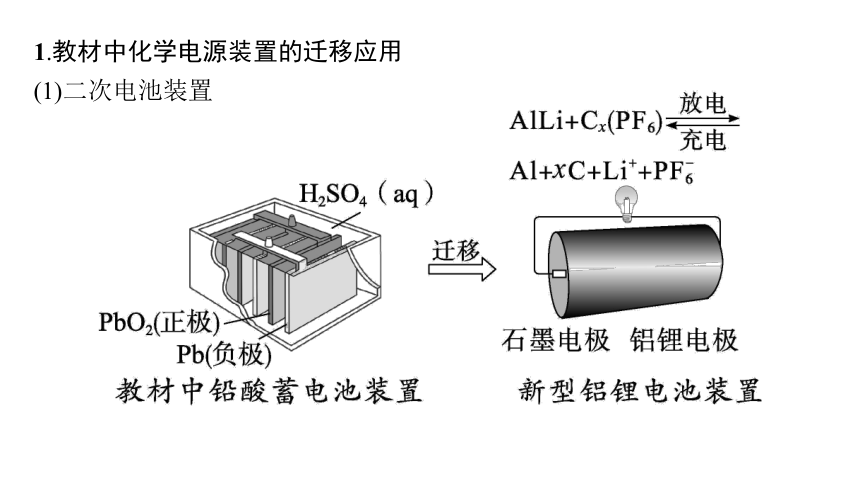
1.教材中化学电源装置的迁移应用
(1)二次电池装置
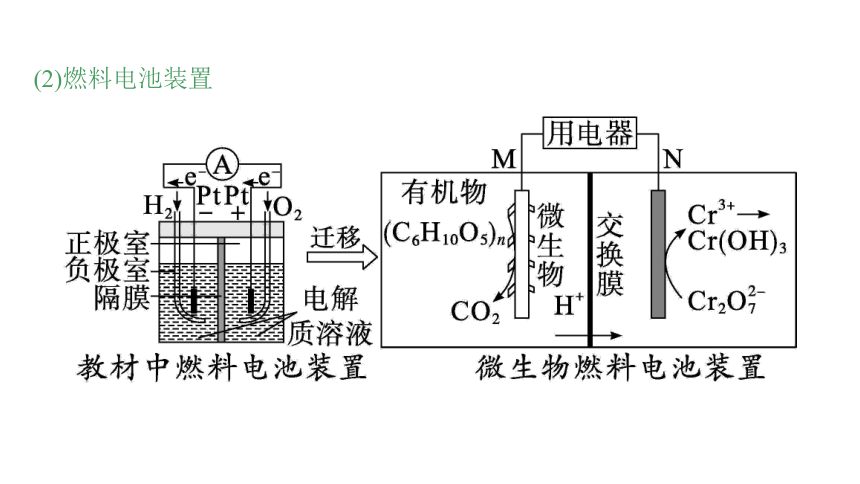
(2)燃料电池装置
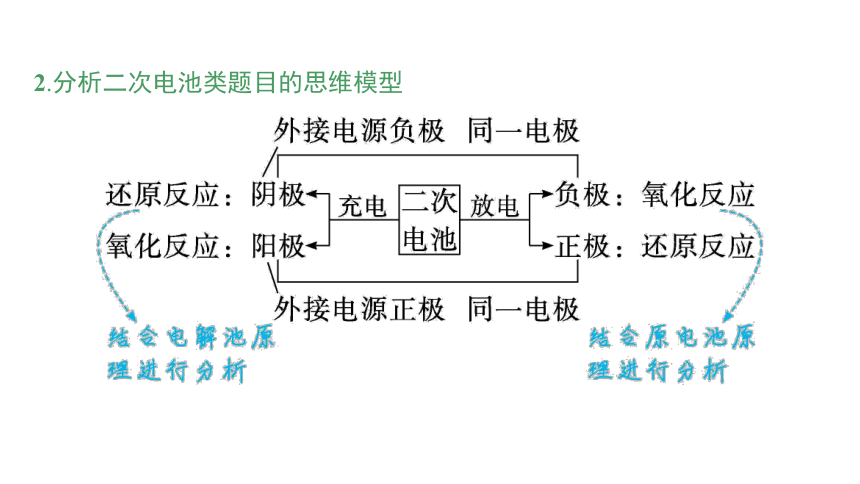
2.分析二次电池类题目的思维模型
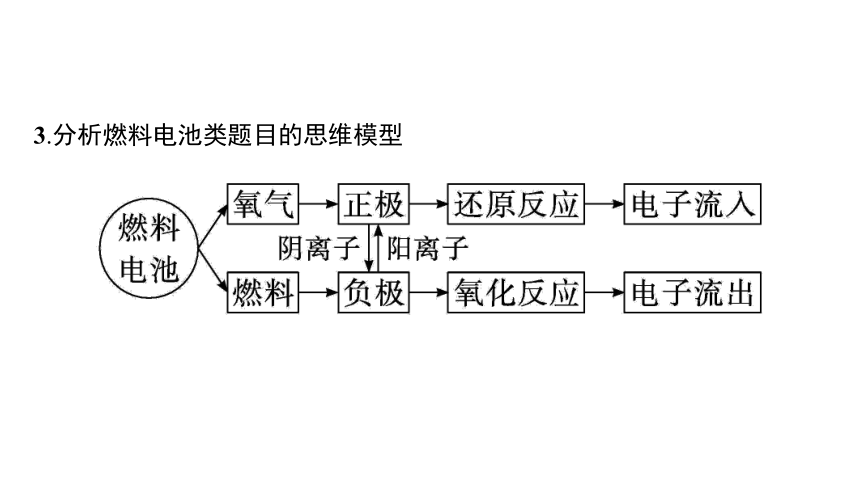
3.分析燃料电池类题目的思维模型
易错辨析
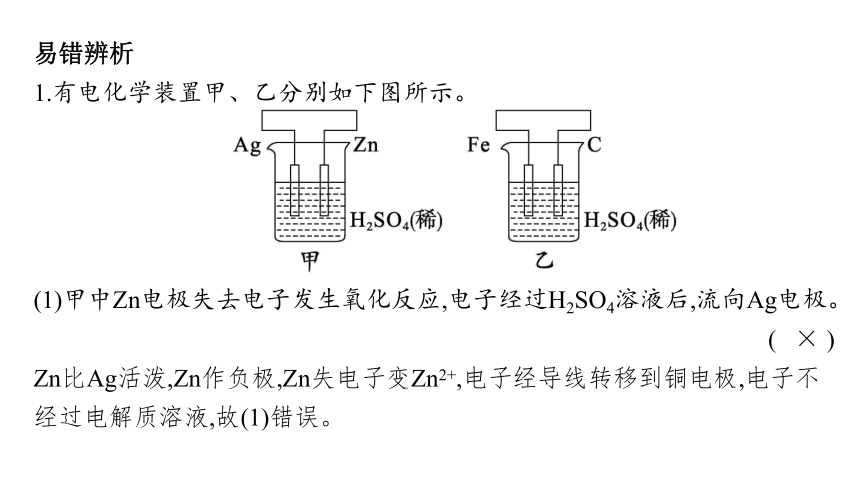
1.有电化学装置甲、乙分别如下图所示。
(1)甲中Zn电极失去电子发生氧化反应,电子经过H2SO4溶液后,流向Ag电极。
( )
×
Zn比Ag活泼,Zn作负极,Zn失电子变Zn2+,电子经导线转移到铜电极,电子不经过电解质溶液,故(1)错误。
(2)乙中H+向Fe电极方向移动。( )
2.实验室用铁片和稀硫酸反应制H2,加少量铜粉能使该反应速率加快。( )
×
Fe为较活泼电极,作负极,C作正极,电解质溶液中阳离子移向正极,则H+向C电极方向移动,故(2)错误。
√
铜、铁及稀硫酸构成原电池,能加快铁和稀硫酸的反应速率。
精研核心命题
命题点1新型化学电源及其分析
典例1 (2022·湖南卷)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的是( )
A.海水起电解质溶液作用
B.N极仅发生的电极反应:
2H2O+2e- ══ 2OH-+H2↑
C.玻璃陶瓷具有传递离子和防水的功能
D.该锂-海水电池属于一次电池
B
解析 海水中含有丰富的电解质,如氯化钠、氯化镁等,可作为电解质溶液,A正确。该电池的总反应可能为4Li+2H2O+O2 ══ 4LiOH,M极上Li失去电子发生氧化反应,则M电极为负极,电极反应为Li-e- ══ Li+,N极为正极,电极反应为O2+2H2O+4e- ══ 4OH-,B错误。Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,并能传递离子,C正确。该电池不可充电,属于一次电池,D正确。
变式演练(2023·湖南常德一模)目前科学家发明了一种利用微生物进行脱硫、脱氮的原电池装置,其基本原理如图所示(图中隔膜为质子交换膜)。下列有关说法正确的是( )
A.a极的电极反应为
B.H+从B室向A室迁移
C.电池工作时,线路中通过1 mol电子,
则在b极析出2.24 L N2
D.若用该电池给铅酸蓄电池充电,应将b极连在正极上
D
命题点2二次电池及其分析
典例2 (2022·广东卷)科学家基于Cl2易溶于CCl4的性质,发展了一种无需离子交换膜的新型氯流电池,可作储能设备(如图)。充电时电极a的反应为NaTi2(PO4)3+2Na++2e- ══ Na3Ti2(PO4)3。下列说法正确的是( )
A.充电时电极b是阴极
B.放电时NaCl溶液的pH减小
C.放电时NaCl溶液的浓度增大
D.每生成1 mol Cl2,电极a质量理论上增加23 g
C
解析 充电时电极a发生还原反应,则电极a是阴极,电极b是阳极,A错误;同一电极上放电时电极反应和充电时相反,由放电时电极a的反应Na3Ti2(PO4)3-2e- ══ NaTi2(PO4)3+2Na+可知,NaCl溶液的pH不变,B错误;放电时负极反应为Na3Ti2(PO4)3-2e- ══ NaTi2(PO4)3+2Na+,正极反应为Cl2+2e- ══ 2Cl-,反应后Na+和Cl-浓度都增大,则放电时NaCl溶液的浓度增大,C正确;充电时阳极反应为2Cl--2e- ══ Cl2↑,阴极反应为NaTi2(PO4)3+2Na++2e- ══ Na3Ti2(PO4)3,据得失电子守恒可知,每生成1 mol Cl2,电极a质量理论上增加23 g·mol-1×2 mol=46 g,D错误。
思路分析 解答本题的思路如下:
(1)分析充电时电极a的反应类型,判断电极a、b的名称。
(2)根据充电和放电时同一电极上物质变化相反,确定放电时电极a、b上发生的反应及NaCl溶液的变化。
(3)根据充电时电极a、b的反应,结合得失电子守恒,确定电极a质量的变化情况。
变式演练(2023·全国新课标卷)一种以V2O5和Zn为电极、Zn(CF3SO3)2水溶液为电解质溶液的电池,其示意图如下所示。放电时,Zn2+可插入V2O5层间形成ZnxV2O5·nH2O。下列说法错误的是( )
A.放电时V2O5为正极
B.放电时Zn2+由负极向正极迁移
C.充电总反应:xZn+V2O5+nH2O ══ ZnxV2O5·nH2O
D.充电阳极反应:ZnxV2O5·nH2O-2xe- ══ xZn2++V2O5+nH2O
C
解析 Zn为活泼金属,放电时发生氧化反应为电源的负极,则V2O5电极为正极,A正确;放电时,阳离子(Zn2+)由负极向正极迁移,B正确;xZn+V2O5+nH2O ══ ZnxV2O5·nH2O反应中Zn发生氧化反应,为放电总反应方程式,C错误;充电时阳极(原电池正极)重新生成V2O5,D正确。
【思维建模】解答二次电池的构成及原理类题目的思维模型
命题点3燃料电池及分析
典例3 (2021·山东卷)以KOH溶液为离子导体,分别组成CH3OH-O2、N2H4-O2、(CH3)2NNH2-O2清洁燃料电池,下列说法正确的是( )
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH3)2NNH2-O2燃料电池的理论放电量最大
D.消耗1 mol O2时,理论上N2H4-O2燃料电池气体产物的体积在标准状况下为11.2 L
C
解析 放电过程为原电池,阳离子向正极移动,K+均向正极移动,A错误;N2H4-O2燃料电池的产物为氮气和水,未消耗KOH,n(KOH)保持不变,其他两种燃料电池均消耗KOH,n(KOH)减小,B错误;理论放电量与燃料的物质的量和转移电子数有关,设消耗燃料的质量均为m g,则甲醇、N2H4和(CH3)2NNH2放电量分别为 ,通过比较可知(CH3)2NNH2的理论放电量最大,C正确;正极反应为O2+2H2O+4e- ══ 4OH-,消耗1 mol O2时电路中通过4 mol电子,根据 N2H4~N2~4e-可知,负极消耗1 mol N2H4,在标准状况下体积为22.4 L,D错误。
变式演练(2023·江西鹰潭一模)利用垃圾假单胞菌株分解有机化合物的电化学原理如图所示。下列说法正确的是( )
A.电子流向:电极B→负载→电极A
B.若有机化合物为葡萄糖,处理0.25 mol有机化合物,电路中转移电子6 mol
C.电极A上的反应为X-4e- ══ Y+4H+
D.若电极B上消耗氧气22.4 L,电极B区域溶液增重36 g
B
解析 由图可知,O2在电极B得电子生成H2O,则电极B为正极,电极A为负极,电子由负极流出沿导线流入正极,则电子流向:电极A→负载→电极B,A错误;葡萄糖分子式为C6H12O6,反应后生成CO2,C元素由0价升高到+4价,处理0.25 mol葡萄糖,电路中转移电子为0.25 mol×4×6=6 mol,B正确;电极A发生氧化反应,电极反应为X-2e- ══ Y+2H+,C错误;题目未说明氧气是否处于标准状况,无法计算22.4 L氧气的物质的量,D错误。
训练分层落实
练真题·明考向
1.(2023·辽宁卷)某低成本储能电池原理如图所示。下列说法正确的是( )
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧H+通过质子交换膜移向左侧
D.充电总反应:
B
2.(2023·全国乙卷)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应:
下列叙述错误的是( )
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为
D.炭化纤维素纸的作用是增强硫电极导电性能
A
练易错·避陷阱
3.(2023·北京朝阳区一模)将铜棒插入浓、稀Cu(NO3)2溶液中(装置如图),观察到电流计指针发生偏转,一段时间后,浸入浓Cu(NO3)2溶液的铜棒变粗。下列说法不正确的是( )
A.铜棒变粗的反应:Cu2++2e- ══ Cu
B.导线中电子移动的方向:b→a
C.随着反应的进行,浓、稀Cu(NO3)2溶液的浓度逐渐接近
D.Cu2+的氧化性随c(Cu2+)增大而增强,Cu的还原性随c(Cu2+)增大而减弱
B
解析 浸入浓Cu(NO3)2溶液的铜棒变粗,说明该电极有铜析出,则b侧电极为正极,电极反应为Cu2++2e- ══ Cu,A正确;导线中电子由负极移向正极,即a→b,B错误;随着反应的进行,右侧不断消耗Cu2+,左侧不断生成Cu2+,浓、稀Cu(NO3)2溶液的浓度逐渐接近,C正确;对比分析可知,Cu2+的氧化性随c(Cu2+)增大而增强,Cu的还原性随c(Cu2+)增大而减弱,D正确。
4.(2023·山东临沂一模)一种光照充电电池结构如图所示,充电时TiO2光辅助电极受光激发产生电子和空穴,空穴作用下NaI转化为NaI3。下列说法正确的是( )
A.充电过程中,光能最终转化为电能
B.充电效率与光照产生的电子和空穴量有关
C.放电时,M电极为正极,电极反应为 +6e- ══ 4S2-
D.放电时N电极室增加2 mol离子,理论上外电路转移1 mol电子
D
5.(2023·安徽淮北一模)一种新型电池装置如图所示,下列叙述错误的是( )
A.镍钴电极反应:N2H4+4OH--4e- ══ N2↑+4H2O
B.Ⅱ区的Na+通过a隔膜向Ⅰ区迁移,Cl-通过b隔膜向Ⅲ区迁移
C.该装置工作时总反应:N2H4+4OH-+4H+ ══ N2↑+4H2O
D.该装置工作时还利用了中和能
C
解析 镍钴电极上N2H4被氧化生成N2,则该电极是负极,电极反应为N2H4+4OH--4e- ══ N2↑+4H2O,A正确;原电池中阳离子向正极迁移,阴离子向负极迁移,Ⅱ区的Na+通过a隔膜向Ⅰ区迁移,Cl-通过b隔膜向Ⅲ区迁移,B正确;正、负极反应相加得到总反应,则该装置工作时的总反应为N2H4 ══ N2↑+2H2↑,C错误;根据正、负极反应可知,该装置工作时还利用了中和能,D正确。
练预测·押考向
6.一款低成本高能效的新型无隔膜铈铅单液流电池装置如图所示,该电池用石墨毡作电极,可溶性铈盐和铅盐的混合酸性溶液作电解质溶液。已知电池反应为Pb+2Ce4+ Pb2++2Ce3+。下列相关说法正确的是( )
A.放电时,Pb2+在b电极发生还原反应
B.该电池可用稀硫酸酸化电解质溶液
C.充电过程中,a电极发生的反应为Ce3+-e- ══ Ce4+
D.放电过程中,电解质溶液中
向a电极移动
D
解析 放电时a电极为负极,电极反应为Pb-2e- ══ Pb2+,在a电极发生氧化反应,A错误; 能与Pb2+反应生成PbSO4沉淀,故不能用稀硫酸酸化电解质溶液,B错误;充电过程中,a电极发生的反应为Pb2++2e- ══ Pb,C错误;放电过程中,电解质溶液中阴离子移向负极,故电解质溶液中的 向a电极移动,D正确。
7.铝-石墨双离子电池是一种全新的高效、低成本储能电池,电池反应为AlLi+CxPF6 Al+xC+Li++ ,电池装置如图所示。下列说法正确的是( )
A.AlLi合金作原电池的正极
B.放电时 移向正极
C.充电时,电路中转移1 mol电子,
阴极质量增加9 g
D.充电时,阳极反应为
xC+ -e- ══ CxPF6
D
8.水系可逆Zn-CO2电池在工作时,复合膜(由a、b膜复合而成,a膜只允许H+通过,b膜只允许OH-通过)层间的H2O解离成H+和OH-,在外加电场中可透过相应的离子膜定向移动。当闭合K1时,Zn-CO2电池工作原理如图所示,下列说法正确的是( )
A.闭合K1时,右侧电极反应为CO2+2H++2e- ══ HCOOH
B.闭合K1时,电池工作一段时间,复合膜两侧溶液的pH左侧升高右侧降低
C.闭合K2时,OH-从复合膜流向Zn电极
D.闭合K2时,每生成65 g Zn,同时一定生成CO2气体11.2 L
答案 A
解析 闭合K1时,Pd电极上物质转化为CO2→HCOOH,则Pd电极反应为CO2+2H++2e- ══ HCOOH,A正确;闭合K1时,Zn电极反应为Zn+4OH--2e- ══[Zn(OH)4]2-,复合膜层间的H2O解离成H+和OH-,移向两极的H+和OH-的物质的量相等,两电极转移电子数相等,则相当于左侧消耗了OH-,右侧未消耗H+,故复合膜两侧溶液的pH左侧降低,右侧不变,B错误;闭合K2时,该装置为电解池,左侧为阴极,右侧为阳极,OH-从Zn电极流向复合膜,C错误;没有指明是否为标准状况,无法计算CO2的体积,D错误。
专题 原电池原理和化学电源
考题统计
原电池原理和化学电源:
湖南卷(2023、2022、2021),广东卷(2023、2022),浙江卷(2022、2021),辽宁卷(2023、2022、2021),河北卷(2021),天津卷(2021、2020),山东卷(2023、2021),全国新课标卷(2023)
聚焦核心要点
要点1原电池的工作原理与应用
课标指引:1.认识化学能与电能相互转化的实际意义及其重要应用。
2.能分析、解释原电池的工作原理,能设计简单的原电池。
1.原电池的工作原理思维模型
2.原电池中电极反应和电池反应的书写方法
3.设计制作原电池的方法
要点2新型化学电源及分析
课标指引:1.能列举常见的化学电源,并能利用相关信息分析化学电源的工作原理。 2.能综合考虑化学变化中的物质变化和能量变化来分析、解决实际问题,如新型电池的开发等。
1.教材中化学电源装置的迁移应用
(1)二次电池装置
(2)燃料电池装置
2.分析二次电池类题目的思维模型
3.分析燃料电池类题目的思维模型
易错辨析
1.有电化学装置甲、乙分别如下图所示。
(1)甲中Zn电极失去电子发生氧化反应,电子经过H2SO4溶液后,流向Ag电极。
( )
×
Zn比Ag活泼,Zn作负极,Zn失电子变Zn2+,电子经导线转移到铜电极,电子不经过电解质溶液,故(1)错误。
(2)乙中H+向Fe电极方向移动。( )
2.实验室用铁片和稀硫酸反应制H2,加少量铜粉能使该反应速率加快。( )
×
Fe为较活泼电极,作负极,C作正极,电解质溶液中阳离子移向正极,则H+向C电极方向移动,故(2)错误。
√
铜、铁及稀硫酸构成原电池,能加快铁和稀硫酸的反应速率。
精研核心命题
命题点1新型化学电源及其分析
典例1 (2022·湖南卷)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的是( )
A.海水起电解质溶液作用
B.N极仅发生的电极反应:
2H2O+2e- ══ 2OH-+H2↑
C.玻璃陶瓷具有传递离子和防水的功能
D.该锂-海水电池属于一次电池
B
解析 海水中含有丰富的电解质,如氯化钠、氯化镁等,可作为电解质溶液,A正确。该电池的总反应可能为4Li+2H2O+O2 ══ 4LiOH,M极上Li失去电子发生氧化反应,则M电极为负极,电极反应为Li-e- ══ Li+,N极为正极,电极反应为O2+2H2O+4e- ══ 4OH-,B错误。Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,并能传递离子,C正确。该电池不可充电,属于一次电池,D正确。
变式演练(2023·湖南常德一模)目前科学家发明了一种利用微生物进行脱硫、脱氮的原电池装置,其基本原理如图所示(图中隔膜为质子交换膜)。下列有关说法正确的是( )
A.a极的电极反应为
B.H+从B室向A室迁移
C.电池工作时,线路中通过1 mol电子,
则在b极析出2.24 L N2
D.若用该电池给铅酸蓄电池充电,应将b极连在正极上
D
命题点2二次电池及其分析
典例2 (2022·广东卷)科学家基于Cl2易溶于CCl4的性质,发展了一种无需离子交换膜的新型氯流电池,可作储能设备(如图)。充电时电极a的反应为NaTi2(PO4)3+2Na++2e- ══ Na3Ti2(PO4)3。下列说法正确的是( )
A.充电时电极b是阴极
B.放电时NaCl溶液的pH减小
C.放电时NaCl溶液的浓度增大
D.每生成1 mol Cl2,电极a质量理论上增加23 g
C
解析 充电时电极a发生还原反应,则电极a是阴极,电极b是阳极,A错误;同一电极上放电时电极反应和充电时相反,由放电时电极a的反应Na3Ti2(PO4)3-2e- ══ NaTi2(PO4)3+2Na+可知,NaCl溶液的pH不变,B错误;放电时负极反应为Na3Ti2(PO4)3-2e- ══ NaTi2(PO4)3+2Na+,正极反应为Cl2+2e- ══ 2Cl-,反应后Na+和Cl-浓度都增大,则放电时NaCl溶液的浓度增大,C正确;充电时阳极反应为2Cl--2e- ══ Cl2↑,阴极反应为NaTi2(PO4)3+2Na++2e- ══ Na3Ti2(PO4)3,据得失电子守恒可知,每生成1 mol Cl2,电极a质量理论上增加23 g·mol-1×2 mol=46 g,D错误。
思路分析 解答本题的思路如下:
(1)分析充电时电极a的反应类型,判断电极a、b的名称。
(2)根据充电和放电时同一电极上物质变化相反,确定放电时电极a、b上发生的反应及NaCl溶液的变化。
(3)根据充电时电极a、b的反应,结合得失电子守恒,确定电极a质量的变化情况。
变式演练(2023·全国新课标卷)一种以V2O5和Zn为电极、Zn(CF3SO3)2水溶液为电解质溶液的电池,其示意图如下所示。放电时,Zn2+可插入V2O5层间形成ZnxV2O5·nH2O。下列说法错误的是( )
A.放电时V2O5为正极
B.放电时Zn2+由负极向正极迁移
C.充电总反应:xZn+V2O5+nH2O ══ ZnxV2O5·nH2O
D.充电阳极反应:ZnxV2O5·nH2O-2xe- ══ xZn2++V2O5+nH2O
C
解析 Zn为活泼金属,放电时发生氧化反应为电源的负极,则V2O5电极为正极,A正确;放电时,阳离子(Zn2+)由负极向正极迁移,B正确;xZn+V2O5+nH2O ══ ZnxV2O5·nH2O反应中Zn发生氧化反应,为放电总反应方程式,C错误;充电时阳极(原电池正极)重新生成V2O5,D正确。
【思维建模】解答二次电池的构成及原理类题目的思维模型
命题点3燃料电池及分析
典例3 (2021·山东卷)以KOH溶液为离子导体,分别组成CH3OH-O2、N2H4-O2、(CH3)2NNH2-O2清洁燃料电池,下列说法正确的是( )
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH3)2NNH2-O2燃料电池的理论放电量最大
D.消耗1 mol O2时,理论上N2H4-O2燃料电池气体产物的体积在标准状况下为11.2 L
C
解析 放电过程为原电池,阳离子向正极移动,K+均向正极移动,A错误;N2H4-O2燃料电池的产物为氮气和水,未消耗KOH,n(KOH)保持不变,其他两种燃料电池均消耗KOH,n(KOH)减小,B错误;理论放电量与燃料的物质的量和转移电子数有关,设消耗燃料的质量均为m g,则甲醇、N2H4和(CH3)2NNH2放电量分别为 ,通过比较可知(CH3)2NNH2的理论放电量最大,C正确;正极反应为O2+2H2O+4e- ══ 4OH-,消耗1 mol O2时电路中通过4 mol电子,根据 N2H4~N2~4e-可知,负极消耗1 mol N2H4,在标准状况下体积为22.4 L,D错误。
变式演练(2023·江西鹰潭一模)利用垃圾假单胞菌株分解有机化合物的电化学原理如图所示。下列说法正确的是( )
A.电子流向:电极B→负载→电极A
B.若有机化合物为葡萄糖,处理0.25 mol有机化合物,电路中转移电子6 mol
C.电极A上的反应为X-4e- ══ Y+4H+
D.若电极B上消耗氧气22.4 L,电极B区域溶液增重36 g
B
解析 由图可知,O2在电极B得电子生成H2O,则电极B为正极,电极A为负极,电子由负极流出沿导线流入正极,则电子流向:电极A→负载→电极B,A错误;葡萄糖分子式为C6H12O6,反应后生成CO2,C元素由0价升高到+4价,处理0.25 mol葡萄糖,电路中转移电子为0.25 mol×4×6=6 mol,B正确;电极A发生氧化反应,电极反应为X-2e- ══ Y+2H+,C错误;题目未说明氧气是否处于标准状况,无法计算22.4 L氧气的物质的量,D错误。
训练分层落实
练真题·明考向
1.(2023·辽宁卷)某低成本储能电池原理如图所示。下列说法正确的是( )
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧H+通过质子交换膜移向左侧
D.充电总反应:
B
2.(2023·全国乙卷)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应:
下列叙述错误的是( )
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为
D.炭化纤维素纸的作用是增强硫电极导电性能
A
练易错·避陷阱
3.(2023·北京朝阳区一模)将铜棒插入浓、稀Cu(NO3)2溶液中(装置如图),观察到电流计指针发生偏转,一段时间后,浸入浓Cu(NO3)2溶液的铜棒变粗。下列说法不正确的是( )
A.铜棒变粗的反应:Cu2++2e- ══ Cu
B.导线中电子移动的方向:b→a
C.随着反应的进行,浓、稀Cu(NO3)2溶液的浓度逐渐接近
D.Cu2+的氧化性随c(Cu2+)增大而增强,Cu的还原性随c(Cu2+)增大而减弱
B
解析 浸入浓Cu(NO3)2溶液的铜棒变粗,说明该电极有铜析出,则b侧电极为正极,电极反应为Cu2++2e- ══ Cu,A正确;导线中电子由负极移向正极,即a→b,B错误;随着反应的进行,右侧不断消耗Cu2+,左侧不断生成Cu2+,浓、稀Cu(NO3)2溶液的浓度逐渐接近,C正确;对比分析可知,Cu2+的氧化性随c(Cu2+)增大而增强,Cu的还原性随c(Cu2+)增大而减弱,D正确。
4.(2023·山东临沂一模)一种光照充电电池结构如图所示,充电时TiO2光辅助电极受光激发产生电子和空穴,空穴作用下NaI转化为NaI3。下列说法正确的是( )
A.充电过程中,光能最终转化为电能
B.充电效率与光照产生的电子和空穴量有关
C.放电时,M电极为正极,电极反应为 +6e- ══ 4S2-
D.放电时N电极室增加2 mol离子,理论上外电路转移1 mol电子
D
5.(2023·安徽淮北一模)一种新型电池装置如图所示,下列叙述错误的是( )
A.镍钴电极反应:N2H4+4OH--4e- ══ N2↑+4H2O
B.Ⅱ区的Na+通过a隔膜向Ⅰ区迁移,Cl-通过b隔膜向Ⅲ区迁移
C.该装置工作时总反应:N2H4+4OH-+4H+ ══ N2↑+4H2O
D.该装置工作时还利用了中和能
C
解析 镍钴电极上N2H4被氧化生成N2,则该电极是负极,电极反应为N2H4+4OH--4e- ══ N2↑+4H2O,A正确;原电池中阳离子向正极迁移,阴离子向负极迁移,Ⅱ区的Na+通过a隔膜向Ⅰ区迁移,Cl-通过b隔膜向Ⅲ区迁移,B正确;正、负极反应相加得到总反应,则该装置工作时的总反应为N2H4 ══ N2↑+2H2↑,C错误;根据正、负极反应可知,该装置工作时还利用了中和能,D正确。
练预测·押考向
6.一款低成本高能效的新型无隔膜铈铅单液流电池装置如图所示,该电池用石墨毡作电极,可溶性铈盐和铅盐的混合酸性溶液作电解质溶液。已知电池反应为Pb+2Ce4+ Pb2++2Ce3+。下列相关说法正确的是( )
A.放电时,Pb2+在b电极发生还原反应
B.该电池可用稀硫酸酸化电解质溶液
C.充电过程中,a电极发生的反应为Ce3+-e- ══ Ce4+
D.放电过程中,电解质溶液中
向a电极移动
D
解析 放电时a电极为负极,电极反应为Pb-2e- ══ Pb2+,在a电极发生氧化反应,A错误; 能与Pb2+反应生成PbSO4沉淀,故不能用稀硫酸酸化电解质溶液,B错误;充电过程中,a电极发生的反应为Pb2++2e- ══ Pb,C错误;放电过程中,电解质溶液中阴离子移向负极,故电解质溶液中的 向a电极移动,D正确。
7.铝-石墨双离子电池是一种全新的高效、低成本储能电池,电池反应为AlLi+CxPF6 Al+xC+Li++ ,电池装置如图所示。下列说法正确的是( )
A.AlLi合金作原电池的正极
B.放电时 移向正极
C.充电时,电路中转移1 mol电子,
阴极质量增加9 g
D.充电时,阳极反应为
xC+ -e- ══ CxPF6
D
8.水系可逆Zn-CO2电池在工作时,复合膜(由a、b膜复合而成,a膜只允许H+通过,b膜只允许OH-通过)层间的H2O解离成H+和OH-,在外加电场中可透过相应的离子膜定向移动。当闭合K1时,Zn-CO2电池工作原理如图所示,下列说法正确的是( )
A.闭合K1时,右侧电极反应为CO2+2H++2e- ══ HCOOH
B.闭合K1时,电池工作一段时间,复合膜两侧溶液的pH左侧升高右侧降低
C.闭合K2时,OH-从复合膜流向Zn电极
D.闭合K2时,每生成65 g Zn,同时一定生成CO2气体11.2 L
答案 A
解析 闭合K1时,Pd电极上物质转化为CO2→HCOOH,则Pd电极反应为CO2+2H++2e- ══ HCOOH,A正确;闭合K1时,Zn电极反应为Zn+4OH--2e- ══[Zn(OH)4]2-,复合膜层间的H2O解离成H+和OH-,移向两极的H+和OH-的物质的量相等,两电极转移电子数相等,则相当于左侧消耗了OH-,右侧未消耗H+,故复合膜两侧溶液的pH左侧降低,右侧不变,B错误;闭合K2时,该装置为电解池,左侧为阴极,右侧为阳极,OH-从Zn电极流向复合膜,C错误;没有指明是否为标准状况,无法计算CO2的体积,D错误。
同课章节目录
