2024苏教版高中化学选择性必修2同步练习题--第2课时 原子核外电子的排布(含解析)
文档属性
| 名称 | 2024苏教版高中化学选择性必修2同步练习题--第2课时 原子核外电子的排布(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-23 10:41:53 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
2024苏教版高中化学选择性必修2同步
第2课时 原子核外电子的排布
基础过关练
题组一 核外电子的排布原理
1.(经典题)(2022浙江诸暨期末)下列符号表述合理的是 ( )
A.4s1 B.2p10 C.2d6 D.3f14
2.(2022湖南长沙期末)下列说法中正确的是( )
A.多电子原子的所有电子在同一区域里运动
B.能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动
C.处于最低能量状态的原子叫基态原子
D.同一原子中,1s、2s、3s所能容纳的电子数越来越多
3.下列说法错误的是( )
A.原子核外电子填充3p、3d、4s能级的顺序为3p→4s→3d
B.某基态原子外围电子排布式为3d64s2
C.每个原子轨道最多容纳两个自旋状态相同的电子,称为泡利不相容原理
D.原子核外电子的运动遵循构造原理的三大内容:能量最低原理、泡利不相容原理和洪特规则
题组二 电子排布式
4.(2022重庆期末)“鸟巢”使用的钒氮合金钢具有高强度、高性能的特点,23V的外围电子排布式为( )
A.3d5 B.3d34s2 C.3d44s1 D.3d54s2
5.(2023河北保定期末)下列粒子中,外围电子排布式为3d5的是( )
A.Fe2+ B.Fe3+ C.Cu2+ D.Cu+
题组三 轨道表示式
下列对基态碳原子外围电子的轨道表示式的书写正确的是( )
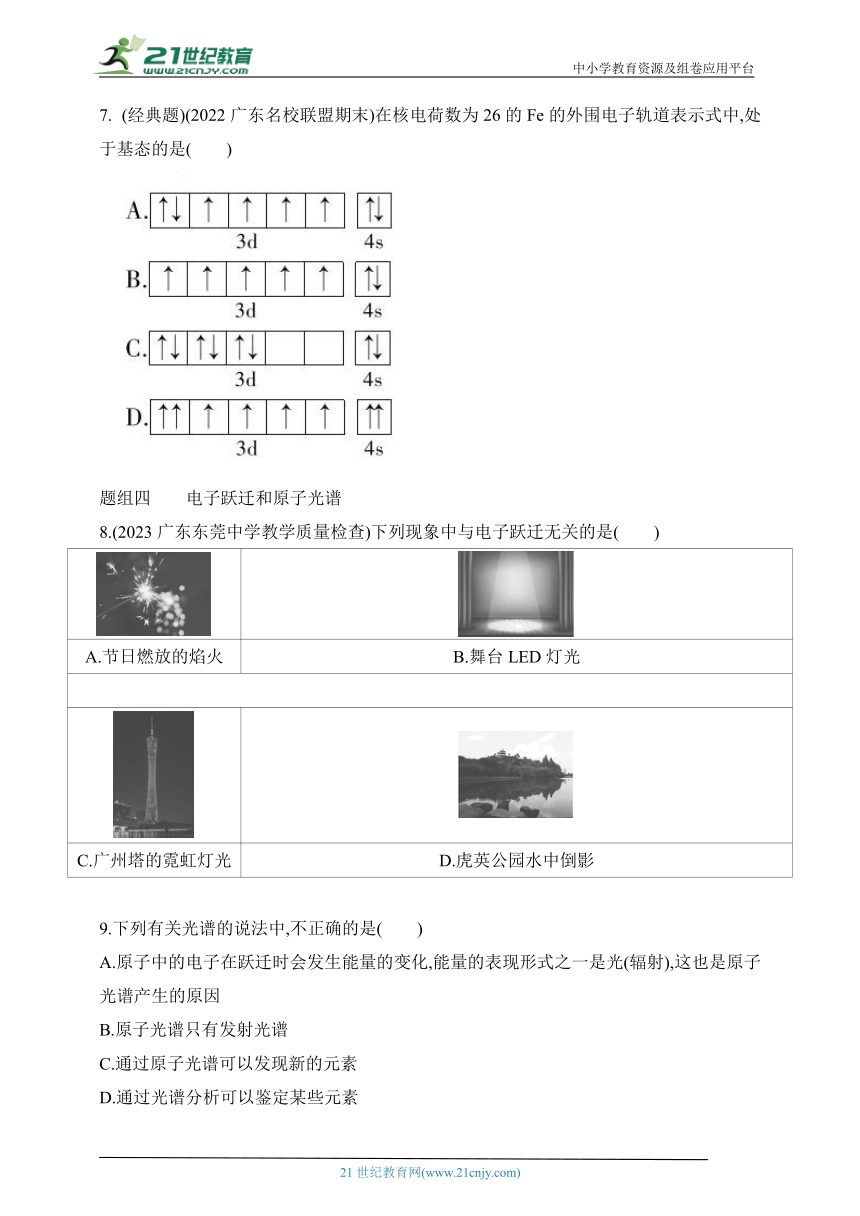
(经典题)(2022广东名校联盟期末)在核电荷数为26的Fe的外围电子轨道表示式中,处于基态的是( )
题组四 电子跃迁和原子光谱
8.(2023广东东莞中学教学质量检查)下列现象中与电子跃迁无关的是( )
A.节日燃放的焰火 B.舞台LED灯光
C.广州塔的霓虹灯光 D.虎英公园水中倒影
9.下列有关光谱的说法中,不正确的是( )
A.原子中的电子在跃迁时会发生能量的变化,能量的表现形式之一是光(辐射),这也是原子光谱产生的原因
B.原子光谱只有发射光谱
C.通过原子光谱可以发现新的元素
D.通过光谱分析可以鉴定某些元素
能力提升练
题组一 原子核外电子排布的表示方法
1.(2022四川资阳中学期中)某原子的电子排布式为 1s22s22p63s23p63d54s2,下列说法中不正确的是( )
A.该原子中共有 25 个电子
B.该原子核外有 4 个电子层
C.该原子共有7种能量不同的电子
D.该原子 M 电子层共有 8 个电子
2.(2023河北邢台教学质量检测,)下列化学用语表示正确的是( )
A.中子数为8的氮原子N
B.基态Cr原子的外围电子轨道表示式:
C.O原子的2s轨道:
D.F-的结构示意图:
3.(2023河北石家庄月考,)下列有关基态原子的电子排布式或轨道表示式的书写及结论错误的是( )
选项 电子排布式或轨道表示式 结论
A 违背洪特规则
B 书写正确
C 违背泡利不 相容原理
D 书写正确
4.(2022辽宁丹东期末)下列说法不正确的是( )
A.基态碳原子的轨道表示式:
B.基态原子的电子填充在6个轨道中的元素有两种
C.基态铜原子的简化电子排布式表示为[Ar]3d94s2,该说法违反了泡利不相容原理
D.基态钾离子(K+)电子占据的最高能级共有3个原子轨道,其形状是纺锤形
5.电影里早期的盔甲材料用的是军用卫星的金钛合金,而不是一般的钛合金。普通钢材在高空容易结冰,而金钛合金在高空完全不惧怕结冰的问题。回答下列问题:
(1)基态钛原子的核外电子排布式是 。
(2)Sm的外围电子排布式为4f66s2,Sm3+的外围电子排布式为 。
(3)基态铁原子外围电子的轨道表示式为 ;基态Fe3+核外电子排布式为 。
(4)基态锌原子核外电子排布式为 。
(5)氮原子的外围电子轨道表示式为 。
(6)基态Cu与Cu2+中未成对电子数之比为 。
题组二 根据原子特征推断核外电子排布
6.某元素原子质量数为60,中子数为35,其基态原子未成对电子数为 ( )
A.0 B.1 C.5 D.3
7.(2023河北唐山高二期末)某元素基态原子外围电子排布式为3d24s2,下列说法正确的是( )
A.该元素原子处于最低能量状态时,原子中共有4个未成对电子
B.该元素基态原子核外有4个电子层填充有电子
C.该元素原子的M层共有8个电子
D.该元素原子的最外层共有4个电子
题组三 利用核外电子的排布推断元素
8.(2022浙江北斗星盟阶段性联考)下列各组原子中化学性质一定相似的是( )
A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子
C.2p轨道上有一个未成对电子的X原子和3p轨道上有一个未成对电子的Y原子
D.L层上有一个空轨道的原子和M层的p轨道上有一个空轨道的原子
9.(2022四川雅安期末检测)下列各组基态原子中,X和Y一定是同一主族元素的是( )
选项 X原子 Y原子
A 1s2 [Ar]4s2
B M层上有1个电子 N层上有1个电子
C 2p轨道上有2个未成对电子 3p轨道上有2个未成对电子
D L层2p轨道上只有一个空轨道 M层3p轨道上只有一个空轨道
10.下列各项原子中,一定不属于同种元素原子的是( )
A.3p能级有一个未成对电子的基态原子和核外电子排布式为1s22s22p63s23p1的原子
B.M层全充满而N层为4s2的原子和核外电子排布式为1s22s22p63s23p63d104s2的原子
C.最外层电子数是核外电子总数的的原子和外围电子排布式为3s23p5的原子
D.2p能级有一个空轨道的基态原子和原子的外围电子排布式为2s22p2的原子
11.有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素,A和E属同一族,它们原子的最外层电子排布式为ns1;B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍;C原子最外层电子数等于D原子最外层电子数的一半。请回答下列问题:
(1)A是 ,B是 ,C是 ,D是 ,E是 。
(2)由这5种元素组成的一种化合物是 (写化学式)。写出该物质的一种主要用途: 。
(3)写出C元素基态原子的电子排布式: 。
(4)D元素原子的外围电子排布式为 。
12.(2022湖北部分省级示范高中期末)X、Y、Z、M、Q、R是元素周期表前四周期的元素,且原子序数依次增大,其相关信息如下表所示:
元素 相关信息
X 原子核外有6种不同运动状态的电子
Y 基态原子中s电子总数与p电子总数相同,是一种非金属元素
Z 形成的氧化物和强酸、强碱都可以反应
M 基态原子的最外层p轨道上有两个电子的自旋状态与其他电子的自旋状态不同
Q 前四周期元素原子核外电子排布中未成对电子数最多的元素
R 基态原子核外有7个能级上有电子,且其外围电子数为8
(1)写出元素Q的基态原子的外围电子轨道表示式: 。
(2)X、Y、Z三种元素的原子半径由小到大的顺序是 (用元素符号表示)。
(3)M元素的基态原子中能量最高的电子的电子云在空间有 个伸展方向,原子轨道呈 形。
(4)小范同学写了某基态原子的两个外围电子的表达式,分析其分别违反了什么原理:
①3s13p4: ;
第2课时 原子核外电子的排布
基础过关练
对应主书P12
1.A 2.C 3.C 4.B 5.B 6.D 7.A 8.D
9.B
1.A p轨道最多能容纳6个电子,2p10不合理,B错误;第二电子层只有s、p轨道,不存在2d轨道,C错误;第三电子层只有s、p、d轨道,不存在3f轨道,D错误。
2.C 原子核外有多个电子时,电子的能量不尽相同,电子不可能都在同一区域里运动,而是分层排布的,A项错误;能量低的电子在离核较近的区域运动,能量高的电子在离核较远的区域运动,B项错误;能量越低越稳定,基态原子的能量最低,C项正确;s轨道最多容纳2个电子,与其所在电子层无关,D项错误。
3.C 根据构造原理知核外电子填充顺序为3p→4s→3d,A项正确;基态铁原子的外围电子排布式为3d64s2,B项正确;每个原子轨道最多容纳两个自旋状态不同的电子,称为泡利不相容原理,C项错误;原子核外电子的运动(也称原子核外电子的排布)遵循构造原理的三大内容:能量最低原理、泡利不相容原理和洪特规则,D项正确。
4.B V的原子序数为23,基态V原子的电子排布式是1s22s22p63s23p63d34s2,V原子的外围电子排布式是3d34s2,选B。
5.B Fe的电子排布式是1s22s22p63s23p63d64s2,则Fe2+的外围电子排布式为3d6,Fe3+的外围电子排布式为3d5,A项错误,B项正确;基态Cu的电子排布式是1s22s22p63s23p63d104s1,则Cu2+的外围电子排布式为3d9,Cu+的外围电子排布式为3d10,C、D项错误。
6.D A项不能表示基态碳原子,错误;在2p轨道上的两个不同轨道上的电子自旋状态应该相同,B项违反了洪特规则,错误;C项违反了能量最低原理,此轨道表示式为激发态碳原子的外围电子轨道表示式,错误。
7.A Fe为26号元素,基态铁原子核外电子排布式为1s22s22p63s23p63d64s2,其外围电子轨道表示式为
选A。
8.D 能看到水中倒影是光线反射的结果,与电子跃迁无关。电子从具有较高能量的激发态跃迁到较低能量的激发态或基态,释放能量,光是释放能量的重要形式之一,节日燃放的焰火、舞台LED灯光、广州塔的霓虹灯光均与电子发生跃迁有关,选D。
9.B 原子光谱有吸收光谱和发射光谱,故B项错误。
能力提升练
对应主书P13
1.D 2.C 3.B 4.C 6.C 7.B 8.D 9.D
10.C
1.D 该原子中共有2+8+13+2=25个电子,A正确;由该原子的电子排布式可知,其核外有4个电子层,B正确;处于相同能级的电子具有相同的能量,该原子中1s、2s、2p、3s、3p、3d、4s 7个能级中填充有电子,C正确;该原子M电子层共有2+6+5=13个电子,D错误。
2.C 中子数为8的氮原子表示为N,A错误;基态Cr原子的外围电子轨道表示式:
B错误;s轨道为球形,C正确;F-的核电荷数为9,D错误。
3.B 当电子排布在能量相同的各个轨道时,总是优先单独占据一个轨道,且自旋状态相同,所以2p能级上轨道表示式违背了洪特规则,A正确;原子核外电子先占据能量较低的轨道,然后依次进入能量较高的轨道,该电子排布式违背了能量最低原理,B错误;每个原子轨道最多容纳2个自旋状态不同的电子,题给轨道表示式违背泡利不相容原理,C正确;1s22s22p63s23p63d54s1为基态Cr的电子排布式,书写正确,D正确。
4.C 基态C原子中电子占据3个能级,分别位于1s、2s、2p能级,且每个能级有2个电子,其轨道表示式为
A正确;s能级中含有1个轨道,p能级含有3个轨道,满足基态原子的核外电子填充在6个轨道中的原子的核外电子排布式有1s22s22p63s1、1s22s22p63s2,分别为Na、Mg,B正确;Cu是29号元素,其基态原子外围电子排布式为3d104s1,[Ar]3d94s2违反了能量最低原理,C错误;基态K+的电子占据的最高能级为3p能级,共有3个原子轨道,其形状为纺锤形,D正确。
5.答案 (1)1s22s22p63s23p63d24s2
(2)4f5
(3)
[Ar]3d5或1s22s22p63s23p63d5
(4)1s22s22p63s23p63d104s2或[Ar]3d104s2
(5)
(6)1∶1
解析 (1)基态钛原子的核外电子排布式是1s22s22p63s23p63d24s2。
(2)Sm的外围电子排布式为4f66s2,失去3个电子变成Sm3+,则Sm3+的外围电子排布式为4f5。
(3)基态铁原子的外围电子轨道表示式为,
其核外电子排布式为[Ar]3d64s2,则Fe3+核外电子排布式为[Ar]3d5或1s22s22p63s23p63d5。
(4)Zn为第4周期第ⅡB族元素,Zn的电子排布式为1s22s22p63s23p63d104s2或[Ar]3d104s2。
(5)氮原子的外围电子轨道表示式为
(6)基态Cu原子的核外电子排布式为1s22s22p63s23p63d104s1,有1个未成对电子;Cu2+的核外电子排布式为1s22s22p63s23p63d9,有1个未成对电子。
6.C 根据质量数=质子数+中子数,可知该原子的质子数为60-35=25,为Mn,基态Mn原子的核外电子排布式为1s22s22p63s23p63d54s2,3d能级上的5个电子均为未成对电子,C正确。
7.B 外围电子排布为3d24s2的原子为Ti,该原子中只有3d轨道中的两个电子为未成对电子,A错误;该元素位于第四周期,其基态原子核外有4个电子层填充有电子,B正确;该元素原子M层的电子排布式为3s23p63d2,共有10个电子,C错误;该元素原子的最外层即第四层,只有2个电子,D错误。
8.D 原子核外电子排布式为1s2的原子为He,1s22s2为Be的电子排布式,He与Be的性质不相似,A错误;X原子为Mg,N层上仅有2个电子的原子有多种,如Y可能为Ca、Fe等,X和Y的化学性质不一定相似,B错误;2p轨道上有一个未成对电子的X原子可能是B或F,3p轨道上有一个未成对电子的Y原子可能是Al或Cl,X和Y的化学性质不一定相似,C错误;L层上有一个空轨道的原子的电子排布式为1s22s22p2,是C,M层的p轨道上有一个空轨道的原子的电子排布式为1s22s22p63s23p2,是Si,两者位于同一主族,化学性质相似,D正确。
9.D 电子排布式为1s2的原子对应的元素是He,电子排布式为[Ar]4s2的原子对应的元素为Ca,前者为0族元素,后者为第ⅡA族元素,A不符合题意;M层上有1个电子的原子对应的元素为Na,N层上有1个电子的原子对应的元素可能是K、Cr、Cu,B不符合题意;2p轨道上有2个未成对电子的原子对应的元素可能是C或O,3p轨道上有2个未成对电子的原子对应的元素可能是Si或S,它们可能属于同一主族,也可能不属于同一主族,C不符合题意;L层2p轨道上只有一个空轨道的原子对应的元素为C,M层3p轨道上只有一个空轨道的原子对应的元素为Si,它们属于同一主族,D符合题意。
10.C 3p能级有一个未成对电子的基态原子,该原子3p能级有1个电子或5个电子,核外电子排布式为1s22s22p63s23p1或1s22s22p63s23p5,故A不符合题意。M层全充满而N层为4s2的原子的核外电子排布式为1s22s22p63s23p63d104s2,故B不符合题意。外围电子排布式为3s23p5的原子核外有17个电子,最外层电子数是核外电子总数的,故C符合题意。2p能级有一个空轨道的基态原子的2p能级有2个电子,其外围电子排布式为2s22p2,故D不符合题意。
11.答案 (1)H O Al S K(写元素名称也可)
(2)KAl(SO4)2·12H2O 作净水剂
(3)1s22s22p63s23p1
(4)3s23p4
解析 由B和D属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,可得B、D的最外层电子排布式为ns2np4,结合5种元素的核电荷数依次增大且都小于20,知B为氧元素、D为硫元素;A和E属同一族,它们原子的最外层电子排布式为ns1,且A为非金属元素,E的核电荷数大于D,所以A为氢元素,E为钾元素;C原子最外层电子数等于D原子最外层电子数的一半,且C核电荷数大于B,所以C原子的最外层电子排布式为3s23p1,即C为铝元素。
12.答案 (1)
(2)O(3)3 纺锤
(4)①能量最低原理 ②泡利不相容原理
解析 X原子核外有6种不同运动状态的电子,则X是C元素;基态Y原子中s电子总数与p电子总数相同,则Y原子核外电子排布可能是1s22s22p4或1s22s22p63s2,又因Y为非金属元素,所以Y是O元素;Z形成的氧化物和强酸、强碱都可以反应,则Z是Al元素;M基态原子的最外层p轨道上有两个电子的自旋状态与其他电子的自旋状态不同,则M原子的电子排布式为1s22s22p63s23p5,则M是Cl元素;Q是前四周期元素原子核外电子排布中未成对电子数最多的元素,则Q是Cr元素;基态R原子核外有7个能级上有电子,且其外围电子数为8,则R的电子排布式为1s22s22p63s23p63d64s2,则R是Fe元素。(1)Q是Cr,其电子排布式为1s22s22p63s23p63d54s1,外围电子轨道表示式为
。(2)X是C,Y是O,Z是Al,原子半径由小到大的顺序为:O违反了泡利不相容原理。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024苏教版高中化学选择性必修2同步
第2课时 原子核外电子的排布
基础过关练
题组一 核外电子的排布原理
1.(经典题)(2022浙江诸暨期末)下列符号表述合理的是 ( )
A.4s1 B.2p10 C.2d6 D.3f14
2.(2022湖南长沙期末)下列说法中正确的是( )
A.多电子原子的所有电子在同一区域里运动
B.能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动
C.处于最低能量状态的原子叫基态原子
D.同一原子中,1s、2s、3s所能容纳的电子数越来越多
3.下列说法错误的是( )
A.原子核外电子填充3p、3d、4s能级的顺序为3p→4s→3d
B.某基态原子外围电子排布式为3d64s2
C.每个原子轨道最多容纳两个自旋状态相同的电子,称为泡利不相容原理
D.原子核外电子的运动遵循构造原理的三大内容:能量最低原理、泡利不相容原理和洪特规则
题组二 电子排布式
4.(2022重庆期末)“鸟巢”使用的钒氮合金钢具有高强度、高性能的特点,23V的外围电子排布式为( )
A.3d5 B.3d34s2 C.3d44s1 D.3d54s2
5.(2023河北保定期末)下列粒子中,外围电子排布式为3d5的是( )
A.Fe2+ B.Fe3+ C.Cu2+ D.Cu+
题组三 轨道表示式
下列对基态碳原子外围电子的轨道表示式的书写正确的是( )
(经典题)(2022广东名校联盟期末)在核电荷数为26的Fe的外围电子轨道表示式中,处于基态的是( )
题组四 电子跃迁和原子光谱
8.(2023广东东莞中学教学质量检查)下列现象中与电子跃迁无关的是( )
A.节日燃放的焰火 B.舞台LED灯光
C.广州塔的霓虹灯光 D.虎英公园水中倒影
9.下列有关光谱的说法中,不正确的是( )
A.原子中的电子在跃迁时会发生能量的变化,能量的表现形式之一是光(辐射),这也是原子光谱产生的原因
B.原子光谱只有发射光谱
C.通过原子光谱可以发现新的元素
D.通过光谱分析可以鉴定某些元素
能力提升练
题组一 原子核外电子排布的表示方法
1.(2022四川资阳中学期中)某原子的电子排布式为 1s22s22p63s23p63d54s2,下列说法中不正确的是( )
A.该原子中共有 25 个电子
B.该原子核外有 4 个电子层
C.该原子共有7种能量不同的电子
D.该原子 M 电子层共有 8 个电子
2.(2023河北邢台教学质量检测,)下列化学用语表示正确的是( )
A.中子数为8的氮原子N
B.基态Cr原子的外围电子轨道表示式:
C.O原子的2s轨道:
D.F-的结构示意图:
3.(2023河北石家庄月考,)下列有关基态原子的电子排布式或轨道表示式的书写及结论错误的是( )
选项 电子排布式或轨道表示式 结论
A 违背洪特规则
B 书写正确
C 违背泡利不 相容原理
D 书写正确
4.(2022辽宁丹东期末)下列说法不正确的是( )
A.基态碳原子的轨道表示式:
B.基态原子的电子填充在6个轨道中的元素有两种
C.基态铜原子的简化电子排布式表示为[Ar]3d94s2,该说法违反了泡利不相容原理
D.基态钾离子(K+)电子占据的最高能级共有3个原子轨道,其形状是纺锤形
5.电影里早期的盔甲材料用的是军用卫星的金钛合金,而不是一般的钛合金。普通钢材在高空容易结冰,而金钛合金在高空完全不惧怕结冰的问题。回答下列问题:
(1)基态钛原子的核外电子排布式是 。
(2)Sm的外围电子排布式为4f66s2,Sm3+的外围电子排布式为 。
(3)基态铁原子外围电子的轨道表示式为 ;基态Fe3+核外电子排布式为 。
(4)基态锌原子核外电子排布式为 。
(5)氮原子的外围电子轨道表示式为 。
(6)基态Cu与Cu2+中未成对电子数之比为 。
题组二 根据原子特征推断核外电子排布
6.某元素原子质量数为60,中子数为35,其基态原子未成对电子数为 ( )
A.0 B.1 C.5 D.3
7.(2023河北唐山高二期末)某元素基态原子外围电子排布式为3d24s2,下列说法正确的是( )
A.该元素原子处于最低能量状态时,原子中共有4个未成对电子
B.该元素基态原子核外有4个电子层填充有电子
C.该元素原子的M层共有8个电子
D.该元素原子的最外层共有4个电子
题组三 利用核外电子的排布推断元素
8.(2022浙江北斗星盟阶段性联考)下列各组原子中化学性质一定相似的是( )
A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子
C.2p轨道上有一个未成对电子的X原子和3p轨道上有一个未成对电子的Y原子
D.L层上有一个空轨道的原子和M层的p轨道上有一个空轨道的原子
9.(2022四川雅安期末检测)下列各组基态原子中,X和Y一定是同一主族元素的是( )
选项 X原子 Y原子
A 1s2 [Ar]4s2
B M层上有1个电子 N层上有1个电子
C 2p轨道上有2个未成对电子 3p轨道上有2个未成对电子
D L层2p轨道上只有一个空轨道 M层3p轨道上只有一个空轨道
10.下列各项原子中,一定不属于同种元素原子的是( )
A.3p能级有一个未成对电子的基态原子和核外电子排布式为1s22s22p63s23p1的原子
B.M层全充满而N层为4s2的原子和核外电子排布式为1s22s22p63s23p63d104s2的原子
C.最外层电子数是核外电子总数的的原子和外围电子排布式为3s23p5的原子
D.2p能级有一个空轨道的基态原子和原子的外围电子排布式为2s22p2的原子
11.有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素,A和E属同一族,它们原子的最外层电子排布式为ns1;B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍;C原子最外层电子数等于D原子最外层电子数的一半。请回答下列问题:
(1)A是 ,B是 ,C是 ,D是 ,E是 。
(2)由这5种元素组成的一种化合物是 (写化学式)。写出该物质的一种主要用途: 。
(3)写出C元素基态原子的电子排布式: 。
(4)D元素原子的外围电子排布式为 。
12.(2022湖北部分省级示范高中期末)X、Y、Z、M、Q、R是元素周期表前四周期的元素,且原子序数依次增大,其相关信息如下表所示:
元素 相关信息
X 原子核外有6种不同运动状态的电子
Y 基态原子中s电子总数与p电子总数相同,是一种非金属元素
Z 形成的氧化物和强酸、强碱都可以反应
M 基态原子的最外层p轨道上有两个电子的自旋状态与其他电子的自旋状态不同
Q 前四周期元素原子核外电子排布中未成对电子数最多的元素
R 基态原子核外有7个能级上有电子,且其外围电子数为8
(1)写出元素Q的基态原子的外围电子轨道表示式: 。
(2)X、Y、Z三种元素的原子半径由小到大的顺序是 (用元素符号表示)。
(3)M元素的基态原子中能量最高的电子的电子云在空间有 个伸展方向,原子轨道呈 形。
(4)小范同学写了某基态原子的两个外围电子的表达式,分析其分别违反了什么原理:
①3s13p4: ;
第2课时 原子核外电子的排布
基础过关练
对应主书P12
1.A 2.C 3.C 4.B 5.B 6.D 7.A 8.D
9.B
1.A p轨道最多能容纳6个电子,2p10不合理,B错误;第二电子层只有s、p轨道,不存在2d轨道,C错误;第三电子层只有s、p、d轨道,不存在3f轨道,D错误。
2.C 原子核外有多个电子时,电子的能量不尽相同,电子不可能都在同一区域里运动,而是分层排布的,A项错误;能量低的电子在离核较近的区域运动,能量高的电子在离核较远的区域运动,B项错误;能量越低越稳定,基态原子的能量最低,C项正确;s轨道最多容纳2个电子,与其所在电子层无关,D项错误。
3.C 根据构造原理知核外电子填充顺序为3p→4s→3d,A项正确;基态铁原子的外围电子排布式为3d64s2,B项正确;每个原子轨道最多容纳两个自旋状态不同的电子,称为泡利不相容原理,C项错误;原子核外电子的运动(也称原子核外电子的排布)遵循构造原理的三大内容:能量最低原理、泡利不相容原理和洪特规则,D项正确。
4.B V的原子序数为23,基态V原子的电子排布式是1s22s22p63s23p63d34s2,V原子的外围电子排布式是3d34s2,选B。
5.B Fe的电子排布式是1s22s22p63s23p63d64s2,则Fe2+的外围电子排布式为3d6,Fe3+的外围电子排布式为3d5,A项错误,B项正确;基态Cu的电子排布式是1s22s22p63s23p63d104s1,则Cu2+的外围电子排布式为3d9,Cu+的外围电子排布式为3d10,C、D项错误。
6.D A项不能表示基态碳原子,错误;在2p轨道上的两个不同轨道上的电子自旋状态应该相同,B项违反了洪特规则,错误;C项违反了能量最低原理,此轨道表示式为激发态碳原子的外围电子轨道表示式,错误。
7.A Fe为26号元素,基态铁原子核外电子排布式为1s22s22p63s23p63d64s2,其外围电子轨道表示式为
选A。
8.D 能看到水中倒影是光线反射的结果,与电子跃迁无关。电子从具有较高能量的激发态跃迁到较低能量的激发态或基态,释放能量,光是释放能量的重要形式之一,节日燃放的焰火、舞台LED灯光、广州塔的霓虹灯光均与电子发生跃迁有关,选D。
9.B 原子光谱有吸收光谱和发射光谱,故B项错误。
能力提升练
对应主书P13
1.D 2.C 3.B 4.C 6.C 7.B 8.D 9.D
10.C
1.D 该原子中共有2+8+13+2=25个电子,A正确;由该原子的电子排布式可知,其核外有4个电子层,B正确;处于相同能级的电子具有相同的能量,该原子中1s、2s、2p、3s、3p、3d、4s 7个能级中填充有电子,C正确;该原子M电子层共有2+6+5=13个电子,D错误。
2.C 中子数为8的氮原子表示为N,A错误;基态Cr原子的外围电子轨道表示式:
B错误;s轨道为球形,C正确;F-的核电荷数为9,D错误。
3.B 当电子排布在能量相同的各个轨道时,总是优先单独占据一个轨道,且自旋状态相同,所以2p能级上轨道表示式违背了洪特规则,A正确;原子核外电子先占据能量较低的轨道,然后依次进入能量较高的轨道,该电子排布式违背了能量最低原理,B错误;每个原子轨道最多容纳2个自旋状态不同的电子,题给轨道表示式违背泡利不相容原理,C正确;1s22s22p63s23p63d54s1为基态Cr的电子排布式,书写正确,D正确。
4.C 基态C原子中电子占据3个能级,分别位于1s、2s、2p能级,且每个能级有2个电子,其轨道表示式为
A正确;s能级中含有1个轨道,p能级含有3个轨道,满足基态原子的核外电子填充在6个轨道中的原子的核外电子排布式有1s22s22p63s1、1s22s22p63s2,分别为Na、Mg,B正确;Cu是29号元素,其基态原子外围电子排布式为3d104s1,[Ar]3d94s2违反了能量最低原理,C错误;基态K+的电子占据的最高能级为3p能级,共有3个原子轨道,其形状为纺锤形,D正确。
5.答案 (1)1s22s22p63s23p63d24s2
(2)4f5
(3)
[Ar]3d5或1s22s22p63s23p63d5
(4)1s22s22p63s23p63d104s2或[Ar]3d104s2
(5)
(6)1∶1
解析 (1)基态钛原子的核外电子排布式是1s22s22p63s23p63d24s2。
(2)Sm的外围电子排布式为4f66s2,失去3个电子变成Sm3+,则Sm3+的外围电子排布式为4f5。
(3)基态铁原子的外围电子轨道表示式为,
其核外电子排布式为[Ar]3d64s2,则Fe3+核外电子排布式为[Ar]3d5或1s22s22p63s23p63d5。
(4)Zn为第4周期第ⅡB族元素,Zn的电子排布式为1s22s22p63s23p63d104s2或[Ar]3d104s2。
(5)氮原子的外围电子轨道表示式为
(6)基态Cu原子的核外电子排布式为1s22s22p63s23p63d104s1,有1个未成对电子;Cu2+的核外电子排布式为1s22s22p63s23p63d9,有1个未成对电子。
6.C 根据质量数=质子数+中子数,可知该原子的质子数为60-35=25,为Mn,基态Mn原子的核外电子排布式为1s22s22p63s23p63d54s2,3d能级上的5个电子均为未成对电子,C正确。
7.B 外围电子排布为3d24s2的原子为Ti,该原子中只有3d轨道中的两个电子为未成对电子,A错误;该元素位于第四周期,其基态原子核外有4个电子层填充有电子,B正确;该元素原子M层的电子排布式为3s23p63d2,共有10个电子,C错误;该元素原子的最外层即第四层,只有2个电子,D错误。
8.D 原子核外电子排布式为1s2的原子为He,1s22s2为Be的电子排布式,He与Be的性质不相似,A错误;X原子为Mg,N层上仅有2个电子的原子有多种,如Y可能为Ca、Fe等,X和Y的化学性质不一定相似,B错误;2p轨道上有一个未成对电子的X原子可能是B或F,3p轨道上有一个未成对电子的Y原子可能是Al或Cl,X和Y的化学性质不一定相似,C错误;L层上有一个空轨道的原子的电子排布式为1s22s22p2,是C,M层的p轨道上有一个空轨道的原子的电子排布式为1s22s22p63s23p2,是Si,两者位于同一主族,化学性质相似,D正确。
9.D 电子排布式为1s2的原子对应的元素是He,电子排布式为[Ar]4s2的原子对应的元素为Ca,前者为0族元素,后者为第ⅡA族元素,A不符合题意;M层上有1个电子的原子对应的元素为Na,N层上有1个电子的原子对应的元素可能是K、Cr、Cu,B不符合题意;2p轨道上有2个未成对电子的原子对应的元素可能是C或O,3p轨道上有2个未成对电子的原子对应的元素可能是Si或S,它们可能属于同一主族,也可能不属于同一主族,C不符合题意;L层2p轨道上只有一个空轨道的原子对应的元素为C,M层3p轨道上只有一个空轨道的原子对应的元素为Si,它们属于同一主族,D符合题意。
10.C 3p能级有一个未成对电子的基态原子,该原子3p能级有1个电子或5个电子,核外电子排布式为1s22s22p63s23p1或1s22s22p63s23p5,故A不符合题意。M层全充满而N层为4s2的原子的核外电子排布式为1s22s22p63s23p63d104s2,故B不符合题意。外围电子排布式为3s23p5的原子核外有17个电子,最外层电子数是核外电子总数的,故C符合题意。2p能级有一个空轨道的基态原子的2p能级有2个电子,其外围电子排布式为2s22p2,故D不符合题意。
11.答案 (1)H O Al S K(写元素名称也可)
(2)KAl(SO4)2·12H2O 作净水剂
(3)1s22s22p63s23p1
(4)3s23p4
解析 由B和D属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,可得B、D的最外层电子排布式为ns2np4,结合5种元素的核电荷数依次增大且都小于20,知B为氧元素、D为硫元素;A和E属同一族,它们原子的最外层电子排布式为ns1,且A为非金属元素,E的核电荷数大于D,所以A为氢元素,E为钾元素;C原子最外层电子数等于D原子最外层电子数的一半,且C核电荷数大于B,所以C原子的最外层电子排布式为3s23p1,即C为铝元素。
12.答案 (1)
(2)O
(4)①能量最低原理 ②泡利不相容原理
解析 X原子核外有6种不同运动状态的电子,则X是C元素;基态Y原子中s电子总数与p电子总数相同,则Y原子核外电子排布可能是1s22s22p4或1s22s22p63s2,又因Y为非金属元素,所以Y是O元素;Z形成的氧化物和强酸、强碱都可以反应,则Z是Al元素;M基态原子的最外层p轨道上有两个电子的自旋状态与其他电子的自旋状态不同,则M原子的电子排布式为1s22s22p63s23p5,则M是Cl元素;Q是前四周期元素原子核外电子排布中未成对电子数最多的元素,则Q是Cr元素;基态R原子核外有7个能级上有电子,且其外围电子数为8,则R的电子排布式为1s22s22p63s23p63d64s2,则R是Fe元素。(1)Q是Cr,其电子排布式为1s22s22p63s23p63d54s1,外围电子轨道表示式为
。(2)X是C,Y是O,Z是Al,原子半径由小到大的顺序为:O
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
