2024苏教版高中化学选择性必修3同步练习题--专题5 药物合成的重要原料——卤代烃、胺、酰胺(含解析)
文档属性
| 名称 | 2024苏教版高中化学选择性必修3同步练习题--专题5 药物合成的重要原料——卤代烃、胺、酰胺(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-23 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2024苏教版高中化学选择性必修3同步
专题5 药物合成的重要原料——
卤代烃、胺、酰胺
注意事项 1.全卷满分100分。考试用时90分钟。
2.可能用到的相对原子质量:H-1 C-12 N-14 O-16。
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一个选项符合题目要求)
1.下列说法错误的是( )
A.石油在国民经济中的地位非常重要,被誉为“工业的血液”
B.乙烯的产量可以用来衡量一个国家的石油化工发展水平
C.氟利昂是含有氟和氯的烷烃衍生物,性质不稳定、难液化,曾被用作制冷剂,但是因其有毒,现在国际上已经禁止或限制其使用
D.研究有机物的一般方法和步骤是分离、提纯后通过李比希燃烧法确定有机物的实验式→通过质谱法确定有机物的分子式→通过核磁共振氢谱、红外光谱、紫外光谱等确定有机物的结构简式
2.下列各组中的反应,属于同一反应类型的是( )
A.由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B.由乙酸和乙醇制乙酸乙酯;由乙醇和氢溴酸反应制溴乙烷
C.由氯代环己烷制环己烯;由丙烯和溴单质制1,2-二溴丙烷
D.由甲苯制对硝基甲苯;由甲苯和酸性KMnO4溶液制苯甲酸
3.如图有机物分子中标“*”碳原子是手性碳原子,该有机物分别发生下列反应,生成的有机物分子中仍含有手性碳原子的是( )
A.在加热、催化剂条件下与H2反应
B.与银氨溶液作用发生银镜反应
C.与乙酸发生酯化反应
D.与NaOH溶液在加热条件下反应
4.某杀虫剂的结构如图,下列关于该化合物的叙述不正确的是( )
A.属于芳香族化合物
B.每个分子中碳原子个数是25
C.具有酯类化合物的性质
D.在一定条件下可以发生加成反应
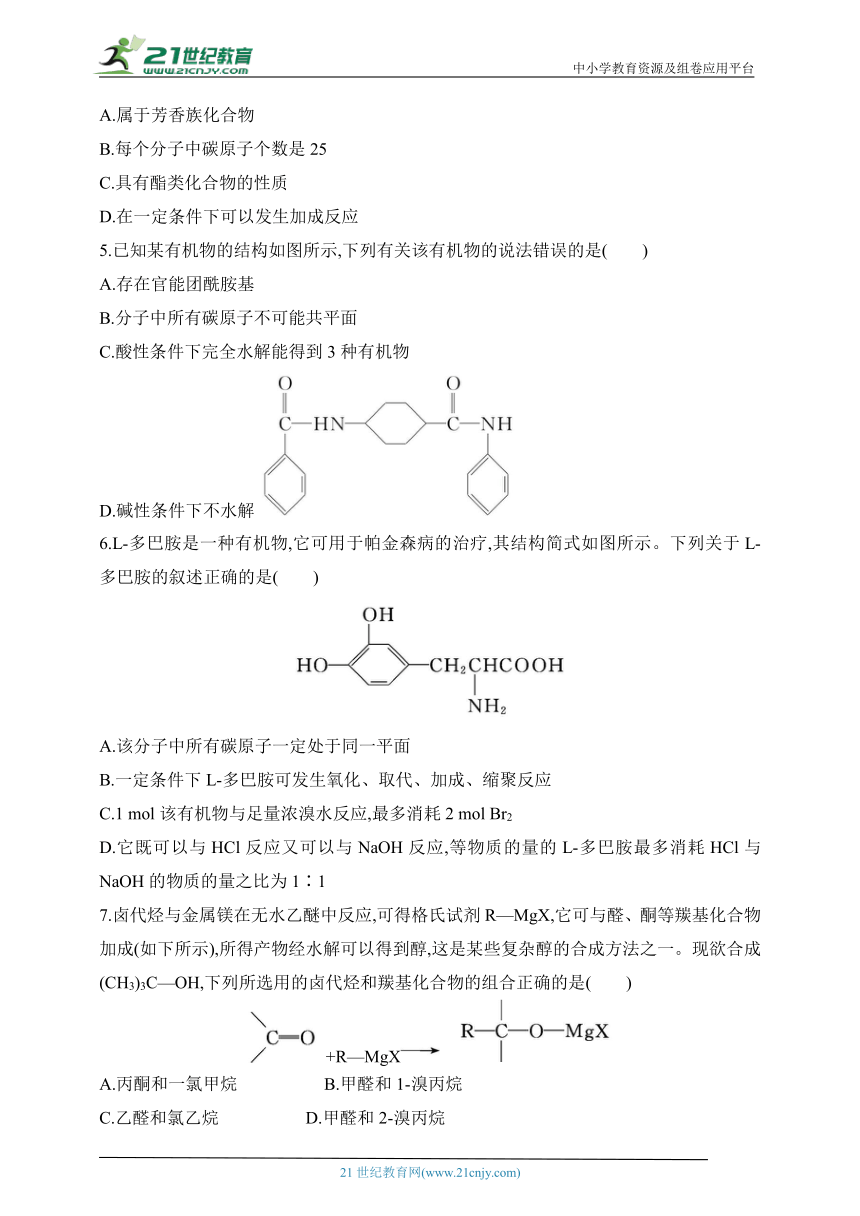
5.已知某有机物的结构如图所示,下列有关该有机物的说法错误的是( )
A.存在官能团酰胺基
B.分子中所有碳原子不可能共平面
C.酸性条件下完全水解能得到3种有机物
D.碱性条件下不水解
6.L-多巴胺是一种有机物,它可用于帕金森病的治疗,其结构简式如图所示。下列关于L-多巴胺的叙述正确的是( )
A.该分子中所有碳原子一定处于同一平面
B.一定条件下L-多巴胺可发生氧化、取代、加成、缩聚反应
C.1 mol该有机物与足量浓溴水反应,最多消耗2 mol Br2
D.它既可以与HCl反应又可以与NaOH反应,等物质的量的L-多巴胺最多消耗HCl与NaOH的物质的量之比为1∶1
7.卤代烃与金属镁在无水乙醚中反应,可得格氏试剂R—MgX,它可与醛、酮等羰基化合物加成(如下所示),所得产物经水解可以得到醇,这是某些复杂醇的合成方法之一。现欲合成(CH3)3C—OH,下列所选用的卤代烃和羰基化合物的组合正确的是( )
+R—MgX
A.丙酮和一氯甲烷 B.甲醛和1-溴丙烷
C.乙醛和氯乙烷 D.甲醛和2-溴丙烷
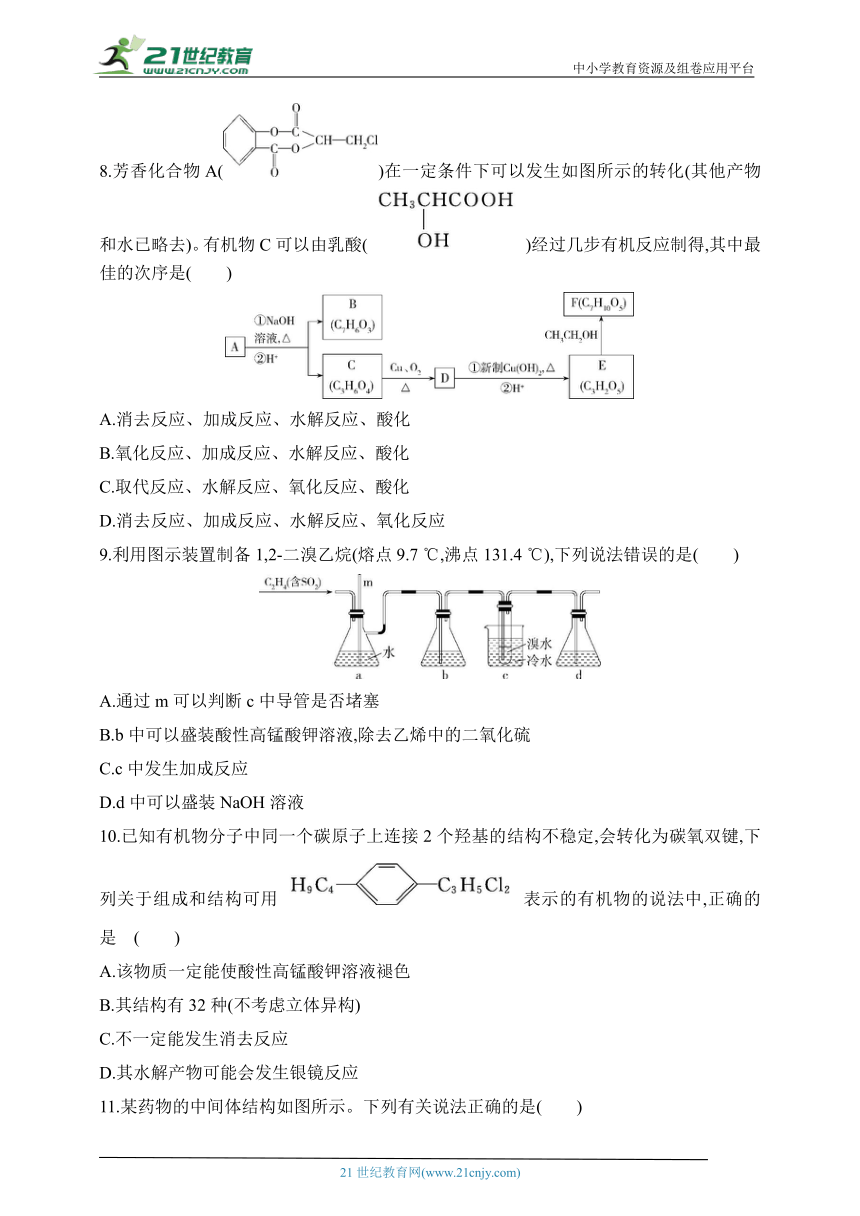
8.芳香化合物A()在一定条件下可以发生如图所示的转化(其他产物和水已略去)。有机物C可以由乳酸()经过几步有机反应制得,其中最佳的次序是( )
A.消去反应、加成反应、水解反应、酸化
B.氧化反应、加成反应、水解反应、酸化
C.取代反应、水解反应、氧化反应、酸化
D.消去反应、加成反应、水解反应、氧化反应
9.利用图示装置制备1,2-二溴乙烷(熔点9.7 ℃,沸点131.4 ℃),下列说法错误的是( )
A.通过m可以判断c中导管是否堵塞
B.b中可以盛装酸性高锰酸钾溶液,除去乙烯中的二氧化硫
C.c中发生加成反应
D.d中可以盛装NaOH溶液
10.已知有机物分子中同一个碳原子上连接2个羟基的结构不稳定,会转化为碳氧双键,下列关于组成和结构可用表示的有机物的说法中,正确的是 ( )
A.该物质一定能使酸性高锰酸钾溶液褪色
B.其结构有32种(不考虑立体异构)
C.不一定能发生消去反应
D.其水解产物可能会发生银镜反应
11.某药物的中间体结构如图所示。下列有关说法正确的是( )
A.利用稀硝酸和硝酸银溶液可直接检验其中的溴元素
B.在浓硫酸作用、加热条件下,可发生消去反应(形成碳碳双键)或取代反应
C.该有机物苯环上的一氯代物有4种(不含立体异构)
D.1 mol该有机物与氢气加成,最多消耗4 mol氢气
12.某有机物的结构如图所示,下列说法不正确的是( )
A.该物质的分子式为C20H24N2SO
B.该物质可发生水解反应、氧化反应、加聚反应
C.1 mol该物质最多可与7 mol H2加成,且完全加成后,产物每个分子中含有2个手性碳原子
D.该物质分子中所有原子可能在同一平面上
13.化合物P具有抗肿瘤活性,结构如图,下列有关P的说法错误的是( )
A.存在顺反异构
B.可发生取代反应、氧化反应、消去反应
C.与酸或碱溶液反应均可生成盐
D.分子中存在手性碳原子
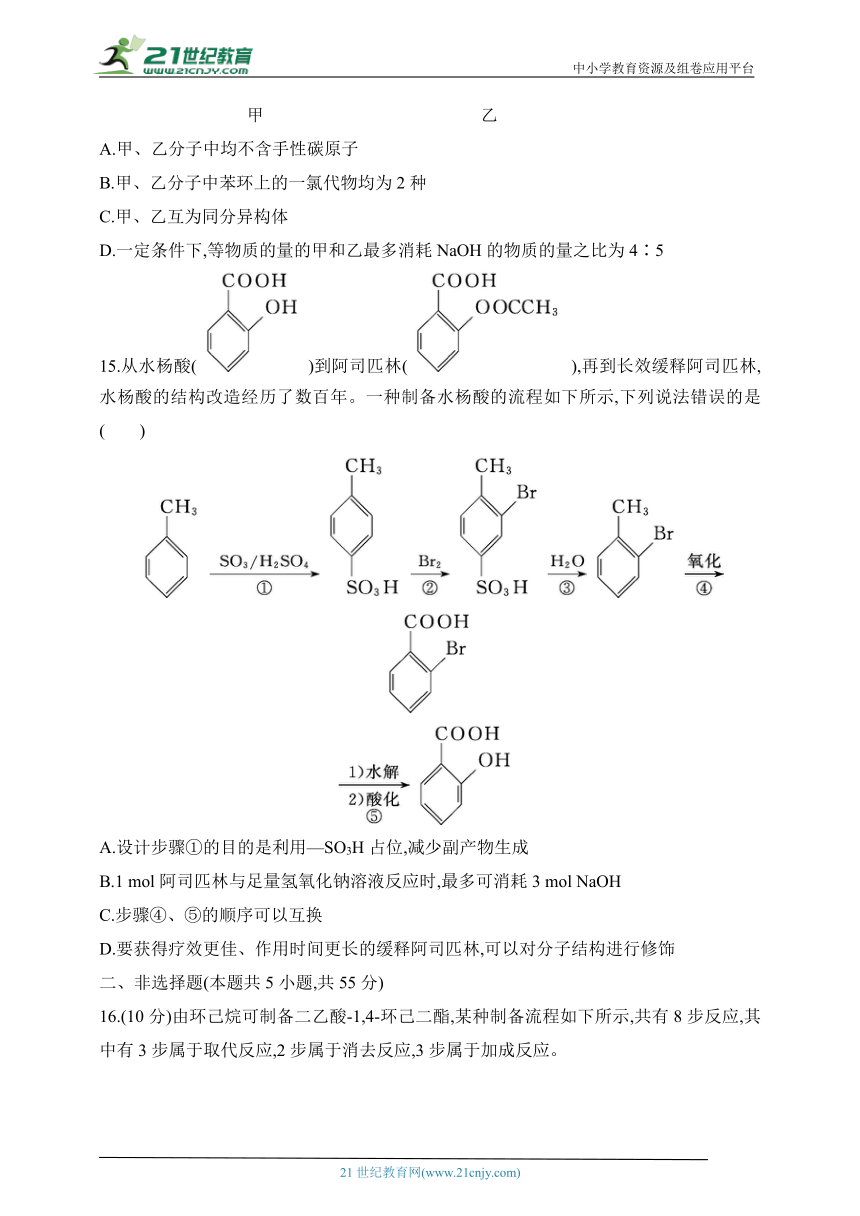
14.溴螨酯是一种杀螨剂。甲、乙两种物质是合成溴螨酯过程的中间产物,结构如图所示,下列有关二者的说法错误的是 ( )
甲 乙
A.甲、乙分子中均不含手性碳原子
B.甲、乙分子中苯环上的一氯代物均为2种
C.甲、乙互为同分异构体
D.一定条件下,等物质的量的甲和乙最多消耗NaOH的物质的量之比为4∶5
15.从水杨酸()到阿司匹林(),再到长效缓释阿司匹林,水杨酸的结构改造经历了数百年。一种制备水杨酸的流程如下所示,下列说法错误的是( )
A.设计步骤①的目的是利用—SO3H占位,减少副产物生成
B.1 mol阿司匹林与足量氢氧化钠溶液反应时,最多可消耗3 mol NaOH
C.步骤④、⑤的顺序可以互换
D.要获得疗效更佳、作用时间更长的缓释阿司匹林,可以对分子结构进行修饰
二、非选择题(本题共5小题,共55分)
16.(10分)由环己烷可制备二乙酸-1,4-环己二酯,某种制备流程如下所示,共有8步反应,其中有3步属于取代反应,2步属于消去反应,3步属于加成反应。
请回答下列问题:
(1)反应①、 和 属于取代反应;反应 和 属于消去反应(填序号)。
(2)C的结构简式为 。
(3)反应④的反应条件是 。
(4)写出第⑧步反应的化学方程式: 。
17.(13分)某同学探究1-溴丁烷发生消去反应产物的实验装置如图所示。先在圆底烧瓶中加入2.0 g NaOH和15 mL无水乙醇,搅拌,再加入5 mL 1-溴丁烷和几片碎瓷片,微热(液体沸腾后,移开酒精灯),产生的气体通过盛有水的试管后,再通入盛有酸性KMnO4溶液的试管中。
试回答下列问题:
(1)写出圆底烧瓶中发生反应的化学方程式: 。
(2)实验时加入碎瓷片的目的是 。
(3)装置Ⅱ的作用是 。
(4)装置Ⅲ中可观察到的现象是 。如果没有装置Ⅱ,则装置Ⅲ中的试剂应换成 。
(5)向圆底烧瓶反应后的溶液中加入金属钠,产生气泡。该同学判断1-溴丁烷同时发生取代反应生成了醇类物质,此判断 (填“正确”或“不正确”),理由是 。
(6)已知:溴乙烷的沸点为38.4 ℃,1-溴丁烷的沸点为101.6 ℃。该同学用溴乙烷代替1-溴丁烷进行实验时,发现酸性KMnO4溶液不褪色。则实验失败的原因可能是 。
18.(9分)苯胺是一种重要精细化工原料,在染料、医药等行业中具有广泛的应用。实验室用硝基苯为原料制取苯胺,其反应原理和装置如下:
+3H2+2H2O
已知:
物质 相对分子质量 沸点 密度 性质
硝基苯 123 210.9 ℃ 1.23 g/mL 不溶于水,易溶于乙醇、乙醚
苯胺 93 184.4 ℃ 1.02 g/mL 微溶于水,易溶于乙醇、乙醚;还原性强、易被氧化
实验步骤如下:
①组装好实验装置并检查装置气密性。
②先向三颈烧瓶中加入沸石及硝基苯,再取下恒压滴液漏斗,换上温度计。
③打开活塞K,通入H2一段时间。
④利用油浴加热。
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰。
⑥调整好温度计的位置,继续加热,收集182~186 ℃的馏分,得到较纯苯胺。
回答下列问题:
(1)步骤④中利用油浴加热的目的是 ;步骤⑤中,加入生石灰的作用是 。
(2)步骤⑥中温度计水银球的位置 。
(3)若实验中硝基苯用量为10 mL,最后得到苯胺5.6 g,苯胺的产率为 (结果精确到0.1%)。
19.(11分)化合物F是一种复合材料的组成成分,其合成路线如下:
(1)C→D的反应类型为 。
(2)已知E+XF+2H2O,则化合物X的结构简式为 。
(3)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式: 。
①在一定条件下能发生水解反应;
②每个分子中含两个苯环且含有4种不同化学环境的氢原子。
(4)苯乙酮肟()常用作杀虫剂。设计以和NH2OH为原料制备苯乙酮肟的合成路线(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
20.(12分)化合物G是一种重要中间体,其合成路线如下:
(1)写出D中官能团的名称: ,D中碳原子轨道杂化类型是 。
(2)F→G的反应类型为 。
(3)C的分子式为C11H14O2,则C的结构简式为 。
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式: 。
①能发生银镜反应;②能与FeCl3溶液发生显色反应;
③分子中有4种不同化学环境的氢原子。
(5)已知:RBr RMgBr。设计以为原料制备的合成路线(无机试剂和有机溶剂任选,合成路线示例见本题题干)。
答案与分层梯度式解析
专题5 药物合成的重要原料——卤代烃、胺、酰胺
1.C 2.B 3.B 4.B 5.D 6.B 7.A 8.A
9.B 10.D 11.B 12.D 13.B 14.C 15.C
1.C 氟利昂是含有氟和氯的烷烃衍生物,性质不稳定、容易液化,曾被用作制冷剂,但是因其会破坏环境,现在国际上已经禁止或限制其使用,C项错误。
2.B 前者为水解反应(或取代反应),后者为加成反应,故A不符合题意;两者都为取代反应,故B符合题意;前者为消去反应,后者为加成反应,故C不符合题意;前者为取代反应,后者为氧化反应,故D不符合题意。
3.B 与H2反应的产物是,不含手性碳原子,A项错误;与银氨溶液反应生成的有机产物是,标“*”碳原子为手性碳原子,B项正确;与乙酸发生酯化反应的有机产物是,不含手性碳原子,C项错误;与NaOH溶液在加热条件下反应生成的有机产物是,不含手性碳原子,D项错误。
4.B 题给物质结构中含有苯环,属于芳香族化合物,A项正确;根据题给物质结构可知,该分子中有18个碳原子,B项错误;题给物质结构中含有酯基,具有酯类化合物的性质,C项正确;题给物质结构中含有碳碳双键和苯环,在一定条件下可发生加成反应,D项正确。
5.D 根据题给结构可知,该物质分子中含有的官能团名称为酰胺基,A正确;该物质分子中含有多个直接相连的饱和碳原子,分子中所有碳原子不可能共平面,B正确;该物质在酸性条件下水解产生、和三种有机化合物,C正确;该物质分子中含有酰胺基,在碱性条件下水解断裂酰胺基中的C—N键,D错误。
6.B 苯是平面结构,与苯环直接相连的碳原子与苯环共平面,饱和碳原子及与之相连的原子最多3个共平面,羰基及与羰基碳原子相连的原子共平面,该分子中所有碳原子不一定处于同一平面,A错误;该有机物所含官能团有(酚)羟基、氨基、羧基,则一定条件下L-多巴胺中酚羟基可发生氧化、取代反应,苯环可发生加成反应,所含羧基和氨基可发生缩聚反应,B正确;分子内所含2个酚羟基的邻位和对位的氢原子都可以被取代,则1 mol该有机物跟足量浓溴水反应,最多消耗3 mol Br2,C错误;氨基有碱性,羧基和酚羟基有酸性,故它既可以与HCl反应又可以与NaOH反应,等物质的量的L-多巴胺最多消耗HCl与NaOH的物质的量之比为1∶3,D错误。
7.A 以丙酮和一氯甲烷为原料反应,可生成2-甲基-2-丙醇,A正确。
8.A 由芳香化合物A的结构简式和反应后B和C的分子式判断,C的结构简式为,制备过程为乳酸经消去反应得到
CH2 CH—COOH,CH2 CHCOOH与Cl2加成得到,然后在NaOH水溶液中水解生成,最后酸化得到。
9.B 导管m与大气相通,可以平衡气压,通过观察m中液面变化可以判断c中导管是否堵塞,故A正确;酸性KMnO4溶液既可以与SO2反应,也可以与乙烯发生反应,故B错误;c中Br2与乙烯发生加成反应生成1,2-二溴乙烷,故C正确;d为尾气吸收装置,可用于吸收挥发出来的溴单质,可以盛装NaOH溶液,故D正确。
10.D 该物质若为结构,则不能使酸性高锰酸钾溶液褪色,A错误;丁基(—C4H9)共有4种结构,—C3H5Cl2共有9种结构,则该有机物共有36种结构,B错误;—C3H5Cl2共有9种结构,每一种结构中都存在所连碳原子的邻位碳原子上有氢原子的氯原子,所以都可以发生消去反应,C错误;和两种结构经水解后连在同一个碳原子上的羟基可转化为醛基,能发生银镜反应,D正确。
11.B 有机物中的卤素原子不能和硝酸银反应,故不能利用稀硝酸和硝酸银溶液直接检验题述有机物中的溴元素,A项错误;有机物分子中羟基连接的碳原子的邻位碳原子上有氢原子,在浓硫酸作用、加热条件下能发生消去反应形成碳碳双键,同时含有羟基和羧基,在浓硫酸作用、加热条件下可发生酯化反应,酯化反应属于取代反应,B项正确;该有机物苯环上的一氯代物有两种,C项错误;1 mol该有机物和氢气加成,最多消耗3 mol氢气,酯基和羧基中的碳氧双键不与H2发生加成反应,D项错误。
12.D 根据题给结构可知该物质的分子式为C20H24N2SO,故A正确;该物质分子中含有酰胺基,可发生水解反应,含有碳碳双键,可以发生加聚反应,也可以被氧化,故B正确;该物质分子中的苯环、碳碳双键可与氢气加成,酰胺基不可与氢气加成,1 mol该物质最多可与7 mol H2加成,加成后的产物每个分子中含有2个手性碳原子,故C正确;分子中含—CH2—,所有原子不可能在同一平面上,故D错误。
13.B 化合物P中碳碳双键的碳原子连接的原子或原子团不同,存在顺反异构,A正确。分子中含羧基、酰胺基,能发生取代反应;含碳碳双键,能发生氧化反应;不能发生消去反应,B错误。分子中存在酰胺基,与酸或碱溶液反应均可生成盐,C正确。由结构可知,分子中存在手性碳原子,D正确。
14.C 连有4个不相同的原子或原子团的碳原子叫手性碳原子,根据甲、乙的结构可知,甲、乙分子中均不含手性碳原子,A项正确。甲、乙分子中苯环均为对位连接不同原子或原子团的结构,存在对称轴,苯环上的一氯代物都有2种,B项正确。甲的分子式为C14H8O2Br2,乙的分子式为C14H10O3Br2,故二者不互为同分异构体,C项错误。一定条件下,1 mol甲最多消耗4 mol NaOH;1 mol 乙最多消耗5 mol NaOH,故等物质的量的甲、乙消耗NaOH的物质的量之比为4∶5,D项正确。
15.C 由步骤①~③分析可知:①中引入—SO3H占位,使②中的—Br定位到甲基的邻位,通过③又去除—SO3H,故A正确;阿司匹林和氢氧化钠溶液反应的化学方程式为+3NaOH +2H2O+CH3COONa,故B正确;酚羟基易被氧化,因此步骤④、⑤的顺序不可以互换,故C错误;修饰分子结构可以优化其性能,故D正确。
16.答案 (除注明外,每空2分)(1)⑦(1分) ⑧(1分) ②(1分)
④(1分) (2) (3)NaOH的醇溶液、加热
(4)+2CH3COOH +2H2O
解析 环己烷和氯气在光照条件下发生取代反应生成一氯环己烷,一氯环己烷与NaOH的乙醇溶液共热发生消去反应生成A,A为环己烯,环己烯和Cl2发生加成反应生成的B为1,2-二氯环己烷,B再发生消去反应生成,和Br2发生1,4-加成反应生成,和氢气在催化剂条件下发生加成反应生成,与NaOH的水溶液共热发生水解反应(也是取代反应)生成,和乙酸在浓硫酸、加热的条件下发生酯化反应(也是取代反应)生成。
(1)反应①、⑦、⑧是取代反应;反应②、④是消去反应。(2)C为1,4-二溴环己烷,结构简式为。(3)反应④是1,2-二氯环己烷的消去反应,卤代烃的消去反应所用试剂是NaOH的醇溶液,条件是加热。(4)第⑧步是酯化反应,反应的化学方程式为+2CH3COOH +2H2O。
17.答案 (除注明外,每空2分)(1)CH3CH2CH2CH2Br+NaOH +NaBr+H2O
(2)防止暴沸(1分)
(3)可吸收挥发出来的乙醇,防止干扰产物的检验
(4)溶液紫红色变浅或褪去 溴水(1分)
(5)不正确(1分) 实验开始时加入了乙醇,无法判断1-溴丁烷是否发生取代反应生成了醇类物质
(6)溴乙烷沸点低,加热时没有充分反应就挥发了
解析 本实验利用1-溴丁烷与NaOH的乙醇溶液共热,探究1-溴丁烷的化学性质,装置Ⅰ中1-溴丁烷与NaOH的乙醇溶液发生消去反应可生成1-丁烯;装置Ⅱ中水的作用是除去挥发出来的乙醇,防止干扰产物的检验;装置Ⅲ中酸性高锰酸钾溶液用于检验烯烃类产物。(4)1-丁烯可以被酸性高锰酸钾溶液氧化,则装置Ⅲ中可观察到的现象为溶液紫红色变浅或褪去;乙醇也可以使酸性高锰酸钾溶液褪色,但不能使溴水褪色,而1-丁烯可以使溴水褪色,因此如果没有装置Ⅱ,装置Ⅲ中的试剂应换成溴水。(5)实验在开始时加入了乙醇,乙醇可以和钠反应生成氢气,无法判断1-溴丁烷是否发生取代反应生成了醇类物质。(6)由已知信息可知,溴乙烷的沸点较低,反应时容易挥发,则实验失败的原因可能是溴乙烷沸点低,加热时没有充分反应就挥发了。
18.答案 (除注明外,每空2分)(1)使反应液温度维持在140 ℃,使反应物充分反应 吸水 (2)与三颈烧瓶出气口处相平 (3)60.2%(3分)
解析 (1)由题中信息可知,利用硝基苯制取苯胺的反应温度为140 ℃,则步骤④中利用油浴加热的目的是使反应液温度维持在140 ℃,有利于反应进行;步骤⑤中,加入生石灰的作用是吸水。(2)步骤⑥蒸馏时,温度计水银球的位置应与三颈烧瓶出气口相平。(3)实验中硝基苯用量为10 mL,质量为10 mL×1.23 g/mL=12.3 g,理论上生成苯胺的质量为=9.3 g,实际生成苯胺的质量为5.6 g,则苯胺的产率为×100%≈60.2%。
19.答案 (除注明外,每空2分)(1)氧化反应 (2)CH3CH2NH2
(3)(3分)
(4)(4分)
解析 (1) C→D是被二氧化锰氧化生成,反应类型为氧化反应。(2)已知E+XF+2H2O,与X在HOAc作用下加热反应生成,根据E、F推知X的结构简式为CH3CH2NH2。(3)①在一定条件下能发生水解反应,则含有酯基或酰胺基;②每个分子中含两个苯环且含有4种不同化学环境的氢原子,说明结构高度对称,符合条件的同分异构体为。(4)以NH2OH和为原料制备苯乙酮肟,首先与氢氧化钠的乙醇溶液共热发生消去反应生成苯乙烯,苯乙烯与水发生加成反应生成,被二氧化锰氧化生成,与NH2OH在HOAc作用下发生反应生成。
20.答案 (除注明外,每空2分)(1)羰基(1分) sp2、sp3
(2)消去反应(1分) (3)
(4)或
(5)
(4分)
解析 (1)D的结构简式为,D中官能团的名称为羰基;D中苯环碳原子和羰基碳原子采取sp2杂化,其余碳原子都是饱和碳原子,采取sp3杂化。(2)对比F、G的结构简式,F→G的反应类型为消去反应。(3)与Zn-Hg、HCl反应生成C,C与PPA反应生成,又知C的分子式为C11H14O2,则C的结构简式为。(4)B的结构简式为,B的分子式为C11H12O3,不饱和度为6;B的同分异构体能发生银镜反应,说明含—CHO,能与FeCl3溶液发生显色反应,说明含酚羟基,分子中有4种不同化学环境的氢原子,说明结构对称性高,则符合条件的同分异构体的结构简式为、。(5)对比与的结构,可仿照流程中D→E→F合成。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024苏教版高中化学选择性必修3同步
专题5 药物合成的重要原料——
卤代烃、胺、酰胺
注意事项 1.全卷满分100分。考试用时90分钟。
2.可能用到的相对原子质量:H-1 C-12 N-14 O-16。
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一个选项符合题目要求)
1.下列说法错误的是( )
A.石油在国民经济中的地位非常重要,被誉为“工业的血液”
B.乙烯的产量可以用来衡量一个国家的石油化工发展水平
C.氟利昂是含有氟和氯的烷烃衍生物,性质不稳定、难液化,曾被用作制冷剂,但是因其有毒,现在国际上已经禁止或限制其使用
D.研究有机物的一般方法和步骤是分离、提纯后通过李比希燃烧法确定有机物的实验式→通过质谱法确定有机物的分子式→通过核磁共振氢谱、红外光谱、紫外光谱等确定有机物的结构简式
2.下列各组中的反应,属于同一反应类型的是( )
A.由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B.由乙酸和乙醇制乙酸乙酯;由乙醇和氢溴酸反应制溴乙烷
C.由氯代环己烷制环己烯;由丙烯和溴单质制1,2-二溴丙烷
D.由甲苯制对硝基甲苯;由甲苯和酸性KMnO4溶液制苯甲酸
3.如图有机物分子中标“*”碳原子是手性碳原子,该有机物分别发生下列反应,生成的有机物分子中仍含有手性碳原子的是( )
A.在加热、催化剂条件下与H2反应
B.与银氨溶液作用发生银镜反应
C.与乙酸发生酯化反应
D.与NaOH溶液在加热条件下反应
4.某杀虫剂的结构如图,下列关于该化合物的叙述不正确的是( )
A.属于芳香族化合物
B.每个分子中碳原子个数是25
C.具有酯类化合物的性质
D.在一定条件下可以发生加成反应
5.已知某有机物的结构如图所示,下列有关该有机物的说法错误的是( )
A.存在官能团酰胺基
B.分子中所有碳原子不可能共平面
C.酸性条件下完全水解能得到3种有机物
D.碱性条件下不水解
6.L-多巴胺是一种有机物,它可用于帕金森病的治疗,其结构简式如图所示。下列关于L-多巴胺的叙述正确的是( )
A.该分子中所有碳原子一定处于同一平面
B.一定条件下L-多巴胺可发生氧化、取代、加成、缩聚反应
C.1 mol该有机物与足量浓溴水反应,最多消耗2 mol Br2
D.它既可以与HCl反应又可以与NaOH反应,等物质的量的L-多巴胺最多消耗HCl与NaOH的物质的量之比为1∶1
7.卤代烃与金属镁在无水乙醚中反应,可得格氏试剂R—MgX,它可与醛、酮等羰基化合物加成(如下所示),所得产物经水解可以得到醇,这是某些复杂醇的合成方法之一。现欲合成(CH3)3C—OH,下列所选用的卤代烃和羰基化合物的组合正确的是( )
+R—MgX
A.丙酮和一氯甲烷 B.甲醛和1-溴丙烷
C.乙醛和氯乙烷 D.甲醛和2-溴丙烷
8.芳香化合物A()在一定条件下可以发生如图所示的转化(其他产物和水已略去)。有机物C可以由乳酸()经过几步有机反应制得,其中最佳的次序是( )
A.消去反应、加成反应、水解反应、酸化
B.氧化反应、加成反应、水解反应、酸化
C.取代反应、水解反应、氧化反应、酸化
D.消去反应、加成反应、水解反应、氧化反应
9.利用图示装置制备1,2-二溴乙烷(熔点9.7 ℃,沸点131.4 ℃),下列说法错误的是( )
A.通过m可以判断c中导管是否堵塞
B.b中可以盛装酸性高锰酸钾溶液,除去乙烯中的二氧化硫
C.c中发生加成反应
D.d中可以盛装NaOH溶液
10.已知有机物分子中同一个碳原子上连接2个羟基的结构不稳定,会转化为碳氧双键,下列关于组成和结构可用表示的有机物的说法中,正确的是 ( )
A.该物质一定能使酸性高锰酸钾溶液褪色
B.其结构有32种(不考虑立体异构)
C.不一定能发生消去反应
D.其水解产物可能会发生银镜反应
11.某药物的中间体结构如图所示。下列有关说法正确的是( )
A.利用稀硝酸和硝酸银溶液可直接检验其中的溴元素
B.在浓硫酸作用、加热条件下,可发生消去反应(形成碳碳双键)或取代反应
C.该有机物苯环上的一氯代物有4种(不含立体异构)
D.1 mol该有机物与氢气加成,最多消耗4 mol氢气
12.某有机物的结构如图所示,下列说法不正确的是( )
A.该物质的分子式为C20H24N2SO
B.该物质可发生水解反应、氧化反应、加聚反应
C.1 mol该物质最多可与7 mol H2加成,且完全加成后,产物每个分子中含有2个手性碳原子
D.该物质分子中所有原子可能在同一平面上
13.化合物P具有抗肿瘤活性,结构如图,下列有关P的说法错误的是( )
A.存在顺反异构
B.可发生取代反应、氧化反应、消去反应
C.与酸或碱溶液反应均可生成盐
D.分子中存在手性碳原子
14.溴螨酯是一种杀螨剂。甲、乙两种物质是合成溴螨酯过程的中间产物,结构如图所示,下列有关二者的说法错误的是 ( )
甲 乙
A.甲、乙分子中均不含手性碳原子
B.甲、乙分子中苯环上的一氯代物均为2种
C.甲、乙互为同分异构体
D.一定条件下,等物质的量的甲和乙最多消耗NaOH的物质的量之比为4∶5
15.从水杨酸()到阿司匹林(),再到长效缓释阿司匹林,水杨酸的结构改造经历了数百年。一种制备水杨酸的流程如下所示,下列说法错误的是( )
A.设计步骤①的目的是利用—SO3H占位,减少副产物生成
B.1 mol阿司匹林与足量氢氧化钠溶液反应时,最多可消耗3 mol NaOH
C.步骤④、⑤的顺序可以互换
D.要获得疗效更佳、作用时间更长的缓释阿司匹林,可以对分子结构进行修饰
二、非选择题(本题共5小题,共55分)
16.(10分)由环己烷可制备二乙酸-1,4-环己二酯,某种制备流程如下所示,共有8步反应,其中有3步属于取代反应,2步属于消去反应,3步属于加成反应。
请回答下列问题:
(1)反应①、 和 属于取代反应;反应 和 属于消去反应(填序号)。
(2)C的结构简式为 。
(3)反应④的反应条件是 。
(4)写出第⑧步反应的化学方程式: 。
17.(13分)某同学探究1-溴丁烷发生消去反应产物的实验装置如图所示。先在圆底烧瓶中加入2.0 g NaOH和15 mL无水乙醇,搅拌,再加入5 mL 1-溴丁烷和几片碎瓷片,微热(液体沸腾后,移开酒精灯),产生的气体通过盛有水的试管后,再通入盛有酸性KMnO4溶液的试管中。
试回答下列问题:
(1)写出圆底烧瓶中发生反应的化学方程式: 。
(2)实验时加入碎瓷片的目的是 。
(3)装置Ⅱ的作用是 。
(4)装置Ⅲ中可观察到的现象是 。如果没有装置Ⅱ,则装置Ⅲ中的试剂应换成 。
(5)向圆底烧瓶反应后的溶液中加入金属钠,产生气泡。该同学判断1-溴丁烷同时发生取代反应生成了醇类物质,此判断 (填“正确”或“不正确”),理由是 。
(6)已知:溴乙烷的沸点为38.4 ℃,1-溴丁烷的沸点为101.6 ℃。该同学用溴乙烷代替1-溴丁烷进行实验时,发现酸性KMnO4溶液不褪色。则实验失败的原因可能是 。
18.(9分)苯胺是一种重要精细化工原料,在染料、医药等行业中具有广泛的应用。实验室用硝基苯为原料制取苯胺,其反应原理和装置如下:
+3H2+2H2O
已知:
物质 相对分子质量 沸点 密度 性质
硝基苯 123 210.9 ℃ 1.23 g/mL 不溶于水,易溶于乙醇、乙醚
苯胺 93 184.4 ℃ 1.02 g/mL 微溶于水,易溶于乙醇、乙醚;还原性强、易被氧化
实验步骤如下:
①组装好实验装置并检查装置气密性。
②先向三颈烧瓶中加入沸石及硝基苯,再取下恒压滴液漏斗,换上温度计。
③打开活塞K,通入H2一段时间。
④利用油浴加热。
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰。
⑥调整好温度计的位置,继续加热,收集182~186 ℃的馏分,得到较纯苯胺。
回答下列问题:
(1)步骤④中利用油浴加热的目的是 ;步骤⑤中,加入生石灰的作用是 。
(2)步骤⑥中温度计水银球的位置 。
(3)若实验中硝基苯用量为10 mL,最后得到苯胺5.6 g,苯胺的产率为 (结果精确到0.1%)。
19.(11分)化合物F是一种复合材料的组成成分,其合成路线如下:
(1)C→D的反应类型为 。
(2)已知E+XF+2H2O,则化合物X的结构简式为 。
(3)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式: 。
①在一定条件下能发生水解反应;
②每个分子中含两个苯环且含有4种不同化学环境的氢原子。
(4)苯乙酮肟()常用作杀虫剂。设计以和NH2OH为原料制备苯乙酮肟的合成路线(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
20.(12分)化合物G是一种重要中间体,其合成路线如下:
(1)写出D中官能团的名称: ,D中碳原子轨道杂化类型是 。
(2)F→G的反应类型为 。
(3)C的分子式为C11H14O2,则C的结构简式为 。
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式: 。
①能发生银镜反应;②能与FeCl3溶液发生显色反应;
③分子中有4种不同化学环境的氢原子。
(5)已知:RBr RMgBr。设计以为原料制备的合成路线(无机试剂和有机溶剂任选,合成路线示例见本题题干)。
答案与分层梯度式解析
专题5 药物合成的重要原料——卤代烃、胺、酰胺
1.C 2.B 3.B 4.B 5.D 6.B 7.A 8.A
9.B 10.D 11.B 12.D 13.B 14.C 15.C
1.C 氟利昂是含有氟和氯的烷烃衍生物,性质不稳定、容易液化,曾被用作制冷剂,但是因其会破坏环境,现在国际上已经禁止或限制其使用,C项错误。
2.B 前者为水解反应(或取代反应),后者为加成反应,故A不符合题意;两者都为取代反应,故B符合题意;前者为消去反应,后者为加成反应,故C不符合题意;前者为取代反应,后者为氧化反应,故D不符合题意。
3.B 与H2反应的产物是,不含手性碳原子,A项错误;与银氨溶液反应生成的有机产物是,标“*”碳原子为手性碳原子,B项正确;与乙酸发生酯化反应的有机产物是,不含手性碳原子,C项错误;与NaOH溶液在加热条件下反应生成的有机产物是,不含手性碳原子,D项错误。
4.B 题给物质结构中含有苯环,属于芳香族化合物,A项正确;根据题给物质结构可知,该分子中有18个碳原子,B项错误;题给物质结构中含有酯基,具有酯类化合物的性质,C项正确;题给物质结构中含有碳碳双键和苯环,在一定条件下可发生加成反应,D项正确。
5.D 根据题给结构可知,该物质分子中含有的官能团名称为酰胺基,A正确;该物质分子中含有多个直接相连的饱和碳原子,分子中所有碳原子不可能共平面,B正确;该物质在酸性条件下水解产生、和三种有机化合物,C正确;该物质分子中含有酰胺基,在碱性条件下水解断裂酰胺基中的C—N键,D错误。
6.B 苯是平面结构,与苯环直接相连的碳原子与苯环共平面,饱和碳原子及与之相连的原子最多3个共平面,羰基及与羰基碳原子相连的原子共平面,该分子中所有碳原子不一定处于同一平面,A错误;该有机物所含官能团有(酚)羟基、氨基、羧基,则一定条件下L-多巴胺中酚羟基可发生氧化、取代反应,苯环可发生加成反应,所含羧基和氨基可发生缩聚反应,B正确;分子内所含2个酚羟基的邻位和对位的氢原子都可以被取代,则1 mol该有机物跟足量浓溴水反应,最多消耗3 mol Br2,C错误;氨基有碱性,羧基和酚羟基有酸性,故它既可以与HCl反应又可以与NaOH反应,等物质的量的L-多巴胺最多消耗HCl与NaOH的物质的量之比为1∶3,D错误。
7.A 以丙酮和一氯甲烷为原料反应,可生成2-甲基-2-丙醇,A正确。
8.A 由芳香化合物A的结构简式和反应后B和C的分子式判断,C的结构简式为,制备过程为乳酸经消去反应得到
CH2 CH—COOH,CH2 CHCOOH与Cl2加成得到,然后在NaOH水溶液中水解生成,最后酸化得到。
9.B 导管m与大气相通,可以平衡气压,通过观察m中液面变化可以判断c中导管是否堵塞,故A正确;酸性KMnO4溶液既可以与SO2反应,也可以与乙烯发生反应,故B错误;c中Br2与乙烯发生加成反应生成1,2-二溴乙烷,故C正确;d为尾气吸收装置,可用于吸收挥发出来的溴单质,可以盛装NaOH溶液,故D正确。
10.D 该物质若为结构,则不能使酸性高锰酸钾溶液褪色,A错误;丁基(—C4H9)共有4种结构,—C3H5Cl2共有9种结构,则该有机物共有36种结构,B错误;—C3H5Cl2共有9种结构,每一种结构中都存在所连碳原子的邻位碳原子上有氢原子的氯原子,所以都可以发生消去反应,C错误;和两种结构经水解后连在同一个碳原子上的羟基可转化为醛基,能发生银镜反应,D正确。
11.B 有机物中的卤素原子不能和硝酸银反应,故不能利用稀硝酸和硝酸银溶液直接检验题述有机物中的溴元素,A项错误;有机物分子中羟基连接的碳原子的邻位碳原子上有氢原子,在浓硫酸作用、加热条件下能发生消去反应形成碳碳双键,同时含有羟基和羧基,在浓硫酸作用、加热条件下可发生酯化反应,酯化反应属于取代反应,B项正确;该有机物苯环上的一氯代物有两种,C项错误;1 mol该有机物和氢气加成,最多消耗3 mol氢气,酯基和羧基中的碳氧双键不与H2发生加成反应,D项错误。
12.D 根据题给结构可知该物质的分子式为C20H24N2SO,故A正确;该物质分子中含有酰胺基,可发生水解反应,含有碳碳双键,可以发生加聚反应,也可以被氧化,故B正确;该物质分子中的苯环、碳碳双键可与氢气加成,酰胺基不可与氢气加成,1 mol该物质最多可与7 mol H2加成,加成后的产物每个分子中含有2个手性碳原子,故C正确;分子中含—CH2—,所有原子不可能在同一平面上,故D错误。
13.B 化合物P中碳碳双键的碳原子连接的原子或原子团不同,存在顺反异构,A正确。分子中含羧基、酰胺基,能发生取代反应;含碳碳双键,能发生氧化反应;不能发生消去反应,B错误。分子中存在酰胺基,与酸或碱溶液反应均可生成盐,C正确。由结构可知,分子中存在手性碳原子,D正确。
14.C 连有4个不相同的原子或原子团的碳原子叫手性碳原子,根据甲、乙的结构可知,甲、乙分子中均不含手性碳原子,A项正确。甲、乙分子中苯环均为对位连接不同原子或原子团的结构,存在对称轴,苯环上的一氯代物都有2种,B项正确。甲的分子式为C14H8O2Br2,乙的分子式为C14H10O3Br2,故二者不互为同分异构体,C项错误。一定条件下,1 mol甲最多消耗4 mol NaOH;1 mol 乙最多消耗5 mol NaOH,故等物质的量的甲、乙消耗NaOH的物质的量之比为4∶5,D项正确。
15.C 由步骤①~③分析可知:①中引入—SO3H占位,使②中的—Br定位到甲基的邻位,通过③又去除—SO3H,故A正确;阿司匹林和氢氧化钠溶液反应的化学方程式为+3NaOH +2H2O+CH3COONa,故B正确;酚羟基易被氧化,因此步骤④、⑤的顺序不可以互换,故C错误;修饰分子结构可以优化其性能,故D正确。
16.答案 (除注明外,每空2分)(1)⑦(1分) ⑧(1分) ②(1分)
④(1分) (2) (3)NaOH的醇溶液、加热
(4)+2CH3COOH +2H2O
解析 环己烷和氯气在光照条件下发生取代反应生成一氯环己烷,一氯环己烷与NaOH的乙醇溶液共热发生消去反应生成A,A为环己烯,环己烯和Cl2发生加成反应生成的B为1,2-二氯环己烷,B再发生消去反应生成,和Br2发生1,4-加成反应生成,和氢气在催化剂条件下发生加成反应生成,与NaOH的水溶液共热发生水解反应(也是取代反应)生成,和乙酸在浓硫酸、加热的条件下发生酯化反应(也是取代反应)生成。
(1)反应①、⑦、⑧是取代反应;反应②、④是消去反应。(2)C为1,4-二溴环己烷,结构简式为。(3)反应④是1,2-二氯环己烷的消去反应,卤代烃的消去反应所用试剂是NaOH的醇溶液,条件是加热。(4)第⑧步是酯化反应,反应的化学方程式为+2CH3COOH +2H2O。
17.答案 (除注明外,每空2分)(1)CH3CH2CH2CH2Br+NaOH +NaBr+H2O
(2)防止暴沸(1分)
(3)可吸收挥发出来的乙醇,防止干扰产物的检验
(4)溶液紫红色变浅或褪去 溴水(1分)
(5)不正确(1分) 实验开始时加入了乙醇,无法判断1-溴丁烷是否发生取代反应生成了醇类物质
(6)溴乙烷沸点低,加热时没有充分反应就挥发了
解析 本实验利用1-溴丁烷与NaOH的乙醇溶液共热,探究1-溴丁烷的化学性质,装置Ⅰ中1-溴丁烷与NaOH的乙醇溶液发生消去反应可生成1-丁烯;装置Ⅱ中水的作用是除去挥发出来的乙醇,防止干扰产物的检验;装置Ⅲ中酸性高锰酸钾溶液用于检验烯烃类产物。(4)1-丁烯可以被酸性高锰酸钾溶液氧化,则装置Ⅲ中可观察到的现象为溶液紫红色变浅或褪去;乙醇也可以使酸性高锰酸钾溶液褪色,但不能使溴水褪色,而1-丁烯可以使溴水褪色,因此如果没有装置Ⅱ,装置Ⅲ中的试剂应换成溴水。(5)实验在开始时加入了乙醇,乙醇可以和钠反应生成氢气,无法判断1-溴丁烷是否发生取代反应生成了醇类物质。(6)由已知信息可知,溴乙烷的沸点较低,反应时容易挥发,则实验失败的原因可能是溴乙烷沸点低,加热时没有充分反应就挥发了。
18.答案 (除注明外,每空2分)(1)使反应液温度维持在140 ℃,使反应物充分反应 吸水 (2)与三颈烧瓶出气口处相平 (3)60.2%(3分)
解析 (1)由题中信息可知,利用硝基苯制取苯胺的反应温度为140 ℃,则步骤④中利用油浴加热的目的是使反应液温度维持在140 ℃,有利于反应进行;步骤⑤中,加入生石灰的作用是吸水。(2)步骤⑥蒸馏时,温度计水银球的位置应与三颈烧瓶出气口相平。(3)实验中硝基苯用量为10 mL,质量为10 mL×1.23 g/mL=12.3 g,理论上生成苯胺的质量为=9.3 g,实际生成苯胺的质量为5.6 g,则苯胺的产率为×100%≈60.2%。
19.答案 (除注明外,每空2分)(1)氧化反应 (2)CH3CH2NH2
(3)(3分)
(4)(4分)
解析 (1) C→D是被二氧化锰氧化生成,反应类型为氧化反应。(2)已知E+XF+2H2O,与X在HOAc作用下加热反应生成,根据E、F推知X的结构简式为CH3CH2NH2。(3)①在一定条件下能发生水解反应,则含有酯基或酰胺基;②每个分子中含两个苯环且含有4种不同化学环境的氢原子,说明结构高度对称,符合条件的同分异构体为。(4)以NH2OH和为原料制备苯乙酮肟,首先与氢氧化钠的乙醇溶液共热发生消去反应生成苯乙烯,苯乙烯与水发生加成反应生成,被二氧化锰氧化生成,与NH2OH在HOAc作用下发生反应生成。
20.答案 (除注明外,每空2分)(1)羰基(1分) sp2、sp3
(2)消去反应(1分) (3)
(4)或
(5)
(4分)
解析 (1)D的结构简式为,D中官能团的名称为羰基;D中苯环碳原子和羰基碳原子采取sp2杂化,其余碳原子都是饱和碳原子,采取sp3杂化。(2)对比F、G的结构简式,F→G的反应类型为消去反应。(3)与Zn-Hg、HCl反应生成C,C与PPA反应生成,又知C的分子式为C11H14O2,则C的结构简式为。(4)B的结构简式为,B的分子式为C11H12O3,不饱和度为6;B的同分异构体能发生银镜反应,说明含—CHO,能与FeCl3溶液发生显色反应,说明含酚羟基,分子中有4种不同化学环境的氢原子,说明结构对称性高,则符合条件的同分异构体的结构简式为、。(5)对比与的结构,可仿照流程中D→E→F合成。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
