化学人教版(2019)选择性必修1 3.1.2弱电解质的电离平衡(共19张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修1 3.1.2弱电解质的电离平衡(共19张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 477.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-23 08:13:22 | ||
图片预览






文档简介
(共19张PPT)
电离平衡
弱电解质的
电离平衡
二
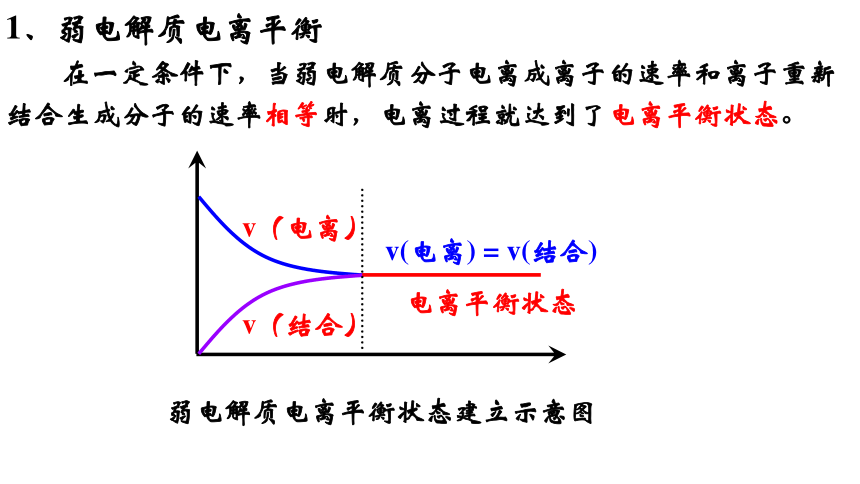
1、弱电解质电离平衡
在一定条件下,当弱电解质分子电离成离子的速率和离子重新结合生成分子的速率相等时,电离过程就达到了电离平衡状态。
弱电解质电离平衡状态建立示意图
v(电离)
v(结合)
v(电离) = v(结合)
电离平衡状态
2、特点
弱:
逆:
等:
动:
定:
变:
v电离 = v结合 ≠ 0
电离平衡是可逆过程
动态平衡
平衡时,溶液中各分子、离子的浓度不变
条件改变时,电离平衡发生移动
研究对象是弱电解质
3、影响因素
【补充】电离度
电离度:表示了弱电解质的电离程度的相对强弱。
电离度(α)= ×100%
n(已电离的电解质分子)
n(起始的电解质分子总量)
3、影响因素
(1)内因:
①越强越电离
eg.电离程度:盐酸>醋酸>碳酸
②多元弱酸的电离程度逐渐变小
eg.电离程度:碳酸的第一步电离>碳酸的第二步电离
弱电解质本身的性质(决定性因素)
3、影响因素
(2)外因
①温度
∵弱电解质的电离吸热
∴当温度升高时,平衡向电离的方向移动。
——符合勒夏特列原理
——越热越电离
3、影响因素
(2)外因
②浓度
以CH3COOH CH3COO- + H+为例
自身
——符合勒夏特列原理
——越稀越电离
加冰醋酸,
加水稀释,
3、影响因素
(2)外因
②浓度
以CH3COOH CH3COO- + H+为例
外加离子
或物质
——符合勒夏特列原理
同离子效应
——化学反应
c(CH3COO-)↑,
c(H+)↑,
加入OH-、CO32-、Mg,
【总结】
【思考】加水后,该溶液中所有离子浓度都减小吗?
CH3COOH CH3COO- + H+ 改变条件 平衡移动方向 c(H+) c(Ac-) c(HAc) 电离程度 导电能力
升高温度
通入HCl(g)
加NaOH(s)
加NaAc(s)
加水
加冰醋酸
→
←
→
←
→
→
↑
↑
↓
↑
↑
↑
↓
↑
↓
↑
↓
↑
↓
↑
↑
↓
↑
↑
↓
↑
↓
↓
↓
↑
↓
↑
↑
↑
↓
↑
×,c(OH-)增大。
【课堂小测】
1.稀氨水中存在着下列平衡,NH3·H2O NH4+ + OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是( )。
①NH4Cl固体 ②硫酸 ③NaOH固体
④水 ⑤加热 ⑥少量MgSO4固体
A、①②③⑤ B、③⑥
C、③ D、③⑤
C
4、强酸、弱酸的比较
(1)等浓度、等体积一元强酸、弱酸的比较
比较内容 一元强酸HA 一元弱酸HB
c(H+)
pH
与金属反应的起始速率
与足量碱反应时消耗碱的量
与足量活泼金属反应产生H2的量
c(A-)、c(B-)的大小
加水稀释相同倍数后的酸性
溶液的导电性
大
小
小
大
大
小
相等
相等
相等
相等
大
小
大
小
大
小
【练习】相同温度下,等浓度、等体积的三种酸,
①HCl ②H2SO4 ③CH3COOH
(1)c(H+): ;
(2)与足量锌反应的起始速率: ;
(3)导电性: ;
(4)溶液pH值: ;
(5)稀释10倍的pH值: ;
(6)与足量锌反应产生H2的量: ;
(7)与NaOH恰好完全反应消耗NaOH的量: 。
② = 2① > ③
② > ① > ③
② > ① > ③
② < ① < ③
② < ① < ③
② = 2① = 2③
② = 2① = 2③
4、强酸、弱酸的比较
(2)等pH、等体积一元强酸、弱酸的比较
比较内容 一元强酸HA 一元弱酸HB
c(H+)
酸的浓度
与金属反应的起始速率
与足量碱反应时消耗碱的量
与足量活泼金属反应产生H2的量
c(A-)、c(B-)的大小
加水稀释相同倍数后的酸性
溶液的导电性
相等
相等
小
大
相等
相等
小
大
小
大
相等
相等
小
大
相等
相等
【练习】相同温度下,等pH、等体积的三种酸,
①HCl ②H2SO4 ③CH3COOH
(1)c(H+): ;
(2)与足量锌反应的起始速率: ;
(3)导电性: ;
(4)酸的浓度: ;
(5)稀释10倍的pH值: ;
(6)与足量锌反应产生H2的量: ;
(7)与NaOH恰好完全反应消耗NaOH的量: 。
① = ② = ③
① = ② = ③
① = ③ > ②
③ > ① = 2②
① = ② > ③
③ > ① = ②
③ > ① = ②
【课堂小测】
1.常温下,现有①醋酸 ②盐酸 ③硫酸三种酸溶液,下列说法正确的是( )。
A、当三种酸的pH相同时,其物质的量浓度由大到小的顺序是①>②>③
B、将pH相同的三种酸溶液均稀释100倍后,pH由大到小的顺序是①>②>③
C、当三种酸溶液pH相同、体积相同时,分别加入足量的锌,相同状况下产生气体的体积关系为①>②>③
D、体积和物质的量浓度都相同的三种酸溶液,与0.01mol/L的NaOH完全中和,消耗NaOH的体积由大到小的顺序为③>②>①
A
【课堂小测】
2.将c(H+)相同的盐酸和醋酸,分别用蒸馏水稀释至原来体积的m倍和n倍,稀释后两溶液的c(H+)仍相同,则m和n的关系是( )。
A、m > n
B、m < n
C、m = n
D、不能确定
B
水
导电能力
O
5、图像
(1)0.1mol/L醋酸加水稀释
①pH:
②电离程度:
A
B
5、图像
(2)冰醋酸加水
①O点不导电:
②pH:
③电离程度:
A
B
C
水
导电能力
O
电离平衡
弱电解质的
电离平衡
二
1、弱电解质电离平衡
在一定条件下,当弱电解质分子电离成离子的速率和离子重新结合生成分子的速率相等时,电离过程就达到了电离平衡状态。
弱电解质电离平衡状态建立示意图
v(电离)
v(结合)
v(电离) = v(结合)
电离平衡状态
2、特点
弱:
逆:
等:
动:
定:
变:
v电离 = v结合 ≠ 0
电离平衡是可逆过程
动态平衡
平衡时,溶液中各分子、离子的浓度不变
条件改变时,电离平衡发生移动
研究对象是弱电解质
3、影响因素
【补充】电离度
电离度:表示了弱电解质的电离程度的相对强弱。
电离度(α)= ×100%
n(已电离的电解质分子)
n(起始的电解质分子总量)
3、影响因素
(1)内因:
①越强越电离
eg.电离程度:盐酸>醋酸>碳酸
②多元弱酸的电离程度逐渐变小
eg.电离程度:碳酸的第一步电离>碳酸的第二步电离
弱电解质本身的性质(决定性因素)
3、影响因素
(2)外因
①温度
∵弱电解质的电离吸热
∴当温度升高时,平衡向电离的方向移动。
——符合勒夏特列原理
——越热越电离
3、影响因素
(2)外因
②浓度
以CH3COOH CH3COO- + H+为例
自身
——符合勒夏特列原理
——越稀越电离
加冰醋酸,
加水稀释,
3、影响因素
(2)外因
②浓度
以CH3COOH CH3COO- + H+为例
外加离子
或物质
——符合勒夏特列原理
同离子效应
——化学反应
c(CH3COO-)↑,
c(H+)↑,
加入OH-、CO32-、Mg,
【总结】
【思考】加水后,该溶液中所有离子浓度都减小吗?
CH3COOH CH3COO- + H+ 改变条件 平衡移动方向 c(H+) c(Ac-) c(HAc) 电离程度 导电能力
升高温度
通入HCl(g)
加NaOH(s)
加NaAc(s)
加水
加冰醋酸
→
←
→
←
→
→
↑
↑
↓
↑
↑
↑
↓
↑
↓
↑
↓
↑
↓
↑
↑
↓
↑
↑
↓
↑
↓
↓
↓
↑
↓
↑
↑
↑
↓
↑
×,c(OH-)增大。
【课堂小测】
1.稀氨水中存在着下列平衡,NH3·H2O NH4+ + OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是( )。
①NH4Cl固体 ②硫酸 ③NaOH固体
④水 ⑤加热 ⑥少量MgSO4固体
A、①②③⑤ B、③⑥
C、③ D、③⑤
C
4、强酸、弱酸的比较
(1)等浓度、等体积一元强酸、弱酸的比较
比较内容 一元强酸HA 一元弱酸HB
c(H+)
pH
与金属反应的起始速率
与足量碱反应时消耗碱的量
与足量活泼金属反应产生H2的量
c(A-)、c(B-)的大小
加水稀释相同倍数后的酸性
溶液的导电性
大
小
小
大
大
小
相等
相等
相等
相等
大
小
大
小
大
小
【练习】相同温度下,等浓度、等体积的三种酸,
①HCl ②H2SO4 ③CH3COOH
(1)c(H+): ;
(2)与足量锌反应的起始速率: ;
(3)导电性: ;
(4)溶液pH值: ;
(5)稀释10倍的pH值: ;
(6)与足量锌反应产生H2的量: ;
(7)与NaOH恰好完全反应消耗NaOH的量: 。
② = 2① > ③
② > ① > ③
② > ① > ③
② < ① < ③
② < ① < ③
② = 2① = 2③
② = 2① = 2③
4、强酸、弱酸的比较
(2)等pH、等体积一元强酸、弱酸的比较
比较内容 一元强酸HA 一元弱酸HB
c(H+)
酸的浓度
与金属反应的起始速率
与足量碱反应时消耗碱的量
与足量活泼金属反应产生H2的量
c(A-)、c(B-)的大小
加水稀释相同倍数后的酸性
溶液的导电性
相等
相等
小
大
相等
相等
小
大
小
大
相等
相等
小
大
相等
相等
【练习】相同温度下,等pH、等体积的三种酸,
①HCl ②H2SO4 ③CH3COOH
(1)c(H+): ;
(2)与足量锌反应的起始速率: ;
(3)导电性: ;
(4)酸的浓度: ;
(5)稀释10倍的pH值: ;
(6)与足量锌反应产生H2的量: ;
(7)与NaOH恰好完全反应消耗NaOH的量: 。
① = ② = ③
① = ② = ③
① = ③ > ②
③ > ① = 2②
① = ② > ③
③ > ① = ②
③ > ① = ②
【课堂小测】
1.常温下,现有①醋酸 ②盐酸 ③硫酸三种酸溶液,下列说法正确的是( )。
A、当三种酸的pH相同时,其物质的量浓度由大到小的顺序是①>②>③
B、将pH相同的三种酸溶液均稀释100倍后,pH由大到小的顺序是①>②>③
C、当三种酸溶液pH相同、体积相同时,分别加入足量的锌,相同状况下产生气体的体积关系为①>②>③
D、体积和物质的量浓度都相同的三种酸溶液,与0.01mol/L的NaOH完全中和,消耗NaOH的体积由大到小的顺序为③>②>①
A
【课堂小测】
2.将c(H+)相同的盐酸和醋酸,分别用蒸馏水稀释至原来体积的m倍和n倍,稀释后两溶液的c(H+)仍相同,则m和n的关系是( )。
A、m > n
B、m < n
C、m = n
D、不能确定
B
水
导电能力
O
5、图像
(1)0.1mol/L醋酸加水稀释
①pH:
②电离程度:
A
B
5、图像
(2)冰醋酸加水
①O点不导电:
②pH:
③电离程度:
A
B
C
水
导电能力
O
