山东省潍坊市2023-2024学年高一上学期期中考试化学试题(含答案)
文档属性
| 名称 | 山东省潍坊市2023-2024学年高一上学期期中考试化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 528.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-23 00:00:00 | ||
图片预览


文档简介
潍坊市2023-2024学年高一上学期期中考试
化学
注意事项:
1.答题前,考生先将自己的学校、班级、姓名、考生号、座号填写在答题卡相应位置。
2.选择题答案必须使用2B铅笔(按填涂样例)正确填涂;非选择题答案必须使用0.5mm黑色签字笔书写在相应答题区域,超出答题区域书写的答案无效;在草稿纸和试卷上答题无效。
3.本试卷满分100分,考试时间90分钟。
可能用到的相对原子质量:H1 C12 O16 Na23 Cl35.5 Cu64
一、选择题:本题共10个小题,每小题2分,共20分。每小题只有一个选项符合题意。
1.化学与生产、生活密切相关。下列说法错误的是( )
A.金属钠导热性好,可用作传热介质 B.二氧化氯可用于自来水消毒
C.硫酸钙可用于由豆浆制豆腐 D.碳酸钠常用于治疗胃酸过多
2.有关物质性质,下列叙述正确的是( )
A.金属钠在空气中燃烧生成淡黄色固体
B.金属钠与水反应后的溶液呈碱性
C.具有刺激性气味,因此可杀灭细菌和病毒
D.氢气在氯气中燃烧产生淡蓝色火焰
3.下列关于实验仪器①~⑤的说法错误的是( )
A.①④使用前需要检查是否漏水
B.②③可以直接加热
C.从NaCl溶液中得到NaCl固体用到的仪器有③
D.在⑤中进行金属钠的燃烧实验
4.生活中用自来水养金鱼时,需将自来水先在阳光下暴晒一段时间的主要目的是( )
A.分解除去次氯酸 B.紫外线杀熊消毒
C.增加水中含量 D.提高水的温度
5.下列变化中,需要通过加入氧化剂实现的是( )
A. B. C. D.
6.为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,22.4 L 中含有的分子数为
B.常温常压下,6.4 g Cu与足量充分反应,转移的电子数为
C.常温常压下,1.5 mol L的溶液中含有的数目为
D.标准状况下,2.24 L CO和混合气体中含有的碳原子数为
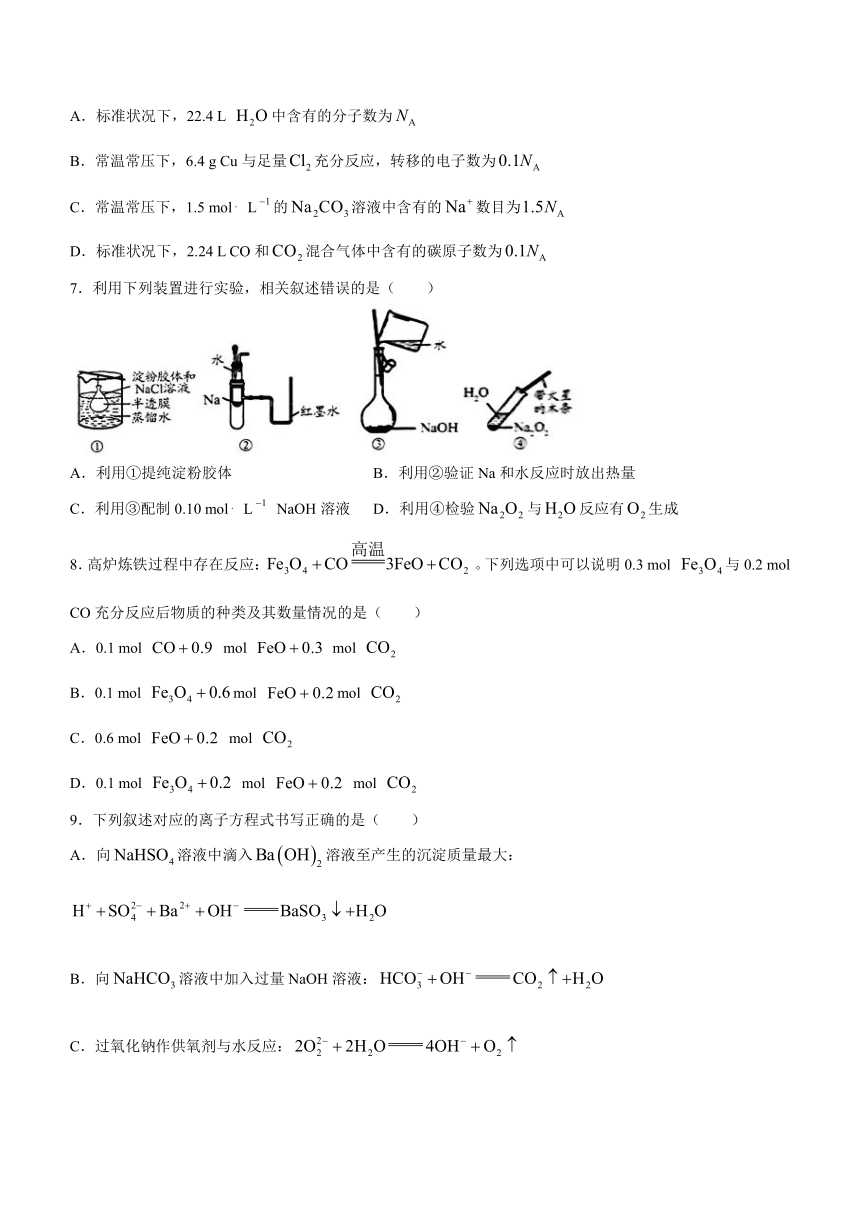
7.利用下列装置进行实验,相关叙述错误的是( )
A.利用①提纯淀粉胶体 B.利用②验证Na和水反应时放出热量
C.利用③配制0.10 mol L NaOH溶液 D.利用④检验与反应有生成
8.高炉炼铁过程中存在反应:。下列选项中可以说明0.3 mol 与0.2 mol CO充分反应后物质的种类及其数量情况的是( )
A.0.1 mol mol mol
B.0.1 mol mol mol
C.0.6 mol mol
D.0.1 mol mol mol
9.下列叙述对应的离子方程式书写正确的是( )
A.向溶液中滴入溶液至产生的沉淀质量最大:
B.向溶液中加入过量NaOH溶液:
C.过氧化钠作供氧剂与水反应:
D.向溶液中通入少量:
10.经检测,某工业废水显酸性,且废水中含有大量、、、下列离子中,不可能大量存在于该废水中的是( )
A. B. C. D.
二、选择题:本题共5小题,每题4分,共20分。每小题有一个或两个选项符合题意,全选对得4分,选对但不全的得2分,有选错的得0分。
11.下列实验中,对应的操作、现象以及结论都正确的是( )
选项 操作 现象 结论
A 干燥氯气通入装有鲜花的集气瓶中 鲜花褪色 氯气有漂白性
B 将KI溶液滴加到酸性溶液中,边加边振荡 溶液褪色 KI具有还原性
C 向某溶液中先加入溶液,再加入稀硝酸 产生白色沉淀 该溶液中一定含有
D 向溶液中加入一小块钠 有红色固体生成 Na与发生了置换反应
12.用途广泛,常用作催化剂、脱水剂。利用金属钠可制备,有关化学方程式为(未配平):ⅰ.;ⅱ.。下列说法错误的是( )
A.、均属于氧化物 B.反应ⅰ、ⅱ均为氧化还原反应
C.氧化性: D.反应ⅱ产生的可做反应保护气
13.常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为。下列说法正确的是( )
A.还原产物为和KCl
B.还原剂和氧化剂的物质的量之比为11∶6
C.可用石灰乳吸收反应产生的制备漂白粉
D.产生1 mol 时,反应中转移5 mol
14.粗食盐中常含有钙盐、镁盐、硫酸盐等可溶性杂质,一种制备精盐的工艺流程如下图所示。下列说法正确的是( )
A.操作Ⅰ、Ⅱ、Ⅲ都要用到玻璃棒
B.若试剂1是NaOH溶液,则试剂2是溶液
C.白色沉淀的成分为氢氧化镁和碳酸钙
D.试剂4的作用是中和,除去
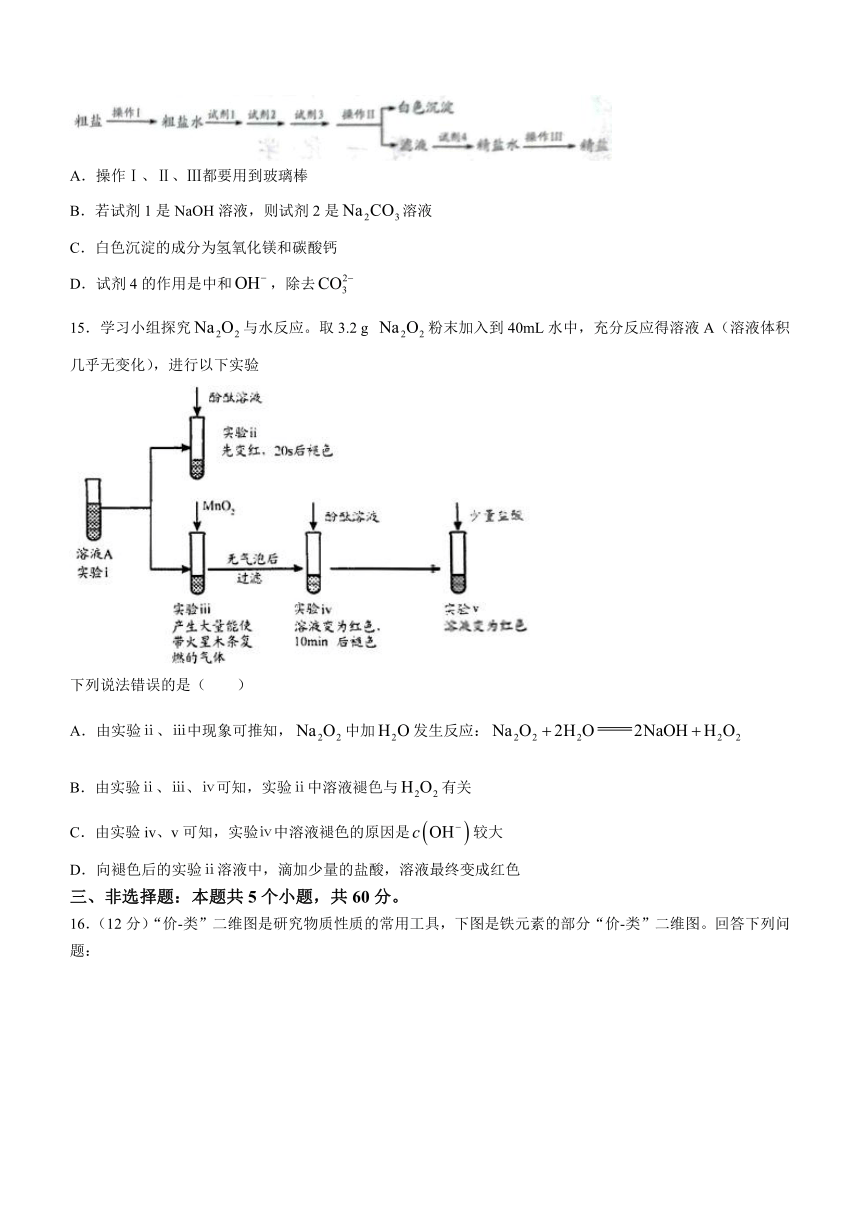
15.学习小组探究与水反应。取3.2 g 粉末加入到40mL水中,充分反应得溶液A(溶液体积几乎无变化),进行以下实验
下列说法错误的是( )
A.由实验ⅱ、ⅲ中现象可推知,中加发生反应:
B.由实验ⅱ、ⅲ、ⅳ可知,实验ⅱ中溶液褪色与有关
C.由实验iv、v可知,实验ⅳ中溶液褪色的原因是较大
D.向褪色后的实验ⅱ溶液中,滴加少量的盐酸,溶液最终变成红色
三、非选择题:本题共5个小题,共60分。
16.(12分)“价-类”二维图是研究物质性质的常用工具,下图是铁元素的部分“价-类”二维图。回答下列问题:
(1)是一种用途广泛的盐类物质。
①用坩埚钳夹住一束铁丝,灼烧后立即放入充满氯气的集气瓶中,观察到的现象是____________,发生反应的化学方程式为____________。
②实验室中制取胶体的步骤依次为:a.用洁净的烧杯取少量蒸馏水;b.用酒精灯加热至沸腾;c.…;d.至液体呈透明的红褐色。其中步骤c是______,证明胶体制备成功的实验是____________。
(2)写出一个能生成且属于氧化还原反应的化学方程式____________。
(3)根据上述“价-类”二维图、判断中Fe元素价态有______,写出与稀盐酸反应的离子方程式____________。
17.(12分)据光明网报道,陕西一名女子在打扫卫生时,误将洁厕灵和84消毒液混合使用,结果产生大量黄绿色气体。某小组同学用84消毒液配制480 mL mol L的溶液,并设计实验探究产生黄绿色气体的原因。
已知:ⅰ.84消毒液标签如下:
【产品名称】84消毒液 【有效成分】NaClO 【规格】1000mL 【浓度】4.0 mol L 注意: ①按一定比例稀释后使用 ②不得与酸性产品(如洁厕灵)同时使用
ⅱ.洁厕灵主要成分为稀盐酸。
回答下列问题:
(1)配制NaClO溶液需用量筒量取上述84消毒液______mL。实验用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、______(填写仪器名称)
(2)配制操作可分解成如下几步,其正确的操作顺序是______(填字母代号).
a.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液一并转移入容量瓶中
b.根据计算,用量筒量取一定体积的84消毒液
e.用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切
d.将84消毒液倒入盛有约50 mL,蒸馏水的烧杯中,并用玻璃橡慢慢搅拌
e.盖好容量瓶瓶塞,反复上下颠倒,摇匀
f.将稀释后的84消毒液沿玻璃棒注入经检查不漏水的容量瓶中
g.继续向容量瓶中加蒸馏水,使液面接近容量瓶上的刻度线
(3)下列操作会导致所配NaClO溶液浓度偏高的是______(填代号)
A.取用的84消毒液久置于空气中
B.用量筒量取84消毒液后,洗涤量筒2~3次,洗涤液一并倒入烧杯中
C.定容操作时,俯视刻度线
D.定容后摇匀,液面低于刻度线,再加水至刻度线
(4)利用如图装置探究84消毒液与洁厕灵混合产生黄绿色气体的原因,当注射器中的洁厕灵注入试管中时,可观察到湿润的淀粉KI试纸变蓝、支管口处产生黄绿色气体。
①湿润的淀粉KI试纸变蓝的原因是____________(用离子方程式回答)。
②上述装置存在缺陷,请提出改进措施______(回答1条)。
③写出产生黄绿色气体反应的离子方程式____________。
18.(12分)化学兴趣小组为探究Na与的反应,设计如图所示实验装置。已知:能被CO还原得到黑色的金属Pd。
回答下列问题:
(1)组装仪器后首先进行的操作是____________。
(2)装置C中的试剂是______。
(3)点燃酒精灯前应通入一段时间,其目的是____________,当观察到______现象时、点燃酒精灯。
(4)小组同学根据氧化还原理论和相关实验现象、分析Na与反应的产物。
①同学甲预测会有CO生成。能确认甲预测正确的实验现象是____________。
②同学乙预测反应后装置B中残留固体的主要成分为,同学丙预测还应该有,丙的理由是____________(用化学方程式表示),若要验证丙同学的预测,需要的试剂为______。
19.(12分)次氯酸消毒液高效安全,适用于一般物体表面消毒、空间和环境消毒实验室利用如下装置制取氯气并制取次氯酸消毒液。
回答下列问题:
(1)装置合理的连接顺序为a→______(按气流方向填各接口的编号)
(2)装置Ⅰ中反应的化学方程式是____________。
(3)装置Ⅱ中试剂X是______;装置Ⅲ的作用是____________;装置Ⅳ中多孔球泡的作用为____________。
(4)反应结束后,取Ⅳ中少量液体于试管中,滴入几滴石蕊观察到的现象是____________,请结合离子方程式说明原因____________。
20.(12分)过碳酸钠(,相对分子质量为314)俗名固体双氧水。是一种新型家用清洁剂和消毒剂,具有碳酸钠和双氧水的双重性质,其3%水溶液显减性。工业上利用和采用“醇析法”制取过碳酸钠晶体的工艺流程等下:
已知:极易溶于水,难溶于乙醇
回答下列问题:
(1)“控温、50℃反应”目的是防止过碳酸钠受热分解,写出过碳酸钠受热分解的化学方程式____________。
(2)“操作a”的名称是______,完成此操作需要的玻璃仪器有烧杯、玻璃棒和______;“洗涤”所用试剂为______。
(3)查阅资料知过碳酸钠在水溶液中氧化性更强,原因是与反应转化为氧化性更强的。写出过碳酸钠溶液中产生的离子方程式____________。
(4)市售过碳酸钠一般都含有碳酸钠,现用以下方案测定某过碳酸钠样品的纯度:称量73.4g样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发结晶;称量所得国体质量为58.5g。
①“全部溶于水中并加入足量稀盐酸”产生两种无色无味的气体,写出该反应的化学方程式__________________;
②该样品中过碳酸钠的质量分数为______(保留小数点后一位)
潍坊市2023-2024学年高一上学期期中考试
化学参考答案及评分标准
1.D 2.B 3.B 4.A 5.D 6.D 7.C 8.B 9.A 10.D
11.B 12.C 13.AC 14.AD 15.D
16.(12分)
(1)①铁丝在氯气中剧烈燃烧,产生棕红色的烟(2分) (2分)
②向烧杯中逐滴滴加饱和溶液(2分)丁达尔现象(1分)
(2)(2分,合理即给分)
(3)+2、+3(1分) (2分)
17.(12分)
(1)7.5(2分,答“7.50”不得分) 500 mL容量瓶(1分,仅回答“容量瓶”不得分)
(2)bdfagce(2分)(3)BC(2分,答对1个得1分,错选或多选不得分)
(4)①(2分)
②在支管口处接气囊或连接盛有NaOH溶液的烧杯中(1分,合理即给分)
③(2分)
18.(12分)
(1)检验装置的气密性(1分)(2)浓硫酸(1分)
(3)排尽装置中空气(2分) D中出现较多白色沉淀(2分)
(4)①装置E中出现黑色固体(2分)
②(2分) 稀盐酸和澄清石灰水(2分)
19.(12分)
(1)d→e→f→g→b→c(2分)
(2)(浓)(2分,不写条件和“浓”扣1分)
(3)氢氧化钠溶液(1分) 除去氯气中的HCl(1分)
增大氯气与水的接触面积让氯气与水充分反应(2分)
(4)溶液先变红后褪色(2分) ;反应后溶液呈酸性,使石蕊变红,生成HClO,使红色褪去(2分)
20.(12分)
(1)(2分)
(2)过滤(1分) 漏斗(1分) 无水乙醇(2分)
(3)(2分)
4)①(2分)②85.6%(2分)
化学
注意事项:
1.答题前,考生先将自己的学校、班级、姓名、考生号、座号填写在答题卡相应位置。
2.选择题答案必须使用2B铅笔(按填涂样例)正确填涂;非选择题答案必须使用0.5mm黑色签字笔书写在相应答题区域,超出答题区域书写的答案无效;在草稿纸和试卷上答题无效。
3.本试卷满分100分,考试时间90分钟。
可能用到的相对原子质量:H1 C12 O16 Na23 Cl35.5 Cu64
一、选择题:本题共10个小题,每小题2分,共20分。每小题只有一个选项符合题意。
1.化学与生产、生活密切相关。下列说法错误的是( )
A.金属钠导热性好,可用作传热介质 B.二氧化氯可用于自来水消毒
C.硫酸钙可用于由豆浆制豆腐 D.碳酸钠常用于治疗胃酸过多
2.有关物质性质,下列叙述正确的是( )
A.金属钠在空气中燃烧生成淡黄色固体
B.金属钠与水反应后的溶液呈碱性
C.具有刺激性气味,因此可杀灭细菌和病毒
D.氢气在氯气中燃烧产生淡蓝色火焰
3.下列关于实验仪器①~⑤的说法错误的是( )
A.①④使用前需要检查是否漏水
B.②③可以直接加热
C.从NaCl溶液中得到NaCl固体用到的仪器有③
D.在⑤中进行金属钠的燃烧实验
4.生活中用自来水养金鱼时,需将自来水先在阳光下暴晒一段时间的主要目的是( )
A.分解除去次氯酸 B.紫外线杀熊消毒
C.增加水中含量 D.提高水的温度
5.下列变化中,需要通过加入氧化剂实现的是( )
A. B. C. D.
6.为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,22.4 L 中含有的分子数为
B.常温常压下,6.4 g Cu与足量充分反应,转移的电子数为
C.常温常压下,1.5 mol L的溶液中含有的数目为
D.标准状况下,2.24 L CO和混合气体中含有的碳原子数为
7.利用下列装置进行实验,相关叙述错误的是( )
A.利用①提纯淀粉胶体 B.利用②验证Na和水反应时放出热量
C.利用③配制0.10 mol L NaOH溶液 D.利用④检验与反应有生成
8.高炉炼铁过程中存在反应:。下列选项中可以说明0.3 mol 与0.2 mol CO充分反应后物质的种类及其数量情况的是( )
A.0.1 mol mol mol
B.0.1 mol mol mol
C.0.6 mol mol
D.0.1 mol mol mol
9.下列叙述对应的离子方程式书写正确的是( )
A.向溶液中滴入溶液至产生的沉淀质量最大:
B.向溶液中加入过量NaOH溶液:
C.过氧化钠作供氧剂与水反应:
D.向溶液中通入少量:
10.经检测,某工业废水显酸性,且废水中含有大量、、、下列离子中,不可能大量存在于该废水中的是( )
A. B. C. D.
二、选择题:本题共5小题,每题4分,共20分。每小题有一个或两个选项符合题意,全选对得4分,选对但不全的得2分,有选错的得0分。
11.下列实验中,对应的操作、现象以及结论都正确的是( )
选项 操作 现象 结论
A 干燥氯气通入装有鲜花的集气瓶中 鲜花褪色 氯气有漂白性
B 将KI溶液滴加到酸性溶液中,边加边振荡 溶液褪色 KI具有还原性
C 向某溶液中先加入溶液,再加入稀硝酸 产生白色沉淀 该溶液中一定含有
D 向溶液中加入一小块钠 有红色固体生成 Na与发生了置换反应
12.用途广泛,常用作催化剂、脱水剂。利用金属钠可制备,有关化学方程式为(未配平):ⅰ.;ⅱ.。下列说法错误的是( )
A.、均属于氧化物 B.反应ⅰ、ⅱ均为氧化还原反应
C.氧化性: D.反应ⅱ产生的可做反应保护气
13.常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为。下列说法正确的是( )
A.还原产物为和KCl
B.还原剂和氧化剂的物质的量之比为11∶6
C.可用石灰乳吸收反应产生的制备漂白粉
D.产生1 mol 时,反应中转移5 mol
14.粗食盐中常含有钙盐、镁盐、硫酸盐等可溶性杂质,一种制备精盐的工艺流程如下图所示。下列说法正确的是( )
A.操作Ⅰ、Ⅱ、Ⅲ都要用到玻璃棒
B.若试剂1是NaOH溶液,则试剂2是溶液
C.白色沉淀的成分为氢氧化镁和碳酸钙
D.试剂4的作用是中和,除去
15.学习小组探究与水反应。取3.2 g 粉末加入到40mL水中,充分反应得溶液A(溶液体积几乎无变化),进行以下实验
下列说法错误的是( )
A.由实验ⅱ、ⅲ中现象可推知,中加发生反应:
B.由实验ⅱ、ⅲ、ⅳ可知,实验ⅱ中溶液褪色与有关
C.由实验iv、v可知,实验ⅳ中溶液褪色的原因是较大
D.向褪色后的实验ⅱ溶液中,滴加少量的盐酸,溶液最终变成红色
三、非选择题:本题共5个小题,共60分。
16.(12分)“价-类”二维图是研究物质性质的常用工具,下图是铁元素的部分“价-类”二维图。回答下列问题:
(1)是一种用途广泛的盐类物质。
①用坩埚钳夹住一束铁丝,灼烧后立即放入充满氯气的集气瓶中,观察到的现象是____________,发生反应的化学方程式为____________。
②实验室中制取胶体的步骤依次为:a.用洁净的烧杯取少量蒸馏水;b.用酒精灯加热至沸腾;c.…;d.至液体呈透明的红褐色。其中步骤c是______,证明胶体制备成功的实验是____________。
(2)写出一个能生成且属于氧化还原反应的化学方程式____________。
(3)根据上述“价-类”二维图、判断中Fe元素价态有______,写出与稀盐酸反应的离子方程式____________。
17.(12分)据光明网报道,陕西一名女子在打扫卫生时,误将洁厕灵和84消毒液混合使用,结果产生大量黄绿色气体。某小组同学用84消毒液配制480 mL mol L的溶液,并设计实验探究产生黄绿色气体的原因。
已知:ⅰ.84消毒液标签如下:
【产品名称】84消毒液 【有效成分】NaClO 【规格】1000mL 【浓度】4.0 mol L 注意: ①按一定比例稀释后使用 ②不得与酸性产品(如洁厕灵)同时使用
ⅱ.洁厕灵主要成分为稀盐酸。
回答下列问题:
(1)配制NaClO溶液需用量筒量取上述84消毒液______mL。实验用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、______(填写仪器名称)
(2)配制操作可分解成如下几步,其正确的操作顺序是______(填字母代号).
a.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液一并转移入容量瓶中
b.根据计算,用量筒量取一定体积的84消毒液
e.用胶头滴管滴加蒸馏水,至溶液的凹液面与刻度线相切
d.将84消毒液倒入盛有约50 mL,蒸馏水的烧杯中,并用玻璃橡慢慢搅拌
e.盖好容量瓶瓶塞,反复上下颠倒,摇匀
f.将稀释后的84消毒液沿玻璃棒注入经检查不漏水的容量瓶中
g.继续向容量瓶中加蒸馏水,使液面接近容量瓶上的刻度线
(3)下列操作会导致所配NaClO溶液浓度偏高的是______(填代号)
A.取用的84消毒液久置于空气中
B.用量筒量取84消毒液后,洗涤量筒2~3次,洗涤液一并倒入烧杯中
C.定容操作时,俯视刻度线
D.定容后摇匀,液面低于刻度线,再加水至刻度线
(4)利用如图装置探究84消毒液与洁厕灵混合产生黄绿色气体的原因,当注射器中的洁厕灵注入试管中时,可观察到湿润的淀粉KI试纸变蓝、支管口处产生黄绿色气体。
①湿润的淀粉KI试纸变蓝的原因是____________(用离子方程式回答)。
②上述装置存在缺陷,请提出改进措施______(回答1条)。
③写出产生黄绿色气体反应的离子方程式____________。
18.(12分)化学兴趣小组为探究Na与的反应,设计如图所示实验装置。已知:能被CO还原得到黑色的金属Pd。
回答下列问题:
(1)组装仪器后首先进行的操作是____________。
(2)装置C中的试剂是______。
(3)点燃酒精灯前应通入一段时间,其目的是____________,当观察到______现象时、点燃酒精灯。
(4)小组同学根据氧化还原理论和相关实验现象、分析Na与反应的产物。
①同学甲预测会有CO生成。能确认甲预测正确的实验现象是____________。
②同学乙预测反应后装置B中残留固体的主要成分为,同学丙预测还应该有,丙的理由是____________(用化学方程式表示),若要验证丙同学的预测,需要的试剂为______。
19.(12分)次氯酸消毒液高效安全,适用于一般物体表面消毒、空间和环境消毒实验室利用如下装置制取氯气并制取次氯酸消毒液。
回答下列问题:
(1)装置合理的连接顺序为a→______(按气流方向填各接口的编号)
(2)装置Ⅰ中反应的化学方程式是____________。
(3)装置Ⅱ中试剂X是______;装置Ⅲ的作用是____________;装置Ⅳ中多孔球泡的作用为____________。
(4)反应结束后,取Ⅳ中少量液体于试管中,滴入几滴石蕊观察到的现象是____________,请结合离子方程式说明原因____________。
20.(12分)过碳酸钠(,相对分子质量为314)俗名固体双氧水。是一种新型家用清洁剂和消毒剂,具有碳酸钠和双氧水的双重性质,其3%水溶液显减性。工业上利用和采用“醇析法”制取过碳酸钠晶体的工艺流程等下:
已知:极易溶于水,难溶于乙醇
回答下列问题:
(1)“控温、50℃反应”目的是防止过碳酸钠受热分解,写出过碳酸钠受热分解的化学方程式____________。
(2)“操作a”的名称是______,完成此操作需要的玻璃仪器有烧杯、玻璃棒和______;“洗涤”所用试剂为______。
(3)查阅资料知过碳酸钠在水溶液中氧化性更强,原因是与反应转化为氧化性更强的。写出过碳酸钠溶液中产生的离子方程式____________。
(4)市售过碳酸钠一般都含有碳酸钠,现用以下方案测定某过碳酸钠样品的纯度:称量73.4g样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发结晶;称量所得国体质量为58.5g。
①“全部溶于水中并加入足量稀盐酸”产生两种无色无味的气体,写出该反应的化学方程式__________________;
②该样品中过碳酸钠的质量分数为______(保留小数点后一位)
潍坊市2023-2024学年高一上学期期中考试
化学参考答案及评分标准
1.D 2.B 3.B 4.A 5.D 6.D 7.C 8.B 9.A 10.D
11.B 12.C 13.AC 14.AD 15.D
16.(12分)
(1)①铁丝在氯气中剧烈燃烧,产生棕红色的烟(2分) (2分)
②向烧杯中逐滴滴加饱和溶液(2分)丁达尔现象(1分)
(2)(2分,合理即给分)
(3)+2、+3(1分) (2分)
17.(12分)
(1)7.5(2分,答“7.50”不得分) 500 mL容量瓶(1分,仅回答“容量瓶”不得分)
(2)bdfagce(2分)(3)BC(2分,答对1个得1分,错选或多选不得分)
(4)①(2分)
②在支管口处接气囊或连接盛有NaOH溶液的烧杯中(1分,合理即给分)
③(2分)
18.(12分)
(1)检验装置的气密性(1分)(2)浓硫酸(1分)
(3)排尽装置中空气(2分) D中出现较多白色沉淀(2分)
(4)①装置E中出现黑色固体(2分)
②(2分) 稀盐酸和澄清石灰水(2分)
19.(12分)
(1)d→e→f→g→b→c(2分)
(2)(浓)(2分,不写条件和“浓”扣1分)
(3)氢氧化钠溶液(1分) 除去氯气中的HCl(1分)
增大氯气与水的接触面积让氯气与水充分反应(2分)
(4)溶液先变红后褪色(2分) ;反应后溶液呈酸性,使石蕊变红,生成HClO,使红色褪去(2分)
20.(12分)
(1)(2分)
(2)过滤(1分) 漏斗(1分) 无水乙醇(2分)
(3)(2分)
4)①(2分)②85.6%(2分)
同课章节目录
