专题 化学反应速率与化学平衡----能力提升练 课件(共39张PPT)
文档属性
| 名称 | 专题 化学反应速率与化学平衡----能力提升练 课件(共39张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-23 00:00:00 | ||
图片预览









文档简介
(共39张PPT)
专题 化学反应速率与化学平衡
----能力提升练
能力提升练
1.(2023·江苏泰州中学调研)高炉炼铁的反应为Fe2O3(s)+3CO(g) ══ 2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1。下列有关说法正确的是( )
A.该反应一定能自发进行,则该反应的ΔS>0
B.升高温度使反应物活化分子数增多,能提高反应速率和CO平衡转化率
C.增加炼铁炉高度,延长CO和铁矿石接触时间,能降低平衡时尾气中CO的体积分数
D.制备的生铁中含少量FexC,相同条件下与酸反应放出氢气的速率比纯铁慢
A
解析 该反应的反应热ΔH<0,要使反应自发进行,要满足ΔH-TΔS<0,则该反应的ΔS>0,A正确;升高温度,使反应物活化分子数增多,能提高反应速率,但由于该反应是放热反应,升高温度,化学平衡会向逆反应方向移动,导致CO平衡转化率降低,B错误;增加炼铁炉高度,延长CO和铁矿石接触时间,不改变其他外界条件,化学平衡不移动,故不能改变平衡时混合气体中CO的体积分数,C错误;制备生铁中若含少量FexC,Fe、FexC及酸溶液构成原电池,使Fe与酸反应放出氢气的速率比纯铁快,D错误。
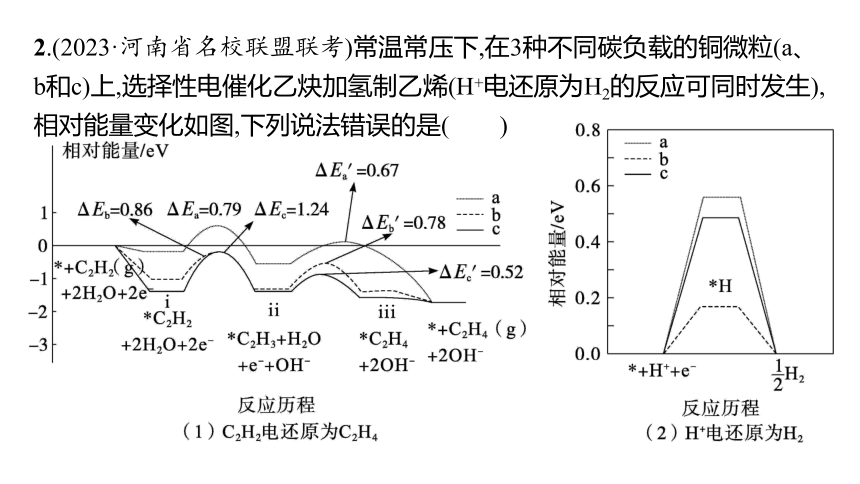
2.(2023·河南省名校联盟联考)常温常压下,在3种不同碳负载的铜微粒(a、b和c)上,选择性电催化乙炔加氢制乙烯(H+电还原为H2的反应可同时发生),相对能量变化如图,下列说法错误的是( )
A.析氢反应是电催化乙炔加氢制乙烯的竞争反应
B.析氢反应的能力:a>c>b
C.吸附C2H2的能力:aD.ⅰ生成ⅱ是乙炔加氢制乙烯反应历程中的决速步骤
答案 B
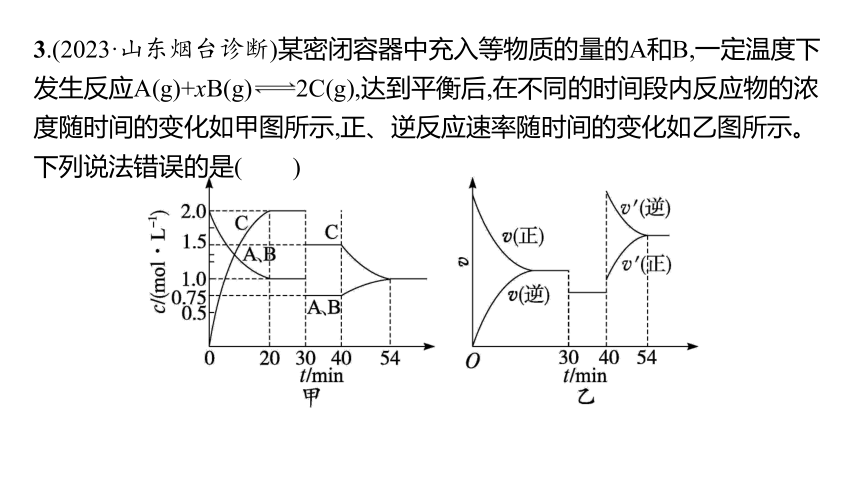
解析 选择性电催化乙炔加氢制乙烯和H+电还原为H2的反应可同时发生,均为得到电子被还原的过程,故析氢反应是电催化乙炔加氢制乙烯的竞争反应,A正确;a对应的活化能最大,b对应的活化能最小,活化能越大反应越难进行,即析氢反应的能力:a3.(2023·山东烟台诊断)某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平衡后,在不同的时间段内反应物的浓度随时间的变化如甲图所示,正、逆反应速率随时间的变化如乙图所示。下列说法错误的是( )
A.前20 min B的平均反应速率为0.05 mol·L-1·min-1
B.30~40 min间该反应使用了催化剂
C.化学方程式中的x=1,正反应为放热反应
D.30 min、40 min时分别改变的条件是减小压强、升高温度
答案 B
解析 前20 min B的平均反应速率为
=0.05 mol·L-1·min-1,A正确;30 min时,C和A、B的浓度都下降,而催化剂只会改变反应速率,不会瞬间改变反应物的浓度,B错误;A、B的浓度变化相同,故A、B的化学计量数相同,则x=1,40 min时正逆反应速率都增大,则改变的条件为升高温度,而条件改变后C浓度减小,A、B浓度增大,说明平衡发生了逆向移动,则正反应为放热反应,C正确;30 min时,C和A、B的浓度都下降了,反应速率也减小,但是平衡不移动,经分析x=1,该反应前后气体分子数目不变,则改变的条件为减小压强,D正确。
4.(2023·天津十二区重点校联考)某温度下,在2 L的密闭容器中,加入1 mol X(g)和2 mol Y(g)发生反应:X(g)+mY(g) 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1 mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是( )
A.m=2
B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为1∶1
D.第二次平衡时,Z的浓度为0.4 mol·L-1
D
解析 向平衡体系中加入1 mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变,说明两种平衡相同,该反应前后气体的总体积不变,则有m+1=3,m=2,A正确;平衡常数只与温度有关,两次平衡温度不变,故两次平衡的平衡常数相同,B正确;起始量X与Y之比为1∶2,等于其化学计量数之比,故X与Y的平衡转化率之比为1∶1,C正确;该反应为反应前后气体总量不变的反应,故第二次平衡时Z的物质的量为4 mol×10%=0.4 mol,c(Z)= =0.2 mol·L-1, D错误。
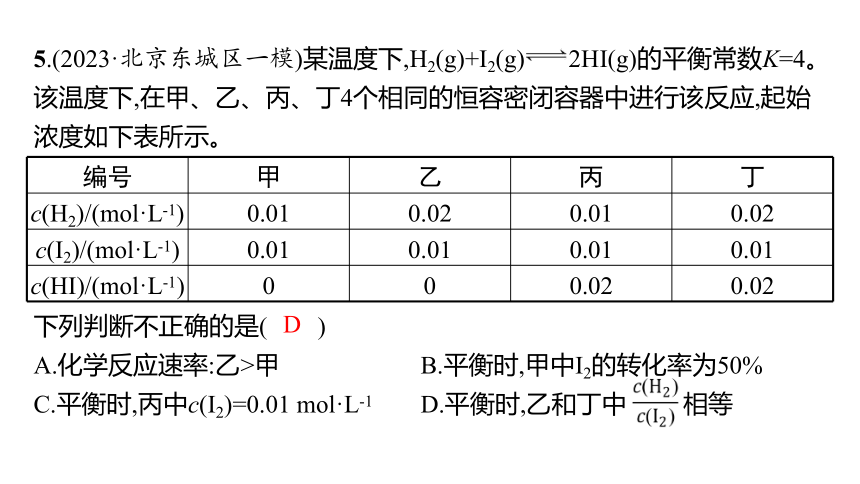
5.(2023·北京东城区一模)某温度下,H2(g)+I2(g) 2HI(g)的平衡常数K=4。该温度下,在甲、乙、丙、丁4个相同的恒容密闭容器中进行该反应,起始浓度如下表所示。
编号 甲 乙 丙 丁
c(H2)/(mol·L-1) 0.01 0.02 0.01 0.02
c(I2)/(mol·L-1) 0.01 0.01 0.01 0.01
c(HI)/(mol·L-1) 0 0 0.02 0.02
下列判断不正确的是( )
A.化学反应速率:乙>甲 B.平衡时,甲中I2的转化率为50%
C.平衡时,丙中c(I2)=0.01 mol·L-1 D.平衡时,乙和丁中 相等
D
解析 据题表中数据可知,其他条件相同,乙中c(H2)为甲中的2倍,乙中反应速率较大,A正确;设甲中I2的转化率为x,根据“三段式”有:
H2(g) + I2(g) 2HI(g)
起始/(mol·L-1) 0.01 0.01 0
变化/(mol·L-1) 0.01x 0.01x 0.02x
平衡/(mol·L-1) 0.01(1-x) 0.01(1-x) 0.02x
6.(2023·辽宁葫芦岛协作校联考)某温度下,在1 L恒容密闭容器中投入10 mol N2O5发生反应N2O5(g) N2O(g)+2O2(g),有关数据如下表所示。下列说法正确的是( )
时间/s 0~10 10~20 20~30 30~40
产物O2的平均生成速率/(mol·L-1·s-1) 0.20 0.16 0.10 0.00
A.O2的平均生成速率越来越小是因为容器的压强越来越小
B.15 s若向体系中充入N2O,平衡一定逆向移动
C.20 s时N2O5的转化率为8%
D.35 s时,向体系中又充入N2O5,再次平衡时,其体积分数将增大
D
解析 O2的平均生成速率越来越小,主要是N2O5的浓度减小,A错误;15 s时,该体系还没有达到平衡状态,如果N2O的量很少,在一定温度下,若Q7.(2023·湖北省部分重点校联考)恒温密闭容器发生可逆反应: Z( )+W( )
X(g)+Y( ) ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后不再改变条件。下列有关说法中,正确的是( )
A.该条件下,Z和W中的一种可能为气态
B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不相等
C.若在该温度下该反应的平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等
D.若该反应ΔH>0,则该反应的平衡常数K随温度升高而增大
D
解析 根据题图可知,正反应速率不随反应时间和压强的改变而改变,故Z和W都不是气体,A错误;结合题图可知,X是气体,Y可能不是气体,也可能是气体,若Y不是气体,产物只有X,反应过程中气体的摩尔质量始终不变,若Y是气体,由于生成的X和Y是按照比例生成的,气体平均摩尔质量不会改变,所以两时间段反应体系中气体的平均摩尔质量一定相等,B错误;由于化学平衡常数只与温度有关,该温度下平衡常数的表达式K=c(X)是定值,则t1~t2时间段与t3时刻后的c(X)相等,C错误;该反应ΔH>0则该反应是吸热反应,升高温度平衡正向移动,平衡常数增大,D正确。
8.(2023·广东东莞一模)恒温恒容条件下,向密闭容器中加入一定量X,发生反应:①X(g) Y(g);②Y(g) Z(g)。已知v=kc(反应物),k为速率常数,如图表明三种物质浓度随时间的变化以及k受温度的影响。下列说法不正确的是( )
A.反应过程体系的压强始终不变
B.c(Y)随时间先增大后减小
C.随c(X)的减小,反应①、②的速率
均逐渐降低
D.温度对反应②的k影响更大
C
解析 由题图1中信息可知,浓度随时间变化逐渐减小的曲线为X,浓度随时间变化逐渐增大的曲线为Z,浓度随时间变化先增大后减小的曲线为Y。由题图2中信息可知,反应①的速率常数随温度升高增大的幅度小于反应②。两反应中,反应物和生成物都只有一种,且化学计量数都为1,故反应过程中气体的物质的量始终不变,压强始终不变,A正确;c(Y)随时间先增大后减小,B正确;随c(X)的减小,c(Y)先增大后减小,c(Z)不断增大,则反应①的速率逐渐降低,但反应②的速率先升高后降低,C错误;随着温度的升高,反应②的速率常数增大的幅度更大,故温度对反应②的k影响更大,D正确。
9.(2023·湖南郴州一模)T0时,在
2 L的密闭容器中发生反应: X(g)+Y(g) Z(g)(未配平),各物质的物质的量随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应,X的物质的量随时间变化的关系如图b所示。下列叙述中正确的是( )
A.该反应的正反应是吸热反应
B.T0时,从反应开始到平衡时:v(X)=0.083 mol·L-1·min-1
C.图a中反应达到平衡时,Y的转化率为37.5%
D.T1时,若该反应的平衡常数K的值为50,则T1D
10.(2023·北京延庆区一模)在一定温度下,将1 mol CO2和3 mol H2充入容积为1 L的恒容密闭容器中发生反应并达到平衡:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,测得平衡混合气体中CH3OH的物质的量分数为25%。下列说法不正确的是( )
A.平衡混合气体中C原子的物质的量是1 mol
B.该反应的反应物的总能量高于生成物的总能量
C.该反应的化学平衡常数K=
D.其他条件相同时,若起始充入2 mol CO2和6 mol H2,达到平衡时CH3OH的物质的量分数大于25%
C
解析 根据质量守恒定律可知,1 mol CO2参与反应,平衡时混合气体中C原子的物质的量仍为1 mol,A正确;该反应的ΔH<0,则该反应的反应物的总能量高于生成物的总能量,B正确;设CO2的转化浓度为x mol·L-1,利用“三段式”计算:
CO2(g) + 3H2(g) CH3OH(g) + H2O(g)
11.(2023·河南洛阳六校联考)氢气是一种清洁能源,工业上用水煤气两步法制氢气,第①、②步的反应原理及反应的lg Kp-T关系如图所示。下列有关说法正确的是( )
A.反应C(s)+H2O(g) CO(g)+H2(g) ΔH1<0
B.NiFe2O4能降低反应的活化能,提高平衡转化率
C.某温度下,将CO和H2O(g)各1 mol通入容积为1 L的密闭容器中反应,达到平衡状态,若该反应的平衡常数是9,则CO的转化率为75%
D.1 300 ℃时,反应C(s)+2H2O(g) CO2(g)+2H2(g)的平衡常数Kp=8
答案 C
解析 对于反应①,升高温度,lg Kp增大,说明升高温度,该反应正向移动,则该反应是吸热反应,ΔH1>0,A错误;NiFe2O4是反应的催化剂,催化剂能降低反应的活化能,但不能改变转化率,B错误;设CO的转化量为x mol,根据已知条件列出“三段式”:
CO(g)+H2O(g) CO2(g) + H2(g)
起始/mol 1 1 0 0
转化/mol x x x x
平衡/mol 1-x 1-x x x
12.(2023·湖南省名校联合体联考)一定条件下,分别向容积为1 L的密闭容器中充入气体,发生反应:X(g)+Y(g) Z(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是( )
实验 充入气体量 反应过程条件
① 2 mol X+1 mol Y 恒温
② 1 mol Z 恒温
③ 1 mol Z 绝热
A.曲线Ⅰ对应实验② B.正反应为吸热反应
C.气体的总物质的量:n(c)D
解析 恒温恒容条件下,气体的压强之比等于其物质的量之比,故起始时实验②与③的压强相等,实验①的压强是实验②、③的3倍,则曲线Ⅰ对应实验①,且m=3p,A错误;若实验②与③的温度相等,最终会达到相同的平衡状态,气体压强应相同,实际上曲线Ⅱ的压强大于曲线Ⅲ,说明Ⅱ对应反应气体的总物质的量大,绝热体系不利于Z的分解反应,故该反应正反应是放热反应,B错误;c、d两点的压强相同,体积相同,由于反应吸热,体系③温度低,c点的温度比d点低,则c点的气体物质的量更多,故气体的总物质的量:n(c)>n(d),C错误;该反应是放热反应,温度越低,平衡常数越大,故b点平衡常数小于c点,D正确。
13.(2023·山西忻州一模)为了实现碳达峰和碳中和目标,二氧化碳的高效利用成为研究的热点。某研究小组采用双合金团簇催化甲烷干法重整法(DRM)取得了良好的效果。已知:CH4、H2、CO的燃烧热分别为-890.3 kJ·mol-1、-285.8 kJ·mol-1和-283 kJ·mol-1。
(1)甲烷干法重整法(DRM)反应为CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH,则ΔH= 。
+247.3 kJ·mol-1
(2)通过大量的研究Pt12Ni、Sn12Ni、Cu12Ni三种双合金团簇可用于催化DRM反应,在催化剂表面涉及多个基元反应,分别为过程1:甲烷逐步脱氢,过程2:CO2的活化(包括直接活化和氢诱导活化),过程3:C*和CH*的氧化,过程4:扩散吸附反应。其反应机理如图1所示。则CO2的氢诱导活化反应方程式
图1
为 ,
过程3的最终产物为 ,过程4发生扩散
吸附的微粒为 。
CO2*+H* ══ CO*+OH*
CO*
H*和OH*
(3)三种催化剂催化甲烷脱氯过程的能量变化如图2所示:
图2
①甲烷脱氢过程中最大活化能步骤为
(用反应方程式表示)。
②Sn12Ni、Pt12Ni、Cu12Ni三种催化剂
催化甲烷脱氢过程的脱氢速率分别为
v1、v2、v3,则脱氢速率由大到小的顺序为 。
③Sn12Ni双合金团簇具有良好的抗积碳
作用,有效抑制碳沉积对催化剂造成的
不良影响,请结合图示解释原因:________________________________________
。
CH3* ══ CH2*+H*
v2>v3>v1
脱氢反应第4步为CH*C*+H*,发生该步反应,
三种催化剂中Sn12Ni需要克服的活化能最大,反应不易发生,故产生的积碳较少
(4)已知:甲烷干法重整法(DRM)过程中发生副反应CO2(g)+H2(g) CO(g)+H2O(g) ΔH>0,T ℃时,在恒压反应器中,通入2 mol CH4和1 mol CO2,总压强为p0,平衡时甲烷的转化率为40%,H2O的分压为p。
①关于上述平衡体系,下列说法正确的是 (填字母)。
A.n(CH4)∶n(CO2)=2∶1
B.将H2O(g)液化,可以提高主反应的速率
C.若反应在恒容条件下进行,甲烷转化率小于40%
D.若降低反应温度,主、副反应均逆向进行
②DRM反应的Kp= (列出计算式即可,分压=总压×物质的量分数)。
CD
(2)CO2的活化包括直接活化和氢诱导活化,在氢诱导活化中,CO2*+H*→COOH*→CO*+OH*,则CO2的氢诱导活化反应方程式为CO2*+H* ══ CO*+OH*。由题图可知,过程3的最终产物为CO*,过程1甲烷逐步脱氢生成H*,过程3 CO2的活化过程中生成OH*,故过程4发生扩散吸附的微粒为H*和OH*。
(3)①活化能最大的过程为反应的决速步骤,由题图可知,过渡态为TS2的反应为决速步骤,对应反应为CH3* ══ CH2*+H*;②催化剂能够降低反应的活化能,活化能越低,则化学反应速率越大,则有v2>v3>v1;③由题图可知,脱氢反应第4步为CH* ══ C*+H*,发生该步反应,三种催化剂中Sn12Ni需要克服的活化能最大,反应不易发生,故产生的积碳较少。
(4)①投入量n(CH4)∶n(CO2)=2∶1,主反应消耗量n(CH4)∶n(CO2)=1∶1,副反应消耗CO2,因此主副反应消耗量n(CH4)∶n(CO2)≠2∶1,则平衡时体系中n(CH4)∶n(CO2)≠2∶1,A错误;将H2O(g)液化,副反应正向移动,导致CO2和H2浓度减小,CO浓度增大,则主反应的速率减慢,B错误;主反应正向为体积增大的反应,若反应在恒容条件下进行,等效于在恒压的基础上,缩小容积加压,主反应平衡逆向移动,则甲烷转化率小于40%,C正确;由于主、副反应正反应均为吸热反应,则若降低反应温度,主、副反应均逆向进行,D正确。
②对主反应列出“三段式”:
CH4(g)+CO2(g) 2CO(g)+2H2(g)
起始量/mol 2 1 0 0
变化量/mol 0.8 0.8 1.6 1.6
平衡量/mol 1.2 0.2 1.6 1.6
平衡时,设水的物质的量为x mol,根据副反应列“三段式”:
H2(g)+CO2(g) CO(g)+H2O(g)
起始量/mol 1.6 0.2 1.6 0
变化量/mol x x x x
平衡量/mol 1.6-x 0.2-x 1.6+x x
专题 化学反应速率与化学平衡
----能力提升练
能力提升练
1.(2023·江苏泰州中学调研)高炉炼铁的反应为Fe2O3(s)+3CO(g) ══ 2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1。下列有关说法正确的是( )
A.该反应一定能自发进行,则该反应的ΔS>0
B.升高温度使反应物活化分子数增多,能提高反应速率和CO平衡转化率
C.增加炼铁炉高度,延长CO和铁矿石接触时间,能降低平衡时尾气中CO的体积分数
D.制备的生铁中含少量FexC,相同条件下与酸反应放出氢气的速率比纯铁慢
A
解析 该反应的反应热ΔH<0,要使反应自发进行,要满足ΔH-TΔS<0,则该反应的ΔS>0,A正确;升高温度,使反应物活化分子数增多,能提高反应速率,但由于该反应是放热反应,升高温度,化学平衡会向逆反应方向移动,导致CO平衡转化率降低,B错误;增加炼铁炉高度,延长CO和铁矿石接触时间,不改变其他外界条件,化学平衡不移动,故不能改变平衡时混合气体中CO的体积分数,C错误;制备生铁中若含少量FexC,Fe、FexC及酸溶液构成原电池,使Fe与酸反应放出氢气的速率比纯铁快,D错误。
2.(2023·河南省名校联盟联考)常温常压下,在3种不同碳负载的铜微粒(a、b和c)上,选择性电催化乙炔加氢制乙烯(H+电还原为H2的反应可同时发生),相对能量变化如图,下列说法错误的是( )
A.析氢反应是电催化乙炔加氢制乙烯的竞争反应
B.析氢反应的能力:a>c>b
C.吸附C2H2的能力:a
答案 B
解析 选择性电催化乙炔加氢制乙烯和H+电还原为H2的反应可同时发生,均为得到电子被还原的过程,故析氢反应是电催化乙炔加氢制乙烯的竞争反应,A正确;a对应的活化能最大,b对应的活化能最小,活化能越大反应越难进行,即析氢反应的能力:a
A.前20 min B的平均反应速率为0.05 mol·L-1·min-1
B.30~40 min间该反应使用了催化剂
C.化学方程式中的x=1,正反应为放热反应
D.30 min、40 min时分别改变的条件是减小压强、升高温度
答案 B
解析 前20 min B的平均反应速率为
=0.05 mol·L-1·min-1,A正确;30 min时,C和A、B的浓度都下降,而催化剂只会改变反应速率,不会瞬间改变反应物的浓度,B错误;A、B的浓度变化相同,故A、B的化学计量数相同,则x=1,40 min时正逆反应速率都增大,则改变的条件为升高温度,而条件改变后C浓度减小,A、B浓度增大,说明平衡发生了逆向移动,则正反应为放热反应,C正确;30 min时,C和A、B的浓度都下降了,反应速率也减小,但是平衡不移动,经分析x=1,该反应前后气体分子数目不变,则改变的条件为减小压强,D正确。
4.(2023·天津十二区重点校联考)某温度下,在2 L的密闭容器中,加入1 mol X(g)和2 mol Y(g)发生反应:X(g)+mY(g) 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1 mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是( )
A.m=2
B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为1∶1
D.第二次平衡时,Z的浓度为0.4 mol·L-1
D
解析 向平衡体系中加入1 mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变,说明两种平衡相同,该反应前后气体的总体积不变,则有m+1=3,m=2,A正确;平衡常数只与温度有关,两次平衡温度不变,故两次平衡的平衡常数相同,B正确;起始量X与Y之比为1∶2,等于其化学计量数之比,故X与Y的平衡转化率之比为1∶1,C正确;该反应为反应前后气体总量不变的反应,故第二次平衡时Z的物质的量为4 mol×10%=0.4 mol,c(Z)= =0.2 mol·L-1, D错误。
5.(2023·北京东城区一模)某温度下,H2(g)+I2(g) 2HI(g)的平衡常数K=4。该温度下,在甲、乙、丙、丁4个相同的恒容密闭容器中进行该反应,起始浓度如下表所示。
编号 甲 乙 丙 丁
c(H2)/(mol·L-1) 0.01 0.02 0.01 0.02
c(I2)/(mol·L-1) 0.01 0.01 0.01 0.01
c(HI)/(mol·L-1) 0 0 0.02 0.02
下列判断不正确的是( )
A.化学反应速率:乙>甲 B.平衡时,甲中I2的转化率为50%
C.平衡时,丙中c(I2)=0.01 mol·L-1 D.平衡时,乙和丁中 相等
D
解析 据题表中数据可知,其他条件相同,乙中c(H2)为甲中的2倍,乙中反应速率较大,A正确;设甲中I2的转化率为x,根据“三段式”有:
H2(g) + I2(g) 2HI(g)
起始/(mol·L-1) 0.01 0.01 0
变化/(mol·L-1) 0.01x 0.01x 0.02x
平衡/(mol·L-1) 0.01(1-x) 0.01(1-x) 0.02x
6.(2023·辽宁葫芦岛协作校联考)某温度下,在1 L恒容密闭容器中投入10 mol N2O5发生反应N2O5(g) N2O(g)+2O2(g),有关数据如下表所示。下列说法正确的是( )
时间/s 0~10 10~20 20~30 30~40
产物O2的平均生成速率/(mol·L-1·s-1) 0.20 0.16 0.10 0.00
A.O2的平均生成速率越来越小是因为容器的压强越来越小
B.15 s若向体系中充入N2O,平衡一定逆向移动
C.20 s时N2O5的转化率为8%
D.35 s时,向体系中又充入N2O5,再次平衡时,其体积分数将增大
D
解析 O2的平均生成速率越来越小,主要是N2O5的浓度减小,A错误;15 s时,该体系还没有达到平衡状态,如果N2O的量很少,在一定温度下,若Q
X(g)+Y( ) ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后不再改变条件。下列有关说法中,正确的是( )
A.该条件下,Z和W中的一种可能为气态
B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不相等
C.若在该温度下该反应的平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等
D.若该反应ΔH>0,则该反应的平衡常数K随温度升高而增大
D
解析 根据题图可知,正反应速率不随反应时间和压强的改变而改变,故Z和W都不是气体,A错误;结合题图可知,X是气体,Y可能不是气体,也可能是气体,若Y不是气体,产物只有X,反应过程中气体的摩尔质量始终不变,若Y是气体,由于生成的X和Y是按照比例生成的,气体平均摩尔质量不会改变,所以两时间段反应体系中气体的平均摩尔质量一定相等,B错误;由于化学平衡常数只与温度有关,该温度下平衡常数的表达式K=c(X)是定值,则t1~t2时间段与t3时刻后的c(X)相等,C错误;该反应ΔH>0则该反应是吸热反应,升高温度平衡正向移动,平衡常数增大,D正确。
8.(2023·广东东莞一模)恒温恒容条件下,向密闭容器中加入一定量X,发生反应:①X(g) Y(g);②Y(g) Z(g)。已知v=kc(反应物),k为速率常数,如图表明三种物质浓度随时间的变化以及k受温度的影响。下列说法不正确的是( )
A.反应过程体系的压强始终不变
B.c(Y)随时间先增大后减小
C.随c(X)的减小,反应①、②的速率
均逐渐降低
D.温度对反应②的k影响更大
C
解析 由题图1中信息可知,浓度随时间变化逐渐减小的曲线为X,浓度随时间变化逐渐增大的曲线为Z,浓度随时间变化先增大后减小的曲线为Y。由题图2中信息可知,反应①的速率常数随温度升高增大的幅度小于反应②。两反应中,反应物和生成物都只有一种,且化学计量数都为1,故反应过程中气体的物质的量始终不变,压强始终不变,A正确;c(Y)随时间先增大后减小,B正确;随c(X)的减小,c(Y)先增大后减小,c(Z)不断增大,则反应①的速率逐渐降低,但反应②的速率先升高后降低,C错误;随着温度的升高,反应②的速率常数增大的幅度更大,故温度对反应②的k影响更大,D正确。
9.(2023·湖南郴州一模)T0时,在
2 L的密闭容器中发生反应: X(g)+Y(g) Z(g)(未配平),各物质的物质的量随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应,X的物质的量随时间变化的关系如图b所示。下列叙述中正确的是( )
A.该反应的正反应是吸热反应
B.T0时,从反应开始到平衡时:v(X)=0.083 mol·L-1·min-1
C.图a中反应达到平衡时,Y的转化率为37.5%
D.T1时,若该反应的平衡常数K的值为50,则T1
10.(2023·北京延庆区一模)在一定温度下,将1 mol CO2和3 mol H2充入容积为1 L的恒容密闭容器中发生反应并达到平衡:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,测得平衡混合气体中CH3OH的物质的量分数为25%。下列说法不正确的是( )
A.平衡混合气体中C原子的物质的量是1 mol
B.该反应的反应物的总能量高于生成物的总能量
C.该反应的化学平衡常数K=
D.其他条件相同时,若起始充入2 mol CO2和6 mol H2,达到平衡时CH3OH的物质的量分数大于25%
C
解析 根据质量守恒定律可知,1 mol CO2参与反应,平衡时混合气体中C原子的物质的量仍为1 mol,A正确;该反应的ΔH<0,则该反应的反应物的总能量高于生成物的总能量,B正确;设CO2的转化浓度为x mol·L-1,利用“三段式”计算:
CO2(g) + 3H2(g) CH3OH(g) + H2O(g)
11.(2023·河南洛阳六校联考)氢气是一种清洁能源,工业上用水煤气两步法制氢气,第①、②步的反应原理及反应的lg Kp-T关系如图所示。下列有关说法正确的是( )
A.反应C(s)+H2O(g) CO(g)+H2(g) ΔH1<0
B.NiFe2O4能降低反应的活化能,提高平衡转化率
C.某温度下,将CO和H2O(g)各1 mol通入容积为1 L的密闭容器中反应,达到平衡状态,若该反应的平衡常数是9,则CO的转化率为75%
D.1 300 ℃时,反应C(s)+2H2O(g) CO2(g)+2H2(g)的平衡常数Kp=8
答案 C
解析 对于反应①,升高温度,lg Kp增大,说明升高温度,该反应正向移动,则该反应是吸热反应,ΔH1>0,A错误;NiFe2O4是反应的催化剂,催化剂能降低反应的活化能,但不能改变转化率,B错误;设CO的转化量为x mol,根据已知条件列出“三段式”:
CO(g)+H2O(g) CO2(g) + H2(g)
起始/mol 1 1 0 0
转化/mol x x x x
平衡/mol 1-x 1-x x x
12.(2023·湖南省名校联合体联考)一定条件下,分别向容积为1 L的密闭容器中充入气体,发生反应:X(g)+Y(g) Z(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是( )
实验 充入气体量 反应过程条件
① 2 mol X+1 mol Y 恒温
② 1 mol Z 恒温
③ 1 mol Z 绝热
A.曲线Ⅰ对应实验② B.正反应为吸热反应
C.气体的总物质的量:n(c)
解析 恒温恒容条件下,气体的压强之比等于其物质的量之比,故起始时实验②与③的压强相等,实验①的压强是实验②、③的3倍,则曲线Ⅰ对应实验①,且m=3p,A错误;若实验②与③的温度相等,最终会达到相同的平衡状态,气体压强应相同,实际上曲线Ⅱ的压强大于曲线Ⅲ,说明Ⅱ对应反应气体的总物质的量大,绝热体系不利于Z的分解反应,故该反应正反应是放热反应,B错误;c、d两点的压强相同,体积相同,由于反应吸热,体系③温度低,c点的温度比d点低,则c点的气体物质的量更多,故气体的总物质的量:n(c)>n(d),C错误;该反应是放热反应,温度越低,平衡常数越大,故b点平衡常数小于c点,D正确。
13.(2023·山西忻州一模)为了实现碳达峰和碳中和目标,二氧化碳的高效利用成为研究的热点。某研究小组采用双合金团簇催化甲烷干法重整法(DRM)取得了良好的效果。已知:CH4、H2、CO的燃烧热分别为-890.3 kJ·mol-1、-285.8 kJ·mol-1和-283 kJ·mol-1。
(1)甲烷干法重整法(DRM)反应为CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH,则ΔH= 。
+247.3 kJ·mol-1
(2)通过大量的研究Pt12Ni、Sn12Ni、Cu12Ni三种双合金团簇可用于催化DRM反应,在催化剂表面涉及多个基元反应,分别为过程1:甲烷逐步脱氢,过程2:CO2的活化(包括直接活化和氢诱导活化),过程3:C*和CH*的氧化,过程4:扩散吸附反应。其反应机理如图1所示。则CO2的氢诱导活化反应方程式
图1
为 ,
过程3的最终产物为 ,过程4发生扩散
吸附的微粒为 。
CO2*+H* ══ CO*+OH*
CO*
H*和OH*
(3)三种催化剂催化甲烷脱氯过程的能量变化如图2所示:
图2
①甲烷脱氢过程中最大活化能步骤为
(用反应方程式表示)。
②Sn12Ni、Pt12Ni、Cu12Ni三种催化剂
催化甲烷脱氢过程的脱氢速率分别为
v1、v2、v3,则脱氢速率由大到小的顺序为 。
③Sn12Ni双合金团簇具有良好的抗积碳
作用,有效抑制碳沉积对催化剂造成的
不良影响,请结合图示解释原因:________________________________________
。
CH3* ══ CH2*+H*
v2>v3>v1
脱氢反应第4步为CH*C*+H*,发生该步反应,
三种催化剂中Sn12Ni需要克服的活化能最大,反应不易发生,故产生的积碳较少
(4)已知:甲烷干法重整法(DRM)过程中发生副反应CO2(g)+H2(g) CO(g)+H2O(g) ΔH>0,T ℃时,在恒压反应器中,通入2 mol CH4和1 mol CO2,总压强为p0,平衡时甲烷的转化率为40%,H2O的分压为p。
①关于上述平衡体系,下列说法正确的是 (填字母)。
A.n(CH4)∶n(CO2)=2∶1
B.将H2O(g)液化,可以提高主反应的速率
C.若反应在恒容条件下进行,甲烷转化率小于40%
D.若降低反应温度,主、副反应均逆向进行
②DRM反应的Kp= (列出计算式即可,分压=总压×物质的量分数)。
CD
(2)CO2的活化包括直接活化和氢诱导活化,在氢诱导活化中,CO2*+H*→COOH*→CO*+OH*,则CO2的氢诱导活化反应方程式为CO2*+H* ══ CO*+OH*。由题图可知,过程3的最终产物为CO*,过程1甲烷逐步脱氢生成H*,过程3 CO2的活化过程中生成OH*,故过程4发生扩散吸附的微粒为H*和OH*。
(3)①活化能最大的过程为反应的决速步骤,由题图可知,过渡态为TS2的反应为决速步骤,对应反应为CH3* ══ CH2*+H*;②催化剂能够降低反应的活化能,活化能越低,则化学反应速率越大,则有v2>v3>v1;③由题图可知,脱氢反应第4步为CH* ══ C*+H*,发生该步反应,三种催化剂中Sn12Ni需要克服的活化能最大,反应不易发生,故产生的积碳较少。
(4)①投入量n(CH4)∶n(CO2)=2∶1,主反应消耗量n(CH4)∶n(CO2)=1∶1,副反应消耗CO2,因此主副反应消耗量n(CH4)∶n(CO2)≠2∶1,则平衡时体系中n(CH4)∶n(CO2)≠2∶1,A错误;将H2O(g)液化,副反应正向移动,导致CO2和H2浓度减小,CO浓度增大,则主反应的速率减慢,B错误;主反应正向为体积增大的反应,若反应在恒容条件下进行,等效于在恒压的基础上,缩小容积加压,主反应平衡逆向移动,则甲烷转化率小于40%,C正确;由于主、副反应正反应均为吸热反应,则若降低反应温度,主、副反应均逆向进行,D正确。
②对主反应列出“三段式”:
CH4(g)+CO2(g) 2CO(g)+2H2(g)
起始量/mol 2 1 0 0
变化量/mol 0.8 0.8 1.6 1.6
平衡量/mol 1.2 0.2 1.6 1.6
平衡时,设水的物质的量为x mol,根据副反应列“三段式”:
H2(g)+CO2(g) CO(g)+H2O(g)
起始量/mol 1.6 0.2 1.6 0
变化量/mol x x x x
平衡量/mol 1.6-x 0.2-x 1.6+x x
同课章节目录
