3.1 构成物质的基本微粒 第3课时原子的结构及相对原子质量(课件)2023-2024学年度沪教版化学九年级上册(共29张PPT)
文档属性
| 名称 | 3.1 构成物质的基本微粒 第3课时原子的结构及相对原子质量(课件)2023-2024学年度沪教版化学九年级上册(共29张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-24 00:00:00 | ||
图片预览

文档简介
(共29张PPT)
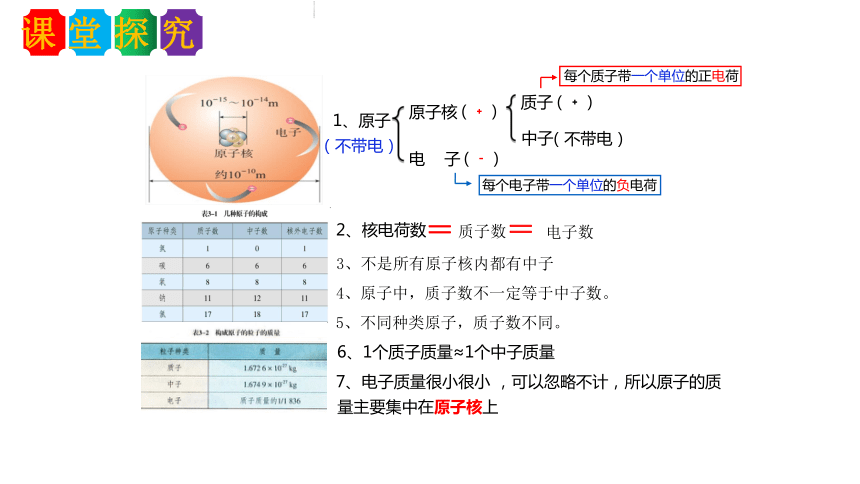
第三课时 原子的结构及相对原子质量第1节 构成物质的基本微粒1、原子
原子核
中子
电 子
质子
每个质子带一个单位的正电荷
每个电子带一个单位的负电荷
)
﹣
(
)
﹢
(
)
﹢
(
赵治原创
佳木斯市第二十中学化学组
(不带电)
2、核电荷数
电子数
=
=
质子数
(不带电)
3、不是所有原子核内都有中子
5、不同种类原子,质子数不同。
4、原子中,质子数不一定等于中子数。
6、1个质子质量≈1个中子质量
,可以忽略不计,所以原子的质量主要集中在原子核上
7、电子质量很小很小
课堂探究
《漫游原子世界》
我是小小的电子,我围绕原子核不停地高速运动,我和我的同伴总想挣脱原子核的吸引。可原子核这个“小老头”很有能耐,它由质子和中子构成,中子不带电,质子带正电,将我身上的负电深深吸引。
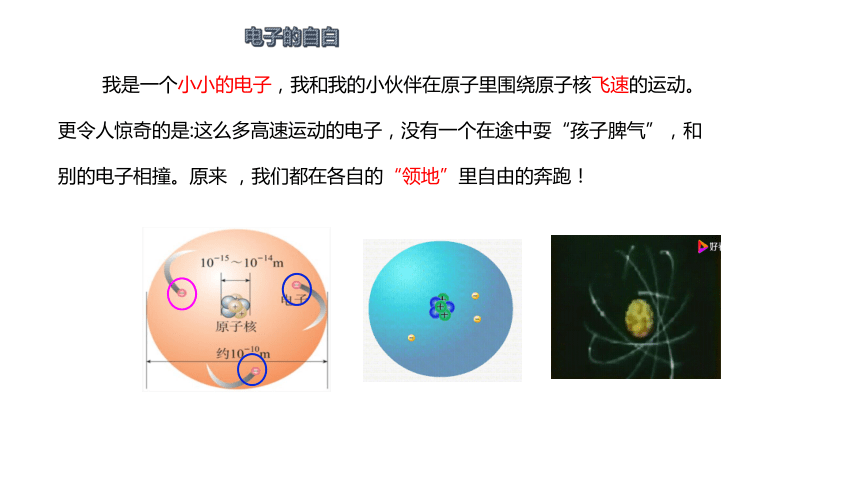
我是一个小小的电子,我和我的小伙伴在原子里围绕原子核飞速的运动。更令人惊奇的是:这么多高速运动的电子,没有一个在途中耍“孩子脾气”,和别的电子相撞。原来 ,我们都在各自的“领地”里自由的奔跑!
电子的自白
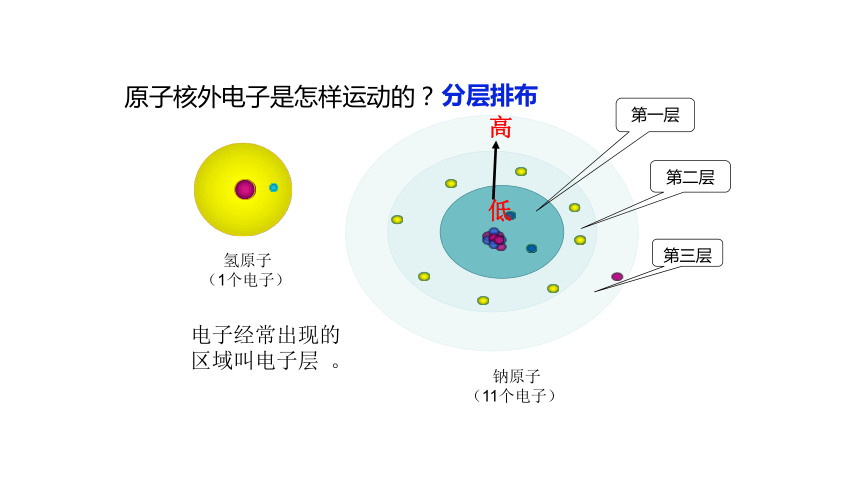
原子核外电子是怎样运动的?
氢原子
(1个电子)
钠原子
(11个电子)
电子经常出现的区域叫电子层 。
第二层
第三层
第一层
低
高
分层排布
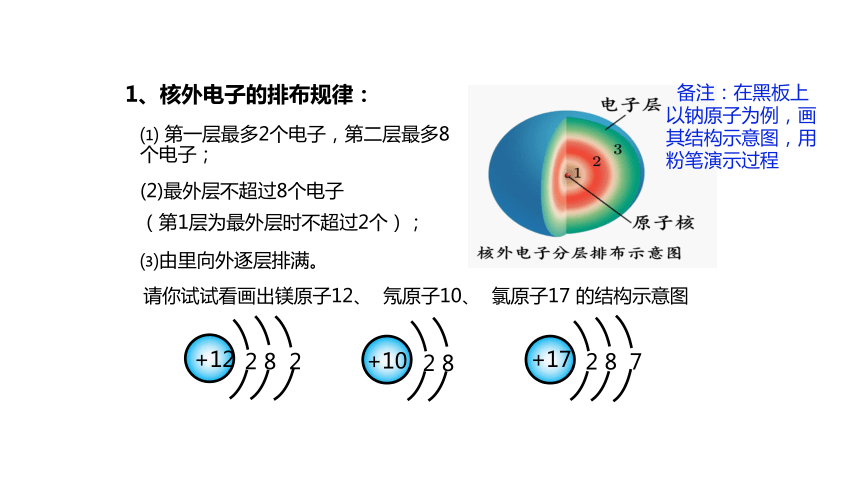
⑴ 第一层最多2个电子,第二层最多8个电子;
⑶由里向外逐层排满。
1、核外电子的排布规律:
(2)最外层不超过8个电子
(第1层为最外层时不超过2个);
请你试试看画出镁原子12、 氖原子10、 氯原子17 的结构示意图
+12
2 8 2
+10
2 8
+17
2 8 7
备注:在黑板上以钠原子为例,画其结构示意图,用粉笔演示过程
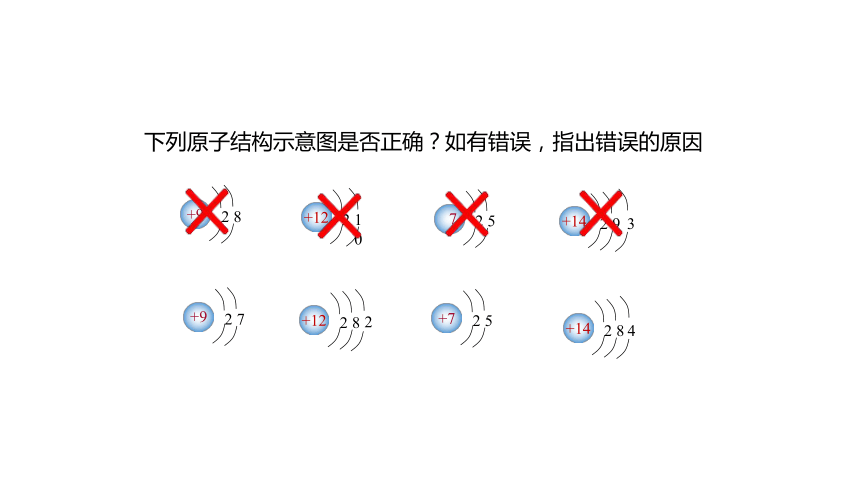
下列原子结构示意图是否正确?如有错误,指出错误的原因
2
+12
10
2
+9
8
2
7
5
2
+14
9
3
2
+9
7
2
+7
5
2
+14
8
4
2
+12
8
2
+11
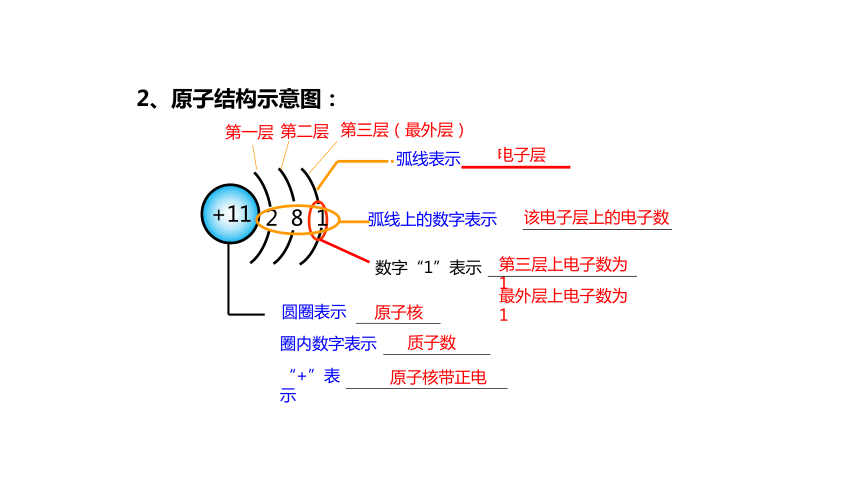
2、原子结构示意图:
电子层
原子核
质子数
该电子层上的电子数
圆圈表示
圈内数字表示
弧线表示
原子核带正电
“+”表示
第三层上电子数为1
数字“1”表示
2 8 1
弧线上的数字表示
第一层
第二层
第三层(最外层)
最外层上电子数为1
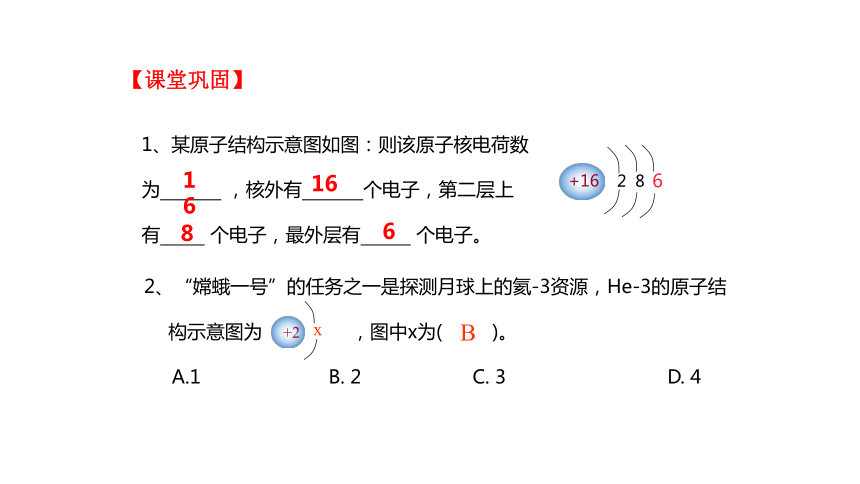
1、某原子结构示意图如图:则该原子核电荷数
为 ,核外有 个电子,第二层上
有 个电子,最外层有 个电子。
16
8
6
B
16
2、“嫦蛾一号”的任务之一是探测月球上的氦-3资源,He-3的原子结构示意图为 ,图中x为( )。
A.1 B. 2 C. 3 D. 4
x
+2
2
+16
8
6
【课堂巩固】
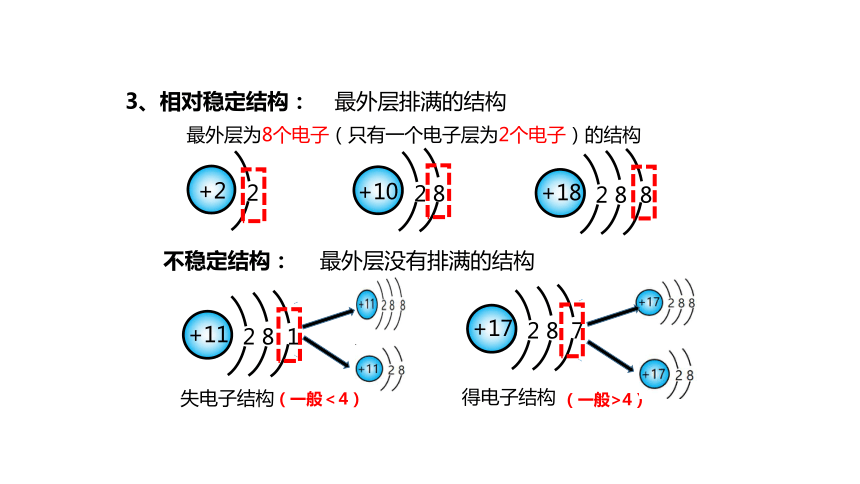
3、相对稳定结构:
最外层为8个电子(只有一个电子层为2个电子)的结构
失电子结构
得电子结构
+10
2 8
+18
2 8 8
+2
2
最外层排满的结构
不稳定结构:
+11
2 8 1
+17
2 8 7
最外层没有排满的结构
(一般<4)
(一般>4)
得7个电子
失1个电子
得1个电子
失7个电子
原子种类比较内容 金属原子 非金属原子 稀有气体原子
最外层电子数
得失电子情况
稳定性
化学性质
一般<4个
易失电子
不 稳 定
一般>4
易得电子
不 稳 定
8个(氦为2个)
不易得失电子
稳 定
活 泼
不 活 泼
活 泼
4、元素的化学性质取决于原子的最外层电子数
一般情况,原子最外层电子数相同,化学性质就相似
易得电子的原子的是 ;
(2)易失电子的原子的是 ;
(1)具有相对稳定结构的是 (填序号,下同);
A
B
C
D
(4)属于稀有气体原子的是 。
A
D
B
根据下列原子的结构示意图,回答下列问题:
+10
2 8
+16
2 8 6
+8
2 6
+11
2 8 1
C
A
(3)化学性质相似的是 。
C和D
【课堂巩固】
原子的体积很小
原子直径约为发丝直径的万分之一
原子的质量约为羽毛质量的10-23
.
原子
乒乓球
、质量也很小
相对原子质量
一个氢原子的质量
0.000 000 000 000 000 000 000 000 01993kg
=1.993×10-26 kg
一个氧原子的质量
=2.657×10-26 kg
0.000 000 000 000 000 000 000 000 001674kg
=1.674×10-27 kg
一个碳原子的质量
0.000 000 000 000 000 000 000 000 02657kg
H
C
O
相对原子质量(Ar)
三层楼高
一箭之地
两袋烟的功夫
两层楼高
相对
高度
相对
长度
相对
时间
三
两
一
两
相对就是要找个标准与其进行比较,相对原子质量的标准又是什么呢?
1803年
1959年
1927年
发现氧含有三种原子
道尔顿提出,以氢原子质量为1作为原子量的标准。
改用氧原子质量的1/16为标准。
后来
经过计算,改用16O的1/16作为标准。
1959年,国际提出以12C的1/12作为最终标准。
发展史:
沿用至今
相对原子质量(Ar)
以一种碳原子质量的1/12为标准,其他原子的质量跟它相比较所得到的比值,作为这种原子的相对原子质量。
相对原子质量(Ar)
1、标准
氧的相对原子质量=
O
O
O
氧原子
=
16
=16
2、公式
Ar(某原子)=
m某原子
Ar(H)=
请写出计算氢原子、氧原子的相对原子质量式子
m碳原子×
C
1.993×10-26 kg
碳原子
H
氢原子
1.674×10-27 kg
O
氧原子
2.657×10-26 kg
1.674x10-26kg
1.993x10-26kg×
Ar(O)=
2.657x10-26kg
1.993x10-26kg×
3、单位:“1”
省略不写
≈16
≈1
定义式:
简便式:
Ar(某原子)≈质子数+中子数
电子质量忽略不计
Ar(某原子)=
=
所有质子质量 + 所有中子质量 + 所有电子质量
1.67×10-27Kg
=
m质子 × 质子数 + m中子 × 中子数 + m电子 × 电子数
1.67×10-27Kg
=
m质子×质子数
m中子×中子数
m电子×电子数
1.67×10-27Kg
1.67×10-27Kg
1.67×10-27Kg
+
+
≈
1.67×10-27Kg×质子数
1.67×10-27Kg×中子数
1.67×10-27Kg
1.67×10-27Kg
+
≈
质子数+中子数
3、注意:
(1)、相对原子质量是一个比值不是实际质量;
(2)、实际质量越大,相对原子质量越大;
(成正比)
(3)、原子的真实质量之比等于其相对原子质量之比。
原子质量 相对原子质量
碳原子 1.993×10-26kg 12
来源
性质
数值
单位
4、比较原子质量 与 相对原子质量
测出来的
比较出来的
绝对的
相对的
非常小
大于等于1
kg
“1”
5、查找相对原子质量
学会在元素周期表中找出原子的相对原子质量,取整数。
注意:计算时如无说明,Cl取35.5,Cu取64
相对原子质量 查表格
在一般的化学计算中,多采用相对原子质量的近似值(如表3-4)。
相对原子质量可从书后附录II中查找。
张青莲 (1908~ 2006) 江苏常熟人。
著名化学家,中国科学院化学部学部委员。 1936年获德国柏林大学博士学位,曾任北京大学教授。80年代以来系统地进行了原子量的精密测定工作,所测定铟原子量[114.818(3)]和锑原子量[121.760(1)]等已被国际纯粹与应用化学联合会确定为新的国际标准数据。
1、核外电子的分层排布规律
2、原子结构示意图
3、相对稳定结构
4、元素的化学性质取决于原子的最外层电子数
一般情况,原子最外层电子数相同,化学性质就相似
原子核
核电荷数(质子数)
最外电子层
电子层
+11
2
8
1
查表格
定义 式
简便式
近似值:
相对原子质量可从书后附录II中,元素周期表中查找。
课堂小结
1.如图是某原子的结构示意图,下列关于该原子的描述正确的是( )
A.容易得到电子
B.属于非金属原子
C.核电荷数为11
D最外层电子数为11
C
+11
2 8 1
当堂达标
2.如图为某粒子的结构示意图,下列说法正确的是( )
A.该粒子有12个质子
B.该粒子有2个电子层
C.该粒子属于非金属原子
D.该粒子已达到相对稳定结构
A
+12
2 8 2
D
3.某粒子的结构示意图如下图所示对该粒子的说法错误的是( )
A.核电荷数为 17
B.核外有 3个电子层
C.带 17个单位正电荷
D.在化学反应中,易失去最外层上的 7个电子
+17
2 8 7
4.下列原子结构示意图所表示的元素,化学性质最稳定的是( )
A
B
C
D
A
2
+11
8
1
2
+17
8
7
2
+12
8
2
2
+10
8
5.下列具有相似化学性质的组别是 。
A.
D.
C.
B.
C、D
6、美国科学家将铅和氪的原子核对撞,获得了一种质子数为118、中子数为175的超重原子,该原子的相对原子质量、核外电子数分别为( )
A.118、175 B.293、118 C.175、118 D.293、175
B
a . Ar=质子数+中子数
b . 在原子中,核电荷数=质子数=核外电子数
7、铁的相对原子质量为56,核外有26个电子,则铁原子核内含有的中子数是( )
A.26 B.28 C.30 D.56
C
8、铁(Fe)的相对原子质量为56,它表示( )
A.铁单质的质量为56g
B.一个铁原子的质量为56g
C.铁的原子核内有56个质子
D.一个铁原子的质量是一个碳12原子质量1/12的56倍
D
9、氧原子的相对原子质量为( )
A. 16g B. 16 C. 2.657×10-26kg D. 16kg
B
第三课时 原子的结构及相对原子质量第1节 构成物质的基本微粒1、原子
原子核
中子
电 子
质子
每个质子带一个单位的正电荷
每个电子带一个单位的负电荷
)
﹣
(
)
﹢
(
)
﹢
(
赵治原创
佳木斯市第二十中学化学组
(不带电)
2、核电荷数
电子数
=
=
质子数
(不带电)
3、不是所有原子核内都有中子
5、不同种类原子,质子数不同。
4、原子中,质子数不一定等于中子数。
6、1个质子质量≈1个中子质量
,可以忽略不计,所以原子的质量主要集中在原子核上
7、电子质量很小很小
课堂探究
《漫游原子世界》
我是小小的电子,我围绕原子核不停地高速运动,我和我的同伴总想挣脱原子核的吸引。可原子核这个“小老头”很有能耐,它由质子和中子构成,中子不带电,质子带正电,将我身上的负电深深吸引。
我是一个小小的电子,我和我的小伙伴在原子里围绕原子核飞速的运动。更令人惊奇的是:这么多高速运动的电子,没有一个在途中耍“孩子脾气”,和别的电子相撞。原来 ,我们都在各自的“领地”里自由的奔跑!
电子的自白
原子核外电子是怎样运动的?
氢原子
(1个电子)
钠原子
(11个电子)
电子经常出现的区域叫电子层 。
第二层
第三层
第一层
低
高
分层排布
⑴ 第一层最多2个电子,第二层最多8个电子;
⑶由里向外逐层排满。
1、核外电子的排布规律:
(2)最外层不超过8个电子
(第1层为最外层时不超过2个);
请你试试看画出镁原子12、 氖原子10、 氯原子17 的结构示意图
+12
2 8 2
+10
2 8
+17
2 8 7
备注:在黑板上以钠原子为例,画其结构示意图,用粉笔演示过程
下列原子结构示意图是否正确?如有错误,指出错误的原因
2
+12
10
2
+9
8
2
7
5
2
+14
9
3
2
+9
7
2
+7
5
2
+14
8
4
2
+12
8
2
+11
2、原子结构示意图:
电子层
原子核
质子数
该电子层上的电子数
圆圈表示
圈内数字表示
弧线表示
原子核带正电
“+”表示
第三层上电子数为1
数字“1”表示
2 8 1
弧线上的数字表示
第一层
第二层
第三层(最外层)
最外层上电子数为1
1、某原子结构示意图如图:则该原子核电荷数
为 ,核外有 个电子,第二层上
有 个电子,最外层有 个电子。
16
8
6
B
16
2、“嫦蛾一号”的任务之一是探测月球上的氦-3资源,He-3的原子结构示意图为 ,图中x为( )。
A.1 B. 2 C. 3 D. 4
x
+2
2
+16
8
6
【课堂巩固】
3、相对稳定结构:
最外层为8个电子(只有一个电子层为2个电子)的结构
失电子结构
得电子结构
+10
2 8
+18
2 8 8
+2
2
最外层排满的结构
不稳定结构:
+11
2 8 1
+17
2 8 7
最外层没有排满的结构
(一般<4)
(一般>4)
得7个电子
失1个电子
得1个电子
失7个电子
原子种类比较内容 金属原子 非金属原子 稀有气体原子
最外层电子数
得失电子情况
稳定性
化学性质
一般<4个
易失电子
不 稳 定
一般>4
易得电子
不 稳 定
8个(氦为2个)
不易得失电子
稳 定
活 泼
不 活 泼
活 泼
4、元素的化学性质取决于原子的最外层电子数
一般情况,原子最外层电子数相同,化学性质就相似
易得电子的原子的是 ;
(2)易失电子的原子的是 ;
(1)具有相对稳定结构的是 (填序号,下同);
A
B
C
D
(4)属于稀有气体原子的是 。
A
D
B
根据下列原子的结构示意图,回答下列问题:
+10
2 8
+16
2 8 6
+8
2 6
+11
2 8 1
C
A
(3)化学性质相似的是 。
C和D
【课堂巩固】
原子的体积很小
原子直径约为发丝直径的万分之一
原子的质量约为羽毛质量的10-23
.
原子
乒乓球
、质量也很小
相对原子质量
一个氢原子的质量
0.000 000 000 000 000 000 000 000 01993kg
=1.993×10-26 kg
一个氧原子的质量
=2.657×10-26 kg
0.000 000 000 000 000 000 000 000 001674kg
=1.674×10-27 kg
一个碳原子的质量
0.000 000 000 000 000 000 000 000 02657kg
H
C
O
相对原子质量(Ar)
三层楼高
一箭之地
两袋烟的功夫
两层楼高
相对
高度
相对
长度
相对
时间
三
两
一
两
相对就是要找个标准与其进行比较,相对原子质量的标准又是什么呢?
1803年
1959年
1927年
发现氧含有三种原子
道尔顿提出,以氢原子质量为1作为原子量的标准。
改用氧原子质量的1/16为标准。
后来
经过计算,改用16O的1/16作为标准。
1959年,国际提出以12C的1/12作为最终标准。
发展史:
沿用至今
相对原子质量(Ar)
以一种碳原子质量的1/12为标准,其他原子的质量跟它相比较所得到的比值,作为这种原子的相对原子质量。
相对原子质量(Ar)
1、标准
氧的相对原子质量=
O
O
O
氧原子
=
16
=16
2、公式
Ar(某原子)=
m某原子
Ar(H)=
请写出计算氢原子、氧原子的相对原子质量式子
m碳原子×
C
1.993×10-26 kg
碳原子
H
氢原子
1.674×10-27 kg
O
氧原子
2.657×10-26 kg
1.674x10-26kg
1.993x10-26kg×
Ar(O)=
2.657x10-26kg
1.993x10-26kg×
3、单位:“1”
省略不写
≈16
≈1
定义式:
简便式:
Ar(某原子)≈质子数+中子数
电子质量忽略不计
Ar(某原子)=
=
所有质子质量 + 所有中子质量 + 所有电子质量
1.67×10-27Kg
=
m质子 × 质子数 + m中子 × 中子数 + m电子 × 电子数
1.67×10-27Kg
=
m质子×质子数
m中子×中子数
m电子×电子数
1.67×10-27Kg
1.67×10-27Kg
1.67×10-27Kg
+
+
≈
1.67×10-27Kg×质子数
1.67×10-27Kg×中子数
1.67×10-27Kg
1.67×10-27Kg
+
≈
质子数+中子数
3、注意:
(1)、相对原子质量是一个比值不是实际质量;
(2)、实际质量越大,相对原子质量越大;
(成正比)
(3)、原子的真实质量之比等于其相对原子质量之比。
原子质量 相对原子质量
碳原子 1.993×10-26kg 12
来源
性质
数值
单位
4、比较原子质量 与 相对原子质量
测出来的
比较出来的
绝对的
相对的
非常小
大于等于1
kg
“1”
5、查找相对原子质量
学会在元素周期表中找出原子的相对原子质量,取整数。
注意:计算时如无说明,Cl取35.5,Cu取64
相对原子质量 查表格
在一般的化学计算中,多采用相对原子质量的近似值(如表3-4)。
相对原子质量可从书后附录II中查找。
张青莲 (1908~ 2006) 江苏常熟人。
著名化学家,中国科学院化学部学部委员。 1936年获德国柏林大学博士学位,曾任北京大学教授。80年代以来系统地进行了原子量的精密测定工作,所测定铟原子量[114.818(3)]和锑原子量[121.760(1)]等已被国际纯粹与应用化学联合会确定为新的国际标准数据。
1、核外电子的分层排布规律
2、原子结构示意图
3、相对稳定结构
4、元素的化学性质取决于原子的最外层电子数
一般情况,原子最外层电子数相同,化学性质就相似
原子核
核电荷数(质子数)
最外电子层
电子层
+11
2
8
1
查表格
定义 式
简便式
近似值:
相对原子质量可从书后附录II中,元素周期表中查找。
课堂小结
1.如图是某原子的结构示意图,下列关于该原子的描述正确的是( )
A.容易得到电子
B.属于非金属原子
C.核电荷数为11
D最外层电子数为11
C
+11
2 8 1
当堂达标
2.如图为某粒子的结构示意图,下列说法正确的是( )
A.该粒子有12个质子
B.该粒子有2个电子层
C.该粒子属于非金属原子
D.该粒子已达到相对稳定结构
A
+12
2 8 2
D
3.某粒子的结构示意图如下图所示对该粒子的说法错误的是( )
A.核电荷数为 17
B.核外有 3个电子层
C.带 17个单位正电荷
D.在化学反应中,易失去最外层上的 7个电子
+17
2 8 7
4.下列原子结构示意图所表示的元素,化学性质最稳定的是( )
A
B
C
D
A
2
+11
8
1
2
+17
8
7
2
+12
8
2
2
+10
8
5.下列具有相似化学性质的组别是 。
A.
D.
C.
B.
C、D
6、美国科学家将铅和氪的原子核对撞,获得了一种质子数为118、中子数为175的超重原子,该原子的相对原子质量、核外电子数分别为( )
A.118、175 B.293、118 C.175、118 D.293、175
B
a . Ar=质子数+中子数
b . 在原子中,核电荷数=质子数=核外电子数
7、铁的相对原子质量为56,核外有26个电子,则铁原子核内含有的中子数是( )
A.26 B.28 C.30 D.56
C
8、铁(Fe)的相对原子质量为56,它表示( )
A.铁单质的质量为56g
B.一个铁原子的质量为56g
C.铁的原子核内有56个质子
D.一个铁原子的质量是一个碳12原子质量1/12的56倍
D
9、氧原子的相对原子质量为( )
A. 16g B. 16 C. 2.657×10-26kg D. 16kg
B
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
