2.1 元素与物质分类 同步练习 (含解析)2023-2024学年高一上学期化学鲁科版(2019)必修第一册
文档属性
| 名称 | 2.1 元素与物质分类 同步练习 (含解析)2023-2024学年高一上学期化学鲁科版(2019)必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 99.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-24 00:00:00 | ||
图片预览




文档简介
2.1 元素与物质分类 同步练习
一、单选题
1.下列各组选项按照电解质、单质、混合物顺序排列的一项是( )
A.氯化钙、石墨、氧气 B.盐酸、铁、空气
C.二氧化碳、氮气、天然气 D.氯化钠、氯气、石灰水
2.下列属于强酸的是( )
A. B. C. D.苯酚
3.下列各组物质按酸、碱、盐顺序排列正确的是( )
A.醋酸、纯碱、氯化钠 B.硝酸、生石灰、硫酸钡
C.盐酸、熟石灰、石英 D.硫酸、烧碱、碳酸氢钠
4.经分析,某物质只含有一种元素,则对该物质的说法正确的是( )
A.可能是混合物 B.一定是纯净物
C.一定是单质 D.可能是化合物
5.下列属于弱酸的是( )
A.H2SO4 B.CO2 C.HClO D.HNO3
6.下列说法正确的是( )
A.铜在氯气中剧烈燃烧并产生蓝色的烟
B.金属钠投入硫酸铜溶液中可观察到的实验现象为有气体产生,同时有红色固体生成
C.Fe2O3为碱性氧化物,可与水反应生成Fe(OH)3
D.可利用丁达尔效应区分FeCl3溶液和Fe(OH)3胶体
7.下列对有机化合物的分类结果正确的是( )
A.乙烯、苯、环己烷都属于脂肪烃
B.苯、环戊烷、环己烷同属于芳香烃
C.乙烯、乙炔同属于烯烃
D. 、 、 同属于环烷烃
8.下列关于胶体,判断错误的是( )
A.胶体的本质特征是胶体粒子直径在1nm~100nm
B.煮沸饱和FeCl3溶液可以制得Fe(OH)3胶体
C.丁达尔现象可以用来区别胶体和溶液
D.溶液和胶体的分散质能通过滤纸孔隙
9.下列各分子式只表示一种纯净物的是( )
A.C2H6 B.C4H8 C.C2H6O D.C6H12O6
10.化学与生活息息相关,下列说法错误的是( )
A.工业上制取NaOH,一般采用Na2O和水反应
B.碳酸氢钠是一种应用广泛的食品疏松剂
C.为了防止食品受潮,在一些食品包装袋中放入生石灰作干燥剂
D.高铁酸钠(Na2FeO4)是一种处理饮水的新型绿色消毒剂
11.下列各组物质中,按化合物、单质、混合物顺序排列的是
A.氯水、氨气、胆矾 B.碘酒、铁、有色玻璃
C.干冰、液氯、汽油 D.生石灰、臭氧、熟石灰
12.下列有关物质的分类正确的是( )
A. 、 、 、 都属于酸性氧化物
B.烧碱、纯碱都属于碱
C.硫酸、醋酸都属于酸
D.硝酸银、水银都属于化合物
13.理化知识中有很多的“相等”.请你判断下列说法中不正确的是( )
A.100体积的水和100体积的酒精混合,所得混合溶液的体积等于200体积
B.串联电路中电流大小处处相等
C.稀盐酸和氢氧化钠溶液混合后,所得溶液质量与反应前溶液的总质量相等
D.在化学反应中,反应物的原子种类和总数等于生成物的原子种类和总数
14.混凝法是净化水常用的方法,在天然水或污水中加入一定的混凝剂,可使水中的悬浮物变为沉淀而除去.下列物质中可以作为混凝剂的是 ( )
A.氯化钠 B.氯气 C.小苏打 D.明矾
15.用聚光手电筒照射下列分散系,可观察到丁达尔效应的是( )
A.KOH溶液 B.NaNO3溶液 C.盐酸 D.Fe(OH)3胶体
16.当光束通过下列分散系时,能产生丁达尔效应的是( )
A.AgNO3溶液 B.KOH溶液 C.Fe(OH)3胶体 D.稀H2SO4
二、综合题
17.对于数以万计的化学物质和化学反应,分类法的作用几乎是无可替代的.
(1)现有下列5种物质:CuO、CO、MgO、Na2O、FeO.按照不同的分类标准,它们中有1种物质与其他4种物质有明显的不同,找出这种物质,并写出依据(写出两种):
① ;
② .
(2)虽然分类的方法不同,但离子反应和氧化还原反应之间也存在着一定的关系,用简单的图示方法表示二者之间的关系 .
(3)生活中的食醋和豆浆分别属于分散系中的 和 ,用 可以鉴别(填化学专用名词).
18.从下列选项中选择确当的字母填入下列横线上
A、过滤 B、聚沉 C、布朗运动 D、电泳E、丁达尔效应
(1)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐加深,这种现象叫 .
(2)光速通过Fe(OH)3胶体,可以看到光亮的通路,这种现象叫 .
(3)Fe(OH)3胶体中加入了硅酸胶体(硅酸胶体带负电),胶体变得浑浊,这是发生了
(4)鉴别Fe(OH)3胶体和盐酸的方法是 .
19.无机化合物可根据其组成和性质进行分类,
(1)如图所示的物质分类方法名称是 .
(2)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,分别填在表中②、④、⑥、⑩后面.
物质类别 酸 碱 盐 氧化物 氢化物
化学式 ①H2SO4 ② ③NaOH ④ ⑤Na2SO4 ⑥ ⑦SO2 ⑧ ⑨NH3 ⑩
(3)SO2和CO2都属于酸性氧化物,在化学性质上有很多相似的地方,请写出少量的⑦与③反应的化学反应方程式为: .
(4)磷的一种化合物叫亚磷酸(H3PO3),从交叉分类的角度看,它属于二元弱酸,则Na2HPO3属于 盐(填正盐、酸式盐或碱式盐).
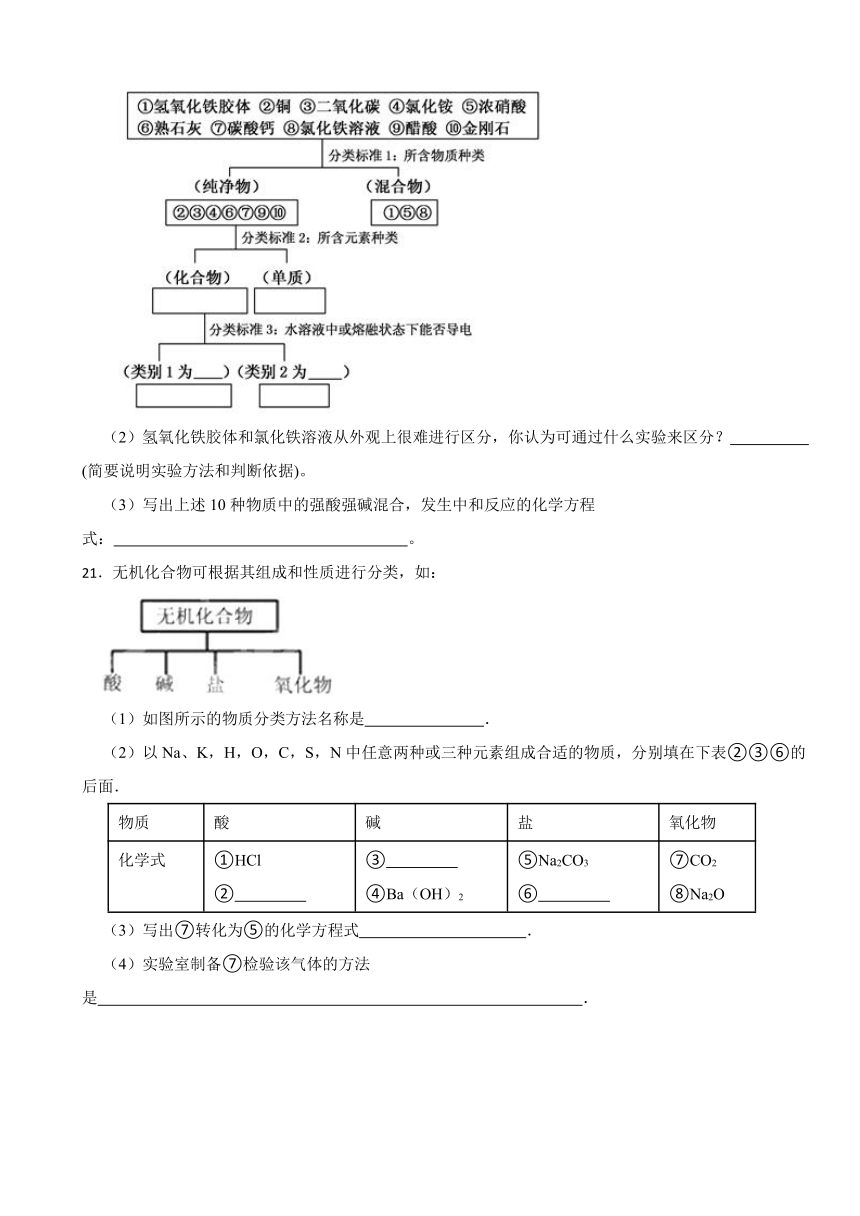
20.运用树状分类法对下列9种物质进行分类,然后按要求回答问题:
(1)进行分类(将各物质序号填入相应方框中),并在相应空格处作答 。
(2)氢氧化铁胶体和氯化铁溶液从外观上很难进行区分,你认为可通过什么实验来区分? (简要说明实验方法和判断依据)。
(3)写出上述10种物质中的强酸强碱混合,发生中和反应的化学方程式: 。
21.无机化合物可根据其组成和性质进行分类,如:
(1)如图所示的物质分类方法名称是 .
(2)以Na、K,H,O,C,S,N中任意两种或三种元素组成合适的物质,分别填在下表②③⑥的后面.
物质 酸 碱 盐 氧化物
化学式 ①HCl ② ③ ④Ba(OH)2 ⑤Na2CO3 ⑥ ⑦CO2 ⑧Na2O
(3)写出⑦转化为⑤的化学方程式 .
(4)实验室制备⑦检验该气体的方法是 .
答案解析部分
1.【答案】D
【解析】【解答】A.氧气属于单质,不是混合物,故A不符合题意;
B.盐酸为HCl的水溶液,为混合物,既不是电解质也不是非电解质,故B不符合题意;
C.二氧化碳的水溶液能导电,但其自身不能电离,属于非电解质, 故C不符合题意;
D.氯化钠属于电解质,氯气为单质,石灰水为混合物,故D符合题意;
故答案为:D。
【分析】电解质必须为化合物,单质和混合物都是属于电解质。
2.【答案】B
【解析】【解答】强酸是在水中完全电离出的阳离子全是氢离子的化合物;
A. 在水中部分电离,是弱酸,故A不符合题意;
B. 在水中全部电离,是强酸,故B符合题意;
C. 在水中电离出钠离子,氢离子,硫酸根,是盐,故C不符合题意;
D.苯酚在水中部分电离,是弱酸,故D不符合题意;
故答案为:B。
【分析】常见的强酸有H2SO4、HNO3、HCl、HBr、HI、HClO4。
3.【答案】D
【解析】【解答】A. 醋酸、纯碱(碳酸钠)、氯化钠分别属于酸、盐和盐,A不选;
B. 硝酸、生石灰(氧化钙)、硫酸钡分别属于酸、碱性氧化物、盐,B不选;
C. 盐酸、熟石灰(氢氧化钙)、石英(二氧化硅)分别属于混合物、碱和酸性氧化物,C不选;
D. 硫酸、烧碱、碳酸氢钠分别属于酸、碱、盐,D选;
故答案为:D。
【分析】电离时生成的阳离子全部是氢离子的化合物为酸;电离出的阴离子全部都是氢氧根离子的化合物为碱;金属离子或铵根离子与酸根离子结合的化合物为盐。
4.【答案】A
【解析】【解答】一种元素可以组成纯净物,例如氧气是由氧元素组成的纯净物,同时氧气是由氧元素组成的单质,也可以组成混合物,例如氧气和臭氧组成的混合物中只含有氧元素,但是一种元素不可能组成化合物,因此某物质只含有一种元素,则该物质可能是混合物,不一定是纯净物,也不一定是单质,不可能是化合物,
故答案为:A。
【分析】没有说明是否由一种分子构成,氧气和臭氧都含有氧元素,混合在一起为混合物。
5.【答案】C
【解析】【解答】A.H2SO4是一种二元强酸,A不符合题意;
B.CO2属于氧化物,不属于酸,B不符合题意;
C.HClO是一种一元弱酸,C符合题意;
D.HNO3是一种一元强酸,D不符合题意。
故答案为:C。
【分析】考查酸的定义;在溶液中几离出的阳离子全部为氢离子的化合物为酸;高中阶段除了六大强酸之外的酸为弱酸。
6.【答案】D
【解析】【解答】A.铜在氯气中剧烈燃烧并产生棕黄色的烟,A不符合题意;
B.金属钠投入硫酸铜溶液中,钠与水反应产生NaOH和H2,NaOH再与溶液中的溶质反应产生Cu(OH)2蓝色沉淀,由于钠的密度比水小,因此可观察到的实验现象为:金属钠浮在水面上,有气体产生,同时有蓝色沉淀生成,B不符合题意;
C.Fe2O3为碱性氧化物,但由于Fe2O3不溶于水,因此Fe2O3不能与水反应生成Fe(OH)3,C不符合题意;
D.Fe(OH)3胶体会产生丁达尔效应,而FeCl3溶液不会产生丁达尔效应,故可以根据能否产生丁达尔效应区分FeCl3溶液和Fe(OH)3胶体,D符合题意;
故答案为:D。
【分析】A.铜在氯气中剧烈燃烧并产生棕黄色的烟;
B.金属钠投入硫酸铜溶液中,钠先与水反应生成氢氧化钠和氢气,氢氧化钠再与硫酸铜反应;
C.Fe2O3不溶于水。
7.【答案】D
【解析】【解答】A. 乙烯、环己烷都属于脂肪烃,苯属于芳香烃,A不符合题意;
B. 苯属于芳香烃,环戊烷、环己烷属于脂肪烃,B不符合题意;
C. 乙烯属于烯烃,乙炔属于炔烃,C不符合题意;
D. 、 、 同属于环烷烃,D符合题意;
故答案为:D。
【分析】A.脂肪烃是指具有脂肪族化合物基本属性的碳氢化合物,脂肪族化合物中,碳原子以直链、支链或环状排列;
B.芳香烃是含有苯环的碳氢化合物;
C.烯烃是含有碳碳双键的碳氢化合物;
D.环烷烃是含有脂环结构的饱和烃;
8.【答案】B
【解析】【解答】A.胶体的本质特征是分散质粒子直径在1nm~100nm,溶液的分散质粒子直径小于1nm,A不符合题意;
B.向沸水中滴加饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即停止加热,来制备Fe(OH)3胶体,B符合题意;
C.鉴别溶液和胶体是利用丁达尔现象,即用激光笔照射,胶体有一条光亮的通路,而溶液没有,C不符合题意;
D. 胶体、溶液的分散质都能通过滤纸孔隙,D不符合题意;
故答案为:B
【分析】A.分散系分类的标准是分散质微粒的直径大小;
B.根据Fe(OH)3胶体的制备分析;
C.胶体具有丁达尔效应,而溶液没有;
D.胶体和溶液中分散质都能透过滤纸;
9.【答案】A
【解析】【解答】解:A.C2H6只有一种结构不存在同分异构体,所以能只表示一种物质,故A正确;
B.C4H8可以表示1﹣丁烯,2﹣丁烯,也可以表示环丁烷,甲基环丙烷,存在同分异构体,所以不能表示一种物质,故B错误;
C.C2H6O可以表示乙醇、甲醚,存在同分异构体,不能表示纯净物,故C错误;
D.C6H12O6可以表示葡萄糖、果糖等,不能表示纯净物,故D错误.
故选A.
【分析】同分异构体是分子式相同,但结构不同的化合物;根据是否存在同分异构体判断正误.
10.【答案】A
【解析】【解答】A.工业上是用电解饱和食盐水的方法制备氢氧化钠,不是采用氧化钠和水反应的方法制备氢氧化钠,成本太高,故A符合题意;
B.碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,是食品工业中一种应用广泛的食品疏松剂,故B不符合题意;
C.生石灰可以吸收空气中的水蒸气做干燥剂,为了防止食品受潮变质,常在食品包装袋中放入生石灰,故C不符合题意;
D.高铁酸钠具有强氧化性,能与水中的细菌发生氧化还原反应生成铁离子,铁离子水解生成具有吸附性的氢氧化铁胶体,吸附水中悬浮杂质形成沉淀而达到净水作用,是一种处理饮水的新型绿色消毒剂,故D不符合题意。
故答案为:A。
【分析】A、工业采用氯碱工业制备氢氧化钠:电解饱和食盐水;
B、根据碳酸氢钠受热分解生成二氧化碳的性质,用作食品疏松剂;
C、生石灰能够与水反应,常用于食品干燥剂;
D、高铁酸钠中铁元素化合价为+6,具有强氧化性,能够杀菌消毒,+3价铁水解生成氢氧化铁具有吸附性;
11.【答案】C
【解析】【解答】A.氯水是氯气的水溶液,为混合物,氨气是化合物,胆矾是化合物,A不符合题意;
B.碘酒是碘单质的酒精溶液,为混合物,铁是单质,有色玻璃是混合物,B不符合题意;
C.干冰是固态二氧化碳,为化合物,液液氯是液态的氯气为单质,汽油是混合物,C符合题意;
D.生石灰是氧化钙,为化合物,臭氧是单质,熟石灰是氢氧化钙,为纯净物,D不符合题意;
故答案为:C。
【分析】A.氯水是氯气的水溶液,为混合物,氨气是化合物,胆矾是化合物;
B.碘酒是碘单质的酒精溶液,为混合物;
C.干冰是固态二氧化碳,为化合物,液液氯是液态的氯气为单质,汽油是混合物;
D.熟石灰是氢氧化钙,为纯净物。
12.【答案】C
【解析】【解答】A. 、 、 都属于酸性氧化物, CO是不成盐氧化物,故A不符合题意;
B. 烧碱是氢氧化钠属于碱,纯碱是碳酸钠,属于盐,故B不符合题意;
C. 硫酸、醋酸电离出的阳离子都是氢离子,都属于酸,故C符合题意;
D. 硝酸银属于化合物,水银是单质,故D不符合题意;
故答案为:C。
【分析】A.和碱反应生成盐和水的氧化物为酸性氧化物;
B.电离出的阴离子全部为氢氧离子的化合物称为碱;
C.溶液中电离出的阳离子全部是氢离子的化合物为酸;
D.不同元素组成的纯净物为化合物。
13.【答案】A
【解析】【解答】解:A.100体积的水和100体积的酒精混合,所得混合溶液的体积小于200体积,故A错误;
B.在串联电路中电流的大小处处相等,故B正确;
C.稀盐酸和氢氧化钠溶液混合后,发生反应产物中无沉淀和气体生成,所以所得溶液质量与反应前溶液的总质量相等,故C正确;
D.根据质量守恒定律的意义可知化学反应物的原子种类和总数等于生成物的原子种类和总数,故D正确;
故选:A.
【分析】A.分子之间有间隙;
B.根据串联电路电流的特征解答;
C.依据质量守恒定律解答;
D.依据质量守恒定律及反应的生成物来判断.
14.【答案】D
【解析】【解答】氯化钠、氯气、碳酸氢钠不能水解,不能生成胶状物或絮状沉淀,不能用作混凝剂;
而明矾在溶液中易水解生成胶状沉淀,可做混凝剂;
故选D.
【分析】当物质在溶液中能形成胶状物时,能够絮凝成大颗粒,具有较强的吸附能力,可在水处理中作混凝剂.
15.【答案】D
【解析】【解答】A.KOH属于溶液,用光束照射不能观察到丁达尔现象,故A不符合题意;
B.NaNO3溶液属于溶液,用光束照射不能观察到丁达尔现象,故B不符合题意;
C.盐酸属于溶液,用光束照射不能观察到丁达尔现象,故C不符合题意;
D.Fe(OH)3胶体属于胶体分散系,用光束照射能观察到丁达尔现象,故D符合题意;
故答案为:D。
【分析】胶体具有丁达尔现象是指当光束通过胶体分散系时能看到一条光亮的通路,丁达尔现象是区分胶体和溶液最常用的简单方法,丁达尔效应的是胶体特有的性质,所以只要判断下列分散系是胶体即可。
16.【答案】C
【解析】【解答】A.AgNO3溶液属于溶液,不是胶体,A项不符合题意;
B.KOH溶液属于溶液,不是胶体,B项不符合题意;
C.Fe(OH)3胶体属于胶体,能产生丁达尔效应,C项符合题意;
D.稀H2SO4属于溶液,不是胶体,D项不符合题意;
故答案为:C。
【分析】丁达尔现象是胶体的特性,结合选项即可判断
17.【答案】(1)CO;常温常压下是气体,其余是固体;CO;非金属氧化物,其余是金属氧化物
(2)
(3)溶液;胶体;丁达尔效应
【解析】【解答】解:(1)①根据物质的状态分析,CO为气体,其余为固体,
故答案为:CO;常温常压下是气体,其余是固体;
②根据物质组成和状态来分类,在CuO、CO、MgO、Na2O、FeO中,CO属于非金属氧化物,CuO、MgO、Na2O、FeO属于金属氧化物,
故答案为:CO;非金属氧化物,其余是金属氧化物;(2)离子反应有的是氧化还原反应,有的不是氧化还原反应,二者的关系可以用右图表示: ,如离子反应H++OH﹣=H2O不属于氧化还原反应,离子反应Cl2+H2O=H++Cl﹣+HClO属于氧化还原反应,
故答案为:; ;(3)食醋属于溶液,淀粉溶液属于胶体,溶液无丁达尔效应,胶体有丁达尔效应,
故答案为:溶液;胶体;丁达尔效应.
【分析】(1)找出不同类的物质,要抓住其余5种物质的共同点,可以从物理性质和化学性质两方面进行分析;(2)离子反应有的是氧化还原反应,有的不是氧化还原反应;(3)食醋属于溶液,淀粉溶液属于胶体,丁达尔效应是胶体的特性;
18.【答案】(1)D
(2)E
(3)B
(4)E
【解析】【解答】解:(1)因Fe(OH)3胶粒带有正电荷,所以在电场的作用下,向阴极区移动,而使该区颜色加深,这种现象称为电泳,
故答案为:D;(2)光束通过胶体时,产生光亮的通路,称为丁达尔效应,
故答案为:E;(3)加入与胶粒带相反电荷的胶体,胶体会发生聚沉,
故答案为:B;(4)鉴别胶体和溶液利用丁达尔效应,故答案为:E.
【分析】(1)Fe(OH)3胶粒在电场的作用下,做定向运动,这种现象称为电泳;(2)光束通过胶体时,产生光亮的通路,称为丁达尔效应;(3)胶体遇胶粒带相反电荷的胶体发生聚沉;(4)丁达尔效应是胶体的特有性质.
19.【答案】(1)树状分类法
(2)HNO3;KOH;K2SO4;SO3;H2S
(3)SO2+2NaOH=Na2SO3+H2O
(4)正盐
【解析】【解答】解:(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树,有叶、枝、杆、根,图示方法就是树状图,
故答案为:树状分类法;(2)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,酸电离出的阳离子全部是氢离子的化合物,如H2SO4,电离方程式为H2SO4═2H++SO42﹣,②可以为HNO3,碱电离出的阴离子全部为氢氧根离子,如NaOH═Na++OH﹣,④可以为KOH,盐电离出得阳离子为金属离子,阴离子为酸根离子,如Na2SO4═2Na++SO42﹣,⑥为K2SO4,氧化物由两种元素组成其中一种为氧元素的化合物,如SO2 为酸性氧化物,则⑧为SO3,两种元素组成,其中一种是氢元素的化合物,属于氢化物,如NH3 ,则⑩为H2S等,
故答案为:HNO3;KOH;K2SO4;SO3;H2S;(3)少量的⑦与③反应的化学反应方程式为:SO2+2NaOH=Na2SO3+H2O,故答案为:SO2+2NaOH=Na2SO3+H2O;(4)由H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3亚磷酸是二元酸,所以Na2HPO3为正盐,故答案为:正盐.
【分析】(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树;(2)酸电离出的阳离子全部是氢离子的化合物;碱电离出的阴离子全部为氢氧根离子;盐电离出得阳离子为金属离子,阴离子为酸根离子;氧化物只有两种元素,且必须有氧元素;两种元素组成,其中一种是氢元素的化合物,属于氢化物;(3)少量二氧化硫和氢氧化钠溶液反应生成亚硫酸钠和水;(4)亚磷酸是二元酸生成的盐Na2HPO3为正盐;
20.【答案】(1)③、④、⑥、⑦、⑨;②、⑩;电解质;非电解质;④、⑥、⑦、⑨;③
(2)分别取样做丁达尔实验,出现丁达尔效应的是氢氧化铁胶体
(3)2HNO3+Ca(OH)2=Ca(NO3)2+2H2O
【解析】【解答】(1)由一种元素组成的纯净物是单质,如②、⑩,由不同种元素组成的纯净物是化合物,如:③、④、⑥、⑦、⑨;根据化合物在水溶液和熔融态下是否导电将化合物分为:电解质和非电解质;在水溶液或熔融状态下能导电的化合物是电解质,如④、⑥、⑦、⑨,在水溶液和熔融状态下均不导电的化合物是非电解质,如③;
(2)氢氧化铁胶体具有丁达尔效应,而溶液不具备该性质,可以做丁达尔实验来区分,即分别取样做丁达尔实验,出现丁达尔效应的是氢氧化铁胶体;
(3)上述10种物质中硝酸是强酸,氢氧化钙是强碱,混合后,发生中和反应生成盐和水,化学方程式为2HNO3+Ca(OH)2=Ca(NO3)2+2H2O。
【分析】(1)根据化合物、单质、电解质、非电解质定义进行分类即可;
(2)胶体具有丁达尔效应,可以用来区分溶液与胶体;
(3)熟悉常见的强酸与强碱。
21.【答案】(1)树状分类法
(2)NaOH;HNO3;NaNO3
(3)Na2O+CO2═Na2CO3
(4)将气体通入澄清的石灰水中,变浑浊,则说明该气体是二氧化碳
【解析】【解答】解:(1)交叉分类法含义:根据物质不同的分类标准,对同一事物进行多种分类的一种分类方式,树状分类法含义:对同一类事物按照某些属性进行在分类的分类法,无机化合物可根据其组成和性质进行分类:无机化合物、盐、碱、酸、氧化物、氢化物属于树状分类法;故答案为:树状分类法;(2)以H、O、S、N、Na五种元素中任意两种或三种元素可组成酸有:H2SO4或HNO3,碱有:NaOH、KOH或NH3 H2O,盐有:NaNO3、Na2SO4、NH4NO3,氧化物有:H2O、NO、NO2、N2O5、SO2、SO3、Na2O,氢化物有:NH3,H2O等,故答案为:②HNO3 ③NaOH、KOH或NH3 H2O ⑥NaNO3、Na2SO4、NH4NO3(任写一种); (3)因CO2能与氧化钠反应生成碳酸钠:Na2O+CO2═Na2CO3;故答案为:Na2O+CO2═Na2CO3;(4)检验二氧化碳气体,把气体通入澄清的石灰水,石灰水变浑浊,说明气体为二氧化碳;故答案为:将气体通入澄清的石灰水中,变浑浊,则说明该气体是二氧化碳.
【分析】(1)根据交叉分类法和树状分类法的定义判断;(2)以H、O、S、N、Na五种元素中任意两种或三种元素可组成酸、碱、盐、氧化物等,根据常见的物质书写;(3)根据二氧化碳可以与氧化钠反应生成碳酸钠;(4)根据CO2的检验方法:把气体通入澄清的石灰水,石灰水变浑浊,说明气体为二氧化碳.
一、单选题
1.下列各组选项按照电解质、单质、混合物顺序排列的一项是( )
A.氯化钙、石墨、氧气 B.盐酸、铁、空气
C.二氧化碳、氮气、天然气 D.氯化钠、氯气、石灰水
2.下列属于强酸的是( )
A. B. C. D.苯酚
3.下列各组物质按酸、碱、盐顺序排列正确的是( )
A.醋酸、纯碱、氯化钠 B.硝酸、生石灰、硫酸钡
C.盐酸、熟石灰、石英 D.硫酸、烧碱、碳酸氢钠
4.经分析,某物质只含有一种元素,则对该物质的说法正确的是( )
A.可能是混合物 B.一定是纯净物
C.一定是单质 D.可能是化合物
5.下列属于弱酸的是( )
A.H2SO4 B.CO2 C.HClO D.HNO3
6.下列说法正确的是( )
A.铜在氯气中剧烈燃烧并产生蓝色的烟
B.金属钠投入硫酸铜溶液中可观察到的实验现象为有气体产生,同时有红色固体生成
C.Fe2O3为碱性氧化物,可与水反应生成Fe(OH)3
D.可利用丁达尔效应区分FeCl3溶液和Fe(OH)3胶体
7.下列对有机化合物的分类结果正确的是( )
A.乙烯、苯、环己烷都属于脂肪烃
B.苯、环戊烷、环己烷同属于芳香烃
C.乙烯、乙炔同属于烯烃
D. 、 、 同属于环烷烃
8.下列关于胶体,判断错误的是( )
A.胶体的本质特征是胶体粒子直径在1nm~100nm
B.煮沸饱和FeCl3溶液可以制得Fe(OH)3胶体
C.丁达尔现象可以用来区别胶体和溶液
D.溶液和胶体的分散质能通过滤纸孔隙
9.下列各分子式只表示一种纯净物的是( )
A.C2H6 B.C4H8 C.C2H6O D.C6H12O6
10.化学与生活息息相关,下列说法错误的是( )
A.工业上制取NaOH,一般采用Na2O和水反应
B.碳酸氢钠是一种应用广泛的食品疏松剂
C.为了防止食品受潮,在一些食品包装袋中放入生石灰作干燥剂
D.高铁酸钠(Na2FeO4)是一种处理饮水的新型绿色消毒剂
11.下列各组物质中,按化合物、单质、混合物顺序排列的是
A.氯水、氨气、胆矾 B.碘酒、铁、有色玻璃
C.干冰、液氯、汽油 D.生石灰、臭氧、熟石灰
12.下列有关物质的分类正确的是( )
A. 、 、 、 都属于酸性氧化物
B.烧碱、纯碱都属于碱
C.硫酸、醋酸都属于酸
D.硝酸银、水银都属于化合物
13.理化知识中有很多的“相等”.请你判断下列说法中不正确的是( )
A.100体积的水和100体积的酒精混合,所得混合溶液的体积等于200体积
B.串联电路中电流大小处处相等
C.稀盐酸和氢氧化钠溶液混合后,所得溶液质量与反应前溶液的总质量相等
D.在化学反应中,反应物的原子种类和总数等于生成物的原子种类和总数
14.混凝法是净化水常用的方法,在天然水或污水中加入一定的混凝剂,可使水中的悬浮物变为沉淀而除去.下列物质中可以作为混凝剂的是 ( )
A.氯化钠 B.氯气 C.小苏打 D.明矾
15.用聚光手电筒照射下列分散系,可观察到丁达尔效应的是( )
A.KOH溶液 B.NaNO3溶液 C.盐酸 D.Fe(OH)3胶体
16.当光束通过下列分散系时,能产生丁达尔效应的是( )
A.AgNO3溶液 B.KOH溶液 C.Fe(OH)3胶体 D.稀H2SO4
二、综合题
17.对于数以万计的化学物质和化学反应,分类法的作用几乎是无可替代的.
(1)现有下列5种物质:CuO、CO、MgO、Na2O、FeO.按照不同的分类标准,它们中有1种物质与其他4种物质有明显的不同,找出这种物质,并写出依据(写出两种):
① ;
② .
(2)虽然分类的方法不同,但离子反应和氧化还原反应之间也存在着一定的关系,用简单的图示方法表示二者之间的关系 .
(3)生活中的食醋和豆浆分别属于分散系中的 和 ,用 可以鉴别(填化学专用名词).
18.从下列选项中选择确当的字母填入下列横线上
A、过滤 B、聚沉 C、布朗运动 D、电泳E、丁达尔效应
(1)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐加深,这种现象叫 .
(2)光速通过Fe(OH)3胶体,可以看到光亮的通路,这种现象叫 .
(3)Fe(OH)3胶体中加入了硅酸胶体(硅酸胶体带负电),胶体变得浑浊,这是发生了
(4)鉴别Fe(OH)3胶体和盐酸的方法是 .
19.无机化合物可根据其组成和性质进行分类,
(1)如图所示的物质分类方法名称是 .
(2)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,分别填在表中②、④、⑥、⑩后面.
物质类别 酸 碱 盐 氧化物 氢化物
化学式 ①H2SO4 ② ③NaOH ④ ⑤Na2SO4 ⑥ ⑦SO2 ⑧ ⑨NH3 ⑩
(3)SO2和CO2都属于酸性氧化物,在化学性质上有很多相似的地方,请写出少量的⑦与③反应的化学反应方程式为: .
(4)磷的一种化合物叫亚磷酸(H3PO3),从交叉分类的角度看,它属于二元弱酸,则Na2HPO3属于 盐(填正盐、酸式盐或碱式盐).
20.运用树状分类法对下列9种物质进行分类,然后按要求回答问题:
(1)进行分类(将各物质序号填入相应方框中),并在相应空格处作答 。
(2)氢氧化铁胶体和氯化铁溶液从外观上很难进行区分,你认为可通过什么实验来区分? (简要说明实验方法和判断依据)。
(3)写出上述10种物质中的强酸强碱混合,发生中和反应的化学方程式: 。
21.无机化合物可根据其组成和性质进行分类,如:
(1)如图所示的物质分类方法名称是 .
(2)以Na、K,H,O,C,S,N中任意两种或三种元素组成合适的物质,分别填在下表②③⑥的后面.
物质 酸 碱 盐 氧化物
化学式 ①HCl ② ③ ④Ba(OH)2 ⑤Na2CO3 ⑥ ⑦CO2 ⑧Na2O
(3)写出⑦转化为⑤的化学方程式 .
(4)实验室制备⑦检验该气体的方法是 .
答案解析部分
1.【答案】D
【解析】【解答】A.氧气属于单质,不是混合物,故A不符合题意;
B.盐酸为HCl的水溶液,为混合物,既不是电解质也不是非电解质,故B不符合题意;
C.二氧化碳的水溶液能导电,但其自身不能电离,属于非电解质, 故C不符合题意;
D.氯化钠属于电解质,氯气为单质,石灰水为混合物,故D符合题意;
故答案为:D。
【分析】电解质必须为化合物,单质和混合物都是属于电解质。
2.【答案】B
【解析】【解答】强酸是在水中完全电离出的阳离子全是氢离子的化合物;
A. 在水中部分电离,是弱酸,故A不符合题意;
B. 在水中全部电离,是强酸,故B符合题意;
C. 在水中电离出钠离子,氢离子,硫酸根,是盐,故C不符合题意;
D.苯酚在水中部分电离,是弱酸,故D不符合题意;
故答案为:B。
【分析】常见的强酸有H2SO4、HNO3、HCl、HBr、HI、HClO4。
3.【答案】D
【解析】【解答】A. 醋酸、纯碱(碳酸钠)、氯化钠分别属于酸、盐和盐,A不选;
B. 硝酸、生石灰(氧化钙)、硫酸钡分别属于酸、碱性氧化物、盐,B不选;
C. 盐酸、熟石灰(氢氧化钙)、石英(二氧化硅)分别属于混合物、碱和酸性氧化物,C不选;
D. 硫酸、烧碱、碳酸氢钠分别属于酸、碱、盐,D选;
故答案为:D。
【分析】电离时生成的阳离子全部是氢离子的化合物为酸;电离出的阴离子全部都是氢氧根离子的化合物为碱;金属离子或铵根离子与酸根离子结合的化合物为盐。
4.【答案】A
【解析】【解答】一种元素可以组成纯净物,例如氧气是由氧元素组成的纯净物,同时氧气是由氧元素组成的单质,也可以组成混合物,例如氧气和臭氧组成的混合物中只含有氧元素,但是一种元素不可能组成化合物,因此某物质只含有一种元素,则该物质可能是混合物,不一定是纯净物,也不一定是单质,不可能是化合物,
故答案为:A。
【分析】没有说明是否由一种分子构成,氧气和臭氧都含有氧元素,混合在一起为混合物。
5.【答案】C
【解析】【解答】A.H2SO4是一种二元强酸,A不符合题意;
B.CO2属于氧化物,不属于酸,B不符合题意;
C.HClO是一种一元弱酸,C符合题意;
D.HNO3是一种一元强酸,D不符合题意。
故答案为:C。
【分析】考查酸的定义;在溶液中几离出的阳离子全部为氢离子的化合物为酸;高中阶段除了六大强酸之外的酸为弱酸。
6.【答案】D
【解析】【解答】A.铜在氯气中剧烈燃烧并产生棕黄色的烟,A不符合题意;
B.金属钠投入硫酸铜溶液中,钠与水反应产生NaOH和H2,NaOH再与溶液中的溶质反应产生Cu(OH)2蓝色沉淀,由于钠的密度比水小,因此可观察到的实验现象为:金属钠浮在水面上,有气体产生,同时有蓝色沉淀生成,B不符合题意;
C.Fe2O3为碱性氧化物,但由于Fe2O3不溶于水,因此Fe2O3不能与水反应生成Fe(OH)3,C不符合题意;
D.Fe(OH)3胶体会产生丁达尔效应,而FeCl3溶液不会产生丁达尔效应,故可以根据能否产生丁达尔效应区分FeCl3溶液和Fe(OH)3胶体,D符合题意;
故答案为:D。
【分析】A.铜在氯气中剧烈燃烧并产生棕黄色的烟;
B.金属钠投入硫酸铜溶液中,钠先与水反应生成氢氧化钠和氢气,氢氧化钠再与硫酸铜反应;
C.Fe2O3不溶于水。
7.【答案】D
【解析】【解答】A. 乙烯、环己烷都属于脂肪烃,苯属于芳香烃,A不符合题意;
B. 苯属于芳香烃,环戊烷、环己烷属于脂肪烃,B不符合题意;
C. 乙烯属于烯烃,乙炔属于炔烃,C不符合题意;
D. 、 、 同属于环烷烃,D符合题意;
故答案为:D。
【分析】A.脂肪烃是指具有脂肪族化合物基本属性的碳氢化合物,脂肪族化合物中,碳原子以直链、支链或环状排列;
B.芳香烃是含有苯环的碳氢化合物;
C.烯烃是含有碳碳双键的碳氢化合物;
D.环烷烃是含有脂环结构的饱和烃;
8.【答案】B
【解析】【解答】A.胶体的本质特征是分散质粒子直径在1nm~100nm,溶液的分散质粒子直径小于1nm,A不符合题意;
B.向沸水中滴加饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即停止加热,来制备Fe(OH)3胶体,B符合题意;
C.鉴别溶液和胶体是利用丁达尔现象,即用激光笔照射,胶体有一条光亮的通路,而溶液没有,C不符合题意;
D. 胶体、溶液的分散质都能通过滤纸孔隙,D不符合题意;
故答案为:B
【分析】A.分散系分类的标准是分散质微粒的直径大小;
B.根据Fe(OH)3胶体的制备分析;
C.胶体具有丁达尔效应,而溶液没有;
D.胶体和溶液中分散质都能透过滤纸;
9.【答案】A
【解析】【解答】解:A.C2H6只有一种结构不存在同分异构体,所以能只表示一种物质,故A正确;
B.C4H8可以表示1﹣丁烯,2﹣丁烯,也可以表示环丁烷,甲基环丙烷,存在同分异构体,所以不能表示一种物质,故B错误;
C.C2H6O可以表示乙醇、甲醚,存在同分异构体,不能表示纯净物,故C错误;
D.C6H12O6可以表示葡萄糖、果糖等,不能表示纯净物,故D错误.
故选A.
【分析】同分异构体是分子式相同,但结构不同的化合物;根据是否存在同分异构体判断正误.
10.【答案】A
【解析】【解答】A.工业上是用电解饱和食盐水的方法制备氢氧化钠,不是采用氧化钠和水反应的方法制备氢氧化钠,成本太高,故A符合题意;
B.碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,是食品工业中一种应用广泛的食品疏松剂,故B不符合题意;
C.生石灰可以吸收空气中的水蒸气做干燥剂,为了防止食品受潮变质,常在食品包装袋中放入生石灰,故C不符合题意;
D.高铁酸钠具有强氧化性,能与水中的细菌发生氧化还原反应生成铁离子,铁离子水解生成具有吸附性的氢氧化铁胶体,吸附水中悬浮杂质形成沉淀而达到净水作用,是一种处理饮水的新型绿色消毒剂,故D不符合题意。
故答案为:A。
【分析】A、工业采用氯碱工业制备氢氧化钠:电解饱和食盐水;
B、根据碳酸氢钠受热分解生成二氧化碳的性质,用作食品疏松剂;
C、生石灰能够与水反应,常用于食品干燥剂;
D、高铁酸钠中铁元素化合价为+6,具有强氧化性,能够杀菌消毒,+3价铁水解生成氢氧化铁具有吸附性;
11.【答案】C
【解析】【解答】A.氯水是氯气的水溶液,为混合物,氨气是化合物,胆矾是化合物,A不符合题意;
B.碘酒是碘单质的酒精溶液,为混合物,铁是单质,有色玻璃是混合物,B不符合题意;
C.干冰是固态二氧化碳,为化合物,液液氯是液态的氯气为单质,汽油是混合物,C符合题意;
D.生石灰是氧化钙,为化合物,臭氧是单质,熟石灰是氢氧化钙,为纯净物,D不符合题意;
故答案为:C。
【分析】A.氯水是氯气的水溶液,为混合物,氨气是化合物,胆矾是化合物;
B.碘酒是碘单质的酒精溶液,为混合物;
C.干冰是固态二氧化碳,为化合物,液液氯是液态的氯气为单质,汽油是混合物;
D.熟石灰是氢氧化钙,为纯净物。
12.【答案】C
【解析】【解答】A. 、 、 都属于酸性氧化物, CO是不成盐氧化物,故A不符合题意;
B. 烧碱是氢氧化钠属于碱,纯碱是碳酸钠,属于盐,故B不符合题意;
C. 硫酸、醋酸电离出的阳离子都是氢离子,都属于酸,故C符合题意;
D. 硝酸银属于化合物,水银是单质,故D不符合题意;
故答案为:C。
【分析】A.和碱反应生成盐和水的氧化物为酸性氧化物;
B.电离出的阴离子全部为氢氧离子的化合物称为碱;
C.溶液中电离出的阳离子全部是氢离子的化合物为酸;
D.不同元素组成的纯净物为化合物。
13.【答案】A
【解析】【解答】解:A.100体积的水和100体积的酒精混合,所得混合溶液的体积小于200体积,故A错误;
B.在串联电路中电流的大小处处相等,故B正确;
C.稀盐酸和氢氧化钠溶液混合后,发生反应产物中无沉淀和气体生成,所以所得溶液质量与反应前溶液的总质量相等,故C正确;
D.根据质量守恒定律的意义可知化学反应物的原子种类和总数等于生成物的原子种类和总数,故D正确;
故选:A.
【分析】A.分子之间有间隙;
B.根据串联电路电流的特征解答;
C.依据质量守恒定律解答;
D.依据质量守恒定律及反应的生成物来判断.
14.【答案】D
【解析】【解答】氯化钠、氯气、碳酸氢钠不能水解,不能生成胶状物或絮状沉淀,不能用作混凝剂;
而明矾在溶液中易水解生成胶状沉淀,可做混凝剂;
故选D.
【分析】当物质在溶液中能形成胶状物时,能够絮凝成大颗粒,具有较强的吸附能力,可在水处理中作混凝剂.
15.【答案】D
【解析】【解答】A.KOH属于溶液,用光束照射不能观察到丁达尔现象,故A不符合题意;
B.NaNO3溶液属于溶液,用光束照射不能观察到丁达尔现象,故B不符合题意;
C.盐酸属于溶液,用光束照射不能观察到丁达尔现象,故C不符合题意;
D.Fe(OH)3胶体属于胶体分散系,用光束照射能观察到丁达尔现象,故D符合题意;
故答案为:D。
【分析】胶体具有丁达尔现象是指当光束通过胶体分散系时能看到一条光亮的通路,丁达尔现象是区分胶体和溶液最常用的简单方法,丁达尔效应的是胶体特有的性质,所以只要判断下列分散系是胶体即可。
16.【答案】C
【解析】【解答】A.AgNO3溶液属于溶液,不是胶体,A项不符合题意;
B.KOH溶液属于溶液,不是胶体,B项不符合题意;
C.Fe(OH)3胶体属于胶体,能产生丁达尔效应,C项符合题意;
D.稀H2SO4属于溶液,不是胶体,D项不符合题意;
故答案为:C。
【分析】丁达尔现象是胶体的特性,结合选项即可判断
17.【答案】(1)CO;常温常压下是气体,其余是固体;CO;非金属氧化物,其余是金属氧化物
(2)
(3)溶液;胶体;丁达尔效应
【解析】【解答】解:(1)①根据物质的状态分析,CO为气体,其余为固体,
故答案为:CO;常温常压下是气体,其余是固体;
②根据物质组成和状态来分类,在CuO、CO、MgO、Na2O、FeO中,CO属于非金属氧化物,CuO、MgO、Na2O、FeO属于金属氧化物,
故答案为:CO;非金属氧化物,其余是金属氧化物;(2)离子反应有的是氧化还原反应,有的不是氧化还原反应,二者的关系可以用右图表示: ,如离子反应H++OH﹣=H2O不属于氧化还原反应,离子反应Cl2+H2O=H++Cl﹣+HClO属于氧化还原反应,
故答案为:; ;(3)食醋属于溶液,淀粉溶液属于胶体,溶液无丁达尔效应,胶体有丁达尔效应,
故答案为:溶液;胶体;丁达尔效应.
【分析】(1)找出不同类的物质,要抓住其余5种物质的共同点,可以从物理性质和化学性质两方面进行分析;(2)离子反应有的是氧化还原反应,有的不是氧化还原反应;(3)食醋属于溶液,淀粉溶液属于胶体,丁达尔效应是胶体的特性;
18.【答案】(1)D
(2)E
(3)B
(4)E
【解析】【解答】解:(1)因Fe(OH)3胶粒带有正电荷,所以在电场的作用下,向阴极区移动,而使该区颜色加深,这种现象称为电泳,
故答案为:D;(2)光束通过胶体时,产生光亮的通路,称为丁达尔效应,
故答案为:E;(3)加入与胶粒带相反电荷的胶体,胶体会发生聚沉,
故答案为:B;(4)鉴别胶体和溶液利用丁达尔效应,故答案为:E.
【分析】(1)Fe(OH)3胶粒在电场的作用下,做定向运动,这种现象称为电泳;(2)光束通过胶体时,产生光亮的通路,称为丁达尔效应;(3)胶体遇胶粒带相反电荷的胶体发生聚沉;(4)丁达尔效应是胶体的特有性质.
19.【答案】(1)树状分类法
(2)HNO3;KOH;K2SO4;SO3;H2S
(3)SO2+2NaOH=Na2SO3+H2O
(4)正盐
【解析】【解答】解:(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树,有叶、枝、杆、根,图示方法就是树状图,
故答案为:树状分类法;(2)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,酸电离出的阳离子全部是氢离子的化合物,如H2SO4,电离方程式为H2SO4═2H++SO42﹣,②可以为HNO3,碱电离出的阴离子全部为氢氧根离子,如NaOH═Na++OH﹣,④可以为KOH,盐电离出得阳离子为金属离子,阴离子为酸根离子,如Na2SO4═2Na++SO42﹣,⑥为K2SO4,氧化物由两种元素组成其中一种为氧元素的化合物,如SO2 为酸性氧化物,则⑧为SO3,两种元素组成,其中一种是氢元素的化合物,属于氢化物,如NH3 ,则⑩为H2S等,
故答案为:HNO3;KOH;K2SO4;SO3;H2S;(3)少量的⑦与③反应的化学反应方程式为:SO2+2NaOH=Na2SO3+H2O,故答案为:SO2+2NaOH=Na2SO3+H2O;(4)由H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3亚磷酸是二元酸,所以Na2HPO3为正盐,故答案为:正盐.
【分析】(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树;(2)酸电离出的阳离子全部是氢离子的化合物;碱电离出的阴离子全部为氢氧根离子;盐电离出得阳离子为金属离子,阴离子为酸根离子;氧化物只有两种元素,且必须有氧元素;两种元素组成,其中一种是氢元素的化合物,属于氢化物;(3)少量二氧化硫和氢氧化钠溶液反应生成亚硫酸钠和水;(4)亚磷酸是二元酸生成的盐Na2HPO3为正盐;
20.【答案】(1)③、④、⑥、⑦、⑨;②、⑩;电解质;非电解质;④、⑥、⑦、⑨;③
(2)分别取样做丁达尔实验,出现丁达尔效应的是氢氧化铁胶体
(3)2HNO3+Ca(OH)2=Ca(NO3)2+2H2O
【解析】【解答】(1)由一种元素组成的纯净物是单质,如②、⑩,由不同种元素组成的纯净物是化合物,如:③、④、⑥、⑦、⑨;根据化合物在水溶液和熔融态下是否导电将化合物分为:电解质和非电解质;在水溶液或熔融状态下能导电的化合物是电解质,如④、⑥、⑦、⑨,在水溶液和熔融状态下均不导电的化合物是非电解质,如③;
(2)氢氧化铁胶体具有丁达尔效应,而溶液不具备该性质,可以做丁达尔实验来区分,即分别取样做丁达尔实验,出现丁达尔效应的是氢氧化铁胶体;
(3)上述10种物质中硝酸是强酸,氢氧化钙是强碱,混合后,发生中和反应生成盐和水,化学方程式为2HNO3+Ca(OH)2=Ca(NO3)2+2H2O。
【分析】(1)根据化合物、单质、电解质、非电解质定义进行分类即可;
(2)胶体具有丁达尔效应,可以用来区分溶液与胶体;
(3)熟悉常见的强酸与强碱。
21.【答案】(1)树状分类法
(2)NaOH;HNO3;NaNO3
(3)Na2O+CO2═Na2CO3
(4)将气体通入澄清的石灰水中,变浑浊,则说明该气体是二氧化碳
【解析】【解答】解:(1)交叉分类法含义:根据物质不同的分类标准,对同一事物进行多种分类的一种分类方式,树状分类法含义:对同一类事物按照某些属性进行在分类的分类法,无机化合物可根据其组成和性质进行分类:无机化合物、盐、碱、酸、氧化物、氢化物属于树状分类法;故答案为:树状分类法;(2)以H、O、S、N、Na五种元素中任意两种或三种元素可组成酸有:H2SO4或HNO3,碱有:NaOH、KOH或NH3 H2O,盐有:NaNO3、Na2SO4、NH4NO3,氧化物有:H2O、NO、NO2、N2O5、SO2、SO3、Na2O,氢化物有:NH3,H2O等,故答案为:②HNO3 ③NaOH、KOH或NH3 H2O ⑥NaNO3、Na2SO4、NH4NO3(任写一种); (3)因CO2能与氧化钠反应生成碳酸钠:Na2O+CO2═Na2CO3;故答案为:Na2O+CO2═Na2CO3;(4)检验二氧化碳气体,把气体通入澄清的石灰水,石灰水变浑浊,说明气体为二氧化碳;故答案为:将气体通入澄清的石灰水中,变浑浊,则说明该气体是二氧化碳.
【分析】(1)根据交叉分类法和树状分类法的定义判断;(2)以H、O、S、N、Na五种元素中任意两种或三种元素可组成酸、碱、盐、氧化物等,根据常见的物质书写;(3)根据二氧化碳可以与氧化钠反应生成碳酸钠;(4)根据CO2的检验方法:把气体通入澄清的石灰水,石灰水变浑浊,说明气体为二氧化碳.
