江苏省徐州市铜山区2023-2024学年高二上学期11月期中考试化学试题(合格考)(含答案)
文档属性
| 名称 | 江苏省徐州市铜山区2023-2024学年高二上学期11月期中考试化学试题(合格考)(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 893.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-25 00:00:00 | ||
图片预览


文档简介
徐州市铜山区2023-2024学年高二上学期11月期中考试
化学试题(合格考)
注意事项
考生在答题前请认真阅读本注意事项及各题答题要求
1.本试卷共6页.考试时间为75分钟,满分100分.考试结束后,请将答题卡或答题纸交回.
2.答题前,请务必将自己的姓名、考试证号用书写黑色字迹的0.5毫米签字笔填写在答题卡或答题纸上的规定位置.
3.使用答题卡作答选择题时,必须用2B铅笔把答题卡上对应选项的方框涂满涂黑;如需改动,请用橡皮擦干净后,再选涂其它答案(不使用答题卡作答选择题的,请将选择题答案写在答题纸选择题答题栏内).作答非选择题,必须用书写黑色字迹的0.5毫米签字笔将各题答案写在答题卡或答题纸上的指定位置,在其它位置作答一律无效.
4.如有作图需要,可用2B铅笔作答,并请加黑加粗,描写清楚.
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Ba-137
一、单项选择题:共28题,每题3分,共84分.每题只有一个选项最符合题意.
阅读下列材料,完成1-4题.
2023年9月23日晚,杭州第19届亚运会主火炬在杭州奥体中心主体育场点燃,本次开幕式主火炬燃料史无前例创新使用零碳甲醇燃料,以全球首创,助力打造史上首届碳中和亚运会,以绿色发展新高度展现“中国新时代,杭州新亚运”.
1.甲醇()属于下列物质中的( )
A.氢化物 B.碱 C.有机化合物 D.氧化物
2.甲醇()的摩尔质量为( )
A. B.32 C. D.
3.对甲醇的性质起着决定作用的基团叫作官能团,甲醇()的官能团为( )
A.羟基 B.氢氧根 C.羧基 D.甲基
4.本次亚运会主火炬燃料甲醇的制取原理是综合利用焦炉气中的副产物氢气与从工业尾气中捕集的二氧化碳合成绿色甲醇,其化学方程式为,对于该反应,下列说法正确的是( )
A.该反应属于置换反应 B.是氧化剂
C.发生氧化反应 D.每消耗1mol转移6mol电子
5.物质的俗名往往反映了物质的组成、性质与用途等,下列对物质俗名的解释不正确的是( )
A.磁性氧化铁——天然矿石的四氧化三铁具有磁性 B.纯碱——属于碱
C.臭氧——具有鱼腥味 D.石灰石——煅烧后可得生石灰
6.新材料的研发离不开化学的贡献.下列说法正确的是( )
A.氮化硅陶瓷属于传统的硅酸盐材料 B.制作太阳能电池板的材料是二氧化硅
C.铝合金材料属于金属材料 D.常用来包装食品的塑料是聚氯乙烯材料
7.下列物质属于电解质的是( )
A.稀盐酸 B.四氯化碳 C.硫酸钡 D.氨气
8.44.8L(标准状况)HCl溶于水配成4L溶液,则物质的量浓度为( )
A. B. C. D.
9.下列物质中存在离子键不存在共价键的是( )
A. B. C. D.
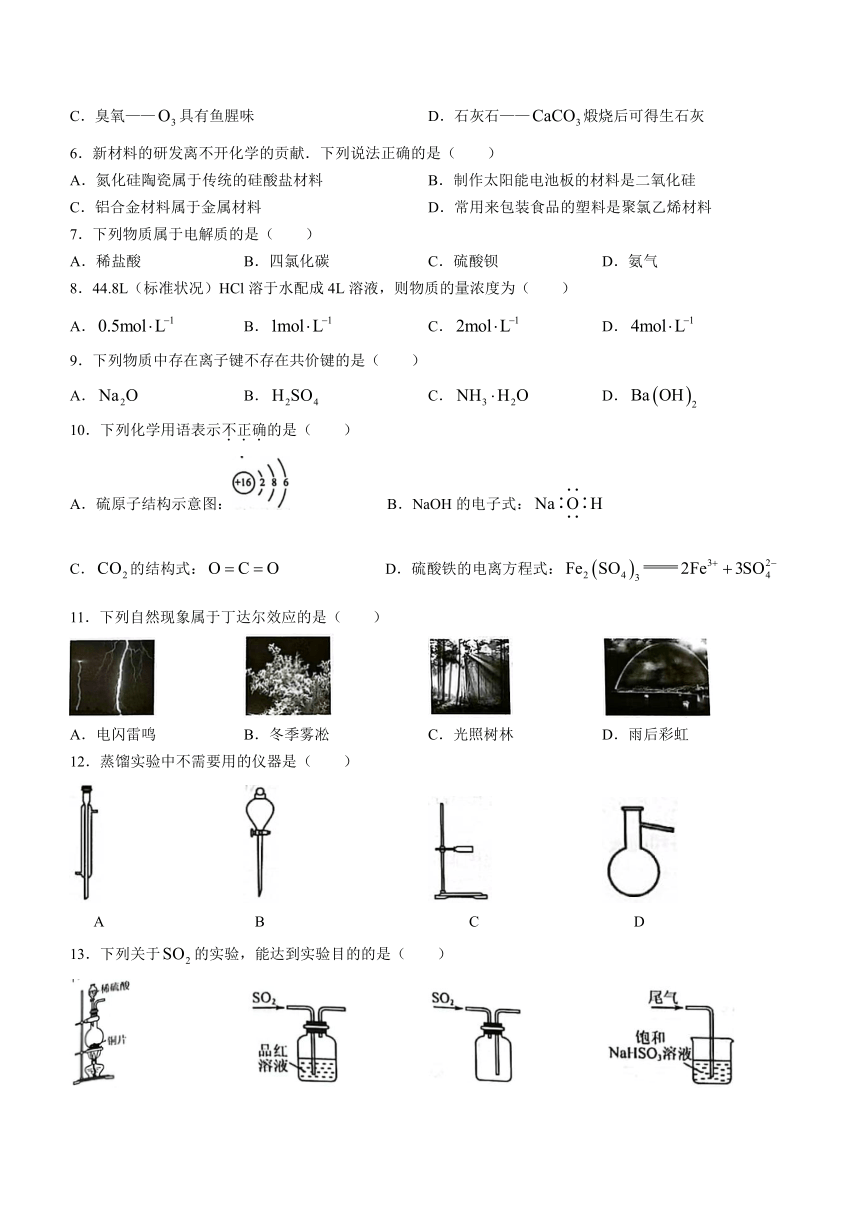
10.下列化学用语表示不正确的是( )
A.硫原子结构示意图: B.NaOH的电子式:
C.的结构式: D.硫酸铁的电离方程式:
11.下列自然现象属于丁达尔效应的是( )
A.电闪雷鸣 B.冬季雾凇 C.光照树林 D.雨后彩虹
12.蒸馏实验中不需要用的仪器是( )
A B C D
13.下列关于的实验,能达到实验目的的是( )
A.制取 B.验证漂白性 C.收集 D.尾气处理
14.下列物质的变化,不能通过一步化学反应完成的是( )
A. B. C. D.
15.一种可用于潜艇的电池的电极材料为锂和钢板,电解质为LiOH,使用时加入水即可放电.电池反应为.下列说法不正确的是( )
A.钢板为正极 B.在正极生成
C.移向正极 D.电子由锂经导线流向钢板
16.日常生活中许多现象与氧化还原反应有关,下列现象与氧化还原反应无关的是( )
A.钟乳石的形成 B.植物的光合作用
C.充有氢气的气球遇明火爆炸 D.铜制自来水龙头表面出现铜绿
17.下列关于浓硫酸的说法不正确的是( )
A.浓硫酸具有吸水性,常做干燥剂 B.浓硫酸具有脱水性,能使纸张变黑
C.常温下浓硫酸不能和铁反应 D.浓硫酸沸点高,难挥发
18.NaCl被称为“化学工业之母”.下列说法不正确的是( )
A.“制皂”:向油脂的碱性水解液中加入热的饱和食盐水,使高级脂肪酸盐析出
B.“侯氏制碱”:将、通入饱和食盐水中,析出碳酸钠晶体
C.“氯碱工业”:电解饱和食盐水可获得、NaOH和
D.“制钠”:电解熔融的NaCl可制备金属Na
19.下列各组物质互为同分异构体的是( )
A.金刚石和石墨 B.和
C.和 D.和
20.下列图示变化为吸热反应的是( )
A B C D
21.下列各组离子中,能在溶液中大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、、、
22.乙醇、乙酸是两种常见的有机化合物,下列对于其共同点的叙述正确的是( )
A.都能使蓝色石蕊试纸变红 B.都能与NaOH溶液反应
C.都能与溶液反应 D.都能与Na反应
23.下列反应的离子方程式书写正确的是( )
A.铁与稀盐酸反应:
B.与水反应
C.鸡蛋壳(主要成分为)与醋酸溶液反应:
D.小苏打与氢氧化钠反应:
24.对于放热反应,下列说法正确的是( )
A.反应物的总能量小于生成物的总能量 B.该反应的逆反应是吸热反应
C.升高温度可以使反应速率减小 D.增大的浓度能使完全转化
25.下列转化能通过加成反应一步实现的是( )
A. B.
C. D.
26.下列有关实验操作的说法,不正确的是( )
A.提纯混有少量氯化钾的硝酸钾,将混合物溶于较高温度的水制得浓溶液,然后冷却到室温,过滤、洗涤、干燥,得到较高纯度的硝酸钾晶体
B.检验溶液中的:取一根洁净的铂丝,放在酒精灯火焰上灼烧至无色,然后蘸取少量试液,置于火焰上灼烧,透过蓝色钻玻璃观察,若火焰呈紫色,则含有
C.分离分液漏斗中互不相溶的两种液体:打开上口活塞,转动旋塞将下层液体放出,然后关闭旋塞,将上层液体从上口倒出
D.配制100mL溶液:称取1.06g固体,放入100mL容量瓶中,加水定容至100mL刻度线
27.已知短周期主族元素W、R、X、Y、Z的原子序数依次增大,W是地壳中含量最多的元素,W、Z同主族,X是短周期中金属性最强的元素,Y元素的原子核外最外层电子数等于电子层数.下列叙述正确的是( )
A.W的简单气态氢化物的热稳定性比R的强
B.原子半径:
C.元素W与X形成的化合物只有一种
D.X、Y、Z的最高价氧化物的水化物两两之间能相互反应
28.某工厂的固体废渣中主要含Cu和CuO,还含有少量.利用该固体废渣制取的部分工艺流程如图所示:
下列说法不正确的是( )
A.为了加快酸溶的速度,可以采取的方法有不断搅拌或适当提高温度等
B.酸溶过程中铜参加反应的离子方程式为
C.滤渣的主要成分为
D.过滤需用到的玻璃仪器有烧杯、漏斗和玻璃瓶
二、非选择题,共2题,共16分.
29.(6分)根据如下物质的转化关系图,回答有关问题:
(1)上述物质中,______ (填结构式)的产量是衡量一个国家石油化工发展水平的标志.
(2)乙酸中的官能团名称是______ 。乙醛与氧气生成乙酸的反应属于______ 反应(填“氧化”或“还原”).
(3)生成乙酸乙酯的化学方程式是______ .
30.某化学兴趣小组为探究的性质,按如图所示装置进行实验.
(已知:)
(1)反应后,装置B中溶液紫色褪去,反应中能生成可溶性的,该反应的离子方程式为______ .
(2)装置C中溶液中有淡黄色沉淀生成,该反应表体现了的______性;
(3)装置D的目的是探究与品红作用的可逆性,请写出实验操作及现象:______.
(4)某硫酸厂周围的空气中含有较多的二氧化硫,某兴趣小组为了测定空气中二氧化硫的体积分数,做了如下实验.取标准状况下的空气2.000L(含氮气、氧气、二氧化碳、二氧化硫等),缓缓通过足量溴水,反应的化学方程式为:
在所得溶液中加入稍过量的氯化钡溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为0.466g.试计算该空气样品中二氧化硫的体积分数.
徐州市铜山区2023-2024学年高二上学期11月期中考试
化学(合格考)试题参考答案与评分标准
阅卷说明:
1.本试卷中每个化学方程式、离子方程式2分,反应物、生成物书写均正确得1分,未配平、未注明或写错反应条件、未注明或写错符号的等共扣1分.
2.本卷中所有合理答案均参照给分.
一、单项选择题:本题包括28题,每题3分,共计84分.每题只有一个选项符合题意.
1.C 2.D 3.A 4.C 5.B 6.C 7.C 8.A 9.A 10.B 11.C 12.B 13.B 14.A
15.C 16.A 17.C 18.B 19.D 20.A 21.C 22.D 23.D 24.B 25.A 26.D 27.D
28.B
二、非选择题(16分)
29.(6分)
(1)(2分) (2)羧基(1分) 氧化(1分)
(3)(2分)
30.(10分)
(1)(2分)
(2)氧化性(2分)
(3)品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,溶液恢复为红色(2分)
(4)解:依题意可知
即
故空气中二氧化硫的体积分数为(4分)
化学试题(合格考)
注意事项
考生在答题前请认真阅读本注意事项及各题答题要求
1.本试卷共6页.考试时间为75分钟,满分100分.考试结束后,请将答题卡或答题纸交回.
2.答题前,请务必将自己的姓名、考试证号用书写黑色字迹的0.5毫米签字笔填写在答题卡或答题纸上的规定位置.
3.使用答题卡作答选择题时,必须用2B铅笔把答题卡上对应选项的方框涂满涂黑;如需改动,请用橡皮擦干净后,再选涂其它答案(不使用答题卡作答选择题的,请将选择题答案写在答题纸选择题答题栏内).作答非选择题,必须用书写黑色字迹的0.5毫米签字笔将各题答案写在答题卡或答题纸上的指定位置,在其它位置作答一律无效.
4.如有作图需要,可用2B铅笔作答,并请加黑加粗,描写清楚.
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Ba-137
一、单项选择题:共28题,每题3分,共84分.每题只有一个选项最符合题意.
阅读下列材料,完成1-4题.
2023年9月23日晚,杭州第19届亚运会主火炬在杭州奥体中心主体育场点燃,本次开幕式主火炬燃料史无前例创新使用零碳甲醇燃料,以全球首创,助力打造史上首届碳中和亚运会,以绿色发展新高度展现“中国新时代,杭州新亚运”.
1.甲醇()属于下列物质中的( )
A.氢化物 B.碱 C.有机化合物 D.氧化物
2.甲醇()的摩尔质量为( )
A. B.32 C. D.
3.对甲醇的性质起着决定作用的基团叫作官能团,甲醇()的官能团为( )
A.羟基 B.氢氧根 C.羧基 D.甲基
4.本次亚运会主火炬燃料甲醇的制取原理是综合利用焦炉气中的副产物氢气与从工业尾气中捕集的二氧化碳合成绿色甲醇,其化学方程式为,对于该反应,下列说法正确的是( )
A.该反应属于置换反应 B.是氧化剂
C.发生氧化反应 D.每消耗1mol转移6mol电子
5.物质的俗名往往反映了物质的组成、性质与用途等,下列对物质俗名的解释不正确的是( )
A.磁性氧化铁——天然矿石的四氧化三铁具有磁性 B.纯碱——属于碱
C.臭氧——具有鱼腥味 D.石灰石——煅烧后可得生石灰
6.新材料的研发离不开化学的贡献.下列说法正确的是( )
A.氮化硅陶瓷属于传统的硅酸盐材料 B.制作太阳能电池板的材料是二氧化硅
C.铝合金材料属于金属材料 D.常用来包装食品的塑料是聚氯乙烯材料
7.下列物质属于电解质的是( )
A.稀盐酸 B.四氯化碳 C.硫酸钡 D.氨气
8.44.8L(标准状况)HCl溶于水配成4L溶液,则物质的量浓度为( )
A. B. C. D.
9.下列物质中存在离子键不存在共价键的是( )
A. B. C. D.
10.下列化学用语表示不正确的是( )
A.硫原子结构示意图: B.NaOH的电子式:
C.的结构式: D.硫酸铁的电离方程式:
11.下列自然现象属于丁达尔效应的是( )
A.电闪雷鸣 B.冬季雾凇 C.光照树林 D.雨后彩虹
12.蒸馏实验中不需要用的仪器是( )
A B C D
13.下列关于的实验,能达到实验目的的是( )
A.制取 B.验证漂白性 C.收集 D.尾气处理
14.下列物质的变化,不能通过一步化学反应完成的是( )
A. B. C. D.
15.一种可用于潜艇的电池的电极材料为锂和钢板,电解质为LiOH,使用时加入水即可放电.电池反应为.下列说法不正确的是( )
A.钢板为正极 B.在正极生成
C.移向正极 D.电子由锂经导线流向钢板
16.日常生活中许多现象与氧化还原反应有关,下列现象与氧化还原反应无关的是( )
A.钟乳石的形成 B.植物的光合作用
C.充有氢气的气球遇明火爆炸 D.铜制自来水龙头表面出现铜绿
17.下列关于浓硫酸的说法不正确的是( )
A.浓硫酸具有吸水性,常做干燥剂 B.浓硫酸具有脱水性,能使纸张变黑
C.常温下浓硫酸不能和铁反应 D.浓硫酸沸点高,难挥发
18.NaCl被称为“化学工业之母”.下列说法不正确的是( )
A.“制皂”:向油脂的碱性水解液中加入热的饱和食盐水,使高级脂肪酸盐析出
B.“侯氏制碱”:将、通入饱和食盐水中,析出碳酸钠晶体
C.“氯碱工业”:电解饱和食盐水可获得、NaOH和
D.“制钠”:电解熔融的NaCl可制备金属Na
19.下列各组物质互为同分异构体的是( )
A.金刚石和石墨 B.和
C.和 D.和
20.下列图示变化为吸热反应的是( )
A B C D
21.下列各组离子中,能在溶液中大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、、、
22.乙醇、乙酸是两种常见的有机化合物,下列对于其共同点的叙述正确的是( )
A.都能使蓝色石蕊试纸变红 B.都能与NaOH溶液反应
C.都能与溶液反应 D.都能与Na反应
23.下列反应的离子方程式书写正确的是( )
A.铁与稀盐酸反应:
B.与水反应
C.鸡蛋壳(主要成分为)与醋酸溶液反应:
D.小苏打与氢氧化钠反应:
24.对于放热反应,下列说法正确的是( )
A.反应物的总能量小于生成物的总能量 B.该反应的逆反应是吸热反应
C.升高温度可以使反应速率减小 D.增大的浓度能使完全转化
25.下列转化能通过加成反应一步实现的是( )
A. B.
C. D.
26.下列有关实验操作的说法,不正确的是( )
A.提纯混有少量氯化钾的硝酸钾,将混合物溶于较高温度的水制得浓溶液,然后冷却到室温,过滤、洗涤、干燥,得到较高纯度的硝酸钾晶体
B.检验溶液中的:取一根洁净的铂丝,放在酒精灯火焰上灼烧至无色,然后蘸取少量试液,置于火焰上灼烧,透过蓝色钻玻璃观察,若火焰呈紫色,则含有
C.分离分液漏斗中互不相溶的两种液体:打开上口活塞,转动旋塞将下层液体放出,然后关闭旋塞,将上层液体从上口倒出
D.配制100mL溶液:称取1.06g固体,放入100mL容量瓶中,加水定容至100mL刻度线
27.已知短周期主族元素W、R、X、Y、Z的原子序数依次增大,W是地壳中含量最多的元素,W、Z同主族,X是短周期中金属性最强的元素,Y元素的原子核外最外层电子数等于电子层数.下列叙述正确的是( )
A.W的简单气态氢化物的热稳定性比R的强
B.原子半径:
C.元素W与X形成的化合物只有一种
D.X、Y、Z的最高价氧化物的水化物两两之间能相互反应
28.某工厂的固体废渣中主要含Cu和CuO,还含有少量.利用该固体废渣制取的部分工艺流程如图所示:
下列说法不正确的是( )
A.为了加快酸溶的速度,可以采取的方法有不断搅拌或适当提高温度等
B.酸溶过程中铜参加反应的离子方程式为
C.滤渣的主要成分为
D.过滤需用到的玻璃仪器有烧杯、漏斗和玻璃瓶
二、非选择题,共2题,共16分.
29.(6分)根据如下物质的转化关系图,回答有关问题:
(1)上述物质中,______ (填结构式)的产量是衡量一个国家石油化工发展水平的标志.
(2)乙酸中的官能团名称是______ 。乙醛与氧气生成乙酸的反应属于______ 反应(填“氧化”或“还原”).
(3)生成乙酸乙酯的化学方程式是______ .
30.某化学兴趣小组为探究的性质,按如图所示装置进行实验.
(已知:)
(1)反应后,装置B中溶液紫色褪去,反应中能生成可溶性的,该反应的离子方程式为______ .
(2)装置C中溶液中有淡黄色沉淀生成,该反应表体现了的______性;
(3)装置D的目的是探究与品红作用的可逆性,请写出实验操作及现象:______.
(4)某硫酸厂周围的空气中含有较多的二氧化硫,某兴趣小组为了测定空气中二氧化硫的体积分数,做了如下实验.取标准状况下的空气2.000L(含氮气、氧气、二氧化碳、二氧化硫等),缓缓通过足量溴水,反应的化学方程式为:
在所得溶液中加入稍过量的氯化钡溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为0.466g.试计算该空气样品中二氧化硫的体积分数.
徐州市铜山区2023-2024学年高二上学期11月期中考试
化学(合格考)试题参考答案与评分标准
阅卷说明:
1.本试卷中每个化学方程式、离子方程式2分,反应物、生成物书写均正确得1分,未配平、未注明或写错反应条件、未注明或写错符号的等共扣1分.
2.本卷中所有合理答案均参照给分.
一、单项选择题:本题包括28题,每题3分,共计84分.每题只有一个选项符合题意.
1.C 2.D 3.A 4.C 5.B 6.C 7.C 8.A 9.A 10.B 11.C 12.B 13.B 14.A
15.C 16.A 17.C 18.B 19.D 20.A 21.C 22.D 23.D 24.B 25.A 26.D 27.D
28.B
二、非选择题(16分)
29.(6分)
(1)(2分) (2)羧基(1分) 氧化(1分)
(3)(2分)
30.(10分)
(1)(2分)
(2)氧化性(2分)
(3)品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,溶液恢复为红色(2分)
(4)解:依题意可知
即
故空气中二氧化硫的体积分数为(4分)
同课章节目录
