专题2 物质的制备、检验、分离及提纯(共39张PPT)
文档属性
| 名称 | 专题2 物质的制备、检验、分离及提纯(共39张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-25 00:00:00 | ||
图片预览







文档简介
(共39张PPT)
专题2 物质的制备、检验、分离及提纯
考题统计
物质的制备、分离、检验、及提纯:
辽宁卷(2023),广东卷(2022),山东卷(2023、2022、2021),海南卷(2021),北京卷(2021),湖南卷(2021),江苏卷(2021),湖北卷(2021)
要点1常见气体的制备、净化、收集及尾气处理
课标指引:1.研究物质性质,探究反应规律,进行物质的制备等不同类型的化学实验。 2.体会实验条件控制对完成科学实验及探究活动的作用。
聚焦核心要点
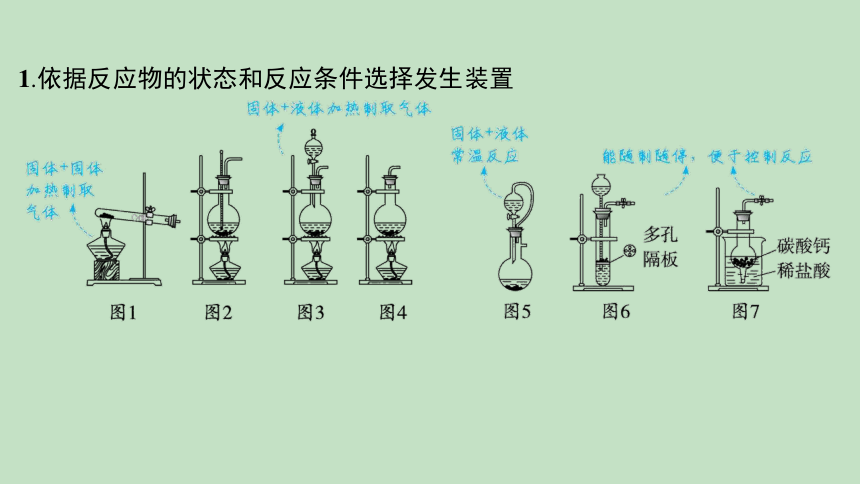
1.依据反应物的状态和反应条件选择发生装置
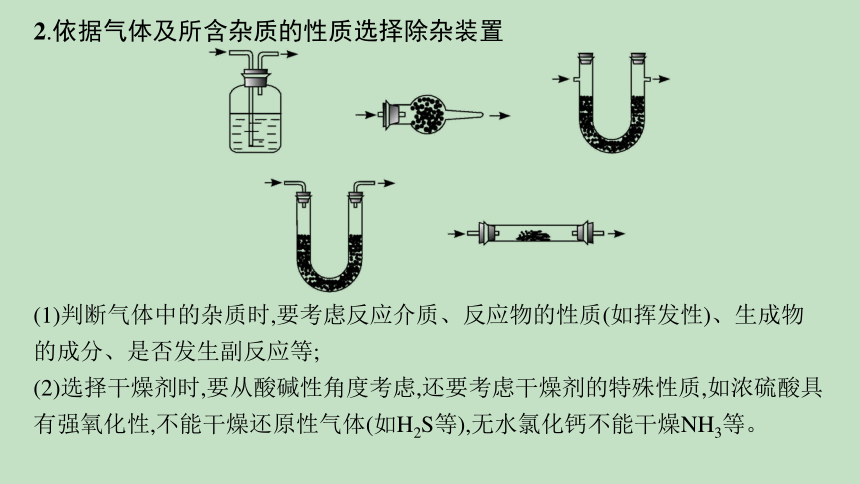
2.依据气体及所含杂质的性质选择除杂装置
(1)判断气体中的杂质时,要考虑反应介质、反应物的性质(如挥发性)、生成物的成分、是否发生副反应等;
(2)选择干燥剂时,要从酸碱性角度考虑,还要考虑干燥剂的特殊性质,如浓硫酸具有强氧化性,不能干燥还原性气体(如H2S等),无水氯化钙不能干燥NH3等。
3.依据气体的密度、水溶性选择收集装置
微点拨
根据气体与空气的相对分子质量(29)判断气体的相对密度:若气体的相对分子质量大于29,则其密度大于空气,反之,则密度小于空气。
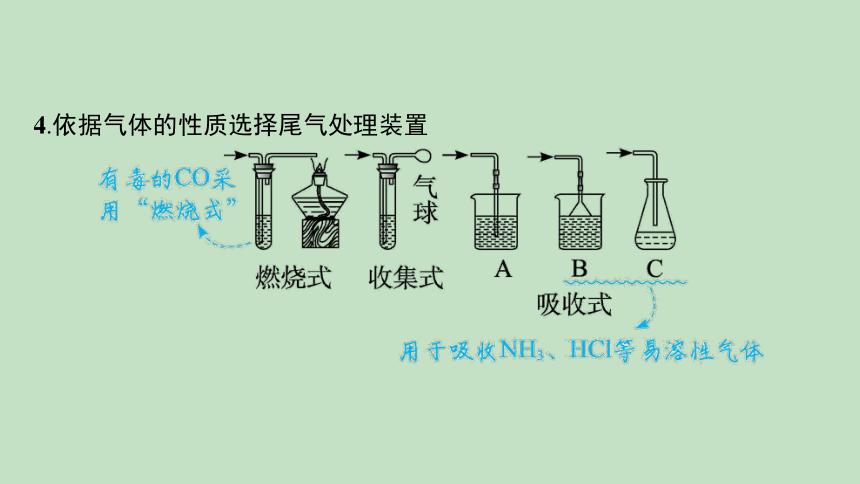
4.依据气体的性质选择尾气处理装置
要点2物质的检验、分离及提纯
课标指引:1.初步学会物质检验、分离、提纯等化学实验基础知识和基本技能。 2.学习进行物质分离、检验和制备等不同类型化学实验及探究活动的核心思路与基本方法。
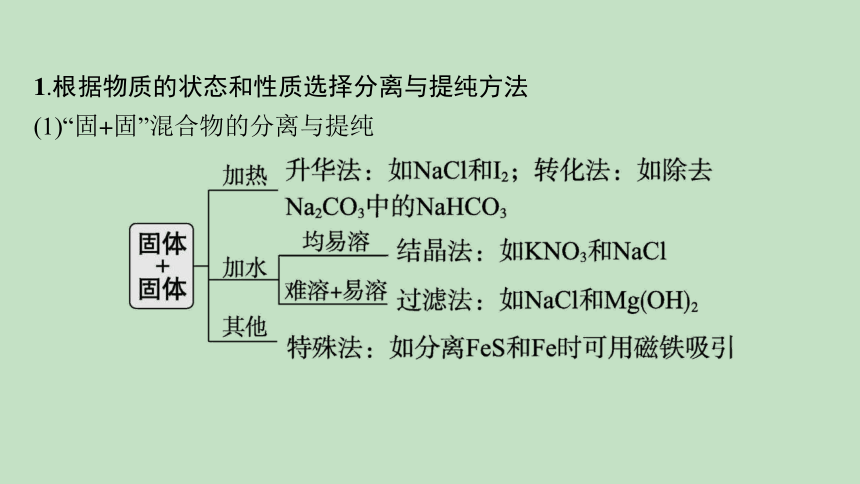
1.根据物质的状态和性质选择分离与提纯方法
(1)“固+固”混合物的分离与提纯
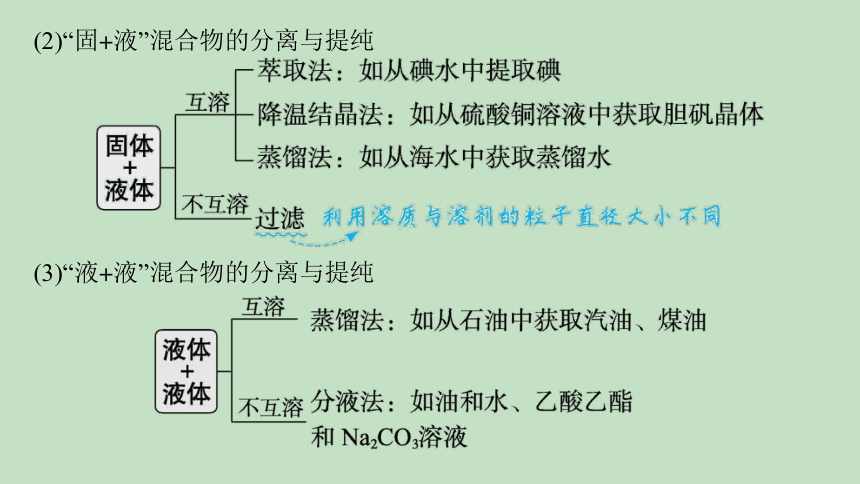
(2)“固+液”混合物的分离与提纯
(3)“液+液”混合物的分离与提纯
(4)“气+气”混合物的分离与提纯
2.基于常见气体的性质掌握其检验方法
常见气体 常用检验方法(或思路)
O2 使带火星的木条复燃
CO 将气体通过灼热的CuO,CuO由黑色变成红色,且气体产物可使澄清石灰水变浑浊
CO2 使澄清石灰水变浑浊,继续通入又可变澄清
SO2 使品红溶液褪色,加热后又恢复红色
Cl2 使湿润的淀粉KI试纸变蓝
NH3 使湿润的红色石蕊试纸变蓝;靠近浓盐酸(或浓硝酸)时冒白烟
CH2=CH2 能使酸性高锰酸钾溶液、溴水、溴的四氯化碳溶液褪色
3.基于官能团掌握常见有机化合物的检验方法
有机化合物 常用检验方法(或思路)
卤代烃 加入NaOH溶液并加热使卤代烃水解,再加稀硝酸中和至弱酸性,滴加AgNO3溶液
醛、葡萄糖 与银氨溶液(水浴加热)反应形成银镜;
与新制的Cu(OH)2(加热)反应生成红色沉淀(Cu2O)
羧酸 加入NaHCO3溶液产生无色无味气体
检验有机化合物中羧基的特征反应
淀粉 淀粉溶液遇碘显蓝色
常用淀粉溶液作碘滴定实验的指示剂
蛋白质 灼烧,有烧焦羽毛的气味;加浓硝酸并微热,颜色变黄(含苯环结构的蛋白质用此法)
易错辨析
1.根据食用油和汽油的密度不同,可选用分液的方法分离。( )
2.分离淀粉胶体中的NaCl溶液,可选用过滤的方法。( )
3.向MgCl2溶液中加入CaCO3粉末,充分搅拌后过滤可除去杂质FeCl3。( )
4.除去硝酸中的NO2:可向硝酸中加入少量水并通入空气。( )
×
二者互溶,应选用蒸馏法分离。
×
胶体粒子和Na+、Cl-均能透过滤纸,应改为渗析法。
×
引入新杂质,应加入MgO等。
√
4NO2+O2+2H2O ══ 4HNO3。
精研核心命题
命题点1常见气体的制备、净化、收集及尾气处理
典例1 (2023·广东卷)1827年,英国科学家法拉第进行了NH3喷泉实验。在此启发下,兴趣小组利用以下装置,进行如下实验。其中,难以达到预期目的的是( )
A.喷泉实验 B.干燥NH3
C.收集NH3 D.制备NH3
B
解析 NH3极易溶于水,挤出胶头滴管中的水,打开止水夹,NH3溶于水形成压强差,引发喷泉实验,A正确;P2O5是酸性干燥剂,不能干燥碱性气体NH3,B错误;NH3的密度小于空气的密度,采用向下排空气法收集NH3,将其从短管通入,将空气从长管排出,C正确;浓氨水加入CaO中发生反应生成Ca(OH)2,同时放出NH3,可制备少量NH3,D正确。
变式演练(2021·北京卷)实验室制备下列气体所选试剂、制备装置及收集方法均正确的是( )
选项 气体 试剂 制备装置 收集方法
A O2 KMnO4 a d
B H2 Zn+稀硫酸 b e
C NO Cu+稀硝酸 b c
D CO2 CaCO3+稀硫酸 b c
B
解析 KMnO4是固体物质,加热分解产生O2,由于O2难溶于水,因此可以使用排水法或向上排空气法收集,故不可以使用a、d装置制取和收集O2,A错误;Zn与稀硫酸发生置换反应产生H2,块状固体与液体反应制取气体,产生的H2难溶于水,可以使用排水法收集,故可以使用装置b、e制取H2,B正确;Cu与稀硝酸反应产生NO气体,NO能够与O2发生反应产生NO2气体,不能使用排空气的方法收集,C错误;CaCO3与稀硫酸反应产生CaSO4、CO2气体,CaSO4微溶于水,使制取CO2气体不能持续发生,不能使用该方法制取CO2气体,D错误。
命题点2物质的分离及提纯
典例2 (2022·北京卷)下列实验中,不能达到实验目的的是( )
答案 D
解析 采用“蒸馏法”除去海水中的盐分制取蒸馏水,装置及操作均合理,A正确;碘在CCl4中溶解度大于在水中溶解度,且CCl4和水互不相溶,故可用CCl4萃取碘水中的碘,B正确;采用“过滤法”分离粗盐中的不溶物,实验装置及操作均合理,C正确;FeCl3易发生水解,要在HCl氛围中加热FeCl3·6H2O晶体获得FeCl3固体,D错误。
变式演练(2023·广东茂名一模)实验室制备纯化乙酸乙酯,下列操作正确的是( )
A.①混合乙醇和浓硫酸
B.②收集乙酸乙酯
C.③分离乙酸乙酯和饱和碳酸钠溶液
D.④提纯乙酸乙酯
C
解析 ①操作错误,混合乙醇和浓硫酸时是将浓硫酸缓缓加入乙醇中,A错误;②操作错误,收集乙酸乙酯时导管不能伸入溶液液面以下,B错误;③操作正确,分离乙酸乙酯和饱和碳酸钠溶液,先将下层液体放出,再从上口倒出乙酸乙酯,C正确;④操作错误,提纯乙酸乙酯时温度计水银部位在支管口处,D错误。
【思维建模】
解答物质的分离及提纯类题目的思维模型
命题点3物质的鉴别与检验
典例3 (2023·辽宁卷)下列鉴别或检验不能达到实验目的的是( )
A.用石灰水鉴别Na2CO3与NaHCO3
B.用KSCN溶液检验FeSO4是否变质
C.用盐酸酸化的BaCl2溶液检验Na2SO3是否被氧化
D.加热条件下用银氨溶液检验乙醇中是否混有乙醛
A
解析 Na2CO3和NaHCO3与石灰水反应都能生成难溶的CaCO3沉淀,A项符合题意;KSCN与Fe3+能生成红色物质,可用于检验FeSO4是否变质,B项不符合题意;Na2SO3被氧化为Na2SO4,Na2SO4与BaCl2反应生成的BaSO4不溶于盐酸,C项不符合题意;乙醛能与银氨溶液发生银镜反应,而乙醇不能,D项不符合题意。
变式演练(2023·天津卷)下列方法(试剂)中,无法鉴别Na2CO3和BaCl2两种物质的是( )
A.焰色试验 B.pH试纸
C.稀氨水 D.Na2SO4
C
解析 进行焰色试验时,Na2CO3呈现黄色火焰,BaCl2呈现绿色火焰,可以鉴别,A正确;Na2CO3溶液呈碱性,BaCl2溶液呈中性,可用pH试纸进行鉴别,B正确;Na2CO3溶液、BaCl2溶液与稀氨水均不发生反应,无法鉴别,C错误;BaCl2溶液与Na2SO4溶液反应生成白色沉淀BaSO4,Na2CO3则不能,可以鉴别,D正确。
训练分层落实
练真题·明考向
1.(2023·山东卷)鉴别浓度均为0.1 mol·L-1的NaClO、Ba(OH)2、Al2(SO4)3三种溶液,仅用下列一种方法不可行的是( )
A.测定溶液pH
B.滴加酚酞试剂
C.滴加0.1 mol·L-1 KI溶液
D.滴加饱和Na2CO3溶液
C
解析 ClO-水解使NaClO溶液显碱性,Ba(OH)2属于强碱,Al3+水解使Al2(SO4)3溶液显酸性,因此可以通过测定溶液pH的方法鉴别这三种浓度相等的溶液,A正确。三种溶液中滴加酚酞试剂的现象分别为NaClO溶液先变红后褪色,Ba(OH)2溶液变红,Al2(SO4)3溶液无明显现象,B正确。KI溶液与Ba(OH)2、Al2(SO4)3都不反应,二者无法鉴别,C错误。三种溶液中滴加饱和Na2CO3溶液的现象分别为NaClO溶液无明显现象,Ba(OH)2溶液中产生白色沉淀,Al2(SO4)3溶液中既有白色沉淀又有气体产生,D正确。
2.(2023·浙江6月选考卷)苯甲酸是一种常用的食品防腐剂。某实验小组设计粗苯甲酸(含有少量NaCl和泥沙)的提纯方案如下:
下列说法不正确的是( )
A.操作Ⅰ中依据苯甲酸的溶解度估算加水量
B.操作Ⅱ趁热过滤的目的是除去泥沙和NaCl
C.操作Ⅲ缓慢冷却结晶可减少杂质被包裹
D.操作Ⅳ可用冷水洗涤晶体
B
解析 操作Ⅰ中,为减少能耗、减少苯甲酸的溶解损失,溶解所用水的量需加以控制,可依据苯甲酸的大致含量、溶解度等估算加水量,A正确;操作Ⅱ趁热过滤的目的,是除去泥沙,同时防止苯甲酸结晶析出,NaCl含量少,通常不结晶析出,B错误;操作Ⅲ缓慢冷却结晶,可形成较大的苯甲酸晶体颗粒,同时可减少杂质被包裹在晶体颗粒内部,C正确;苯甲酸微溶于冷水,易溶于热水,所以操作Ⅳ可用冷水洗涤晶体,既可去除晶体表面吸附的杂质离子,又能减少溶解损失,D正确。
3.(2022·山东卷)已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲苯、苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是( )
A.苯胺既可与盐酸也可与NaOH溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
C
解析 本题考查有机化合物的性质,实验室分离、提纯有机化合物的方法。
由题给流程可知,向甲苯、苯胺、苯甲酸的混合溶液中加入盐酸,盐酸将微溶于水的苯胺转化为易溶于水的苯胺盐酸盐,分液得到水相Ⅰ和有机相Ⅰ;向水相Ⅰ中加入氢氧化钠溶液将苯胺盐酸盐转化为苯胺,分液得到苯胺粗品①;向有机相Ⅰ中加入水洗涤除去混有的盐酸,分液得到废液和有机相Ⅱ,向有机相Ⅱ中加入碳酸钠溶液将微溶于水的苯甲酸转化为易溶于水的苯甲酸钠,分液得到甲苯粗品②和水相Ⅱ;向水相Ⅱ中加入盐酸,将苯甲酸钠转化为苯甲酸,经蒸发结晶、过滤、洗涤得到苯甲酸粗品③。苯胺分子中含有的氨基能与盐酸反应,不能与NaOH溶液反应,A项错误;由分析可知,得到苯胺粗品①的分离方法为分液,得到苯甲酸粗品③的分离方法为蒸发结晶、过滤、洗涤,获取两者粗品的操作方法不同,B项错误;苯胺粗品、甲苯粗品、苯甲酸粗品依次由①、②、③获得,C项正确;①、②为有机相,③为固相,都不是两相混合体系,D项错误。
练易错·避陷阱
4.(2023·河南郑州一模)下列实验中,所采取的实验方法与对应原理都正确的是( )
选项 实验目的 实验方法 实验原理
A 分离乙酸乙酯和乙醇 用分液漏斗分液 乙酸乙酯和乙醇的密度不同
B 除去CO2中少量的SO2 用饱和 NaHCO3溶液洗气 SO2能与
NaHCO3反应生成CO2
C 检验溶液中的 滴加稀盐酸,产生无色无味且能使澄清石灰水变浑浊的气体 +2H+══H2O+CO2↑
D 得到纯净的Cl2 将混有HCl的Cl2通过饱和食盐水 HCl极易溶于水
B
解析 乙酸乙酯和乙醇互溶,不能采取分液的方法分离,A错误;SO2能与NaHCO3反应生成CO2,故用饱和NaHCO3溶液可除去CO2中少量的SO2,B正确;加入足量稀盐酸,将生成的无色无味气体通入澄清石灰水,若澄清石灰水变浑浊,不能说明溶液中一定含有 ,也有可能含有 ,C错误;将Cl2与HCl的混合气体通过饱和食盐水,可以除去HCl,但是Cl2中还会混有水,得不到纯净的Cl2,D错误。
练预测·押考向
5.(2023·北京丰台区一模)实验室中,下列气体制备的试剂和装置正确的是
( )
选项 A B C D
气体 C2H2 SO2 NH3 Cl2
试剂 电石、饱和食盐水 Na2SO3、浓硫酸 NH4Cl、NaOH 稀盐酸、MnO2
装置 c、f c、e b、e a、d
A
解析 电石遇水会发生剧烈反应,生成氢氧化钙和乙炔气体,该反应不用加热,发生装置选c,收集装置选f,A正确;Na2SO3与浓硫酸反应制取二氧化硫,由于二氧化硫密度比空气大且会污染空气,不能选用向下排空气法,B错误;实验室常利用NH4Cl与Ca(OH)2共热反应制取氨气,试剂选择不合适,C错误;实验室制取氯气应该选择浓盐酸与二氧化锰共热反应,而不是稀盐酸,D错误。
6.(2023·河南省名校联盟联考)以镀镍行业产生的含铁、铜、锌等杂质的酸性硫酸镍废液为原料获得NiSO4·6H2O,已知:Ksp[Ni(OH)2]=2.0×10-15、Ksp[Cu(OH)2]=4.8×10-20,Ksp[Zn(OH)2]=2.09×10-20,其工艺流程如下。下列说法错误的是( )
A.用KSCN溶液可以检验滤液中Fe3+是否除干净
B.萃取的目的是除去Cu2+和Zn2+,反萃取获得的有机化合物可循环使用
C.萃取振荡时分液漏斗的下口应倾斜向上
D.操作Ⅱ的名称为蒸发结晶、过滤、洗涤干燥
D
解析 含镍酸性废水加入过氧化氢可把Fe2+氧化为Fe3+、加石灰石调pH生成氢氧化铁沉淀,过滤除铁,滤液中加萃取剂除去Cu2+和Zn2+,分液后,水相为硫酸镍溶液,蒸发浓缩、冷却结晶、过滤、洗涤、干燥得NiSO4·6H2O。Fe3+遇KSCN溶液变红,用KSCN溶液可以检验滤液中Fe3+是否除干净,A正确;含镍酸性废水加入过氧化氢、石灰石调pH的目的是除铁,萃取的目的是除去Cu2+和Zn2+,反萃取获得的有机化合物可在萃取时循环使用,B正确;萃取振荡时要通过下口放气,分液漏斗的下口应倾斜向上,C正确;为防止NiSO4·6H2O失去结晶水,操作Ⅱ的名称为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,D错误。
专题2 物质的制备、检验、分离及提纯
考题统计
物质的制备、分离、检验、及提纯:
辽宁卷(2023),广东卷(2022),山东卷(2023、2022、2021),海南卷(2021),北京卷(2021),湖南卷(2021),江苏卷(2021),湖北卷(2021)
要点1常见气体的制备、净化、收集及尾气处理
课标指引:1.研究物质性质,探究反应规律,进行物质的制备等不同类型的化学实验。 2.体会实验条件控制对完成科学实验及探究活动的作用。
聚焦核心要点
1.依据反应物的状态和反应条件选择发生装置
2.依据气体及所含杂质的性质选择除杂装置
(1)判断气体中的杂质时,要考虑反应介质、反应物的性质(如挥发性)、生成物的成分、是否发生副反应等;
(2)选择干燥剂时,要从酸碱性角度考虑,还要考虑干燥剂的特殊性质,如浓硫酸具有强氧化性,不能干燥还原性气体(如H2S等),无水氯化钙不能干燥NH3等。
3.依据气体的密度、水溶性选择收集装置
微点拨
根据气体与空气的相对分子质量(29)判断气体的相对密度:若气体的相对分子质量大于29,则其密度大于空气,反之,则密度小于空气。
4.依据气体的性质选择尾气处理装置
要点2物质的检验、分离及提纯
课标指引:1.初步学会物质检验、分离、提纯等化学实验基础知识和基本技能。 2.学习进行物质分离、检验和制备等不同类型化学实验及探究活动的核心思路与基本方法。
1.根据物质的状态和性质选择分离与提纯方法
(1)“固+固”混合物的分离与提纯
(2)“固+液”混合物的分离与提纯
(3)“液+液”混合物的分离与提纯
(4)“气+气”混合物的分离与提纯
2.基于常见气体的性质掌握其检验方法
常见气体 常用检验方法(或思路)
O2 使带火星的木条复燃
CO 将气体通过灼热的CuO,CuO由黑色变成红色,且气体产物可使澄清石灰水变浑浊
CO2 使澄清石灰水变浑浊,继续通入又可变澄清
SO2 使品红溶液褪色,加热后又恢复红色
Cl2 使湿润的淀粉KI试纸变蓝
NH3 使湿润的红色石蕊试纸变蓝;靠近浓盐酸(或浓硝酸)时冒白烟
CH2=CH2 能使酸性高锰酸钾溶液、溴水、溴的四氯化碳溶液褪色
3.基于官能团掌握常见有机化合物的检验方法
有机化合物 常用检验方法(或思路)
卤代烃 加入NaOH溶液并加热使卤代烃水解,再加稀硝酸中和至弱酸性,滴加AgNO3溶液
醛、葡萄糖 与银氨溶液(水浴加热)反应形成银镜;
与新制的Cu(OH)2(加热)反应生成红色沉淀(Cu2O)
羧酸 加入NaHCO3溶液产生无色无味气体
检验有机化合物中羧基的特征反应
淀粉 淀粉溶液遇碘显蓝色
常用淀粉溶液作碘滴定实验的指示剂
蛋白质 灼烧,有烧焦羽毛的气味;加浓硝酸并微热,颜色变黄(含苯环结构的蛋白质用此法)
易错辨析
1.根据食用油和汽油的密度不同,可选用分液的方法分离。( )
2.分离淀粉胶体中的NaCl溶液,可选用过滤的方法。( )
3.向MgCl2溶液中加入CaCO3粉末,充分搅拌后过滤可除去杂质FeCl3。( )
4.除去硝酸中的NO2:可向硝酸中加入少量水并通入空气。( )
×
二者互溶,应选用蒸馏法分离。
×
胶体粒子和Na+、Cl-均能透过滤纸,应改为渗析法。
×
引入新杂质,应加入MgO等。
√
4NO2+O2+2H2O ══ 4HNO3。
精研核心命题
命题点1常见气体的制备、净化、收集及尾气处理
典例1 (2023·广东卷)1827年,英国科学家法拉第进行了NH3喷泉实验。在此启发下,兴趣小组利用以下装置,进行如下实验。其中,难以达到预期目的的是( )
A.喷泉实验 B.干燥NH3
C.收集NH3 D.制备NH3
B
解析 NH3极易溶于水,挤出胶头滴管中的水,打开止水夹,NH3溶于水形成压强差,引发喷泉实验,A正确;P2O5是酸性干燥剂,不能干燥碱性气体NH3,B错误;NH3的密度小于空气的密度,采用向下排空气法收集NH3,将其从短管通入,将空气从长管排出,C正确;浓氨水加入CaO中发生反应生成Ca(OH)2,同时放出NH3,可制备少量NH3,D正确。
变式演练(2021·北京卷)实验室制备下列气体所选试剂、制备装置及收集方法均正确的是( )
选项 气体 试剂 制备装置 收集方法
A O2 KMnO4 a d
B H2 Zn+稀硫酸 b e
C NO Cu+稀硝酸 b c
D CO2 CaCO3+稀硫酸 b c
B
解析 KMnO4是固体物质,加热分解产生O2,由于O2难溶于水,因此可以使用排水法或向上排空气法收集,故不可以使用a、d装置制取和收集O2,A错误;Zn与稀硫酸发生置换反应产生H2,块状固体与液体反应制取气体,产生的H2难溶于水,可以使用排水法收集,故可以使用装置b、e制取H2,B正确;Cu与稀硝酸反应产生NO气体,NO能够与O2发生反应产生NO2气体,不能使用排空气的方法收集,C错误;CaCO3与稀硫酸反应产生CaSO4、CO2气体,CaSO4微溶于水,使制取CO2气体不能持续发生,不能使用该方法制取CO2气体,D错误。
命题点2物质的分离及提纯
典例2 (2022·北京卷)下列实验中,不能达到实验目的的是( )
答案 D
解析 采用“蒸馏法”除去海水中的盐分制取蒸馏水,装置及操作均合理,A正确;碘在CCl4中溶解度大于在水中溶解度,且CCl4和水互不相溶,故可用CCl4萃取碘水中的碘,B正确;采用“过滤法”分离粗盐中的不溶物,实验装置及操作均合理,C正确;FeCl3易发生水解,要在HCl氛围中加热FeCl3·6H2O晶体获得FeCl3固体,D错误。
变式演练(2023·广东茂名一模)实验室制备纯化乙酸乙酯,下列操作正确的是( )
A.①混合乙醇和浓硫酸
B.②收集乙酸乙酯
C.③分离乙酸乙酯和饱和碳酸钠溶液
D.④提纯乙酸乙酯
C
解析 ①操作错误,混合乙醇和浓硫酸时是将浓硫酸缓缓加入乙醇中,A错误;②操作错误,收集乙酸乙酯时导管不能伸入溶液液面以下,B错误;③操作正确,分离乙酸乙酯和饱和碳酸钠溶液,先将下层液体放出,再从上口倒出乙酸乙酯,C正确;④操作错误,提纯乙酸乙酯时温度计水银部位在支管口处,D错误。
【思维建模】
解答物质的分离及提纯类题目的思维模型
命题点3物质的鉴别与检验
典例3 (2023·辽宁卷)下列鉴别或检验不能达到实验目的的是( )
A.用石灰水鉴别Na2CO3与NaHCO3
B.用KSCN溶液检验FeSO4是否变质
C.用盐酸酸化的BaCl2溶液检验Na2SO3是否被氧化
D.加热条件下用银氨溶液检验乙醇中是否混有乙醛
A
解析 Na2CO3和NaHCO3与石灰水反应都能生成难溶的CaCO3沉淀,A项符合题意;KSCN与Fe3+能生成红色物质,可用于检验FeSO4是否变质,B项不符合题意;Na2SO3被氧化为Na2SO4,Na2SO4与BaCl2反应生成的BaSO4不溶于盐酸,C项不符合题意;乙醛能与银氨溶液发生银镜反应,而乙醇不能,D项不符合题意。
变式演练(2023·天津卷)下列方法(试剂)中,无法鉴别Na2CO3和BaCl2两种物质的是( )
A.焰色试验 B.pH试纸
C.稀氨水 D.Na2SO4
C
解析 进行焰色试验时,Na2CO3呈现黄色火焰,BaCl2呈现绿色火焰,可以鉴别,A正确;Na2CO3溶液呈碱性,BaCl2溶液呈中性,可用pH试纸进行鉴别,B正确;Na2CO3溶液、BaCl2溶液与稀氨水均不发生反应,无法鉴别,C错误;BaCl2溶液与Na2SO4溶液反应生成白色沉淀BaSO4,Na2CO3则不能,可以鉴别,D正确。
训练分层落实
练真题·明考向
1.(2023·山东卷)鉴别浓度均为0.1 mol·L-1的NaClO、Ba(OH)2、Al2(SO4)3三种溶液,仅用下列一种方法不可行的是( )
A.测定溶液pH
B.滴加酚酞试剂
C.滴加0.1 mol·L-1 KI溶液
D.滴加饱和Na2CO3溶液
C
解析 ClO-水解使NaClO溶液显碱性,Ba(OH)2属于强碱,Al3+水解使Al2(SO4)3溶液显酸性,因此可以通过测定溶液pH的方法鉴别这三种浓度相等的溶液,A正确。三种溶液中滴加酚酞试剂的现象分别为NaClO溶液先变红后褪色,Ba(OH)2溶液变红,Al2(SO4)3溶液无明显现象,B正确。KI溶液与Ba(OH)2、Al2(SO4)3都不反应,二者无法鉴别,C错误。三种溶液中滴加饱和Na2CO3溶液的现象分别为NaClO溶液无明显现象,Ba(OH)2溶液中产生白色沉淀,Al2(SO4)3溶液中既有白色沉淀又有气体产生,D正确。
2.(2023·浙江6月选考卷)苯甲酸是一种常用的食品防腐剂。某实验小组设计粗苯甲酸(含有少量NaCl和泥沙)的提纯方案如下:
下列说法不正确的是( )
A.操作Ⅰ中依据苯甲酸的溶解度估算加水量
B.操作Ⅱ趁热过滤的目的是除去泥沙和NaCl
C.操作Ⅲ缓慢冷却结晶可减少杂质被包裹
D.操作Ⅳ可用冷水洗涤晶体
B
解析 操作Ⅰ中,为减少能耗、减少苯甲酸的溶解损失,溶解所用水的量需加以控制,可依据苯甲酸的大致含量、溶解度等估算加水量,A正确;操作Ⅱ趁热过滤的目的,是除去泥沙,同时防止苯甲酸结晶析出,NaCl含量少,通常不结晶析出,B错误;操作Ⅲ缓慢冷却结晶,可形成较大的苯甲酸晶体颗粒,同时可减少杂质被包裹在晶体颗粒内部,C正确;苯甲酸微溶于冷水,易溶于热水,所以操作Ⅳ可用冷水洗涤晶体,既可去除晶体表面吸附的杂质离子,又能减少溶解损失,D正确。
3.(2022·山东卷)已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲苯、苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是( )
A.苯胺既可与盐酸也可与NaOH溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
C
解析 本题考查有机化合物的性质,实验室分离、提纯有机化合物的方法。
由题给流程可知,向甲苯、苯胺、苯甲酸的混合溶液中加入盐酸,盐酸将微溶于水的苯胺转化为易溶于水的苯胺盐酸盐,分液得到水相Ⅰ和有机相Ⅰ;向水相Ⅰ中加入氢氧化钠溶液将苯胺盐酸盐转化为苯胺,分液得到苯胺粗品①;向有机相Ⅰ中加入水洗涤除去混有的盐酸,分液得到废液和有机相Ⅱ,向有机相Ⅱ中加入碳酸钠溶液将微溶于水的苯甲酸转化为易溶于水的苯甲酸钠,分液得到甲苯粗品②和水相Ⅱ;向水相Ⅱ中加入盐酸,将苯甲酸钠转化为苯甲酸,经蒸发结晶、过滤、洗涤得到苯甲酸粗品③。苯胺分子中含有的氨基能与盐酸反应,不能与NaOH溶液反应,A项错误;由分析可知,得到苯胺粗品①的分离方法为分液,得到苯甲酸粗品③的分离方法为蒸发结晶、过滤、洗涤,获取两者粗品的操作方法不同,B项错误;苯胺粗品、甲苯粗品、苯甲酸粗品依次由①、②、③获得,C项正确;①、②为有机相,③为固相,都不是两相混合体系,D项错误。
练易错·避陷阱
4.(2023·河南郑州一模)下列实验中,所采取的实验方法与对应原理都正确的是( )
选项 实验目的 实验方法 实验原理
A 分离乙酸乙酯和乙醇 用分液漏斗分液 乙酸乙酯和乙醇的密度不同
B 除去CO2中少量的SO2 用饱和 NaHCO3溶液洗气 SO2能与
NaHCO3反应生成CO2
C 检验溶液中的 滴加稀盐酸,产生无色无味且能使澄清石灰水变浑浊的气体 +2H+══H2O+CO2↑
D 得到纯净的Cl2 将混有HCl的Cl2通过饱和食盐水 HCl极易溶于水
B
解析 乙酸乙酯和乙醇互溶,不能采取分液的方法分离,A错误;SO2能与NaHCO3反应生成CO2,故用饱和NaHCO3溶液可除去CO2中少量的SO2,B正确;加入足量稀盐酸,将生成的无色无味气体通入澄清石灰水,若澄清石灰水变浑浊,不能说明溶液中一定含有 ,也有可能含有 ,C错误;将Cl2与HCl的混合气体通过饱和食盐水,可以除去HCl,但是Cl2中还会混有水,得不到纯净的Cl2,D错误。
练预测·押考向
5.(2023·北京丰台区一模)实验室中,下列气体制备的试剂和装置正确的是
( )
选项 A B C D
气体 C2H2 SO2 NH3 Cl2
试剂 电石、饱和食盐水 Na2SO3、浓硫酸 NH4Cl、NaOH 稀盐酸、MnO2
装置 c、f c、e b、e a、d
A
解析 电石遇水会发生剧烈反应,生成氢氧化钙和乙炔气体,该反应不用加热,发生装置选c,收集装置选f,A正确;Na2SO3与浓硫酸反应制取二氧化硫,由于二氧化硫密度比空气大且会污染空气,不能选用向下排空气法,B错误;实验室常利用NH4Cl与Ca(OH)2共热反应制取氨气,试剂选择不合适,C错误;实验室制取氯气应该选择浓盐酸与二氧化锰共热反应,而不是稀盐酸,D错误。
6.(2023·河南省名校联盟联考)以镀镍行业产生的含铁、铜、锌等杂质的酸性硫酸镍废液为原料获得NiSO4·6H2O,已知:Ksp[Ni(OH)2]=2.0×10-15、Ksp[Cu(OH)2]=4.8×10-20,Ksp[Zn(OH)2]=2.09×10-20,其工艺流程如下。下列说法错误的是( )
A.用KSCN溶液可以检验滤液中Fe3+是否除干净
B.萃取的目的是除去Cu2+和Zn2+,反萃取获得的有机化合物可循环使用
C.萃取振荡时分液漏斗的下口应倾斜向上
D.操作Ⅱ的名称为蒸发结晶、过滤、洗涤干燥
D
解析 含镍酸性废水加入过氧化氢可把Fe2+氧化为Fe3+、加石灰石调pH生成氢氧化铁沉淀,过滤除铁,滤液中加萃取剂除去Cu2+和Zn2+,分液后,水相为硫酸镍溶液,蒸发浓缩、冷却结晶、过滤、洗涤、干燥得NiSO4·6H2O。Fe3+遇KSCN溶液变红,用KSCN溶液可以检验滤液中Fe3+是否除干净,A正确;含镍酸性废水加入过氧化氢、石灰石调pH的目的是除铁,萃取的目的是除去Cu2+和Zn2+,反萃取获得的有机化合物可在萃取时循环使用,B正确;萃取振荡时要通过下口放气,分液漏斗的下口应倾斜向上,C正确;为防止NiSO4·6H2O失去结晶水,操作Ⅱ的名称为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,D错误。
同课章节目录
