专题10 化学实验基础与综合探究——专题突破练 专题突破练(共24张PPT)
文档属性
| 名称 | 专题10 化学实验基础与综合探究——专题突破练 专题突破练(共24张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-25 11:27:22 | ||
图片预览








文档简介
(共24张PPT)
专题 化学实验基础与综合探究----专题突破练
能力提升
能力提升练
1.(2023·辽宁大连一模)下列实验设计和操作合理的是( )
A.用浓磷酸与碘化钠固体共热制备HI气体
B.用饱和碳酸钠溶液除去CO2中混有的少量HCl气体
C.用乙醛作萃取剂萃取溴水中的溴
D.用NaOH标准液滴定未知浓度的醋酸溶液,可以选择甲基橙为指示剂
A
解析 用浓磷酸与碘化钠固体共热时发生反应:3NaI+H3PO4 ══ Na3PO4+3HI(气体),可以制备HI气体,A正确;CO2能和饱和碳酸钠溶液反应,应选用饱和NaHCO3溶液除去CO2中混有的少量HCl气体,B错误;乙醛溶于水,且会和溴水反应,不能作萃取剂萃取溴水中的溴,C错误;醋酸为弱酸,滴定终点呈碱性,应用酚酞为指示剂,D错误。
2.(2023·广东江门一模)化学是一门以实验为基础的学科。下列实验操作或做法不能达到目的的是( )
选项 操作或做法 实验目的
A 将装有NO2的注射器的活塞往外拉 探究压强对平衡移动的影响
B 常温下将铁丝插入浓硫酸中 制备SO2
C 向溶有液溴的溴苯中加入足量NaOH溶液,振荡,静置后分液 提纯溴苯
D 实验结束,将剩余白磷固体放回原试剂瓶 防止白磷自燃
B
解析 铁和浓硫酸常温发生钝化形成致密的氧化膜而无法再进行反应,不能制备SO2,B错误。
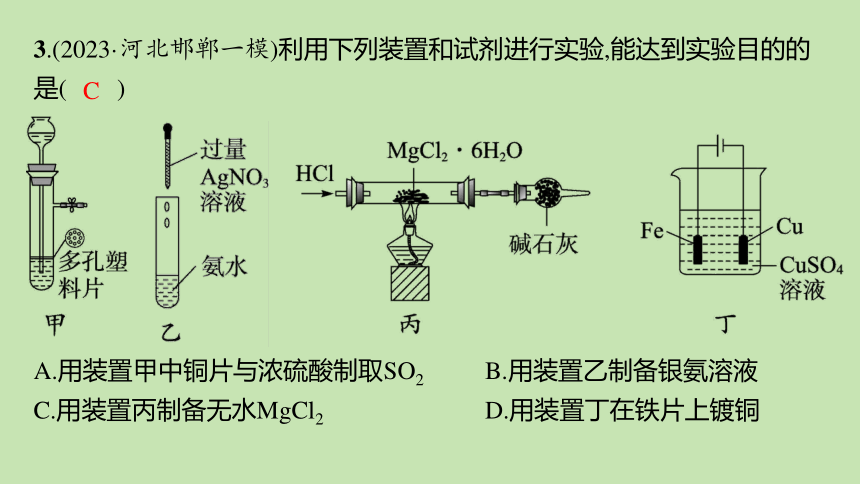
3.(2023·河北邯郸一模)利用下列装置和试剂进行实验,能达到实验目的的是( )
A.用装置甲中铜片与浓硫酸制取SO2 B.用装置乙制备银氨溶液
C.用装置丙制备无水MgCl2 D.用装置丁在铁片上镀铜
C
解析 铜和浓硫酸在常温下不发生反应,缺少酒精灯加热,A错误;应该向硝酸银溶液滴加氨水配制银氨溶液,试剂加入顺序颠倒,B错误;HCl可以抑制氯化镁的水解,氯化氢氛围中加热氯化镁晶体制取无水氯化镁,C正确;在铁上镀铜,镀层金属铜作阳极,镀件铁作阴极,故铁作阴极连接电源负极,D错误。
4.(2023·广东惠州一模)水合肼(N2H4·H2O)为无色透明的油状发烟液体,是一种重要的精细化工原料,其制备的反应原理为NaClO+2NH3 ══ N2H4·H2O+NaCl。下列关于实验室制备水合肼的操作不正确的是( )
A.装置甲中试剂X可以选择生石灰 B.装置乙作为反应过程的安全瓶
C.装置丙制备水合肼时氨气从b口进入 D.装置丁可用于吸收多余的尾气
C
解析 装置甲用于制备氨气,试剂X可以是生石灰,利用CaO与水反应放热使氨气从溶液中逸出,A正确;氨气极易溶于水,为防止倒吸,用装置乙作为安全瓶,B正确;为有利于氨气与NaClO溶液反应,制备水合肼时氨气应从装置丙a口进入,C错误;氨气会污染环境,实验时用装置丁进行尾气处理并防倒吸,D正确。
5.(2023·湖南邵阳一模)下列设计的实验方案能达到相应实验目的的是( )
选项 实验目的 实验方案
A 证明SO2有漂白性 将SO2通入酸性高锰酸钾溶液中,溶液褪色
B 证明碳和浓硫酸共热产生的气体中含有CO2 将产生的气体直接通入澄清石灰水中,有白色沉淀生成
C 测定0.1 mol·L-1氨水的pH 用洁净的玻璃棒蘸取氨水点在湿润的pH试纸上,与标准比色卡对照读取pH
D 证明“84”消毒液的氧化能力随溶液pH的减小而增强 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入醋酸,红色很快褪为无色
D
解析 二氧化硫具有还原性,与酸性高锰酸钾溶液发生氧化还原反应使溶液褪色,A错误;二氧化硫也能与澄清石灰水反应生成亚硫酸钙使溶液变浑浊,有白色沉淀生成,不能说明碳和浓硫酸共热产生的气体中含有二氧化碳,B错误;用洁净的玻璃棒蘸取氨水点在湿润的pH试纸上,与标准比色卡对照读取pH测得的是稀释后0.1 mol·L-1氨水的pH,C错误;将“84”消毒液滴入品红溶液中,褪色缓慢,若同时加入醋酸,红色很快褪为无色说明“84”消毒液的氧化能力随溶液pH的减小而增强,D正确。
操作步骤如下:
ⅰ.向三颈烧瓶内加入环己醇、
冰醋酸,逐滴加入NaClO溶液,
30 ℃条件下反应30分钟后冷却。
ⅱ.向三颈烧瓶内加入适量饱和NaHSO3溶液,用NaOH调节溶液显中性后加入饱和氯化钠溶液,然后经分液、干燥、蒸馏得到环己酮。
下列叙述错误的是( )
A.冰醋酸既作为溶剂,同时可增强NaClO溶液的氧化性
B.若NaClO溶液滴加过快,三颈烧瓶中会产生少量黄绿色气体
C.饱和亚硫酸氢钠的主要作用是除去CH3COOH
D.饱和氯化钠可促进有机相和无机相分层
答案 C
解析 冰醋酸为有机溶剂,同时可增强NaClO溶液的氧化性,次氯酸根离子在酸性条件下氧化性增强,A正确;若NaClO溶液滴加过快,酸性条件下与氯化钠溶液反应产生氯气,故三颈烧瓶中会产生少量黄绿色气体,B正确;饱和亚硫酸氢钠的主要作用是除去未反应的NaClO,C错误;饱和氯化钠可促进有机相和无机相分层,D正确。
7.(2023·广东汕头一模)化学实验源于生活。下列实验方案设计、现象与结论均正确的是( )
选项 目的 方案设计 现象与结论
A 检验食盐中是否含碘元素 向某食盐溶液中滴加淀粉溶液 溶液颜色不变,说明该食盐属于无碘盐
B 检验火柴头中是否含有氯元素 将几根未燃过的火柴头浸入水中,稍后取少量溶液于试管中,加入稀硝酸、AgNO3溶液 若有白色沉淀产生,说明火柴头中含有氯元素
C 检验菠菜中的铁元素 取少量菠菜叶剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硝酸后再加入KSCN溶液 若溶液变红,说明菠菜中含有铁元素
D 检验鸡皮中是否含有脂肪 取一小块鸡皮于表面皿上,将几滴浓硝酸滴到鸡皮上 一段时间后鸡皮变黄,说明鸡皮中含有脂肪
C
解析 食盐中所加碘一般为碘酸钾,碘酸钾遇淀粉不变蓝色,实验设计不合理,A错误;火柴头中的氯元素存在于氯酸钾中,氯酸钾溶于水不能直接电离出氯离子,加入硝酸酸化的硝酸银溶液,不能生成AgCl白色沉淀,B错误;加硝酸后再加KSCN溶液变红,说明溶液中存在Fe3+,从而可说明菠菜中含有铁元素,C正确;加浓硝酸鸡皮变黄,是蛋白质的性质,不能证明脂肪存在,D错误。
8.(2023·江西九江二模)碳酸亚铁(FeCO3)是生产补血剂的重要原料,制取碳酸亚铁的过程中涉及以下探究实验。
实验一:为探究某固体化合物X(仅含有三种元素)的组成和性质,设计并完成如下实验:
已知:气体甲、气体乙均为单质。
请回答下列问题:
(1)气体甲与碘化钾溶液反应的离子方程式为 。化合物X含有的元素为
(写元素符号)。化合物A的化学式为 。
2I-+Cl2 ══ I2+2Cl-
Fe、Cl、O
FeO
实验二:下图装置利用实验一所得溶液B制取FeCO3(白色固体,难溶于水):
装置丙中,先将导管移出液面通入一段时间气体,再向Na2CO3溶液(pH=11.9)通入一段时间CO2至其pH为7,滴加一定量B溶液产生白色沉淀和无色气体,过滤、洗涤、干燥,得到FeCO3固体。
请回答:
(2)试剂a是 。向Na2CO3溶液通入CO2的目的是 。丙装置中制取FeCO3的离子方程式为 。
饱和NaHCO3溶液
降低溶液中OH-浓度,防止生成Fe(OH)2
(3)不可用酸性高锰酸钾溶液检验溶液B中的金属阳离子的原因是 。
(4)100 mL 0.8 mol·L-1 B溶液完全反应,最终得到5 g FeCO3固体,则产率为
(结果保留2位小数)。
溶液B中的氯离子也能使高锰酸钾溶液褪色
53.88%
解析 溶液B中加入KSCN溶液不显红色,加入适量双氧水后再加入KSCN溶液显红色,说明溶液B中含有Fe2+,不含Fe3+,则X中含有Fe元素;气体乙可以使带火星的木条复燃,应为氧气,则X中含有O元素;气体甲可以使淀粉碘化钾溶液变蓝色,说明气体甲具有氧化性,根据所学知识,淀粉碘化钾试纸通常用来检验氯气,且若为氯气符合气体甲为单质的条件,则气体甲为氯气,则X中含有Cl元素;化合物A中含有二价铁,X中又含有O元素,A应为FeO。
(2)溶液B为FeCl2溶液,甲装置中稀盐酸与碳酸钙反应生成CO2,盐酸具有挥发性,所以试剂a为饱和NaHCO3溶液,用于除去CO2中混有的HCl气体;向Na2CO3溶液通入CO2可以降低溶液中OH-浓度,防止生成Fe(OH)2。
(3)溶液B中含有Cl-,也能使KMnO4溶液褪色,故不可用酸性KMnO4溶液检验溶液B中的金属阳离子。
9.(2023·辽宁卷)2-噻吩乙醇(Mr=128)是抗血栓药物氯吡格雷的重要中间体,其制备方法如下:
Ⅰ.制钠砂。向烧瓶中加入300 mL液体A和4.60 g金属钠,加热至钠熔化后,盖紧塞子,振荡至大量微小钠珠出现。
Ⅱ.制噻吩钠。降温至10 ℃,加入25 mL噻吩,反应至钠砂消失。
Ⅲ.制噻吩乙醇钠。降温至-10 ℃,加入
稍过量的环氧乙烷的四氢呋喃溶液,反应30 min。
Ⅳ.水解。恢复室温,加入70 mL水,搅拌30 min;加盐酸调pH至4~6,继续反应2 h,分液;用水洗涤有机相,二次分液。
Ⅴ.分离。向有机相中加入无水MgSO4,静置,过滤,对滤液进行蒸馏,蒸出四氢呋喃、噻吩和液体A后,得到产品17.92 g。
回答下列问题:
(1)步骤Ⅰ中液体A可以选择 。
a.乙醇 b.水 c.甲苯 d.液氨
(2)噻吩沸点低于吡咯( )的原因是___________________________
。
(3)步骤Ⅱ的化学方程式为 。
(4)步骤Ⅲ中反应放热,为防止温度过高引发副反应,加入环氧乙烷溶液的方法是 。
c
噻吩与吡咯均为分子晶体,噻吩
分子间仅存在范德华力,而吡咯分子间还存在氢键,沸点更高
少量多次加入
(5)步骤Ⅳ中用盐酸调节pH的目的是
。
(6)下列仪器在步骤Ⅴ中无需使用的是 (填名称);无水MgSO4的作用为 。
(7)产品的产率为 (用Na计算,精确至0.1%)。
提供酸性环境,利于水解并生成可溶性的钠盐便于后续分液
球形冷凝管与分液漏斗
干燥吸水
70.0%
解析 (1)钠能与乙醇、水、液氨发生置换反应,因此只能选择甲苯作为溶剂。
(2)通过实验中的物质对结构化学的内容进行考查,噻吩与吡咯均为分子晶体,噻吩分子间仅存在范德华力,而吡咯分子间还存在氢键,沸点更高。
(3)该反应为置换反应,其化学方程式为
(4)因反应放热,为防止温度过高引发副反应,应将环氧乙烷溶液少量多次加入。
(5)该过程为将2-噻吩乙醇钠水解为2-噻吩乙醇,提供酸性环境,利于水解并产生可溶性的NaCl,便于后续分液。
(6)向有机相中加入无水硫酸镁的目的为吸水干燥。进行过滤所需的装置为:漏斗、烧杯、玻璃棒;后续的蒸馏过程中所需的仪器有:酒精灯、蒸馏烧瓶、温度计、直形冷凝管、尾接管、锥形瓶。因此用不到的仪器为球形冷凝管和分液漏斗。
(7)按Na计算,根据反应物Na的物质的量为0.2 mol可知理论上产物的物质的量为0.2 mol,质量为25.6 g,实际得到的产物为17.92 g,因此其产率为70.0%。
专题 化学实验基础与综合探究----专题突破练
能力提升
能力提升练
1.(2023·辽宁大连一模)下列实验设计和操作合理的是( )
A.用浓磷酸与碘化钠固体共热制备HI气体
B.用饱和碳酸钠溶液除去CO2中混有的少量HCl气体
C.用乙醛作萃取剂萃取溴水中的溴
D.用NaOH标准液滴定未知浓度的醋酸溶液,可以选择甲基橙为指示剂
A
解析 用浓磷酸与碘化钠固体共热时发生反应:3NaI+H3PO4 ══ Na3PO4+3HI(气体),可以制备HI气体,A正确;CO2能和饱和碳酸钠溶液反应,应选用饱和NaHCO3溶液除去CO2中混有的少量HCl气体,B错误;乙醛溶于水,且会和溴水反应,不能作萃取剂萃取溴水中的溴,C错误;醋酸为弱酸,滴定终点呈碱性,应用酚酞为指示剂,D错误。
2.(2023·广东江门一模)化学是一门以实验为基础的学科。下列实验操作或做法不能达到目的的是( )
选项 操作或做法 实验目的
A 将装有NO2的注射器的活塞往外拉 探究压强对平衡移动的影响
B 常温下将铁丝插入浓硫酸中 制备SO2
C 向溶有液溴的溴苯中加入足量NaOH溶液,振荡,静置后分液 提纯溴苯
D 实验结束,将剩余白磷固体放回原试剂瓶 防止白磷自燃
B
解析 铁和浓硫酸常温发生钝化形成致密的氧化膜而无法再进行反应,不能制备SO2,B错误。
3.(2023·河北邯郸一模)利用下列装置和试剂进行实验,能达到实验目的的是( )
A.用装置甲中铜片与浓硫酸制取SO2 B.用装置乙制备银氨溶液
C.用装置丙制备无水MgCl2 D.用装置丁在铁片上镀铜
C
解析 铜和浓硫酸在常温下不发生反应,缺少酒精灯加热,A错误;应该向硝酸银溶液滴加氨水配制银氨溶液,试剂加入顺序颠倒,B错误;HCl可以抑制氯化镁的水解,氯化氢氛围中加热氯化镁晶体制取无水氯化镁,C正确;在铁上镀铜,镀层金属铜作阳极,镀件铁作阴极,故铁作阴极连接电源负极,D错误。
4.(2023·广东惠州一模)水合肼(N2H4·H2O)为无色透明的油状发烟液体,是一种重要的精细化工原料,其制备的反应原理为NaClO+2NH3 ══ N2H4·H2O+NaCl。下列关于实验室制备水合肼的操作不正确的是( )
A.装置甲中试剂X可以选择生石灰 B.装置乙作为反应过程的安全瓶
C.装置丙制备水合肼时氨气从b口进入 D.装置丁可用于吸收多余的尾气
C
解析 装置甲用于制备氨气,试剂X可以是生石灰,利用CaO与水反应放热使氨气从溶液中逸出,A正确;氨气极易溶于水,为防止倒吸,用装置乙作为安全瓶,B正确;为有利于氨气与NaClO溶液反应,制备水合肼时氨气应从装置丙a口进入,C错误;氨气会污染环境,实验时用装置丁进行尾气处理并防倒吸,D正确。
5.(2023·湖南邵阳一模)下列设计的实验方案能达到相应实验目的的是( )
选项 实验目的 实验方案
A 证明SO2有漂白性 将SO2通入酸性高锰酸钾溶液中,溶液褪色
B 证明碳和浓硫酸共热产生的气体中含有CO2 将产生的气体直接通入澄清石灰水中,有白色沉淀生成
C 测定0.1 mol·L-1氨水的pH 用洁净的玻璃棒蘸取氨水点在湿润的pH试纸上,与标准比色卡对照读取pH
D 证明“84”消毒液的氧化能力随溶液pH的减小而增强 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入醋酸,红色很快褪为无色
D
解析 二氧化硫具有还原性,与酸性高锰酸钾溶液发生氧化还原反应使溶液褪色,A错误;二氧化硫也能与澄清石灰水反应生成亚硫酸钙使溶液变浑浊,有白色沉淀生成,不能说明碳和浓硫酸共热产生的气体中含有二氧化碳,B错误;用洁净的玻璃棒蘸取氨水点在湿润的pH试纸上,与标准比色卡对照读取pH测得的是稀释后0.1 mol·L-1氨水的pH,C错误;将“84”消毒液滴入品红溶液中,褪色缓慢,若同时加入醋酸,红色很快褪为无色说明“84”消毒液的氧化能力随溶液pH的减小而增强,D正确。
操作步骤如下:
ⅰ.向三颈烧瓶内加入环己醇、
冰醋酸,逐滴加入NaClO溶液,
30 ℃条件下反应30分钟后冷却。
ⅱ.向三颈烧瓶内加入适量饱和NaHSO3溶液,用NaOH调节溶液显中性后加入饱和氯化钠溶液,然后经分液、干燥、蒸馏得到环己酮。
下列叙述错误的是( )
A.冰醋酸既作为溶剂,同时可增强NaClO溶液的氧化性
B.若NaClO溶液滴加过快,三颈烧瓶中会产生少量黄绿色气体
C.饱和亚硫酸氢钠的主要作用是除去CH3COOH
D.饱和氯化钠可促进有机相和无机相分层
答案 C
解析 冰醋酸为有机溶剂,同时可增强NaClO溶液的氧化性,次氯酸根离子在酸性条件下氧化性增强,A正确;若NaClO溶液滴加过快,酸性条件下与氯化钠溶液反应产生氯气,故三颈烧瓶中会产生少量黄绿色气体,B正确;饱和亚硫酸氢钠的主要作用是除去未反应的NaClO,C错误;饱和氯化钠可促进有机相和无机相分层,D正确。
7.(2023·广东汕头一模)化学实验源于生活。下列实验方案设计、现象与结论均正确的是( )
选项 目的 方案设计 现象与结论
A 检验食盐中是否含碘元素 向某食盐溶液中滴加淀粉溶液 溶液颜色不变,说明该食盐属于无碘盐
B 检验火柴头中是否含有氯元素 将几根未燃过的火柴头浸入水中,稍后取少量溶液于试管中,加入稀硝酸、AgNO3溶液 若有白色沉淀产生,说明火柴头中含有氯元素
C 检验菠菜中的铁元素 取少量菠菜叶剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硝酸后再加入KSCN溶液 若溶液变红,说明菠菜中含有铁元素
D 检验鸡皮中是否含有脂肪 取一小块鸡皮于表面皿上,将几滴浓硝酸滴到鸡皮上 一段时间后鸡皮变黄,说明鸡皮中含有脂肪
C
解析 食盐中所加碘一般为碘酸钾,碘酸钾遇淀粉不变蓝色,实验设计不合理,A错误;火柴头中的氯元素存在于氯酸钾中,氯酸钾溶于水不能直接电离出氯离子,加入硝酸酸化的硝酸银溶液,不能生成AgCl白色沉淀,B错误;加硝酸后再加KSCN溶液变红,说明溶液中存在Fe3+,从而可说明菠菜中含有铁元素,C正确;加浓硝酸鸡皮变黄,是蛋白质的性质,不能证明脂肪存在,D错误。
8.(2023·江西九江二模)碳酸亚铁(FeCO3)是生产补血剂的重要原料,制取碳酸亚铁的过程中涉及以下探究实验。
实验一:为探究某固体化合物X(仅含有三种元素)的组成和性质,设计并完成如下实验:
已知:气体甲、气体乙均为单质。
请回答下列问题:
(1)气体甲与碘化钾溶液反应的离子方程式为 。化合物X含有的元素为
(写元素符号)。化合物A的化学式为 。
2I-+Cl2 ══ I2+2Cl-
Fe、Cl、O
FeO
实验二:下图装置利用实验一所得溶液B制取FeCO3(白色固体,难溶于水):
装置丙中,先将导管移出液面通入一段时间气体,再向Na2CO3溶液(pH=11.9)通入一段时间CO2至其pH为7,滴加一定量B溶液产生白色沉淀和无色气体,过滤、洗涤、干燥,得到FeCO3固体。
请回答:
(2)试剂a是 。向Na2CO3溶液通入CO2的目的是 。丙装置中制取FeCO3的离子方程式为 。
饱和NaHCO3溶液
降低溶液中OH-浓度,防止生成Fe(OH)2
(3)不可用酸性高锰酸钾溶液检验溶液B中的金属阳离子的原因是 。
(4)100 mL 0.8 mol·L-1 B溶液完全反应,最终得到5 g FeCO3固体,则产率为
(结果保留2位小数)。
溶液B中的氯离子也能使高锰酸钾溶液褪色
53.88%
解析 溶液B中加入KSCN溶液不显红色,加入适量双氧水后再加入KSCN溶液显红色,说明溶液B中含有Fe2+,不含Fe3+,则X中含有Fe元素;气体乙可以使带火星的木条复燃,应为氧气,则X中含有O元素;气体甲可以使淀粉碘化钾溶液变蓝色,说明气体甲具有氧化性,根据所学知识,淀粉碘化钾试纸通常用来检验氯气,且若为氯气符合气体甲为单质的条件,则气体甲为氯气,则X中含有Cl元素;化合物A中含有二价铁,X中又含有O元素,A应为FeO。
(2)溶液B为FeCl2溶液,甲装置中稀盐酸与碳酸钙反应生成CO2,盐酸具有挥发性,所以试剂a为饱和NaHCO3溶液,用于除去CO2中混有的HCl气体;向Na2CO3溶液通入CO2可以降低溶液中OH-浓度,防止生成Fe(OH)2。
(3)溶液B中含有Cl-,也能使KMnO4溶液褪色,故不可用酸性KMnO4溶液检验溶液B中的金属阳离子。
9.(2023·辽宁卷)2-噻吩乙醇(Mr=128)是抗血栓药物氯吡格雷的重要中间体,其制备方法如下:
Ⅰ.制钠砂。向烧瓶中加入300 mL液体A和4.60 g金属钠,加热至钠熔化后,盖紧塞子,振荡至大量微小钠珠出现。
Ⅱ.制噻吩钠。降温至10 ℃,加入25 mL噻吩,反应至钠砂消失。
Ⅲ.制噻吩乙醇钠。降温至-10 ℃,加入
稍过量的环氧乙烷的四氢呋喃溶液,反应30 min。
Ⅳ.水解。恢复室温,加入70 mL水,搅拌30 min;加盐酸调pH至4~6,继续反应2 h,分液;用水洗涤有机相,二次分液。
Ⅴ.分离。向有机相中加入无水MgSO4,静置,过滤,对滤液进行蒸馏,蒸出四氢呋喃、噻吩和液体A后,得到产品17.92 g。
回答下列问题:
(1)步骤Ⅰ中液体A可以选择 。
a.乙醇 b.水 c.甲苯 d.液氨
(2)噻吩沸点低于吡咯( )的原因是___________________________
。
(3)步骤Ⅱ的化学方程式为 。
(4)步骤Ⅲ中反应放热,为防止温度过高引发副反应,加入环氧乙烷溶液的方法是 。
c
噻吩与吡咯均为分子晶体,噻吩
分子间仅存在范德华力,而吡咯分子间还存在氢键,沸点更高
少量多次加入
(5)步骤Ⅳ中用盐酸调节pH的目的是
。
(6)下列仪器在步骤Ⅴ中无需使用的是 (填名称);无水MgSO4的作用为 。
(7)产品的产率为 (用Na计算,精确至0.1%)。
提供酸性环境,利于水解并生成可溶性的钠盐便于后续分液
球形冷凝管与分液漏斗
干燥吸水
70.0%
解析 (1)钠能与乙醇、水、液氨发生置换反应,因此只能选择甲苯作为溶剂。
(2)通过实验中的物质对结构化学的内容进行考查,噻吩与吡咯均为分子晶体,噻吩分子间仅存在范德华力,而吡咯分子间还存在氢键,沸点更高。
(3)该反应为置换反应,其化学方程式为
(4)因反应放热,为防止温度过高引发副反应,应将环氧乙烷溶液少量多次加入。
(5)该过程为将2-噻吩乙醇钠水解为2-噻吩乙醇,提供酸性环境,利于水解并产生可溶性的NaCl,便于后续分液。
(6)向有机相中加入无水硫酸镁的目的为吸水干燥。进行过滤所需的装置为:漏斗、烧杯、玻璃棒;后续的蒸馏过程中所需的仪器有:酒精灯、蒸馏烧瓶、温度计、直形冷凝管、尾接管、锥形瓶。因此用不到的仪器为球形冷凝管和分液漏斗。
(7)按Na计算,根据反应物Na的物质的量为0.2 mol可知理论上产物的物质的量为0.2 mol,质量为25.6 g,实际得到的产物为17.92 g,因此其产率为70.0%。
同课章节目录
