专题 选择题专项练 课件(共33张PPT)
文档属性
| 名称 | 专题 选择题专项练 课件(共33张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-25 00:00:00 | ||
图片预览








文档简介
(共33张PPT)
选择题专项练(上)
1
2
3
4
5
6
7
1.(2023·广东广州二模)我国的科技发展改变着人们的生活、生产方式。下列说法正确的是( )
A.闻名世界的秦兵马俑是陶制品,由石灰石经高温烧结而成
B.“嫦娥四号”使用的SiC-Al材料属于复合材料
C.5G芯片“巴龙5 000”的主要材料是SiO2
D.港珠澳大桥采用超高分子量聚乙烯纤维吊绳,其商品名为“力纶”,是有机高分子化合物,属于纯净物
B
解析 复合材料是人们运用先进的材料制备技术将不同性质的材料组分优化组合而成的新材料,“嫦娥四号”使用的SiC-Al材料属于复合材料,B正确。
1
2
3
4
5
6
7
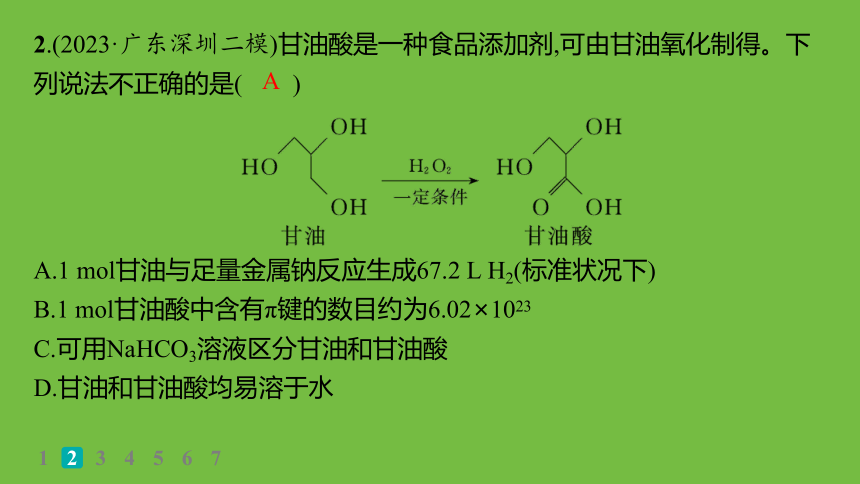
2.(2023·广东深圳二模)甘油酸是一种食品添加剂,可由甘油氧化制得。下列说法不正确的是( )
A.1 mol甘油与足量金属钠反应生成67.2 L H2(标准状况下)
B.1 mol甘油酸中含有π键的数目约为6.02×1023
C.可用NaHCO3溶液区分甘油和甘油酸
D.甘油和甘油酸均易溶于水
A
解析 1 mol甘油与足量金属钠反应生成 ×22.4 L·mol-1=33.6 L H2(标准状况下),A错误;每个甘油酸分子中含有1个π键,1 mol甘油酸中含有π键的数目约为6.02×1023,B正确;甘油酸能与NaHCO3反应产生气泡,可用NaHCO3溶液区分甘油和甘油酸,C正确;—OH和—COOH均为亲水基,甘油和甘油酸含有亲水基,易溶于水,D正确。
1
2
3
4
5
6
7
1
2
3
4
5
6
7
3.(2023·北京房山区二模)下列关于第ⅣA族元素及其化合物的性质比较中,不正确的是( )
A.原子半径:CC.热稳定性:CH4>SiH4>GeH4 D.酸性:CH3COOH>H2CO3>H2SiO3
B
解析 同主族元素从上往下原子半径依次增大,则原子半径CSi>Ge,则热稳定性CH4>SiH4>GeH4,C正确;酸性:CH3COOH>H2CO3>H2SiO3,D正确。
1
2
3
4
5
6
7
4.(2023·湖北名校联盟联考)某化学兴趣小组设计如下实验,探究电解过程中溶液pH的变化。装置、所得数据结果如图所示。电解过程中,充分搅拌使溶液均匀,忽略溶液体积的变化。下列说法错误的是( )
A.硝酸银溶液浓度为0.1 mol·L-1
B.若进行到t2时刻共有0.224 L气体(标准状况)产生,则外电路有0.01 mol电子通过
C.若使用甲烷燃料电池为电源,t1时,理论上负极消耗的气体物质的量为0.001 25 mol
D.电解到t1时刻,加入1.16 g Ag2O可使溶液复原
答案 B
1
2
3
4
5
6
7
1
2
3
4
5
6
7
1
2
3
4
5
6
7
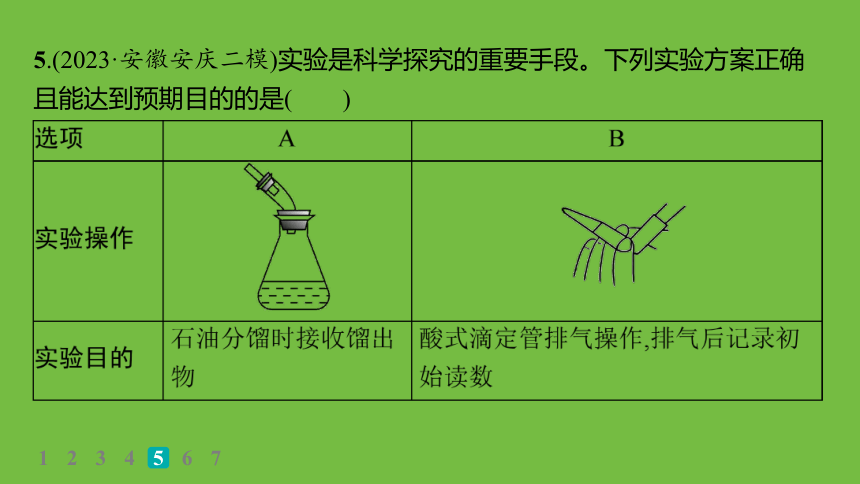
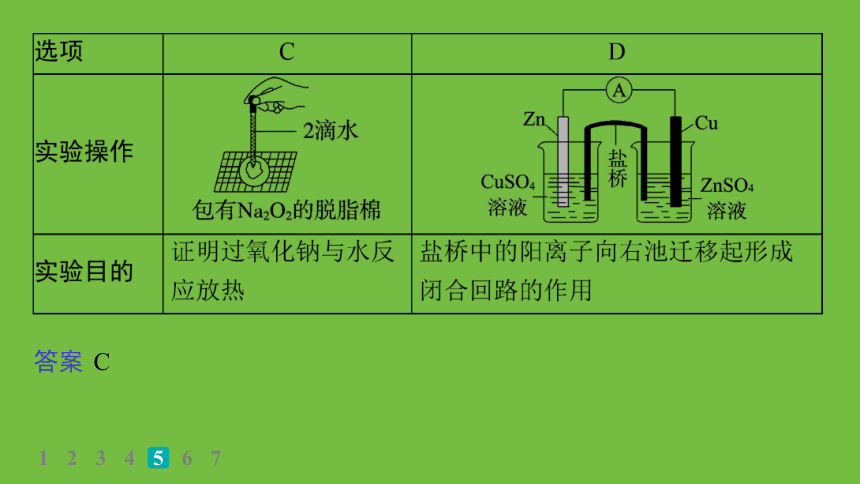
5.(2023·安徽安庆二模)实验是科学探究的重要手段。下列实验方案正确且能达到预期目的的是( )
1
2
3
4
5
6
7
答案 C
1
2
3
4
5
6
7
解析 石油分馏时,接收馏出物的锥形瓶不能塞橡胶塞,否则会因气体体积膨胀导致气体压强增大而发生意外事故,A错误;带橡胶管的滴定管不是酸式滴定管,而是碱式滴定管,B错误;过氧化钠与水反应生成氢氧化钠和氧气,脱脂棉燃烧能证明过氧化钠与水的反应为放热反应,C正确;锌与硫酸铜溶液会发生反应,故左侧烧杯中不能选用硫酸铜溶液,应选择硫酸锌溶液,D错误。
1
2
3
4
5
6
7
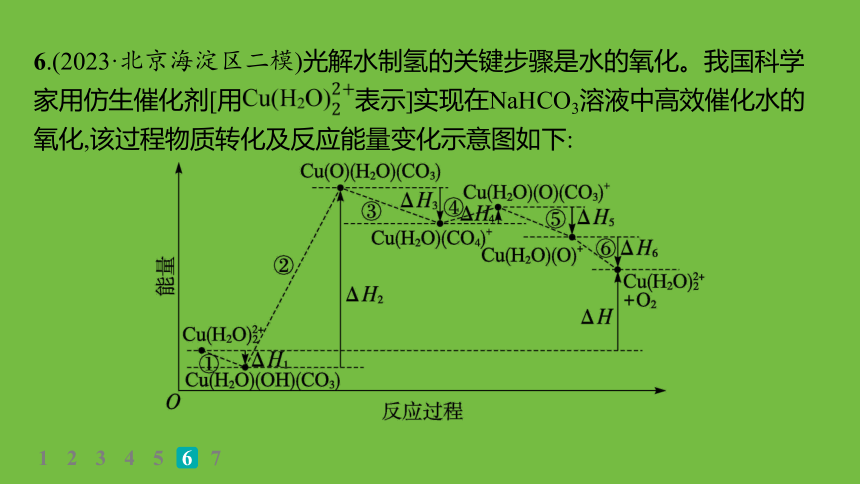
6.(2023·北京海淀区二模)光解水制氢的关键步骤是水的氧化。我国科学家用仿生催化剂[用 表示]实现在NaHCO3溶液中高效催化水的氧化,该过程物质转化及反应能量变化示意图如下:
C.ΔH=ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6
D.催化剂参与反应,降低活化能,加快反应速率
答案 A
1
2
3
4
5
6
7
下列说法不正确的是( )
1
2
3
4
5
6
7
1
2
3
4
5
6
7
7.(2023·湖北十一校联考)常温下,各种形态五价钒粒子总浓度的对数[lg c总(V)]与pH关系如图所示。已知(VO2)2SO4是易溶于水的强电解质。下列说法错误的是( )
B
1
2
3
4
5
6
7
选择题专项练(下)
1
2
3
4
5
6
7
1.(2022·河北卷)定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的是( )
A.传统陶瓷是典型的绝缘材料 B.陶瓷主要成分为SiO2和MgO
C.陶瓷烧制的过程为物理变化 D.白瓷的白色是因铁含量较高
A
解析 陶瓷的主要成分为硅酸盐,而不是SiO2和MgO,B错误;陶瓷烧制过程发生复杂的化学反应,有新物质生成,属于化学变化,C错误;由于Fe2+、Fe3+和铁的氧化物均有颜色,故陶瓷中含铁量越多,陶瓷的颜色越深,白瓷的白色是因为铁含量较低甚至几乎不含,D错误。
1
2
3
4
5
6
7
2.(2023·广西南宁二模)M是锂离子电池中一种重要的有机物,结构如图所示,下列说法正确的是( )
A.有机物M的分子式为C10H9O4
B.在一定条件下,1 mol M与足量H2反应,最多消耗4 mol H2
C.有机物M能发生加成、取代、氧化、还原反应
D.与M互为同分异构体,苯环上只有一个侧链且含有两个羧基的结构有4种(不考虑立体异构)
C
解析 由结构简式可知,M的分子式为C10H10O4,A错误;该结构中苯环可与氢气加成,1个苯环结构加成3 mol氢气,则1 mol M最多消耗3 mol氢气,B错误;M中含有苯环能发生加成反应,含醇羟基能发生取代反应,能被氧化,加氢也属于还原反应,C正确;与M互为同分异构体,苯环上只有一个侧链且含有两个羧基的结构有
1
2
3
4
5
6
7
1
2
3
4
5
6
7
3.(2023·广东潮州二模)提纯粗硅时可通过反应SiHCl3+H2 Si+3HCl获取晶体硅。下列说法正确的是( )
A.1 mol Si晶体中含有2 mol非极性键
B.基态Si原子的轨道表示式
C.SiHCl3的空间填充模型为
A
1
2
3
4
5
6
7
解析 晶体硅中,每个硅原子周围4个Si—Si,根据均摊法可知,一个硅原子平均占有2个Si—Si,故1 mol Si晶体中含有2 mol非极性键,A正确;违反了洪特规则,3p能级的两个电子自旋状态应该相同,B错误;该模型为球棍模型,C错误;HCl为共价化合物,其电子式为 ,D错误。
1
2
3
4
5
6
7
4.(2023·湖南教研联盟4月联考)硅作为地壳中第二丰富的元素,将其用于制作电池有很大的应用前景。某硅-酸电池,其电极材料分别为碳包覆硅和铜的CuSi@C以及α-MnO2,电解质溶液为酸性硫酸钠溶液,工作原理如图所示,下列说法错误的是( )
A.硅-酸电池比碱性硅-空气电池更能实现持续放电
B.放电时,当电路中转移4 mol电子时,负极区电解质溶液质量减少36 g
C.放电时,负极电极反应为Si+2H2O-4e- ══ SiO2+4H+
D.α-MnO2电极反应仅为O2+4H++4e- ══ 2H2O
D
1
2
3
4
5
6
7
解析 碱性硅-空气电池的碱性电解液会腐蚀硅电极,故硅-酸电池比碱性硅-空气电池更能实现持续放电,A正确;放电时,负极电极反应为Si+2H2O-4e- ══ SiO2+4H+,电解质溶液中H+通过离子交换膜从负极移向正极,当电路中转移4 mol电子时,负极区电解质溶液消耗2 mol H2O(生成1 mol SiO2,4 mol氢离子向右移动),故负极区质量总共减少2 mol×18 g·mol-1=36 g,B、C正确;α-MnO2电极为正极,电极反应为O2+4H++4e- ══ 2H2O和MnO2+4H++2e- ══ Mn2++2H2O,D错误。
1
2
3
4
5
6
7
5.(2023·华中师大附中二模)如下图所示的“化学多米诺实验”装置中分别盛放的物质为①稀硫酸;②锌粒;装置③、④、⑤、⑥中的试剂及反应现象见下表,其中设计合理且实验现象符合预测的是( )
选项 ③中试剂 ④中固体逐渐消失 ⑤中溶液褪色 ⑥中尾气处理
A 浓盐酸 KMnO4 石蕊溶液 NaOH溶液
B 浓硝酸 Cu FeSO4溶液 水
C 浓硫酸 木炭 品红溶液 饱和NaHSO3溶液
D 浓NaOH溶液 NH4Cl固体 少量CuSO4溶液 CCl4和水
A
1
2
3
4
5
6
7
解析 ③中浓盐酸会进入④试管中,浓盐酸与KMnO4反应会生成氯气,氯气可以使石蕊溶液褪色,用氢氧化钠溶液来吸收多余的氯气,A正确;③中浓硝酸会进入④试管中,Cu与浓硝酸反应会生成二氧化氮气体,二氧化氮与FeSO4溶液反应,会氧化二价铁离子变为三价铁离子,溶液呈现棕黄色,不会褪色,且二氧化氮不能用水吸收,会有一氧化氮的生成,故应用氢氧化钠溶液吸收尾气,B错误;③中浓硫酸会进入④试管中,木炭与浓硫酸的反应需要加热,④中试管没有加热,木炭与浓硫酸不发生反应,C错误;③中浓NaOH溶液会进入④试管中,浓NaOH溶液与NH4Cl固体混合,可以得到氨气,氨气与少量CuSO4溶液反应,开始得到蓝色氢氧化铜沉淀,随着氨气不断通入,最后沉淀会转化为铜氨络离子,铜氨络离子溶液颜色是蓝色,⑤中溶液颜色没有褪去,不符合题意,最后用CCl4和水除去多余的氨气,还可以防止倒吸现象,D错误。
1
2
3
4
5
6
7
6.(2023·湖北鄂州二模)有文献报道异辛醇在一定条件下选择性合成异辛酸可能的反应机理如图所示,下列说法错误的是( )
A.反应过程中A为催化剂
B.反应过程中钨(W)的成键数目
发生了改变
B
解析 从反应机理图中可以判断,物质A参与反应,但最后物质A的性质没有改变,故A为催化剂,A正确。反应机理图中钨(W)的成键数目均是4,未发生改变,B错误。
1
2
3
4
5
6
7
1
2
3
4
5
6
7
7.(2023·齐鲁名校第三次联考)常温下,用0.1 mol·L-1 NaOH标准溶液滴定20 mL等浓度的三元酸H3A,得到pH与V(NaOH溶液)、
图2
图1
答案 D
1
2
3
4
5
6
7
1
2
3
4
5
6
7
1
2
3
4
5
6
7
本 课 结 束
选择题专项练(上)
1
2
3
4
5
6
7
1.(2023·广东广州二模)我国的科技发展改变着人们的生活、生产方式。下列说法正确的是( )
A.闻名世界的秦兵马俑是陶制品,由石灰石经高温烧结而成
B.“嫦娥四号”使用的SiC-Al材料属于复合材料
C.5G芯片“巴龙5 000”的主要材料是SiO2
D.港珠澳大桥采用超高分子量聚乙烯纤维吊绳,其商品名为“力纶”,是有机高分子化合物,属于纯净物
B
解析 复合材料是人们运用先进的材料制备技术将不同性质的材料组分优化组合而成的新材料,“嫦娥四号”使用的SiC-Al材料属于复合材料,B正确。
1
2
3
4
5
6
7
2.(2023·广东深圳二模)甘油酸是一种食品添加剂,可由甘油氧化制得。下列说法不正确的是( )
A.1 mol甘油与足量金属钠反应生成67.2 L H2(标准状况下)
B.1 mol甘油酸中含有π键的数目约为6.02×1023
C.可用NaHCO3溶液区分甘油和甘油酸
D.甘油和甘油酸均易溶于水
A
解析 1 mol甘油与足量金属钠反应生成 ×22.4 L·mol-1=33.6 L H2(标准状况下),A错误;每个甘油酸分子中含有1个π键,1 mol甘油酸中含有π键的数目约为6.02×1023,B正确;甘油酸能与NaHCO3反应产生气泡,可用NaHCO3溶液区分甘油和甘油酸,C正确;—OH和—COOH均为亲水基,甘油和甘油酸含有亲水基,易溶于水,D正确。
1
2
3
4
5
6
7
1
2
3
4
5
6
7
3.(2023·北京房山区二模)下列关于第ⅣA族元素及其化合物的性质比较中,不正确的是( )
A.原子半径:C
B
解析 同主族元素从上往下原子半径依次增大,则原子半径C
1
2
3
4
5
6
7
4.(2023·湖北名校联盟联考)某化学兴趣小组设计如下实验,探究电解过程中溶液pH的变化。装置、所得数据结果如图所示。电解过程中,充分搅拌使溶液均匀,忽略溶液体积的变化。下列说法错误的是( )
A.硝酸银溶液浓度为0.1 mol·L-1
B.若进行到t2时刻共有0.224 L气体(标准状况)产生,则外电路有0.01 mol电子通过
C.若使用甲烷燃料电池为电源,t1时,理论上负极消耗的气体物质的量为0.001 25 mol
D.电解到t1时刻,加入1.16 g Ag2O可使溶液复原
答案 B
1
2
3
4
5
6
7
1
2
3
4
5
6
7
1
2
3
4
5
6
7
5.(2023·安徽安庆二模)实验是科学探究的重要手段。下列实验方案正确且能达到预期目的的是( )
1
2
3
4
5
6
7
答案 C
1
2
3
4
5
6
7
解析 石油分馏时,接收馏出物的锥形瓶不能塞橡胶塞,否则会因气体体积膨胀导致气体压强增大而发生意外事故,A错误;带橡胶管的滴定管不是酸式滴定管,而是碱式滴定管,B错误;过氧化钠与水反应生成氢氧化钠和氧气,脱脂棉燃烧能证明过氧化钠与水的反应为放热反应,C正确;锌与硫酸铜溶液会发生反应,故左侧烧杯中不能选用硫酸铜溶液,应选择硫酸锌溶液,D错误。
1
2
3
4
5
6
7
6.(2023·北京海淀区二模)光解水制氢的关键步骤是水的氧化。我国科学家用仿生催化剂[用 表示]实现在NaHCO3溶液中高效催化水的氧化,该过程物质转化及反应能量变化示意图如下:
C.ΔH=ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6
D.催化剂参与反应,降低活化能,加快反应速率
答案 A
1
2
3
4
5
6
7
下列说法不正确的是( )
1
2
3
4
5
6
7
1
2
3
4
5
6
7
7.(2023·湖北十一校联考)常温下,各种形态五价钒粒子总浓度的对数[lg c总(V)]与pH关系如图所示。已知(VO2)2SO4是易溶于水的强电解质。下列说法错误的是( )
B
1
2
3
4
5
6
7
选择题专项练(下)
1
2
3
4
5
6
7
1.(2022·河北卷)定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的是( )
A.传统陶瓷是典型的绝缘材料 B.陶瓷主要成分为SiO2和MgO
C.陶瓷烧制的过程为物理变化 D.白瓷的白色是因铁含量较高
A
解析 陶瓷的主要成分为硅酸盐,而不是SiO2和MgO,B错误;陶瓷烧制过程发生复杂的化学反应,有新物质生成,属于化学变化,C错误;由于Fe2+、Fe3+和铁的氧化物均有颜色,故陶瓷中含铁量越多,陶瓷的颜色越深,白瓷的白色是因为铁含量较低甚至几乎不含,D错误。
1
2
3
4
5
6
7
2.(2023·广西南宁二模)M是锂离子电池中一种重要的有机物,结构如图所示,下列说法正确的是( )
A.有机物M的分子式为C10H9O4
B.在一定条件下,1 mol M与足量H2反应,最多消耗4 mol H2
C.有机物M能发生加成、取代、氧化、还原反应
D.与M互为同分异构体,苯环上只有一个侧链且含有两个羧基的结构有4种(不考虑立体异构)
C
解析 由结构简式可知,M的分子式为C10H10O4,A错误;该结构中苯环可与氢气加成,1个苯环结构加成3 mol氢气,则1 mol M最多消耗3 mol氢气,B错误;M中含有苯环能发生加成反应,含醇羟基能发生取代反应,能被氧化,加氢也属于还原反应,C正确;与M互为同分异构体,苯环上只有一个侧链且含有两个羧基的结构有
1
2
3
4
5
6
7
1
2
3
4
5
6
7
3.(2023·广东潮州二模)提纯粗硅时可通过反应SiHCl3+H2 Si+3HCl获取晶体硅。下列说法正确的是( )
A.1 mol Si晶体中含有2 mol非极性键
B.基态Si原子的轨道表示式
C.SiHCl3的空间填充模型为
A
1
2
3
4
5
6
7
解析 晶体硅中,每个硅原子周围4个Si—Si,根据均摊法可知,一个硅原子平均占有2个Si—Si,故1 mol Si晶体中含有2 mol非极性键,A正确;违反了洪特规则,3p能级的两个电子自旋状态应该相同,B错误;该模型为球棍模型,C错误;HCl为共价化合物,其电子式为 ,D错误。
1
2
3
4
5
6
7
4.(2023·湖南教研联盟4月联考)硅作为地壳中第二丰富的元素,将其用于制作电池有很大的应用前景。某硅-酸电池,其电极材料分别为碳包覆硅和铜的CuSi@C以及α-MnO2,电解质溶液为酸性硫酸钠溶液,工作原理如图所示,下列说法错误的是( )
A.硅-酸电池比碱性硅-空气电池更能实现持续放电
B.放电时,当电路中转移4 mol电子时,负极区电解质溶液质量减少36 g
C.放电时,负极电极反应为Si+2H2O-4e- ══ SiO2+4H+
D.α-MnO2电极反应仅为O2+4H++4e- ══ 2H2O
D
1
2
3
4
5
6
7
解析 碱性硅-空气电池的碱性电解液会腐蚀硅电极,故硅-酸电池比碱性硅-空气电池更能实现持续放电,A正确;放电时,负极电极反应为Si+2H2O-4e- ══ SiO2+4H+,电解质溶液中H+通过离子交换膜从负极移向正极,当电路中转移4 mol电子时,负极区电解质溶液消耗2 mol H2O(生成1 mol SiO2,4 mol氢离子向右移动),故负极区质量总共减少2 mol×18 g·mol-1=36 g,B、C正确;α-MnO2电极为正极,电极反应为O2+4H++4e- ══ 2H2O和MnO2+4H++2e- ══ Mn2++2H2O,D错误。
1
2
3
4
5
6
7
5.(2023·华中师大附中二模)如下图所示的“化学多米诺实验”装置中分别盛放的物质为①稀硫酸;②锌粒;装置③、④、⑤、⑥中的试剂及反应现象见下表,其中设计合理且实验现象符合预测的是( )
选项 ③中试剂 ④中固体逐渐消失 ⑤中溶液褪色 ⑥中尾气处理
A 浓盐酸 KMnO4 石蕊溶液 NaOH溶液
B 浓硝酸 Cu FeSO4溶液 水
C 浓硫酸 木炭 品红溶液 饱和NaHSO3溶液
D 浓NaOH溶液 NH4Cl固体 少量CuSO4溶液 CCl4和水
A
1
2
3
4
5
6
7
解析 ③中浓盐酸会进入④试管中,浓盐酸与KMnO4反应会生成氯气,氯气可以使石蕊溶液褪色,用氢氧化钠溶液来吸收多余的氯气,A正确;③中浓硝酸会进入④试管中,Cu与浓硝酸反应会生成二氧化氮气体,二氧化氮与FeSO4溶液反应,会氧化二价铁离子变为三价铁离子,溶液呈现棕黄色,不会褪色,且二氧化氮不能用水吸收,会有一氧化氮的生成,故应用氢氧化钠溶液吸收尾气,B错误;③中浓硫酸会进入④试管中,木炭与浓硫酸的反应需要加热,④中试管没有加热,木炭与浓硫酸不发生反应,C错误;③中浓NaOH溶液会进入④试管中,浓NaOH溶液与NH4Cl固体混合,可以得到氨气,氨气与少量CuSO4溶液反应,开始得到蓝色氢氧化铜沉淀,随着氨气不断通入,最后沉淀会转化为铜氨络离子,铜氨络离子溶液颜色是蓝色,⑤中溶液颜色没有褪去,不符合题意,最后用CCl4和水除去多余的氨气,还可以防止倒吸现象,D错误。
1
2
3
4
5
6
7
6.(2023·湖北鄂州二模)有文献报道异辛醇在一定条件下选择性合成异辛酸可能的反应机理如图所示,下列说法错误的是( )
A.反应过程中A为催化剂
B.反应过程中钨(W)的成键数目
发生了改变
B
解析 从反应机理图中可以判断,物质A参与反应,但最后物质A的性质没有改变,故A为催化剂,A正确。反应机理图中钨(W)的成键数目均是4,未发生改变,B错误。
1
2
3
4
5
6
7
1
2
3
4
5
6
7
7.(2023·齐鲁名校第三次联考)常温下,用0.1 mol·L-1 NaOH标准溶液滴定20 mL等浓度的三元酸H3A,得到pH与V(NaOH溶液)、
图2
图1
答案 D
1
2
3
4
5
6
7
1
2
3
4
5
6
7
1
2
3
4
5
6
7
本 课 结 束
同课章节目录
