专题 选择题专项练 课件(共32张PPT)
文档属性
| 名称 | 专题 选择题专项练 课件(共32张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-25 00:00:00 | ||
图片预览










文档简介
(共32张PPT)
选择题专项练(上)
1
2
3
4
5
6
7
1.(2023·河北沧州二模)青矾矿石在《唐本草》中有记载:“本来绿色,新出窟未见风者,正如瑠璃……烧之赤色……”。明末学者方以智所著《物理小识》中说:“青矾厂气熏人,衣服当之易烂,栽木不茂。”有关说法正确的是( )
A.青矾矿石主要成分是CuSO4·5H2O
B.烧之赤色,是发生了分解反应生成Cu2O的缘故
C.青矾应密封保存,主要目的是防止风化
D.熏人的“厂气”是SO2、SO3
D
1
2
3
4
5
6
7
解析 青矾矿石的描述为“本来绿色,新出窟未见风者,正如瑠璃……烧之赤色……”,说明“青矾”的颜色为绿色,其主要成分应为FeSO4·7H2O,A错误;“烧之赤色”说明经煅烧后,分解成颗粒度非常细而活性又很强的Fe2O3,同时生成SO2,受热分解的化学方程式为2FeSO4·7H2O ══ Fe2O3+SO2↑+SO3↑+14H2O,B错误;青矾含Fe2+易被氧化,故需密封保存防氧化,C错误;根据上述分析可知,熏人的“厂气”是SO2、SO3,D正确。
1
2
3
4
5
6
7
2.(2023·福建莆田二模)我国科学家在寻找“点击反应”的砌块过程中,发现一种新的化合物,结构如图所示,其中X、Y、Z和W是原子序数依次增大的短周期主族元素,Y与W是同一主族元素。下列说法正确的是( )
A.元素电负性:Z>Y>W
B.简单氢化物沸点:X>Y>W
C.简单离子半径:Z>Y>X
D.X、W氧化物的水化物均为强酸
A
1
2
3
4
5
6
7
解析 X、Y、Z和W是原子序数依次增大的短周期主族元素,Y与W是同一主族元素,W能形成6个键,则Y为氧、W为硫;Z形成1个共价键,Z为氟;X可形成3个共价键,则X为氮。一般来说,同周期从左到右,元素的电负性变强;同主族由上而下,元素电负性减弱,则元素电负性:Z>Y>W,A正确;常温下水为液体、氨气为气体,则水沸点较高,氨气能形成氢键,导致沸点高于硫化氢,故简单氢化物沸点:Y>X>W,B错误;电子层数越多半径越大,电子层数相同时,核电荷数越大,半径越小,简单离子半径:X>Y>Z,C错误;亚硝酸、亚硫酸不是强酸,D错误。
1
2
3
4
5
6
7
3.(2022·重庆卷)工业上用N2和H2合成NH3,NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.消耗14 g N2生成NH3分子数为2NA
B.消耗1 mol H2,生成N—H键数为2NA
C.生成标准状况下22.4 L NH3,电子转移数为2NA
D.氧化1 mol NH3生成NO,需O2分子数为2NA
B
1
2
3
4
5
6
7
1
2
3
4
5
6
7
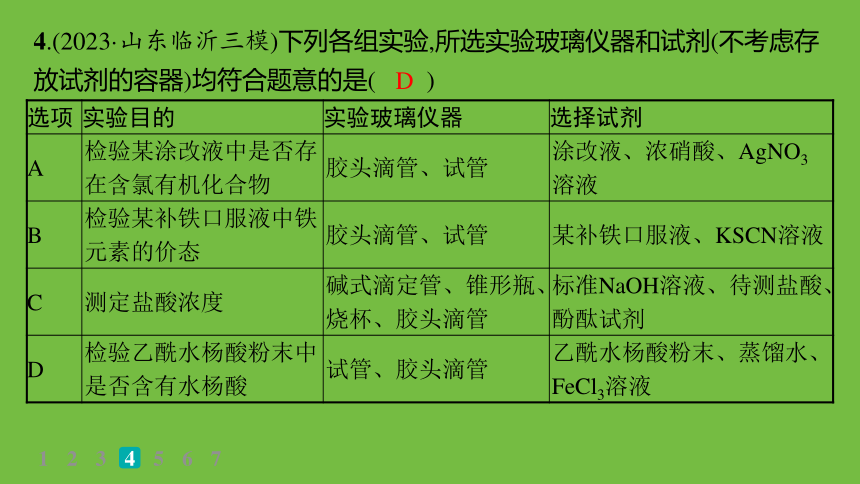
4.(2023·山东临沂三模)下列各组实验,所选实验玻璃仪器和试剂(不考虑存放试剂的容器)均符合题意的是( )
选项 实验目的 实验玻璃仪器 选择试剂
A 检验某涂改液中是否存在含氯有机化合物 胶头滴管、试管 涂改液、浓硝酸、AgNO3溶液
B 检验某补铁口服液中铁元素的价态 胶头滴管、试管 某补铁口服液、KSCN溶液
C 测定盐酸浓度 碱式滴定管、锥形瓶、烧杯、胶头滴管 标准NaOH溶液、待测盐酸、酚酞试剂
D 检验乙酰水杨酸粉末中是否含有水杨酸 试管、胶头滴管 乙酰水杨酸粉末、蒸馏水、FeCl3溶液
D
1
2
3
4
5
6
7
解析 检验某涂改液中是否存在含氯有机化合物,氯元素一般为氯原子,故无法用硝酸和硝酸银溶液直接检验,A错误;取一支干净的试管,用胶头滴管向试管中注入口服液少许,再加入KSCN溶液,若溶液变红,则证明含有Fe3+,若溶液不变红,则证明不含有Fe3+,但无法证明里面的铁元素的价态情况,溶液可能既含有Fe2+又含有Fe3+,B错误;用标准氢氧化钠溶液滴定法测定盐酸浓度,酚酞做指示剂,所需的玻璃仪器为移液管或酸式滴定管(量取一定体积盐酸)、碱式滴定管、锥形瓶、胶头滴管等,C错误;乙酰水杨酸不含有酚羟基,水杨酸含有酚羟基,将乙酰水杨酸粉末加入盛有蒸馏水的试管,振荡摇匀后,加入1~2滴FeCl3溶液,若变紫色,证明有水杨酸,D正确。
1
2
3
4
5
6
7
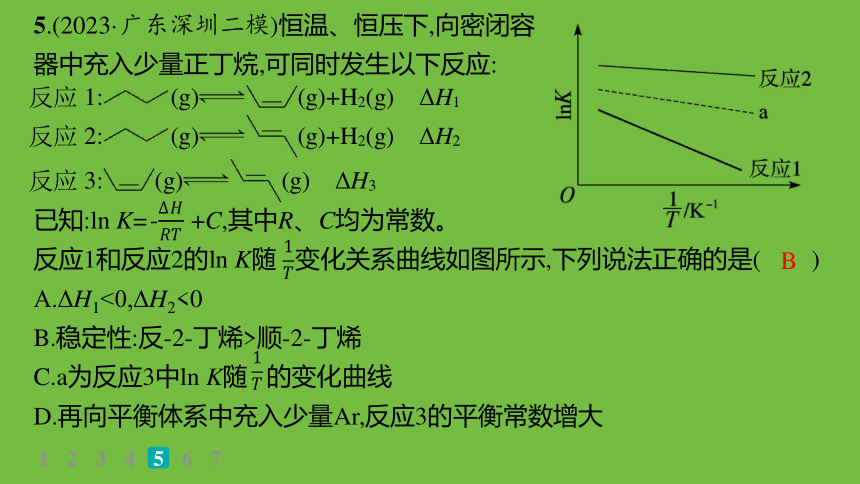
5.(2023·广东深圳二模)恒温、恒压下,向密闭容
器中充入少量正丁烷,可同时发生以下反应:
A.ΔH1<0,ΔH2<0
B.稳定性:反-2-丁烯>顺-2-丁烯
C.a为反应3中ln K随 的变化曲线
D.再向平衡体系中充入少量Ar,反应3的平衡常数增大
已知:ln K= +C,其中R、C均为常数。
反应1和反应2的ln K随 变化关系曲线如图所示,下列说法正确的是( )
B
1
2
3
4
5
6
7
1
2
3
4
5
6
7
6.(2022·河北衡水二模)工业氢氧化锂在重结晶提纯时,采取了下述办法,巧妙地分离出杂质 。工艺流程如下:
t/℃ 0 20 40 60 80 100
12.7 12.8 13 13.8 15.3 17.5
下列说法错误的是( )
A.LiOH的溶解度随温度升高变化不大
B.操作Ⅰ为过滤,除去 等形成的难溶物
C.操作Ⅱ得到LiOH晶体应采用降温结晶
D.操作Ⅲ为趁热过滤,分离含 的可溶性杂质
C
1
2
3
4
5
6
7
1
2
3
4
5
6
7
7.(2023·湖北大学附中二模)CdSe是一种重要的半导体材料。其晶体的晶胞结构如图所示,已知m的坐标参数为 ,晶胞参数为a pm。下列说法正确的是( )
B
1
2
3
4
5
6
7
选择题专项练(下)
1
2
3
4
5
6
7
1.(2023·广东湛江二模)“乌铜走银”是我国传统铜制工艺品。它以铜为胎,在胎上雕刻各种花纹图案,然后将熔化的银水填入花纹图案中,冷却后打磨光滑处理,时间久了底铜自然变为乌黑,透出银纹图案,呈现出黑白分明的装饰效果,古香古色,典雅别致。下列叙述正确的是( )
A.“乌铜走银”发生的是物理变化
B.铜和银在任何条件下都不能形成原电池
C.铜表面变黑是由于生成了Cu2(OH)2CO3
D.铜和银在元素周期表中均位于长周期
D
解析 “乌铜走银”过程中,铜本身为光亮红色,时间久了底铜变为黑色,是生成了CuO,该过程是化学变化,A错误;铜比银活泼,用铜、银和硝酸银溶液可以形成原电池,铜为负极,银为正极,B错误;Cu2(OH)2CO3是绿色的,铜表面变黑是由于生成了氧化铜,C错误;铜在第四周期,银在第五周期,均属于长周期元素,D正确。
1
2
3
4
5
6
7
1
2
3
4
5
6
7
2.(2023·北京海淀区二模)某种超分子聚合物网络生物电极的制备原料CB和PDMA的结构如图。下列说法正确的是( )
PDMA
A.CB中核磁共振氢谱有两组峰
B.PDMA单体的分子式为C10H20N2O2
C.CB与PDMA均为高分子化合物
D.CB与PDMA都具有良好的耐酸碱性
A
1
2
3
4
5
6
7
解析 根据等效氢原理可知,CB分子中有2种氢原子,故核磁共振氢谱有两
组峰,A正确;PDMA单体为 ,则其分子式为C5H9NO,B错
误;高分子是指相对分子质量成千上万的物质,CB的相对分子质量为1 328,不是高分子化合物,C错误;CB与PDMA中都含有酰胺键,在酸性和碱性条件下均能发生水解,故CB与PDMA都不耐酸碱性,D错误。
1
2
3
4
5
6
7
3.(2023·湖北宜昌4月调研)化合物A的结构如图所示,其广泛应用于新材料的生产及电化学研究。其中X、Y、Z、E、Q、W为原子序数依次增大的短周期主族元素,Z与Q、E与W分别位于同一主族。下列有关说法错误的是( )
化合物A
A.Y2X2是含有极性键的非极性分子
B.E—E键能大于W—W键能
C.原子序数为83的元素与Z位于同一主族
D.第一电离能:E>W>Q
B
1
2
3
4
5
6
7
解析 X、Y、Z、E、Q、W为原子序数依次增大的短周期主族元素,根据原子形成共价键的数量和所带电荷数可判断X为H,Y为C,Z为N。根据原子序数大小,且Z与Q、E与W分别位于同一主族,可知Q为P,E为F,W为Cl。Y2X2为乙炔,是含有极性键的非极性分子,A正确;Cl2比F2更稳定,其原因是F—F键能小于Cl—Cl键能,B错误;原子序数为83的元素为铋,其位于第六周期第ⅤA族,与N位于同一主族,C正确;第一电离能:F>Cl>P,D正确。
1
2
3
4
5
6
7
4.(2023·广东潮州二模)硫及其化合物的“价—类二维图”体现了化学变化之美。NA为阿伏加德罗常数的值,下列有关说法正确的是( )
A.1 L 1 mol·L-1 H2S水溶液中粒子关系存在:N(HS-)+N(S2-)=NA
B.标准状况下,22.4 L Y的分子数目为NA
C.工业上用NaClO3和X制备1 mol ClO2时,消耗X分子数为0.5NA
D.“价—类二维图”中盐N可由其相应单质直接化合生成
C
1
2
3
4
5
6
7
解析 由题图可知,X为二氧化硫、Y为三氧化硫、Z为硫酸、M为硫酸铜、N为硫化铜。1 L 1 mol·L-1氢硫酸溶液中,据元素守恒可得:N(H2S)+N(HS-) +N(S2-)=1 mol·L-1×1 L×NA mol-1=NA,A错误;标准状况下,三氧化硫为固态,无法计算22.4 L三氧化硫的物质的量和含有的分子数目,B错误;由得失电子数目守恒可知,氯酸钠溶液与二氧化硫反应制备1 mol二氧化氯时,反应消耗二氧化硫的分子数为 ×NA mol-1=0.5NA,C正确;铜与硫共热反应生成硫化亚铜,不能生成硫化铜,则硫化铜不能由相应单质直接化合生成,D错误。
1
2
3
4
5
6
7
5.(2023·山东潍坊二模)纯碱在食品加工、制药等方面有重要应用。实验室以碳酸氢铵(温度高于35 ℃分解)和食盐水为原料模拟纯碱的制取,流程如下:
下列说法错误的是( )
A.“搅拌、加热”操作中,应采用水浴加热,且温度控制在35 ℃以下
B.NH4HCO3、NaCl、NaHCO3、NH4Cl四种物质中,NaHCO3溶解度最低
C.“洗涤、抽滤”操作中用到的主要仪器有:普通漏斗、烧杯、玻璃棒
D.利用“双指示剂”法测定碳酸钠中碳酸氢钠的含量时,第1指示剂为“酚酞”、第2指示剂为“甲基橙”
C
1
2
3
4
5
6
7
解析 为防止温度高于35 ℃时碳酸氢铵受热分解,“搅拌、加热”操作中,应采用水浴加热,且温度控制在35 ℃以下,A正确;向饱和食盐水中加入碳酸氢铵粉末,在搅拌、加热条件下发生反应得到碳酸氢钠沉淀说明溶液中碳酸氢铵、氯化钠、碳酸氢钠、氯化铵四种物质中碳酸氢钠的溶解度最低,B正确;“洗涤、抽滤”操作中用到的主要仪器为布氏漏斗、烧杯、玻璃棒,C错误;利用“双指示剂”法测定碳酸钠中碳酸氢钠的含量时,第1指示剂为“酚酞”,酚酞作指示剂条件下碳酸钠溶液与盐酸反应生成碳酸氢钠和氯化钠,第2指示剂为“甲基橙”,甲基橙作指示剂条件下NaHCO3溶液与盐酸反应生成氯化钠、二氧化碳和水,D正确。
1
2
3
4
5
6
7
6.(2023·湖北武汉4月调研)烯烃与HX发生加成反应时,第一步H+加到双键碳原子上形成碳正离子中间体,第二步碳正离子再结合X-,其历程如下:
答案 C
1
2
3
4
5
6
7
1
2
3
4
5
6
7
解析 碳正离子的相对稳定性越强,越容易和卤素离子结合,根据题目给出的碳正离子的相对稳定性可推测,CH2=C(CH3)CH2CH=CH2与足量HCl充
分加成得到的产物中,含量最大的为 。
1
2
3
4
5
6
7
7.(2022·辽宁名校联盟联考)Cu、Au能形成多种组成固定的合金,其中一种晶体的晶胞结构(立方体)如图所示,下列说法正确的是( )
A.该晶体的化学组成可表示为CuAu
B.与1个Cu原子距离最近的Au原子是4个
C.Au填充了与之距离最近的Cu原子构成的正四面体空隙
D.根据图中信息,铜原子a的分数坐标为(0.5,0.5,0.5)
B
1
2
3
4
5
6
7
解析 晶胞中位于面心Cu原子的个数为6× =3,位于顶点的Au原子的个数为8× =1,则晶体的化学式为Cu3Au,A错误;晶胞中Au原子和距离最近的Cu原子为顶点和面心的位置关系,则与1个Cu原子距离最近的Au原子是4个,B正确;晶胞中Au原子和距离最近的Cu原子为顶点和面心的位置关系,则Au原子没有填充Cu原子构成的正四面体空隙,C错误;晶胞的边长为1,铜原子a位于晶胞右侧面的面心,分数坐标为(1,0.5,0.5),D错误。
本 课 结 束
选择题专项练(上)
1
2
3
4
5
6
7
1.(2023·河北沧州二模)青矾矿石在《唐本草》中有记载:“本来绿色,新出窟未见风者,正如瑠璃……烧之赤色……”。明末学者方以智所著《物理小识》中说:“青矾厂气熏人,衣服当之易烂,栽木不茂。”有关说法正确的是( )
A.青矾矿石主要成分是CuSO4·5H2O
B.烧之赤色,是发生了分解反应生成Cu2O的缘故
C.青矾应密封保存,主要目的是防止风化
D.熏人的“厂气”是SO2、SO3
D
1
2
3
4
5
6
7
解析 青矾矿石的描述为“本来绿色,新出窟未见风者,正如瑠璃……烧之赤色……”,说明“青矾”的颜色为绿色,其主要成分应为FeSO4·7H2O,A错误;“烧之赤色”说明经煅烧后,分解成颗粒度非常细而活性又很强的Fe2O3,同时生成SO2,受热分解的化学方程式为2FeSO4·7H2O ══ Fe2O3+SO2↑+SO3↑+14H2O,B错误;青矾含Fe2+易被氧化,故需密封保存防氧化,C错误;根据上述分析可知,熏人的“厂气”是SO2、SO3,D正确。
1
2
3
4
5
6
7
2.(2023·福建莆田二模)我国科学家在寻找“点击反应”的砌块过程中,发现一种新的化合物,结构如图所示,其中X、Y、Z和W是原子序数依次增大的短周期主族元素,Y与W是同一主族元素。下列说法正确的是( )
A.元素电负性:Z>Y>W
B.简单氢化物沸点:X>Y>W
C.简单离子半径:Z>Y>X
D.X、W氧化物的水化物均为强酸
A
1
2
3
4
5
6
7
解析 X、Y、Z和W是原子序数依次增大的短周期主族元素,Y与W是同一主族元素,W能形成6个键,则Y为氧、W为硫;Z形成1个共价键,Z为氟;X可形成3个共价键,则X为氮。一般来说,同周期从左到右,元素的电负性变强;同主族由上而下,元素电负性减弱,则元素电负性:Z>Y>W,A正确;常温下水为液体、氨气为气体,则水沸点较高,氨气能形成氢键,导致沸点高于硫化氢,故简单氢化物沸点:Y>X>W,B错误;电子层数越多半径越大,电子层数相同时,核电荷数越大,半径越小,简单离子半径:X>Y>Z,C错误;亚硝酸、亚硫酸不是强酸,D错误。
1
2
3
4
5
6
7
3.(2022·重庆卷)工业上用N2和H2合成NH3,NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.消耗14 g N2生成NH3分子数为2NA
B.消耗1 mol H2,生成N—H键数为2NA
C.生成标准状况下22.4 L NH3,电子转移数为2NA
D.氧化1 mol NH3生成NO,需O2分子数为2NA
B
1
2
3
4
5
6
7
1
2
3
4
5
6
7
4.(2023·山东临沂三模)下列各组实验,所选实验玻璃仪器和试剂(不考虑存放试剂的容器)均符合题意的是( )
选项 实验目的 实验玻璃仪器 选择试剂
A 检验某涂改液中是否存在含氯有机化合物 胶头滴管、试管 涂改液、浓硝酸、AgNO3溶液
B 检验某补铁口服液中铁元素的价态 胶头滴管、试管 某补铁口服液、KSCN溶液
C 测定盐酸浓度 碱式滴定管、锥形瓶、烧杯、胶头滴管 标准NaOH溶液、待测盐酸、酚酞试剂
D 检验乙酰水杨酸粉末中是否含有水杨酸 试管、胶头滴管 乙酰水杨酸粉末、蒸馏水、FeCl3溶液
D
1
2
3
4
5
6
7
解析 检验某涂改液中是否存在含氯有机化合物,氯元素一般为氯原子,故无法用硝酸和硝酸银溶液直接检验,A错误;取一支干净的试管,用胶头滴管向试管中注入口服液少许,再加入KSCN溶液,若溶液变红,则证明含有Fe3+,若溶液不变红,则证明不含有Fe3+,但无法证明里面的铁元素的价态情况,溶液可能既含有Fe2+又含有Fe3+,B错误;用标准氢氧化钠溶液滴定法测定盐酸浓度,酚酞做指示剂,所需的玻璃仪器为移液管或酸式滴定管(量取一定体积盐酸)、碱式滴定管、锥形瓶、胶头滴管等,C错误;乙酰水杨酸不含有酚羟基,水杨酸含有酚羟基,将乙酰水杨酸粉末加入盛有蒸馏水的试管,振荡摇匀后,加入1~2滴FeCl3溶液,若变紫色,证明有水杨酸,D正确。
1
2
3
4
5
6
7
5.(2023·广东深圳二模)恒温、恒压下,向密闭容
器中充入少量正丁烷,可同时发生以下反应:
A.ΔH1<0,ΔH2<0
B.稳定性:反-2-丁烯>顺-2-丁烯
C.a为反应3中ln K随 的变化曲线
D.再向平衡体系中充入少量Ar,反应3的平衡常数增大
已知:ln K= +C,其中R、C均为常数。
反应1和反应2的ln K随 变化关系曲线如图所示,下列说法正确的是( )
B
1
2
3
4
5
6
7
1
2
3
4
5
6
7
6.(2022·河北衡水二模)工业氢氧化锂在重结晶提纯时,采取了下述办法,巧妙地分离出杂质 。工艺流程如下:
t/℃ 0 20 40 60 80 100
12.7 12.8 13 13.8 15.3 17.5
下列说法错误的是( )
A.LiOH的溶解度随温度升高变化不大
B.操作Ⅰ为过滤,除去 等形成的难溶物
C.操作Ⅱ得到LiOH晶体应采用降温结晶
D.操作Ⅲ为趁热过滤,分离含 的可溶性杂质
C
1
2
3
4
5
6
7
1
2
3
4
5
6
7
7.(2023·湖北大学附中二模)CdSe是一种重要的半导体材料。其晶体的晶胞结构如图所示,已知m的坐标参数为 ,晶胞参数为a pm。下列说法正确的是( )
B
1
2
3
4
5
6
7
选择题专项练(下)
1
2
3
4
5
6
7
1.(2023·广东湛江二模)“乌铜走银”是我国传统铜制工艺品。它以铜为胎,在胎上雕刻各种花纹图案,然后将熔化的银水填入花纹图案中,冷却后打磨光滑处理,时间久了底铜自然变为乌黑,透出银纹图案,呈现出黑白分明的装饰效果,古香古色,典雅别致。下列叙述正确的是( )
A.“乌铜走银”发生的是物理变化
B.铜和银在任何条件下都不能形成原电池
C.铜表面变黑是由于生成了Cu2(OH)2CO3
D.铜和银在元素周期表中均位于长周期
D
解析 “乌铜走银”过程中,铜本身为光亮红色,时间久了底铜变为黑色,是生成了CuO,该过程是化学变化,A错误;铜比银活泼,用铜、银和硝酸银溶液可以形成原电池,铜为负极,银为正极,B错误;Cu2(OH)2CO3是绿色的,铜表面变黑是由于生成了氧化铜,C错误;铜在第四周期,银在第五周期,均属于长周期元素,D正确。
1
2
3
4
5
6
7
1
2
3
4
5
6
7
2.(2023·北京海淀区二模)某种超分子聚合物网络生物电极的制备原料CB和PDMA的结构如图。下列说法正确的是( )
PDMA
A.CB中核磁共振氢谱有两组峰
B.PDMA单体的分子式为C10H20N2O2
C.CB与PDMA均为高分子化合物
D.CB与PDMA都具有良好的耐酸碱性
A
1
2
3
4
5
6
7
解析 根据等效氢原理可知,CB分子中有2种氢原子,故核磁共振氢谱有两
组峰,A正确;PDMA单体为 ,则其分子式为C5H9NO,B错
误;高分子是指相对分子质量成千上万的物质,CB的相对分子质量为1 328,不是高分子化合物,C错误;CB与PDMA中都含有酰胺键,在酸性和碱性条件下均能发生水解,故CB与PDMA都不耐酸碱性,D错误。
1
2
3
4
5
6
7
3.(2023·湖北宜昌4月调研)化合物A的结构如图所示,其广泛应用于新材料的生产及电化学研究。其中X、Y、Z、E、Q、W为原子序数依次增大的短周期主族元素,Z与Q、E与W分别位于同一主族。下列有关说法错误的是( )
化合物A
A.Y2X2是含有极性键的非极性分子
B.E—E键能大于W—W键能
C.原子序数为83的元素与Z位于同一主族
D.第一电离能:E>W>Q
B
1
2
3
4
5
6
7
解析 X、Y、Z、E、Q、W为原子序数依次增大的短周期主族元素,根据原子形成共价键的数量和所带电荷数可判断X为H,Y为C,Z为N。根据原子序数大小,且Z与Q、E与W分别位于同一主族,可知Q为P,E为F,W为Cl。Y2X2为乙炔,是含有极性键的非极性分子,A正确;Cl2比F2更稳定,其原因是F—F键能小于Cl—Cl键能,B错误;原子序数为83的元素为铋,其位于第六周期第ⅤA族,与N位于同一主族,C正确;第一电离能:F>Cl>P,D正确。
1
2
3
4
5
6
7
4.(2023·广东潮州二模)硫及其化合物的“价—类二维图”体现了化学变化之美。NA为阿伏加德罗常数的值,下列有关说法正确的是( )
A.1 L 1 mol·L-1 H2S水溶液中粒子关系存在:N(HS-)+N(S2-)=NA
B.标准状况下,22.4 L Y的分子数目为NA
C.工业上用NaClO3和X制备1 mol ClO2时,消耗X分子数为0.5NA
D.“价—类二维图”中盐N可由其相应单质直接化合生成
C
1
2
3
4
5
6
7
解析 由题图可知,X为二氧化硫、Y为三氧化硫、Z为硫酸、M为硫酸铜、N为硫化铜。1 L 1 mol·L-1氢硫酸溶液中,据元素守恒可得:N(H2S)+N(HS-) +N(S2-)=1 mol·L-1×1 L×NA mol-1=NA,A错误;标准状况下,三氧化硫为固态,无法计算22.4 L三氧化硫的物质的量和含有的分子数目,B错误;由得失电子数目守恒可知,氯酸钠溶液与二氧化硫反应制备1 mol二氧化氯时,反应消耗二氧化硫的分子数为 ×NA mol-1=0.5NA,C正确;铜与硫共热反应生成硫化亚铜,不能生成硫化铜,则硫化铜不能由相应单质直接化合生成,D错误。
1
2
3
4
5
6
7
5.(2023·山东潍坊二模)纯碱在食品加工、制药等方面有重要应用。实验室以碳酸氢铵(温度高于35 ℃分解)和食盐水为原料模拟纯碱的制取,流程如下:
下列说法错误的是( )
A.“搅拌、加热”操作中,应采用水浴加热,且温度控制在35 ℃以下
B.NH4HCO3、NaCl、NaHCO3、NH4Cl四种物质中,NaHCO3溶解度最低
C.“洗涤、抽滤”操作中用到的主要仪器有:普通漏斗、烧杯、玻璃棒
D.利用“双指示剂”法测定碳酸钠中碳酸氢钠的含量时,第1指示剂为“酚酞”、第2指示剂为“甲基橙”
C
1
2
3
4
5
6
7
解析 为防止温度高于35 ℃时碳酸氢铵受热分解,“搅拌、加热”操作中,应采用水浴加热,且温度控制在35 ℃以下,A正确;向饱和食盐水中加入碳酸氢铵粉末,在搅拌、加热条件下发生反应得到碳酸氢钠沉淀说明溶液中碳酸氢铵、氯化钠、碳酸氢钠、氯化铵四种物质中碳酸氢钠的溶解度最低,B正确;“洗涤、抽滤”操作中用到的主要仪器为布氏漏斗、烧杯、玻璃棒,C错误;利用“双指示剂”法测定碳酸钠中碳酸氢钠的含量时,第1指示剂为“酚酞”,酚酞作指示剂条件下碳酸钠溶液与盐酸反应生成碳酸氢钠和氯化钠,第2指示剂为“甲基橙”,甲基橙作指示剂条件下NaHCO3溶液与盐酸反应生成氯化钠、二氧化碳和水,D正确。
1
2
3
4
5
6
7
6.(2023·湖北武汉4月调研)烯烃与HX发生加成反应时,第一步H+加到双键碳原子上形成碳正离子中间体,第二步碳正离子再结合X-,其历程如下:
答案 C
1
2
3
4
5
6
7
1
2
3
4
5
6
7
解析 碳正离子的相对稳定性越强,越容易和卤素离子结合,根据题目给出的碳正离子的相对稳定性可推测,CH2=C(CH3)CH2CH=CH2与足量HCl充
分加成得到的产物中,含量最大的为 。
1
2
3
4
5
6
7
7.(2022·辽宁名校联盟联考)Cu、Au能形成多种组成固定的合金,其中一种晶体的晶胞结构(立方体)如图所示,下列说法正确的是( )
A.该晶体的化学组成可表示为CuAu
B.与1个Cu原子距离最近的Au原子是4个
C.Au填充了与之距离最近的Cu原子构成的正四面体空隙
D.根据图中信息,铜原子a的分数坐标为(0.5,0.5,0.5)
B
1
2
3
4
5
6
7
解析 晶胞中位于面心Cu原子的个数为6× =3,位于顶点的Au原子的个数为8× =1,则晶体的化学式为Cu3Au,A错误;晶胞中Au原子和距离最近的Cu原子为顶点和面心的位置关系,则与1个Cu原子距离最近的Au原子是4个,B正确;晶胞中Au原子和距离最近的Cu原子为顶点和面心的位置关系,则Au原子没有填充Cu原子构成的正四面体空隙,C错误;晶胞的边长为1,铜原子a位于晶胞右侧面的面心,分数坐标为(1,0.5,0.5),D错误。
本 课 结 束
同课章节目录
