2023—2024学年人教化学九年级下册第11单元 盐 化肥 单元练习(含答案)
文档属性
| 名称 | 2023—2024学年人教化学九年级下册第11单元 盐 化肥 单元练习(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 341.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-26 21:17:52 | ||
图片预览




文档简介
2023—2024学年人教化学九年级下册第11单元 盐 化肥 单元练习附答案
人教第11单元 盐 化肥
一、选择题。
1、下列物质属于盐的是( )
A.H2SO4 B.CaCO3 C.Ca(OH)2 D.MnO2
2、蒸馒头时,在发酵面团中加入某种物质,既能除去面团中的酸又能使馒头松软,该物质是( )
A.碳酸氢钠 B.生石灰 C.氢氧化钠 D.氯化钠
3、甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示,关于该转化关系图,下列说法正确的是( )
A. 如果丙是碳酸钠,乙是氢氧化钠,则甲是硝酸钠
B. 若甲、乙、丁都是氧化物,则丙一定是碳酸钙
C. 甲、乙、丙、丁之间的转化可以全部通过复分解反应实现
D. 若甲、乙、丙、丁均含有同一种元素,且乙可用来灭火,则丙一定是单质碳
4、下列关于酸、碱、盐的用途不合理的是( )
A. 盐酸除铁锈
B. 氢氧化钠改良酸性土壤
C. 硫酸铜与氢氧化钙混合配制农药波尔多液
D. 纯碱除油污
5、蒸馒头时,在发酵面团中加入某种物质,既能除去面团中的酸又能使馒头松软,该物质是( )
A.碳酸氢钠 B.生石灰 C.氢氧化钠 D.氯化钠
6、科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为4NH3+3O22X + 6H2O。下列说法中不正确的是( )
A.氨气在常压下液化是物理变化 B.X的化学式为N2
C.液氨具有可燃性,属于化学性质 D.液氨属于混合物
7、某同学想要鉴别NH4HCO3、NH4Cl、KCl三种化肥,操作过程如图所示,其中试剂甲和乙可能是( )
A.甲:水,乙:氢氧化钠
B.甲:熟石灰,乙:稀盐酸
C.甲:稀盐酸,乙:氯化钠溶液
D.甲:氢氧化钠,乙:硫酸钠溶液
8、粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
9、造成水体污染的主要原因是( )。
①天然水与空气、岩石和土壤的长期接触
②工业生产中的废气、废液和废渣的随意排放
③农业生产中化肥、农药的使用不当
④城市生活污水的大量排放
A.①② B.①③ C.②③ D.②③④
10、海水晒盐的原理是( )
A. 日晒风吹使氯化钠的溶解度降低
B. 日晒风吹使溶液由饱和变为不饱和
C. 日晒风吹使水分蒸发,食盐晶体析出
D. 日晒风吹使海水发生分解
11、碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一,它的俗称是( )
A.小苏打 B.苛性钠 C.烧碱 D.苏打
12、下列盐的用途中,错误的是( )
A.用含亚硝酸钠的工业盐制香肠 B.用碳酸钙做补钙剂
C.用氯化钠配制生理盐水 D.用碳酸氢钠做焙制糕点的发酵粉
13、以下常见化肥中,属于复合肥的是( )
A. K2SO4 B. NH4NO3 C. KNO3 D. Ca(H2PO4)2
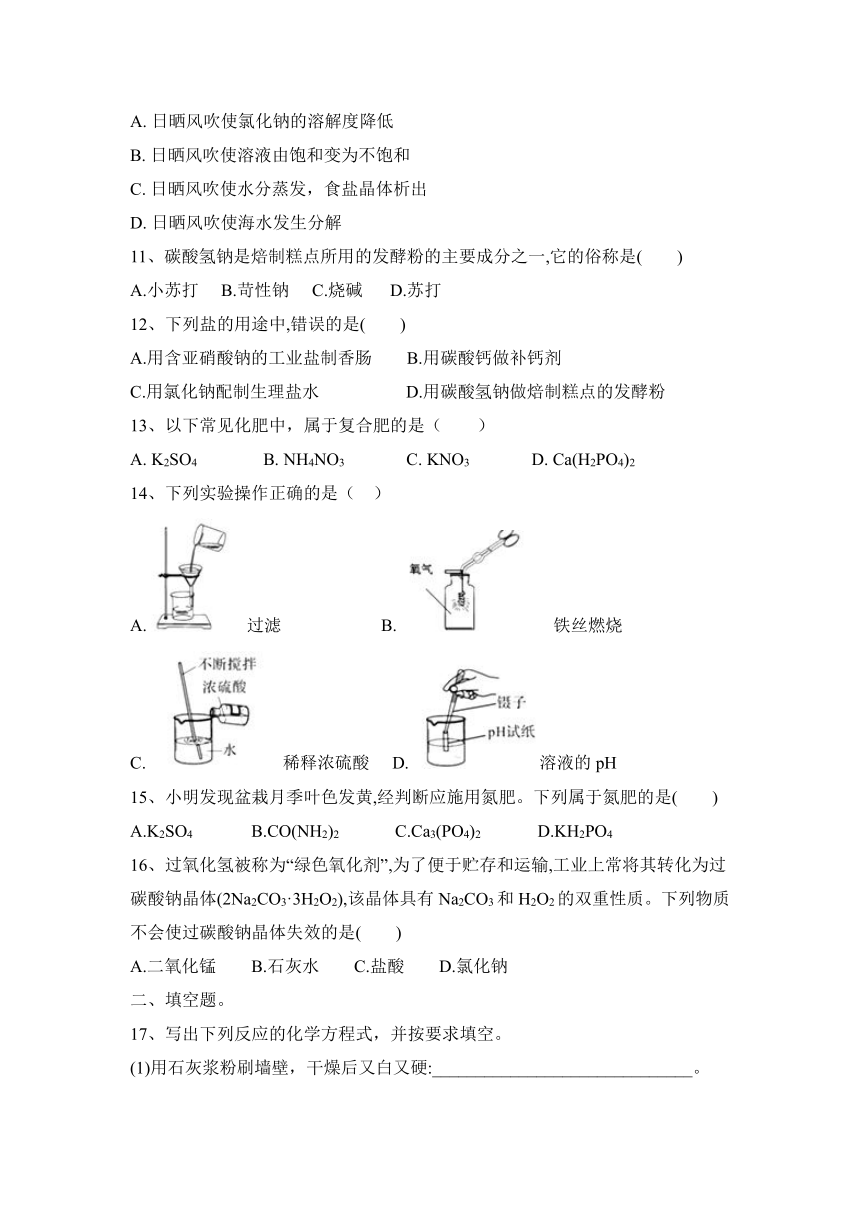
14、下列实验操作正确的是( )
A. 过滤 B. 铁丝燃烧
C. 稀释浓硫酸 D. 溶液的pH
15、小明发现盆栽月季叶色发黄,经判断应施用氮肥。下列属于氮肥的是( )
A.K2SO4 B.CO(NH2)2 C.Ca3(PO4)2 D.KH2PO4
16、过氧化氢被称为“绿色氧化剂”,为了便于贮存和运输,工业上常将其转化为过碳酸钠晶体(2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠晶体失效的是( )
A.二氧化锰 B.石灰水 C.盐酸 D.氯化钠
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。
(2)工业炼铁的主要原理是一氧化碳和氧化铁在高温下反应:_______________________ 。工业炼铁的主要设备是__________________。
(3)车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产。乙醇(C2H5OH)完全燃烧的化学方程式为_______________,该反应属于____________(选填:“吸热”或“放热”)反应。
(4)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(5)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
18、阅读教材表格11—1内容,填写下列表格。
类别 氮肥 磷肥 钾肥 复合肥
名称 尿素 碳酸氢铵 磷矿粉 过磷酸钙 硫酸钾 氯化钾 硝酸钾 磷酸二氢铵
主要作用 促使作物的茎、叶生长______,叶色______ 促进作物根系发达,增强______能力,穗多粒满 促进作物生长健壮,增强______和______能力 —
缺少引起的症状 植株矮小瘦弱、叶片______ 生长迟缓,产量降低 容易倒伏,叶片边缘和尖端呈褐色 —
19、已知A与B、甲与乙均为初中化学常见的物质,其转化关系如图所示。
(1)若甲为氧气,则A的化学式为________ 。
(2)若甲是一种红色的氧化物,乙的溶液呈黄色,则反应的化学方程式为________ 。
(3)若甲、乙是常见的碱,A、B是常见的盐,而且当甲转化为B、乙转化为A时,都是与同一种气体X发生反应。
①A的化学式为________ ;②甲转化为B的化学方程式为________ 。
(4)若甲和A发生中和反应,而且当甲转化为B、乙转化为A时,都是与同一物质Y发生反应,则Y的化学式为________ ,此中和反应的化学方程式为________ 。
20、春节是中华民族的传统佳节,在访亲拜友中迎接新年的到来。表达自己的观点。
(1)花馍是最具山西特色的美食之一。春节蒸花馍会用到发酵粉,其主要成分是小苏打,化学式为______ 。蒸好的花馍松软多孔是______气体受热膨胀所留下的空隙。
(2)美食之后,洗碗—碗盘上附着的油污常用洗涤剂清洗,这是因为洗涤剂具有______作用。泡茶使用茶漏可以很好的分离茶叶和茶水,这相当于化学实验操作中的______。
(3)正月十五元宵节,很多地方有“点旺火”的习俗,有兴旺之意。垒旺火很有讲究,技术高超的师傅用大块煤炭垒成底小、肚大、顶尖、内空的宝瓶形状,这样才能达到燃烧净尽而旺火不塌。从燃烧的角度分析,这样的形状主要是为了______ ,旺火上方出现的蓝色火焰是______燃烧产生的。当然点旺火也有不利的一面,如______。
(4)节能出行靠高铁,中国高铁世界瞩目。列车车体主要采用铝合金材料,其优良的性能有______ (写一条);车头前端部采用玻璃钢,玻璃钢属于______材料;受电弓的滑板使用石墨材料,这体现了石墨具有良好的______性(写一条即可)。
三、简答题。
21、小明同学在做《粗盐中难溶性杂质的去除》实验时,用到了如图所示装置
(1)请指出该装置图中的一处错误;
(2)改进装置后过滤,发现滤液仍然浑浊,其原因可能是什么?(写出一条即可)
(3)经初步提纯所得精盐是否为纯净物?请写出你的判断和理由.
四、实验题。
22、氯化钠和氯化镁是重要的化工原料。某粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4等物质,为了从中提取较纯的氯化镁和氯化钠,设计以下实验方案:
请回答下列问题:
Ⅰ、步骤①溶解过程中用玻璃棒搅拌的目的是___________________________。
Ⅱ、步骤④⑤的顺序颠倒会引发的后果是______________________________。
Ⅲ、滤液乙中所含的溶质除氯化钠外还含有________;沉淀B中除含碳酸钙、碳酸钡外还含有________;在步骤⑦中若加入的盐酸略过量是否对实验结果有影响?原因是_____________________________________________________。
Ⅳ、写出步骤⑨中反应的化学方程式 _________________________________。
Ⅴ、实验最终所得的精盐的质量大于粗盐中氯化钠的质量,整个过程中产生新的NaCl的反应共有________个。
23、某学习小组在帮助实验员整理化学试剂时发现了一瓶标签残缺的无色溶液(如图所示),经实验员分析可知原瓶溶液中的溶质可能是NaHCO3、NaOH、Na2CO3、NaCl中的一种,请你对该试剂作出猜想并进行实验探究:
【提出问题】 这瓶试剂是什么溶液
【猜想与假设】
甲猜想:NaHCO3溶液
乙猜想:NaOH溶液
丙猜想:Na2CO3溶液
丁猜想:NaCl溶液
【查阅资料】 上述四种物质相关信息如下
【实验探究1】 取瓶中溶液少许于试管中,滴加几滴酚酞溶液,溶液变红。
【实验探究2】 另取瓶中溶液少许于试管中,滴加足量的稀盐酸,产生气泡。
【实验分析】 通过【实验探究1】 可知 同学的猜想一定错误。
甲同学仔细分析四种物质的相关信息表后发现自己的猜想错误,他的理由是 。
丙同学分析【实验探究2】 并结合以上同学的实验结论,认为原瓶溶液是Na2CO3溶液。
【实验探究2】 中发生反应的化学方程式为 。
【讨论质疑】 乙认为以上同学分析有漏洞,需要进一步实验确定,于是又进行了如下探究。
【实验探究3】 在【实验探究1】 试管中的红色溶液中滴加过量氯化钙溶液(中性),充分反应后,试管中溶液仍呈红色,但有白色沉淀产生。
【得出结论】 通过【实验探究3】 可证明这瓶试剂为 溶液,但已经部分变质。
【反思与拓展】学习小组反思了这瓶试剂因为 而变质,得出了该溶液正确的保存方法,若要除去该溶液变质部分所采用的方法是 (用化学反应方程式表示)。
五、计算类综合题。
24、某石油化工厂化验室的实验员用15%的NaOH溶液洗涤一定量石油产品中的残余硫酸,测得实验数据如下表。
实验序号 消耗NaOH溶液的质量 洗涤后溶液的pH
① 30 g pH<7
② 40 g pH=7
③ 50 g pH>7
(1)欲计算出一定量石油产品中所含H2SO4的质量,应该选择实验序号 的数据。
(2)若一定量石油产品中残余硫酸的质量为100 g,请计算该残余硫酸中溶质的质量分数。
2023—2024学年人教化学九年级下册第11单元 盐 化肥 单元练习附答案
人教第11单元 盐 化肥
一、选择题。
1、下列物质属于盐的是( )
A.H2SO4 B.CaCO3 C.Ca(OH)2 D.MnO2
【答案】.B
2、蒸馒头时,在发酵面团中加入某种物质,既能除去面团中的酸又能使馒头松软,该物质是( )
A.碳酸氢钠 B.生石灰 C.氢氧化钠 D.氯化钠
【答案】A
3、甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示,关于该转化关系图,下列说法正确的是( )
A. 如果丙是碳酸钠,乙是氢氧化钠,则甲是硝酸钠
B. 若甲、乙、丁都是氧化物,则丙一定是碳酸钙
C. 甲、乙、丙、丁之间的转化可以全部通过复分解反应实现
D. 若甲、乙、丙、丁均含有同一种元素,且乙可用来灭火,则丙一定是单质碳
【答案】C
4、下列关于酸、碱、盐的用途不合理的是( )
A. 盐酸除铁锈
B. 氢氧化钠改良酸性土壤
C. 硫酸铜与氢氧化钙混合配制农药波尔多液
D. 纯碱除油污
【答案】B
5、蒸馒头时,在发酵面团中加入某种物质,既能除去面团中的酸又能使馒头松软,该物质是( )
A.碳酸氢钠 B.生石灰 C.氢氧化钠 D.氯化钠
【答案】A
6、科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为4NH3+3O22X + 6H2O。下列说法中不正确的是( )
A.氨气在常压下液化是物理变化 B.X的化学式为N2
C.液氨具有可燃性,属于化学性质 D.液氨属于混合物
【答案】D
7、某同学想要鉴别NH4HCO3、NH4Cl、KCl三种化肥,操作过程如图所示,其中试剂甲和乙可能是( )
A.甲:水,乙:氢氧化钠
B.甲:熟石灰,乙:稀盐酸
C.甲:稀盐酸,乙:氯化钠溶液
D.甲:氢氧化钠,乙:硫酸钠溶液
【答案】B
8、粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
【答案】C
9、造成水体污染的主要原因是( )。
①天然水与空气、岩石和土壤的长期接触
②工业生产中的废气、废液和废渣的随意排放
③农业生产中化肥、农药的使用不当
④城市生活污水的大量排放
A.①② B.①③ C.②③ D.②③④
【答案】D
10、海水晒盐的原理是( )
A. 日晒风吹使氯化钠的溶解度降低
B. 日晒风吹使溶液由饱和变为不饱和
C. 日晒风吹使水分蒸发,食盐晶体析出
D. 日晒风吹使海水发生分解
【答案】C
11、碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一,它的俗称是( )
A.小苏打 B.苛性钠 C.烧碱 D.苏打
【答案】A
12、下列盐的用途中,错误的是( )
A.用含亚硝酸钠的工业盐制香肠 B.用碳酸钙做补钙剂
C.用氯化钠配制生理盐水 D.用碳酸氢钠做焙制糕点的发酵粉
【答案】A
13、以下常见化肥中,属于复合肥的是( )
A. K2SO4 B. NH4NO3 C. KNO3 D. Ca(H2PO4)2
【答案】C
14、下列实验操作正确的是( )
A. 过滤 B. 铁丝燃烧
C. 稀释浓硫酸 D. 溶液的pH
【答案】C
15、小明发现盆栽月季叶色发黄,经判断应施用氮肥。下列属于氮肥的是( )
A.K2SO4 B.CO(NH2)2 C.Ca3(PO4)2 D.KH2PO4
【答案】B
16、过氧化氢被称为“绿色氧化剂”,为了便于贮存和运输,工业上常将其转化为过碳酸钠晶体(2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠晶体失效的是( )
A.二氧化锰 B.石灰水 C.盐酸 D.氯化钠
【答案】D
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。
(2)工业炼铁的主要原理是一氧化碳和氧化铁在高温下反应:_______________________ 。工业炼铁的主要设备是__________________。
(3)车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产。乙醇(C2H5OH)完全燃烧的化学方程式为_______________,该反应属于____________(选填:“吸热”或“放热”)反应。
(4)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(5)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
【答案】CO2 + Ca(OH)2 == CaCO3↓+ H2O Fe2O3+3CO 2Fe+3CO2 高炉 C2H5OH+3O23H2O+2CO2 放热 2NaCl+ H2O2NaOH + H2↑+Cl2↑ BaCO3+2HCl == BaCl2 + H2O + CO2↑ 复分解反应
18、阅读教材表格11—1内容,填写下列表格。
类别 氮肥 磷肥 钾肥 复合肥
名称 尿素 碳酸氢铵 磷矿粉 过磷酸钙 硫酸钾 氯化钾 硝酸钾 磷酸二氢铵
主要作用 促使作物的茎、叶生长______,叶色______ 促进作物根系发达,增强______能力,穗多粒满 促进作物生长健壮,增强______和______能力 —
缺少引起的症状 植株矮小瘦弱、叶片______ 生长迟缓,产量降低 容易倒伏,叶片边缘和尖端呈褐色 —
【答案】茂盛 浓绿 抗旱抗寒 抗病虫害 抗倒伏 发黄
19、已知A与B、甲与乙均为初中化学常见的物质,其转化关系如图所示。
(1)若甲为氧气,则A的化学式为________ 。
(2)若甲是一种红色的氧化物,乙的溶液呈黄色,则反应的化学方程式为________ 。
(3)若甲、乙是常见的碱,A、B是常见的盐,而且当甲转化为B、乙转化为A时,都是与同一种气体X发生反应。
①A的化学式为________ ;②甲转化为B的化学方程式为________ 。
(4)若甲和A发生中和反应,而且当甲转化为B、乙转化为A时,都是与同一物质Y发生反应,则Y的化学式为________ ,此中和反应的化学方程式为________ 。
【答案】CH4 (或C2H5OH);
Fe2O3+6HCl= 2FeCl3+3H2O(或Fe2O3+3H2SO4= Fe2(SO4)3+3 H2O);
Na2CO3;Ca(OH)2+CO2=CaCO3↓+ H2O;CaO ;Ca(OH)2+2HCl= CaCl2+2 H2O
20、春节是中华民族的传统佳节,在访亲拜友中迎接新年的到来。表达自己的观点。
(1)花馍是最具山西特色的美食之一。春节蒸花馍会用到发酵粉,其主要成分是小苏打,化学式为______ 。蒸好的花馍松软多孔是______气体受热膨胀所留下的空隙。
(2)美食之后,洗碗—碗盘上附着的油污常用洗涤剂清洗,这是因为洗涤剂具有______作用。泡茶使用茶漏可以很好的分离茶叶和茶水,这相当于化学实验操作中的______。
(3)正月十五元宵节,很多地方有“点旺火”的习俗,有兴旺之意。垒旺火很有讲究,技术高超的师傅用大块煤炭垒成底小、肚大、顶尖、内空的宝瓶形状,这样才能达到燃烧净尽而旺火不塌。从燃烧的角度分析,这样的形状主要是为了______ ,旺火上方出现的蓝色火焰是______燃烧产生的。当然点旺火也有不利的一面,如______。
(4)节能出行靠高铁,中国高铁世界瞩目。列车车体主要采用铝合金材料,其优良的性能有______ (写一条);车头前端部采用玻璃钢,玻璃钢属于______材料;受电弓的滑板使用石墨材料,这体现了石墨具有良好的______性(写一条即可)。
【答案】 (1)NaHCO3 CO2 (2)乳化 (2)过滤
(3)增大与氧气的接触面积,使燃烧更充分 CO 造成空气污染
(4)密度小 复合 导电
三、简答题。
21、小明同学在做《粗盐中难溶性杂质的去除》实验时,用到了如图所示装置
(1)请指出该装置图中的一处错误;
(2)改进装置后过滤,发现滤液仍然浑浊,其原因可能是什么?(写出一条即可)
(3)经初步提纯所得精盐是否为纯净物?请写出你的判断和理由.
【答案】
(1)缺少玻璃棒引流
(2)滤纸破损(或滤液高于滤纸边缘或盛接滤液的烧杯不干净等)
(3)不是纯净物;精盐中含有氯化钠、氯化钙、氯化镁等。
四、实验题。
22、氯化钠和氯化镁是重要的化工原料。某粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4等物质,为了从中提取较纯的氯化镁和氯化钠,设计以下实验方案:
请回答下列问题:
Ⅰ、步骤①溶解过程中用玻璃棒搅拌的目的是___________________________。
Ⅱ、步骤④⑤的顺序颠倒会引发的后果是______________________________。
Ⅲ、滤液乙中所含的溶质除氯化钠外还含有________;沉淀B中除含碳酸钙、碳酸钡外还含有________;在步骤⑦中若加入的盐酸略过量是否对实验结果有影响?原因是_____________________________________________________。
Ⅳ、写出步骤⑨中反应的化学方程式 _________________________________。
Ⅴ、实验最终所得的精盐的质量大于粗盐中氯化钠的质量,整个过程中产生新的NaCl的反应共有________个。
【答案】Ⅰ、加快溶解的速度
Ⅱ、精盐中会混有氯化钡或无法除去过量的氯化钡
Ⅲ、氢氧化钠、碳酸钠 硫酸钡 无影响,加热蒸发时氯化氢会挥发
Ⅳ、Mg(OH)2+2HCl===Mg Cl2+2H2O Ⅴ、6
23、某学习小组在帮助实验员整理化学试剂时发现了一瓶标签残缺的无色溶液(如图所示),经实验员分析可知原瓶溶液中的溶质可能是NaHCO3、NaOH、Na2CO3、NaCl中的一种,请你对该试剂作出猜想并进行实验探究:
【提出问题】 这瓶试剂是什么溶液
【猜想与假设】
甲猜想:NaHCO3溶液
乙猜想:NaOH溶液
丙猜想:Na2CO3溶液
丁猜想:NaCl溶液
【查阅资料】 上述四种物质相关信息如下
【实验探究1】 取瓶中溶液少许于试管中,滴加几滴酚酞溶液,溶液变红。
【实验探究2】 另取瓶中溶液少许于试管中,滴加足量的稀盐酸,产生气泡。
【实验分析】 通过【实验探究1】 可知 同学的猜想一定错误。
甲同学仔细分析四种物质的相关信息表后发现自己的猜想错误,他的理由是 。
丙同学分析【实验探究2】 并结合以上同学的实验结论,认为原瓶溶液是Na2CO3溶液。
【实验探究2】 中发生反应的化学方程式为 。
【讨论质疑】 乙认为以上同学分析有漏洞,需要进一步实验确定,于是又进行了如下探究。
【实验探究3】 在【实验探究1】 试管中的红色溶液中滴加过量氯化钙溶液(中性),充分反应后,试管中溶液仍呈红色,但有白色沉淀产生。
【得出结论】 通过【实验探究3】 可证明这瓶试剂为 溶液,但已经部分变质。
【反思与拓展】学习小组反思了这瓶试剂因为 而变质,得出了该溶液正确的保存方法,若要除去该溶液变质部分所采用的方法是 (用化学反应方程式表示)。
【答案】丁 在该温度下,碳酸氢钠的饱和溶液的溶质质量分数小于10%
氢氧化钠 敞口放置
五、计算类综合题。
24、某石油化工厂化验室的实验员用15%的NaOH溶液洗涤一定量石油产品中的残余硫酸,测得实验数据如下表。
实验序号 消耗NaOH溶液的质量 洗涤后溶液的pH
① 30 g pH<7
② 40 g pH=7
③ 50 g pH>7
(1)欲计算出一定量石油产品中所含H2SO4的质量,应该选择实验序号 的数据。
(2)若一定量石油产品中残余硫酸的质量为100 g,请计算该残余硫酸中溶质的质量分数。
【答案】(1)②
(2)设该残余硫酸中溶质的质量为x。
2NaOH + H2SO4Na2SO4+2H2O
80 98
40 g×15% x
=
x=7.35 g
该残余硫酸中溶质的质量分数为
×100%=7.35%。
答:该残余硫酸中溶质的质量分数为7.35%。
人教第11单元 盐 化肥
一、选择题。
1、下列物质属于盐的是( )
A.H2SO4 B.CaCO3 C.Ca(OH)2 D.MnO2
2、蒸馒头时,在发酵面团中加入某种物质,既能除去面团中的酸又能使馒头松软,该物质是( )
A.碳酸氢钠 B.生石灰 C.氢氧化钠 D.氯化钠
3、甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示,关于该转化关系图,下列说法正确的是( )
A. 如果丙是碳酸钠,乙是氢氧化钠,则甲是硝酸钠
B. 若甲、乙、丁都是氧化物,则丙一定是碳酸钙
C. 甲、乙、丙、丁之间的转化可以全部通过复分解反应实现
D. 若甲、乙、丙、丁均含有同一种元素,且乙可用来灭火,则丙一定是单质碳
4、下列关于酸、碱、盐的用途不合理的是( )
A. 盐酸除铁锈
B. 氢氧化钠改良酸性土壤
C. 硫酸铜与氢氧化钙混合配制农药波尔多液
D. 纯碱除油污
5、蒸馒头时,在发酵面团中加入某种物质,既能除去面团中的酸又能使馒头松软,该物质是( )
A.碳酸氢钠 B.生石灰 C.氢氧化钠 D.氯化钠
6、科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为4NH3+3O22X + 6H2O。下列说法中不正确的是( )
A.氨气在常压下液化是物理变化 B.X的化学式为N2
C.液氨具有可燃性,属于化学性质 D.液氨属于混合物
7、某同学想要鉴别NH4HCO3、NH4Cl、KCl三种化肥,操作过程如图所示,其中试剂甲和乙可能是( )
A.甲:水,乙:氢氧化钠
B.甲:熟石灰,乙:稀盐酸
C.甲:稀盐酸,乙:氯化钠溶液
D.甲:氢氧化钠,乙:硫酸钠溶液
8、粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
9、造成水体污染的主要原因是( )。
①天然水与空气、岩石和土壤的长期接触
②工业生产中的废气、废液和废渣的随意排放
③农业生产中化肥、农药的使用不当
④城市生活污水的大量排放
A.①② B.①③ C.②③ D.②③④
10、海水晒盐的原理是( )
A. 日晒风吹使氯化钠的溶解度降低
B. 日晒风吹使溶液由饱和变为不饱和
C. 日晒风吹使水分蒸发,食盐晶体析出
D. 日晒风吹使海水发生分解
11、碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一,它的俗称是( )
A.小苏打 B.苛性钠 C.烧碱 D.苏打
12、下列盐的用途中,错误的是( )
A.用含亚硝酸钠的工业盐制香肠 B.用碳酸钙做补钙剂
C.用氯化钠配制生理盐水 D.用碳酸氢钠做焙制糕点的发酵粉
13、以下常见化肥中,属于复合肥的是( )
A. K2SO4 B. NH4NO3 C. KNO3 D. Ca(H2PO4)2
14、下列实验操作正确的是( )
A. 过滤 B. 铁丝燃烧
C. 稀释浓硫酸 D. 溶液的pH
15、小明发现盆栽月季叶色发黄,经判断应施用氮肥。下列属于氮肥的是( )
A.K2SO4 B.CO(NH2)2 C.Ca3(PO4)2 D.KH2PO4
16、过氧化氢被称为“绿色氧化剂”,为了便于贮存和运输,工业上常将其转化为过碳酸钠晶体(2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠晶体失效的是( )
A.二氧化锰 B.石灰水 C.盐酸 D.氯化钠
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。
(2)工业炼铁的主要原理是一氧化碳和氧化铁在高温下反应:_______________________ 。工业炼铁的主要设备是__________________。
(3)车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产。乙醇(C2H5OH)完全燃烧的化学方程式为_______________,该反应属于____________(选填:“吸热”或“放热”)反应。
(4)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(5)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
18、阅读教材表格11—1内容,填写下列表格。
类别 氮肥 磷肥 钾肥 复合肥
名称 尿素 碳酸氢铵 磷矿粉 过磷酸钙 硫酸钾 氯化钾 硝酸钾 磷酸二氢铵
主要作用 促使作物的茎、叶生长______,叶色______ 促进作物根系发达,增强______能力,穗多粒满 促进作物生长健壮,增强______和______能力 —
缺少引起的症状 植株矮小瘦弱、叶片______ 生长迟缓,产量降低 容易倒伏,叶片边缘和尖端呈褐色 —
19、已知A与B、甲与乙均为初中化学常见的物质,其转化关系如图所示。
(1)若甲为氧气,则A的化学式为________ 。
(2)若甲是一种红色的氧化物,乙的溶液呈黄色,则反应的化学方程式为________ 。
(3)若甲、乙是常见的碱,A、B是常见的盐,而且当甲转化为B、乙转化为A时,都是与同一种气体X发生反应。
①A的化学式为________ ;②甲转化为B的化学方程式为________ 。
(4)若甲和A发生中和反应,而且当甲转化为B、乙转化为A时,都是与同一物质Y发生反应,则Y的化学式为________ ,此中和反应的化学方程式为________ 。
20、春节是中华民族的传统佳节,在访亲拜友中迎接新年的到来。表达自己的观点。
(1)花馍是最具山西特色的美食之一。春节蒸花馍会用到发酵粉,其主要成分是小苏打,化学式为______ 。蒸好的花馍松软多孔是______气体受热膨胀所留下的空隙。
(2)美食之后,洗碗—碗盘上附着的油污常用洗涤剂清洗,这是因为洗涤剂具有______作用。泡茶使用茶漏可以很好的分离茶叶和茶水,这相当于化学实验操作中的______。
(3)正月十五元宵节,很多地方有“点旺火”的习俗,有兴旺之意。垒旺火很有讲究,技术高超的师傅用大块煤炭垒成底小、肚大、顶尖、内空的宝瓶形状,这样才能达到燃烧净尽而旺火不塌。从燃烧的角度分析,这样的形状主要是为了______ ,旺火上方出现的蓝色火焰是______燃烧产生的。当然点旺火也有不利的一面,如______。
(4)节能出行靠高铁,中国高铁世界瞩目。列车车体主要采用铝合金材料,其优良的性能有______ (写一条);车头前端部采用玻璃钢,玻璃钢属于______材料;受电弓的滑板使用石墨材料,这体现了石墨具有良好的______性(写一条即可)。
三、简答题。
21、小明同学在做《粗盐中难溶性杂质的去除》实验时,用到了如图所示装置
(1)请指出该装置图中的一处错误;
(2)改进装置后过滤,发现滤液仍然浑浊,其原因可能是什么?(写出一条即可)
(3)经初步提纯所得精盐是否为纯净物?请写出你的判断和理由.
四、实验题。
22、氯化钠和氯化镁是重要的化工原料。某粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4等物质,为了从中提取较纯的氯化镁和氯化钠,设计以下实验方案:
请回答下列问题:
Ⅰ、步骤①溶解过程中用玻璃棒搅拌的目的是___________________________。
Ⅱ、步骤④⑤的顺序颠倒会引发的后果是______________________________。
Ⅲ、滤液乙中所含的溶质除氯化钠外还含有________;沉淀B中除含碳酸钙、碳酸钡外还含有________;在步骤⑦中若加入的盐酸略过量是否对实验结果有影响?原因是_____________________________________________________。
Ⅳ、写出步骤⑨中反应的化学方程式 _________________________________。
Ⅴ、实验最终所得的精盐的质量大于粗盐中氯化钠的质量,整个过程中产生新的NaCl的反应共有________个。
23、某学习小组在帮助实验员整理化学试剂时发现了一瓶标签残缺的无色溶液(如图所示),经实验员分析可知原瓶溶液中的溶质可能是NaHCO3、NaOH、Na2CO3、NaCl中的一种,请你对该试剂作出猜想并进行实验探究:
【提出问题】 这瓶试剂是什么溶液
【猜想与假设】
甲猜想:NaHCO3溶液
乙猜想:NaOH溶液
丙猜想:Na2CO3溶液
丁猜想:NaCl溶液
【查阅资料】 上述四种物质相关信息如下
【实验探究1】 取瓶中溶液少许于试管中,滴加几滴酚酞溶液,溶液变红。
【实验探究2】 另取瓶中溶液少许于试管中,滴加足量的稀盐酸,产生气泡。
【实验分析】 通过【实验探究1】 可知 同学的猜想一定错误。
甲同学仔细分析四种物质的相关信息表后发现自己的猜想错误,他的理由是 。
丙同学分析【实验探究2】 并结合以上同学的实验结论,认为原瓶溶液是Na2CO3溶液。
【实验探究2】 中发生反应的化学方程式为 。
【讨论质疑】 乙认为以上同学分析有漏洞,需要进一步实验确定,于是又进行了如下探究。
【实验探究3】 在【实验探究1】 试管中的红色溶液中滴加过量氯化钙溶液(中性),充分反应后,试管中溶液仍呈红色,但有白色沉淀产生。
【得出结论】 通过【实验探究3】 可证明这瓶试剂为 溶液,但已经部分变质。
【反思与拓展】学习小组反思了这瓶试剂因为 而变质,得出了该溶液正确的保存方法,若要除去该溶液变质部分所采用的方法是 (用化学反应方程式表示)。
五、计算类综合题。
24、某石油化工厂化验室的实验员用15%的NaOH溶液洗涤一定量石油产品中的残余硫酸,测得实验数据如下表。
实验序号 消耗NaOH溶液的质量 洗涤后溶液的pH
① 30 g pH<7
② 40 g pH=7
③ 50 g pH>7
(1)欲计算出一定量石油产品中所含H2SO4的质量,应该选择实验序号 的数据。
(2)若一定量石油产品中残余硫酸的质量为100 g,请计算该残余硫酸中溶质的质量分数。
2023—2024学年人教化学九年级下册第11单元 盐 化肥 单元练习附答案
人教第11单元 盐 化肥
一、选择题。
1、下列物质属于盐的是( )
A.H2SO4 B.CaCO3 C.Ca(OH)2 D.MnO2
【答案】.B
2、蒸馒头时,在发酵面团中加入某种物质,既能除去面团中的酸又能使馒头松软,该物质是( )
A.碳酸氢钠 B.生石灰 C.氢氧化钠 D.氯化钠
【答案】A
3、甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示,关于该转化关系图,下列说法正确的是( )
A. 如果丙是碳酸钠,乙是氢氧化钠,则甲是硝酸钠
B. 若甲、乙、丁都是氧化物,则丙一定是碳酸钙
C. 甲、乙、丙、丁之间的转化可以全部通过复分解反应实现
D. 若甲、乙、丙、丁均含有同一种元素,且乙可用来灭火,则丙一定是单质碳
【答案】C
4、下列关于酸、碱、盐的用途不合理的是( )
A. 盐酸除铁锈
B. 氢氧化钠改良酸性土壤
C. 硫酸铜与氢氧化钙混合配制农药波尔多液
D. 纯碱除油污
【答案】B
5、蒸馒头时,在发酵面团中加入某种物质,既能除去面团中的酸又能使馒头松软,该物质是( )
A.碳酸氢钠 B.生石灰 C.氢氧化钠 D.氯化钠
【答案】A
6、科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为4NH3+3O22X + 6H2O。下列说法中不正确的是( )
A.氨气在常压下液化是物理变化 B.X的化学式为N2
C.液氨具有可燃性,属于化学性质 D.液氨属于混合物
【答案】D
7、某同学想要鉴别NH4HCO3、NH4Cl、KCl三种化肥,操作过程如图所示,其中试剂甲和乙可能是( )
A.甲:水,乙:氢氧化钠
B.甲:熟石灰,乙:稀盐酸
C.甲:稀盐酸,乙:氯化钠溶液
D.甲:氢氧化钠,乙:硫酸钠溶液
【答案】B
8、粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
【答案】C
9、造成水体污染的主要原因是( )。
①天然水与空气、岩石和土壤的长期接触
②工业生产中的废气、废液和废渣的随意排放
③农业生产中化肥、农药的使用不当
④城市生活污水的大量排放
A.①② B.①③ C.②③ D.②③④
【答案】D
10、海水晒盐的原理是( )
A. 日晒风吹使氯化钠的溶解度降低
B. 日晒风吹使溶液由饱和变为不饱和
C. 日晒风吹使水分蒸发,食盐晶体析出
D. 日晒风吹使海水发生分解
【答案】C
11、碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一,它的俗称是( )
A.小苏打 B.苛性钠 C.烧碱 D.苏打
【答案】A
12、下列盐的用途中,错误的是( )
A.用含亚硝酸钠的工业盐制香肠 B.用碳酸钙做补钙剂
C.用氯化钠配制生理盐水 D.用碳酸氢钠做焙制糕点的发酵粉
【答案】A
13、以下常见化肥中,属于复合肥的是( )
A. K2SO4 B. NH4NO3 C. KNO3 D. Ca(H2PO4)2
【答案】C
14、下列实验操作正确的是( )
A. 过滤 B. 铁丝燃烧
C. 稀释浓硫酸 D. 溶液的pH
【答案】C
15、小明发现盆栽月季叶色发黄,经判断应施用氮肥。下列属于氮肥的是( )
A.K2SO4 B.CO(NH2)2 C.Ca3(PO4)2 D.KH2PO4
【答案】B
16、过氧化氢被称为“绿色氧化剂”,为了便于贮存和运输,工业上常将其转化为过碳酸钠晶体(2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠晶体失效的是( )
A.二氧化锰 B.石灰水 C.盐酸 D.氯化钠
【答案】D
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。
(2)工业炼铁的主要原理是一氧化碳和氧化铁在高温下反应:_______________________ 。工业炼铁的主要设备是__________________。
(3)车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产。乙醇(C2H5OH)完全燃烧的化学方程式为_______________,该反应属于____________(选填:“吸热”或“放热”)反应。
(4)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(5)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
【答案】CO2 + Ca(OH)2 == CaCO3↓+ H2O Fe2O3+3CO 2Fe+3CO2 高炉 C2H5OH+3O23H2O+2CO2 放热 2NaCl+ H2O2NaOH + H2↑+Cl2↑ BaCO3+2HCl == BaCl2 + H2O + CO2↑ 复分解反应
18、阅读教材表格11—1内容,填写下列表格。
类别 氮肥 磷肥 钾肥 复合肥
名称 尿素 碳酸氢铵 磷矿粉 过磷酸钙 硫酸钾 氯化钾 硝酸钾 磷酸二氢铵
主要作用 促使作物的茎、叶生长______,叶色______ 促进作物根系发达,增强______能力,穗多粒满 促进作物生长健壮,增强______和______能力 —
缺少引起的症状 植株矮小瘦弱、叶片______ 生长迟缓,产量降低 容易倒伏,叶片边缘和尖端呈褐色 —
【答案】茂盛 浓绿 抗旱抗寒 抗病虫害 抗倒伏 发黄
19、已知A与B、甲与乙均为初中化学常见的物质,其转化关系如图所示。
(1)若甲为氧气,则A的化学式为________ 。
(2)若甲是一种红色的氧化物,乙的溶液呈黄色,则反应的化学方程式为________ 。
(3)若甲、乙是常见的碱,A、B是常见的盐,而且当甲转化为B、乙转化为A时,都是与同一种气体X发生反应。
①A的化学式为________ ;②甲转化为B的化学方程式为________ 。
(4)若甲和A发生中和反应,而且当甲转化为B、乙转化为A时,都是与同一物质Y发生反应,则Y的化学式为________ ,此中和反应的化学方程式为________ 。
【答案】CH4 (或C2H5OH);
Fe2O3+6HCl= 2FeCl3+3H2O(或Fe2O3+3H2SO4= Fe2(SO4)3+3 H2O);
Na2CO3;Ca(OH)2+CO2=CaCO3↓+ H2O;CaO ;Ca(OH)2+2HCl= CaCl2+2 H2O
20、春节是中华民族的传统佳节,在访亲拜友中迎接新年的到来。表达自己的观点。
(1)花馍是最具山西特色的美食之一。春节蒸花馍会用到发酵粉,其主要成分是小苏打,化学式为______ 。蒸好的花馍松软多孔是______气体受热膨胀所留下的空隙。
(2)美食之后,洗碗—碗盘上附着的油污常用洗涤剂清洗,这是因为洗涤剂具有______作用。泡茶使用茶漏可以很好的分离茶叶和茶水,这相当于化学实验操作中的______。
(3)正月十五元宵节,很多地方有“点旺火”的习俗,有兴旺之意。垒旺火很有讲究,技术高超的师傅用大块煤炭垒成底小、肚大、顶尖、内空的宝瓶形状,这样才能达到燃烧净尽而旺火不塌。从燃烧的角度分析,这样的形状主要是为了______ ,旺火上方出现的蓝色火焰是______燃烧产生的。当然点旺火也有不利的一面,如______。
(4)节能出行靠高铁,中国高铁世界瞩目。列车车体主要采用铝合金材料,其优良的性能有______ (写一条);车头前端部采用玻璃钢,玻璃钢属于______材料;受电弓的滑板使用石墨材料,这体现了石墨具有良好的______性(写一条即可)。
【答案】 (1)NaHCO3 CO2 (2)乳化 (2)过滤
(3)增大与氧气的接触面积,使燃烧更充分 CO 造成空气污染
(4)密度小 复合 导电
三、简答题。
21、小明同学在做《粗盐中难溶性杂质的去除》实验时,用到了如图所示装置
(1)请指出该装置图中的一处错误;
(2)改进装置后过滤,发现滤液仍然浑浊,其原因可能是什么?(写出一条即可)
(3)经初步提纯所得精盐是否为纯净物?请写出你的判断和理由.
【答案】
(1)缺少玻璃棒引流
(2)滤纸破损(或滤液高于滤纸边缘或盛接滤液的烧杯不干净等)
(3)不是纯净物;精盐中含有氯化钠、氯化钙、氯化镁等。
四、实验题。
22、氯化钠和氯化镁是重要的化工原料。某粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4等物质,为了从中提取较纯的氯化镁和氯化钠,设计以下实验方案:
请回答下列问题:
Ⅰ、步骤①溶解过程中用玻璃棒搅拌的目的是___________________________。
Ⅱ、步骤④⑤的顺序颠倒会引发的后果是______________________________。
Ⅲ、滤液乙中所含的溶质除氯化钠外还含有________;沉淀B中除含碳酸钙、碳酸钡外还含有________;在步骤⑦中若加入的盐酸略过量是否对实验结果有影响?原因是_____________________________________________________。
Ⅳ、写出步骤⑨中反应的化学方程式 _________________________________。
Ⅴ、实验最终所得的精盐的质量大于粗盐中氯化钠的质量,整个过程中产生新的NaCl的反应共有________个。
【答案】Ⅰ、加快溶解的速度
Ⅱ、精盐中会混有氯化钡或无法除去过量的氯化钡
Ⅲ、氢氧化钠、碳酸钠 硫酸钡 无影响,加热蒸发时氯化氢会挥发
Ⅳ、Mg(OH)2+2HCl===Mg Cl2+2H2O Ⅴ、6
23、某学习小组在帮助实验员整理化学试剂时发现了一瓶标签残缺的无色溶液(如图所示),经实验员分析可知原瓶溶液中的溶质可能是NaHCO3、NaOH、Na2CO3、NaCl中的一种,请你对该试剂作出猜想并进行实验探究:
【提出问题】 这瓶试剂是什么溶液
【猜想与假设】
甲猜想:NaHCO3溶液
乙猜想:NaOH溶液
丙猜想:Na2CO3溶液
丁猜想:NaCl溶液
【查阅资料】 上述四种物质相关信息如下
【实验探究1】 取瓶中溶液少许于试管中,滴加几滴酚酞溶液,溶液变红。
【实验探究2】 另取瓶中溶液少许于试管中,滴加足量的稀盐酸,产生气泡。
【实验分析】 通过【实验探究1】 可知 同学的猜想一定错误。
甲同学仔细分析四种物质的相关信息表后发现自己的猜想错误,他的理由是 。
丙同学分析【实验探究2】 并结合以上同学的实验结论,认为原瓶溶液是Na2CO3溶液。
【实验探究2】 中发生反应的化学方程式为 。
【讨论质疑】 乙认为以上同学分析有漏洞,需要进一步实验确定,于是又进行了如下探究。
【实验探究3】 在【实验探究1】 试管中的红色溶液中滴加过量氯化钙溶液(中性),充分反应后,试管中溶液仍呈红色,但有白色沉淀产生。
【得出结论】 通过【实验探究3】 可证明这瓶试剂为 溶液,但已经部分变质。
【反思与拓展】学习小组反思了这瓶试剂因为 而变质,得出了该溶液正确的保存方法,若要除去该溶液变质部分所采用的方法是 (用化学反应方程式表示)。
【答案】丁 在该温度下,碳酸氢钠的饱和溶液的溶质质量分数小于10%
氢氧化钠 敞口放置
五、计算类综合题。
24、某石油化工厂化验室的实验员用15%的NaOH溶液洗涤一定量石油产品中的残余硫酸,测得实验数据如下表。
实验序号 消耗NaOH溶液的质量 洗涤后溶液的pH
① 30 g pH<7
② 40 g pH=7
③ 50 g pH>7
(1)欲计算出一定量石油产品中所含H2SO4的质量,应该选择实验序号 的数据。
(2)若一定量石油产品中残余硫酸的质量为100 g,请计算该残余硫酸中溶质的质量分数。
【答案】(1)②
(2)设该残余硫酸中溶质的质量为x。
2NaOH + H2SO4Na2SO4+2H2O
80 98
40 g×15% x
=
x=7.35 g
该残余硫酸中溶质的质量分数为
×100%=7.35%。
答:该残余硫酸中溶质的质量分数为7.35%。
同课章节目录
