第4章 基础实验3 物质燃烧的条件课件(共17张PPT)-2023-2024学年化学沪教版(全国)九年级上册
文档属性
| 名称 | 第4章 基础实验3 物质燃烧的条件课件(共17张PPT)-2023-2024学年化学沪教版(全国)九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-27 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
基础实验三 物质燃烧的条件
生活中常见的燃烧现象
化学实验中物质的燃烧
1、着火点是物质燃烧时的最低温度 . 2、着火点是物质固有的属性,不同的物质着火点不同
物质 白磷 红磷 纸 木材 木炭 无烟煤
着火点/0C 40 240 180 250-330 320-370 700-750
认识“着火点”认识“着火点”
⑴提出问题:燃烧需要什么条件?
⑵作出猜想:燃烧需要的条件是 。
⑶设计实验:实验方法是 。
⑷进行实验:实验的现象是 。
⑸得出结论:燃烧的条件是 。
猜想 (填“正确”或“不正确”)。
我来探究:燃烧的条件
学生分小组讨论完成导学案的内容
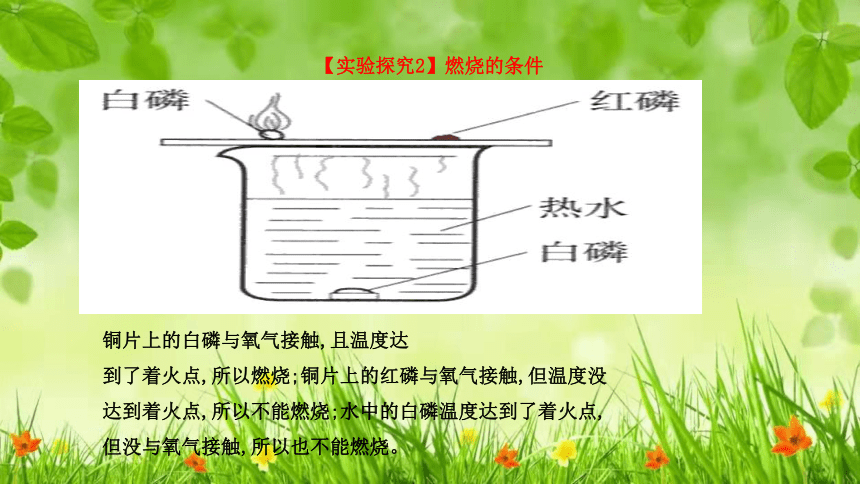
【实验探究2】燃烧的条件
铜片上的白磷与氧气接触,且温度达
到了着火点,所以燃烧;铜片上的红磷与氧气接触,但温度没
达到着火点,所以不能燃烧;水中的白磷温度达到了着火点,
但没与氧气接触,所以也不能燃烧。
归纳总结:物质燃烧的条件(同时满足)
(1)物质具有_______。
(2)可燃物与_____接触。
(3)可燃物达到燃烧所需要的_________。
可燃性
氧气
最低温度
应用于反思:如何让水中的白磷和铜片的红磷燃烧起来?
我们一起来研究燃烧的条件
分别点燃一根小木条和一小块煤块,比较哪个容易被点燃。
小木条容易被点燃
温度必须达到可燃物燃烧所需要的最低温度
着火点着火点
实验 设计意图 实验现象 实验结论
1
2
3
实验探讨:物质燃烧的条件
请你分析3组对比实验,归纳物质燃烧的条件。
燃烧与物质性质的关系
木条燃烧,
玻璃棒不燃烧
物质必须是可燃物
燃烧与氧气的关系
不罩玻璃杯的蜡烛燃烧时间长
燃烧需要
氧气
温度达到物质的着火点
小木条燃烧,
小煤块不燃烧
燃烧与温度
的关系
CO的物理性质及毒性:
(1)无色、无味的剧毒气体,极易与血红蛋白结合,使之丧失
了输氧的功能。
(2)发生CO中毒时,应立即打开门窗通风,并迅速将中毒者移
至空气清新处,严重者送医院救治。
含碳、氢元素的可燃物燃烧:
(1)完全燃烧时,碳、氢元素分别生成二氧化碳和水。
(2)不完全燃烧时,部分碳、氢元素生成一氧化碳、
碳氢化合物等有毒气体和微小的炭黑颗粒等物质。
不完全燃烧的现象及危害
解释下面实验:
1、为什么烧杯中的白磷不燃烧?
原因是 ;
2、为什么铜片上的红磷不燃烧?
原因是 ;
3、为什么铜片上的白磷燃烧?
原因是① ;
② ;
③ ;
没有跟氧气接触
温度未达到着火点
跟氧气接触
温度达到着火点
白磷具有可燃性
小组比赛:
——灭火
用不同的方法熄灭蜡烛
创设场景 亲身体验
用多支燃烧的蜡烛模拟火灾场面,并给出一些灭火的材料(水、细砂、湿抹布、扇子等),让学生开动脑筋,展开丰富联想。然后让学生上讲台展示自己的灭火方法,并说明自己的灭火原理。
实验演示:粉尘爆炸实验
生活防火防爆常识:
常见的易燃易爆物:
(1)可燃性气体:氢气、一氧化碳、甲烷等,这些气体在点燃
前必须_________。
易燃、可燃性液体:酒精、汽油等
(2)可燃性粉尘:面粉、煤粉等。在产生可燃性粉尘的场所,
应杜绝一切火种。
检验纯度
课堂小结
1、燃烧的条件:
(1)物质具有可燃性
(2)可燃物与空气(或氧气)接触
(3)温度达到可燃物的着火点
2、灭火的原理:
(1)清除可燃物
(2)隔离空气(或氧气)
(3)使温度降低到着火点以下
板书设计:
物质燃烧的条件
1、定义:燃烧是可燃物跟氧气发生的发光、发热的氧化反应 。
2、燃烧的条件:
(1)物质具有可燃性;
(2)可燃物与空气(或氧气)接触 燃烧
(3)温度达到可燃物的着火点
同时具备
3、灭火的原理:
(1)清除可燃物;
(2)隔离空气(或氧气) 熄灭
(3)使温度降低到着火点以下
三者任意满足其一
基础实验三 物质燃烧的条件
生活中常见的燃烧现象
化学实验中物质的燃烧
1、着火点是物质燃烧时的最低温度 . 2、着火点是物质固有的属性,不同的物质着火点不同
物质 白磷 红磷 纸 木材 木炭 无烟煤
着火点/0C 40 240 180 250-330 320-370 700-750
认识“着火点”认识“着火点”
⑴提出问题:燃烧需要什么条件?
⑵作出猜想:燃烧需要的条件是 。
⑶设计实验:实验方法是 。
⑷进行实验:实验的现象是 。
⑸得出结论:燃烧的条件是 。
猜想 (填“正确”或“不正确”)。
我来探究:燃烧的条件
学生分小组讨论完成导学案的内容
【实验探究2】燃烧的条件
铜片上的白磷与氧气接触,且温度达
到了着火点,所以燃烧;铜片上的红磷与氧气接触,但温度没
达到着火点,所以不能燃烧;水中的白磷温度达到了着火点,
但没与氧气接触,所以也不能燃烧。
归纳总结:物质燃烧的条件(同时满足)
(1)物质具有_______。
(2)可燃物与_____接触。
(3)可燃物达到燃烧所需要的_________。
可燃性
氧气
最低温度
应用于反思:如何让水中的白磷和铜片的红磷燃烧起来?
我们一起来研究燃烧的条件
分别点燃一根小木条和一小块煤块,比较哪个容易被点燃。
小木条容易被点燃
温度必须达到可燃物燃烧所需要的最低温度
着火点着火点
实验 设计意图 实验现象 实验结论
1
2
3
实验探讨:物质燃烧的条件
请你分析3组对比实验,归纳物质燃烧的条件。
燃烧与物质性质的关系
木条燃烧,
玻璃棒不燃烧
物质必须是可燃物
燃烧与氧气的关系
不罩玻璃杯的蜡烛燃烧时间长
燃烧需要
氧气
温度达到物质的着火点
小木条燃烧,
小煤块不燃烧
燃烧与温度
的关系
CO的物理性质及毒性:
(1)无色、无味的剧毒气体,极易与血红蛋白结合,使之丧失
了输氧的功能。
(2)发生CO中毒时,应立即打开门窗通风,并迅速将中毒者移
至空气清新处,严重者送医院救治。
含碳、氢元素的可燃物燃烧:
(1)完全燃烧时,碳、氢元素分别生成二氧化碳和水。
(2)不完全燃烧时,部分碳、氢元素生成一氧化碳、
碳氢化合物等有毒气体和微小的炭黑颗粒等物质。
不完全燃烧的现象及危害
解释下面实验:
1、为什么烧杯中的白磷不燃烧?
原因是 ;
2、为什么铜片上的红磷不燃烧?
原因是 ;
3、为什么铜片上的白磷燃烧?
原因是① ;
② ;
③ ;
没有跟氧气接触
温度未达到着火点
跟氧气接触
温度达到着火点
白磷具有可燃性
小组比赛:
——灭火
用不同的方法熄灭蜡烛
创设场景 亲身体验
用多支燃烧的蜡烛模拟火灾场面,并给出一些灭火的材料(水、细砂、湿抹布、扇子等),让学生开动脑筋,展开丰富联想。然后让学生上讲台展示自己的灭火方法,并说明自己的灭火原理。
实验演示:粉尘爆炸实验
生活防火防爆常识:
常见的易燃易爆物:
(1)可燃性气体:氢气、一氧化碳、甲烷等,这些气体在点燃
前必须_________。
易燃、可燃性液体:酒精、汽油等
(2)可燃性粉尘:面粉、煤粉等。在产生可燃性粉尘的场所,
应杜绝一切火种。
检验纯度
课堂小结
1、燃烧的条件:
(1)物质具有可燃性
(2)可燃物与空气(或氧气)接触
(3)温度达到可燃物的着火点
2、灭火的原理:
(1)清除可燃物
(2)隔离空气(或氧气)
(3)使温度降低到着火点以下
板书设计:
物质燃烧的条件
1、定义:燃烧是可燃物跟氧气发生的发光、发热的氧化反应 。
2、燃烧的条件:
(1)物质具有可燃性;
(2)可燃物与空气(或氧气)接触 燃烧
(3)温度达到可燃物的着火点
同时具备
3、灭火的原理:
(1)清除可燃物;
(2)隔离空气(或氧气) 熄灭
(3)使温度降低到着火点以下
三者任意满足其一
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
