湖北省利川市部分中学2023-2024学年高一上学期11月期中考试化学试题(含答案)
文档属性
| 名称 | 湖北省利川市部分中学2023-2024学年高一上学期11月期中考试化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 534.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-27 00:00:00 | ||
图片预览



文档简介
利川市部分中学2023-2024学年高一上学期11月期中考试
化学试卷
可能用到的相对原子质量:H 1 C 12 O 16 23
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项
是符合题目要求。
1.化学与生活等密切相关,下列说法错误的是( )
A.冰水混合物属于纯净物
B.“铁质菜刀生锈”与氧化还原反应有关
C.为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
D.维生素C可将转变为,所以维生素C具有还原性,常用作抗氧化剂
2.豆腐是大众喜爱的传统食品,文斗柴火豆腐的传统制法的主要过程如下图所示,下列说法不正确的是( )
磨豆 过滤 煮浆 点卤
A.“磨豆”过程为物理变化
B.“过滤”所得豆浆属于胶体
C.“煮浆”通过高温将豆浆中混入的土壤菌(包括大量的芽孢菌)杀死
D.“点卤”过程使用的石膏()为非电解质
3.下列属于能导电的分散系是( )
A.液态 B.浓氨水 C.熔融 D.酒精溶液
4.下列反应中,水只做还原剂的氧化还原反应是( )
A.
B.
C.
D.
5.通过分门别类的研究,可以发现物质及其变化的规律。下列有关物质的分类正确的是( )
选项 碱 酸 碱性氧化物 酸性氧化物 纯净物
A 液氯
B 纯碱 碘酒
C 盐酸
D 空气
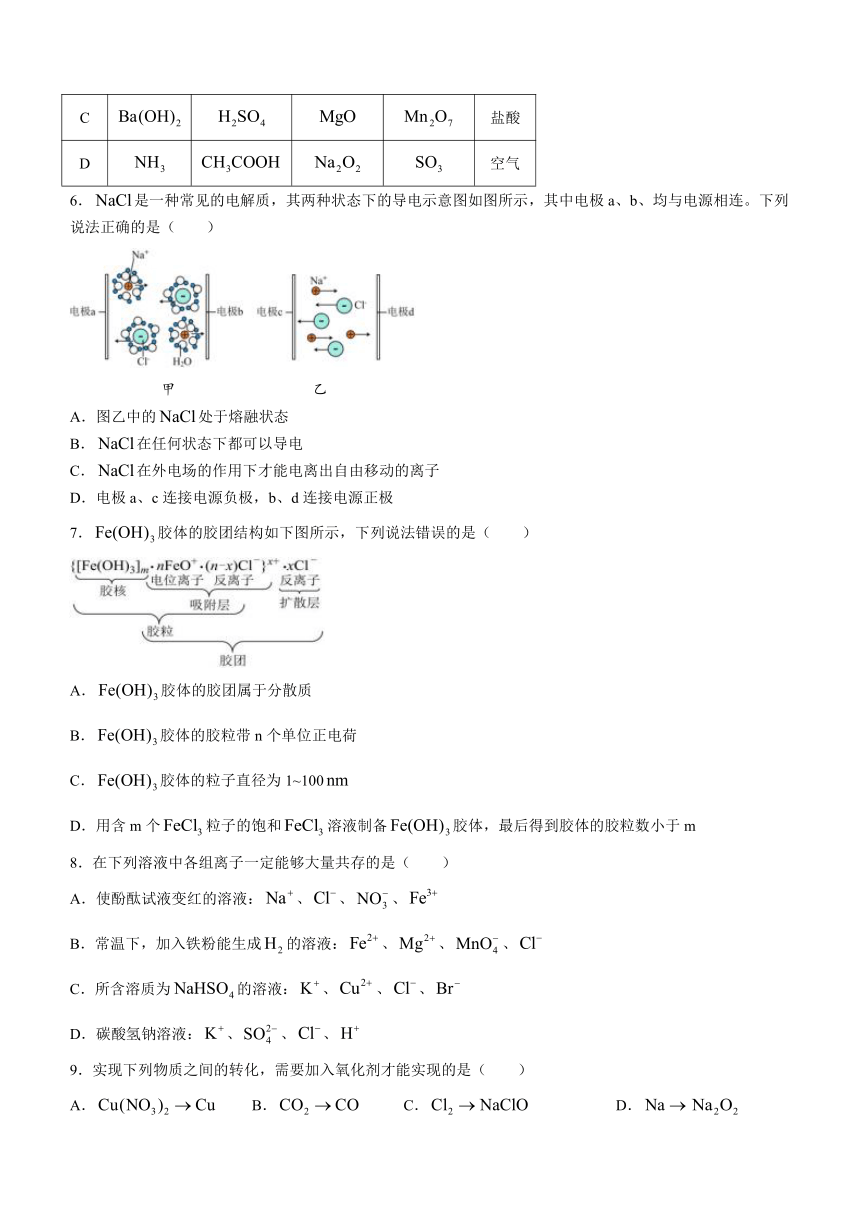
6.是一种常见的电解质,其两种状态下的导电示意图如图所示,其中电极a、b、均与电源相连。下列说法正确的是( )
甲 乙
A.图乙中的处于熔融状态
B.在任何状态下都可以导电
C.在外电场的作用下才能电离出自由移动的离子
D.电极a、c连接电源负极,b、d连接电源正极
7.胶体的胶团结构如下图所示,下列说法错误的是( )
A.胶体的胶团属于分散质
B.胶体的胶粒带n个单位正电荷
C.胶体的粒子直径为1~100
D.用含m个粒子的饱和溶液制备胶体,最后得到胶体的胶粒数小于m
8.在下列溶液中各组离子一定能够大量共存的是( )
A.使酚酞试液变红的溶液:、、、
B.常温下,加入铁粉能生成的溶液:、、、
C.所含溶质为的溶液:、、、
D.碳酸氢钠溶液:、、、
9.实现下列物质之间的转化,需要加入氧化剂才能实现的是( )
A. B. C. D.
10.下列离子方程式正确的是( )
A.通入冷的溶液:
B.放入水中:
C.饱和溶液中通入过量
D.溶液与少量的溶液混合:
11.元素铬()的几种化合物存在如图转化关系,下列判断不正确的是( )
A.反应①③中铬元素的化合价均未发生变化
B.反应①表明有酸性氧化物的性质
C.反应②利用了氧化性
D.反应③的离子方程式为
12.已知反应、和可以发生。下列说法正确的是( )
A.还原性:
B.氧化性:
C.反应可以发生
D.反应可以发生
13.对于下列反应说法错误的是( )
A.中,被氧化的分子与被还原的分子的个数比为
B.中,氧化剂和还原剂的物质个数之比为
C.中,既是氧化产物又是还原产物
D.既是分解反应又是氧化还原反应
14.滴有酚酞的溶液显红色,在上述溶液中分别滴加X溶液后有下列现象。下列说法不
正确的是( )
序号 装置 X溶液 现象
盐酸 溶液红色褪去,无沉淀,灯泡亮度没有明显变化
溶液 溶液红色不变,有白色沉淀生成,灯泡亮度没有明显变化
溶液 溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗
A.实验中溶液红色褪去,说明发生了反应:
B.实验中溶液红色不变,且灯泡亮度没有明显变化,说明溶液中依然存在大量的与
C.实验中溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗,说明发生了反应;
D.将实验中溶液换成溶液,现象与原实验中的现象相同
15.某无色、澄清溶液中可能含有①、②、③、④、⑤、⑥、⑦中的几种,且每种离子的数目相等。依次进行下列实验,每步所加试剂均过量,观察到的现象如下:
步骤 操作 现象
(1) 取部分溶液,滴入2滴紫色石蕊溶液 溶液变红
(2) 另取部分溶液,加入适量固体 产生无色无味的气体和白色沉淀
(3) 向溶液中滴加溶液和稀盐酸 有白色沉淀生成
(4) 将(3)中所得沉淀过滤,向滤液中加入溶液和稀硝酸 有白色沉淀生成
下列结论正确的是( )
A.该实验无法确定是否含有③
B.肯定含有的离子是②③④⑦
C.可能含有的离子是①③
D.①③⑤⑥离子肯定不含有
二、非选择题:本题共四个小题,共55分。
16.(15分)有一含、和的混合物,某同学设计如图所示的实验装置,通过测量反应产生的和的质量,来确定该混合物中各组分的质量分数。
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是_________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开弹簧夹、,关闭,缓缓鼓入空气数分钟,其目的是_________。
④关闭弹簧夹、,打开,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为_________(写出其中一个即可)。
⑤打开弹簧夹,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,会分别导致、、的质量分数测定结果_________、_________、_________(填“偏大”、“偏小”、“不影响”)。
②E处干燥管中盛放的药品是碱石灰,其作用是_________,如果实验中没有该装置,则会导致测量结果的质量分数_________(填“偏大”“偏小”或“无影响”)。
③若样品质量为,反应后C、D装置增加的质量分别为、,则混合物中的质量分数为_________(用含、、的代数式表示)。
17.(12分)用下列装置制备并检验的性质,请按要求回答相关问题:
I II III IV
(1)装置中盛放浓盐酸的仪器名称是_________,烧杯中溶液的作用是_________。
(2)装置应该接入到装置中集气瓶前面,其目的是_________。
(3)为了探究干燥的氯气是否有漂白性,选择装置进行相关实验,若从口进气,装置中的现象是_________,其中无水的作用是_________。
(4)写出装置中发生反应的化学方程式_________。
18.(12分)某溶液中只可能大量含有、、、、、、中的若干种,对其进行如下实验:
:取少量该溶液于试管中,加入过量溶液,产生白色沉淀,过滤;
:向中所得滤渣中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
:向中所得滤液中加入足量硝酸酸化后,再加入溶液,有白色沉淀生成。
回答下列问题:
(1)无需实验即可推断溶液中一定不会大量存在的离子为_________。
(2)实验中过滤时用到的玻璃仪器为烧杯、_________。
(3)实验中发生反应的离子方程式为_________。
(4)实验_________(填“能”或“不能”)说明该溶液中存在;若能请说明理由,若不能请简单设计实验证明该溶液中是否存在:_________。
(5)上述实验_________(填“能”或“不能”)说明该溶液中存在,若能请说明理由,若不能请简单设计实验证明该溶液中是否存在:_________。
19.(16分).氧化还原反应与离子反应在生产生活与科学实验中有重要作用,过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.
B.
C.
D.
(1)上述反应中,仅体现氧化性的反应是_________(填字母序号,下同),既体现氧化性又体现还原性的反应是_________,、、的氧化性由强到弱的顺序是_________。
(2)某酸性反应体系中发生的一个属于氧化还原的离子反应,反应物和生成物共六种微粒:、、、、、,则反应的离子方程式为_________。
.氯元素是中学化学中常见的重要非金属元素之一,氯元素的单质及其化合物在生产与生活中有着重要的用途,依据所学知识完成下列问题:
(3)实验室利用制备氯气的离子方程式是_________:若多余的氯气用氢氧化钠溶液吸收,其离子方程式为_________。
.在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
①将软锰矿(主要成分)粉碎后,与固体混合,通入空气充分焙烧,生成暗绿色)
熔融态物质。
②冷却,将固体研细,用溶液浸取,过滤,得暗绿色溶液。
③向暗绿色溶液中通入,溶液变为紫红色。
④将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得固体。
资料:为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应(的化合价既升高又降低)。
(4)①中生成的化学方程式是_________。
(5)②中浸取时用溶液的原因是_________。
(6)③中产生两种盐,写出③的方程式,并用单线桥标出电子转移_________。
利川市部分中学2023-2024学年高一上学期11月期中考试
化学试题答案
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C D B B A A B C D B D D A D B
16.(除标注外,每空2分,共15分)
(1)①检查装置气密性③除去装置中的水蒸气和二氧化碳
④或者
(2)①偏小(1分)、偏小(1分)、偏大(1分)
②防止空气中的和水蒸气进入D中影响测定结果:偏大 ③
17.(每空2分,共12分)
(1)分液漏斗;氯气尾气处理,防止污染空气 (2)除去氯气中的和水蒸气
(3)a处布条无变化,b处红色布条褪色:干燥吸水 (4)(写“=”也给分)
18.(除标注外,每空2分,共12分)
(1)(2)漏斗、玻璃棒
(3)
(4)不能(1分)取原溶液少许,加入足量硝酸酸化后,再加入溶液,若有白色沉淀生成则证明含,反之则不含
(5)不能(1分)取洁净的铂丝,蘸取原溶液少许,在酒精灯外焰上灼烧,若透过蓝色钴玻璃观察到火焰呈紫色则证明含,反之则不含
19.(除标注外每空2分,共16分)
(1)D(1分)C(1分)
(2)
(3)
(4)
(5)保持溶液呈强碱性,防止发生歧化反应
(6)
化学试卷
可能用到的相对原子质量:H 1 C 12 O 16 23
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项
是符合题目要求。
1.化学与生活等密切相关,下列说法错误的是( )
A.冰水混合物属于纯净物
B.“铁质菜刀生锈”与氧化还原反应有关
C.为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
D.维生素C可将转变为,所以维生素C具有还原性,常用作抗氧化剂
2.豆腐是大众喜爱的传统食品,文斗柴火豆腐的传统制法的主要过程如下图所示,下列说法不正确的是( )
磨豆 过滤 煮浆 点卤
A.“磨豆”过程为物理变化
B.“过滤”所得豆浆属于胶体
C.“煮浆”通过高温将豆浆中混入的土壤菌(包括大量的芽孢菌)杀死
D.“点卤”过程使用的石膏()为非电解质
3.下列属于能导电的分散系是( )
A.液态 B.浓氨水 C.熔融 D.酒精溶液
4.下列反应中,水只做还原剂的氧化还原反应是( )
A.
B.
C.
D.
5.通过分门别类的研究,可以发现物质及其变化的规律。下列有关物质的分类正确的是( )
选项 碱 酸 碱性氧化物 酸性氧化物 纯净物
A 液氯
B 纯碱 碘酒
C 盐酸
D 空气
6.是一种常见的电解质,其两种状态下的导电示意图如图所示,其中电极a、b、均与电源相连。下列说法正确的是( )
甲 乙
A.图乙中的处于熔融状态
B.在任何状态下都可以导电
C.在外电场的作用下才能电离出自由移动的离子
D.电极a、c连接电源负极,b、d连接电源正极
7.胶体的胶团结构如下图所示,下列说法错误的是( )
A.胶体的胶团属于分散质
B.胶体的胶粒带n个单位正电荷
C.胶体的粒子直径为1~100
D.用含m个粒子的饱和溶液制备胶体,最后得到胶体的胶粒数小于m
8.在下列溶液中各组离子一定能够大量共存的是( )
A.使酚酞试液变红的溶液:、、、
B.常温下,加入铁粉能生成的溶液:、、、
C.所含溶质为的溶液:、、、
D.碳酸氢钠溶液:、、、
9.实现下列物质之间的转化,需要加入氧化剂才能实现的是( )
A. B. C. D.
10.下列离子方程式正确的是( )
A.通入冷的溶液:
B.放入水中:
C.饱和溶液中通入过量
D.溶液与少量的溶液混合:
11.元素铬()的几种化合物存在如图转化关系,下列判断不正确的是( )
A.反应①③中铬元素的化合价均未发生变化
B.反应①表明有酸性氧化物的性质
C.反应②利用了氧化性
D.反应③的离子方程式为
12.已知反应、和可以发生。下列说法正确的是( )
A.还原性:
B.氧化性:
C.反应可以发生
D.反应可以发生
13.对于下列反应说法错误的是( )
A.中,被氧化的分子与被还原的分子的个数比为
B.中,氧化剂和还原剂的物质个数之比为
C.中,既是氧化产物又是还原产物
D.既是分解反应又是氧化还原反应
14.滴有酚酞的溶液显红色,在上述溶液中分别滴加X溶液后有下列现象。下列说法不
正确的是( )
序号 装置 X溶液 现象
盐酸 溶液红色褪去,无沉淀,灯泡亮度没有明显变化
溶液 溶液红色不变,有白色沉淀生成,灯泡亮度没有明显变化
溶液 溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗
A.实验中溶液红色褪去,说明发生了反应:
B.实验中溶液红色不变,且灯泡亮度没有明显变化,说明溶液中依然存在大量的与
C.实验中溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗,说明发生了反应;
D.将实验中溶液换成溶液,现象与原实验中的现象相同
15.某无色、澄清溶液中可能含有①、②、③、④、⑤、⑥、⑦中的几种,且每种离子的数目相等。依次进行下列实验,每步所加试剂均过量,观察到的现象如下:
步骤 操作 现象
(1) 取部分溶液,滴入2滴紫色石蕊溶液 溶液变红
(2) 另取部分溶液,加入适量固体 产生无色无味的气体和白色沉淀
(3) 向溶液中滴加溶液和稀盐酸 有白色沉淀生成
(4) 将(3)中所得沉淀过滤,向滤液中加入溶液和稀硝酸 有白色沉淀生成
下列结论正确的是( )
A.该实验无法确定是否含有③
B.肯定含有的离子是②③④⑦
C.可能含有的离子是①③
D.①③⑤⑥离子肯定不含有
二、非选择题:本题共四个小题,共55分。
16.(15分)有一含、和的混合物,某同学设计如图所示的实验装置,通过测量反应产生的和的质量,来确定该混合物中各组分的质量分数。
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是_________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开弹簧夹、,关闭,缓缓鼓入空气数分钟,其目的是_________。
④关闭弹簧夹、,打开,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为_________(写出其中一个即可)。
⑤打开弹簧夹,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,会分别导致、、的质量分数测定结果_________、_________、_________(填“偏大”、“偏小”、“不影响”)。
②E处干燥管中盛放的药品是碱石灰,其作用是_________,如果实验中没有该装置,则会导致测量结果的质量分数_________(填“偏大”“偏小”或“无影响”)。
③若样品质量为,反应后C、D装置增加的质量分别为、,则混合物中的质量分数为_________(用含、、的代数式表示)。
17.(12分)用下列装置制备并检验的性质,请按要求回答相关问题:
I II III IV
(1)装置中盛放浓盐酸的仪器名称是_________,烧杯中溶液的作用是_________。
(2)装置应该接入到装置中集气瓶前面,其目的是_________。
(3)为了探究干燥的氯气是否有漂白性,选择装置进行相关实验,若从口进气,装置中的现象是_________,其中无水的作用是_________。
(4)写出装置中发生反应的化学方程式_________。
18.(12分)某溶液中只可能大量含有、、、、、、中的若干种,对其进行如下实验:
:取少量该溶液于试管中,加入过量溶液,产生白色沉淀,过滤;
:向中所得滤渣中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
:向中所得滤液中加入足量硝酸酸化后,再加入溶液,有白色沉淀生成。
回答下列问题:
(1)无需实验即可推断溶液中一定不会大量存在的离子为_________。
(2)实验中过滤时用到的玻璃仪器为烧杯、_________。
(3)实验中发生反应的离子方程式为_________。
(4)实验_________(填“能”或“不能”)说明该溶液中存在;若能请说明理由,若不能请简单设计实验证明该溶液中是否存在:_________。
(5)上述实验_________(填“能”或“不能”)说明该溶液中存在,若能请说明理由,若不能请简单设计实验证明该溶液中是否存在:_________。
19.(16分).氧化还原反应与离子反应在生产生活与科学实验中有重要作用,过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A.
B.
C.
D.
(1)上述反应中,仅体现氧化性的反应是_________(填字母序号,下同),既体现氧化性又体现还原性的反应是_________,、、的氧化性由强到弱的顺序是_________。
(2)某酸性反应体系中发生的一个属于氧化还原的离子反应,反应物和生成物共六种微粒:、、、、、,则反应的离子方程式为_________。
.氯元素是中学化学中常见的重要非金属元素之一,氯元素的单质及其化合物在生产与生活中有着重要的用途,依据所学知识完成下列问题:
(3)实验室利用制备氯气的离子方程式是_________:若多余的氯气用氢氧化钠溶液吸收,其离子方程式为_________。
.在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
①将软锰矿(主要成分)粉碎后,与固体混合,通入空气充分焙烧,生成暗绿色)
熔融态物质。
②冷却,将固体研细,用溶液浸取,过滤,得暗绿色溶液。
③向暗绿色溶液中通入,溶液变为紫红色。
④将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得固体。
资料:为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应(的化合价既升高又降低)。
(4)①中生成的化学方程式是_________。
(5)②中浸取时用溶液的原因是_________。
(6)③中产生两种盐,写出③的方程式,并用单线桥标出电子转移_________。
利川市部分中学2023-2024学年高一上学期11月期中考试
化学试题答案
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C D B B A A B C D B D D A D B
16.(除标注外,每空2分,共15分)
(1)①检查装置气密性③除去装置中的水蒸气和二氧化碳
④或者
(2)①偏小(1分)、偏小(1分)、偏大(1分)
②防止空气中的和水蒸气进入D中影响测定结果:偏大 ③
17.(每空2分,共12分)
(1)分液漏斗;氯气尾气处理,防止污染空气 (2)除去氯气中的和水蒸气
(3)a处布条无变化,b处红色布条褪色:干燥吸水 (4)(写“=”也给分)
18.(除标注外,每空2分,共12分)
(1)(2)漏斗、玻璃棒
(3)
(4)不能(1分)取原溶液少许,加入足量硝酸酸化后,再加入溶液,若有白色沉淀生成则证明含,反之则不含
(5)不能(1分)取洁净的铂丝,蘸取原溶液少许,在酒精灯外焰上灼烧,若透过蓝色钴玻璃观察到火焰呈紫色则证明含,反之则不含
19.(除标注外每空2分,共16分)
(1)D(1分)C(1分)
(2)
(3)
(4)
(5)保持溶液呈强碱性,防止发生歧化反应
(6)
同课章节目录
