专题1 有机化学的发展及研究思路 单元检测(含解析) 2023-2024学年高二下学期化学苏教版(2019)选择性必修3
文档属性
| 名称 | 专题1 有机化学的发展及研究思路 单元检测(含解析) 2023-2024学年高二下学期化学苏教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 256.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-28 00:00:00 | ||
图片预览



文档简介
专题1 有机化学的发展及研究思路 单元检测
一、单选题
1.下列各组混合物,能用分液漏斗进行分离的是( )
A.汽油和植物油 B.水和四氯化碳
C.酒精和水 D.溴和四氯化碳
2.下列实验操作中错误的是( )
A.蒸发操作时,应使混合物中的水分少量剩余时,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
3.从海带中提取碘的一种实验流程如图所示,下列说法错误的是( )
A.灼烧海带可在坩埚中进行
B.操作①为加水浸泡、过滤、洗涤残渣
C.反应②中发生的主要反应为
D.试剂③可以选用无水乙醇
4.十九世纪,初步发现元素周期律并发明元素周期表的科学家是( )
A.道尔顿 B.门捷列夫 C.舍勒 D.拉瓦锡
5.提出元素周期律并绘制了第一个元素周期表的科学家是( )
A.盖斯 B.阿伏加德罗 C.门捷列夫 D.道尔顿
6.青蒿素是高效的抗疟疾药,为无色针状晶体,易溶于有机溶剂,在水中几乎不溶,熔点为156℃~157℃,热稳定性差。提取青蒿素的主要工艺如下。(已知: 乙醚的沸点为35℃)
下列说法不正确的是( )
A.破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素浸取率
B.操作I需要用到玻璃仪器有漏斗、玻璃棒、烧杯
C.操作II蒸馏时最好选用水浴加热
D.操作III的主要过程为加水溶解、蒸发浓缩、冷却结晶、过滤
7.下列图示的四种实验操作名称从左到右依次是( )
A.过滤、蒸发、蒸馏、分液 B.过滤、蒸馏、蒸发、分液
C.蒸发、蒸馏、过滤、分液 D.分液、蒸馏、蒸发、过滤
8.下列关于蒸馏操作的有关叙述不正确的是 ( )
A.蒸馏操作的主要仪器是:蒸馏烧瓶、酒精灯、铁架台、冷凝管、锥形瓶、牛角管、温度计等
B.蒸馏操作使用的温度计的水银球应插入到液体内
C.在蒸馏烧瓶内放入少量碎瓷片,目的是防止暴沸
D.冷凝管进出水的方向是下口进、上口出
9.从溴水中萃取溴,下列试剂中能用做萃取剂的是()
A.乙酸 B.水 C.四氯化碳 D.酒精
10.核磁共振氢谱中根据分子中不同化学环境的氢原子在谱图中给出的信号峰不同来确定分子中氢原子种类的。在下列5种有机分子中,核磁共振氢谱中给出的信号峰数目相同的一组是( )
A.①② B.②④ C.④⑤ D.③⑤
11.化学发展史是科学史重要组成部分,下列科学家与主要成就不匹配的是( )
A.道尔顿——发现元素周期律
B.侯德榜——发明联合制碱法
C.屠呦呦——从菁蒿中提取菁蒿素
D.卢瑟福——提出原子核式模型
12.苯是一种不溶于水的无色液体,有特殊气味,密度比水小,沸点为80.1℃.现有苯和水的混合物,能将苯从该混合物中提取出来的最合理的方法是( )
A.过滤 B.分液 C.萃取 D.蒸馏
13.我国屠呦呦等科学家用乙醚从青蒿中提取出抗疟疾有效成分青蒿素,下列有关研究青蒿素方法不正确的是( )
A.可用质谱仪测定青蒿素的相对分子质量
B.可从红外光谱和核磁共振谱分析青蒿素中的基团
C.可通过X射线衍射测定青蒿素的分子结构
D.可用乙醇从青蒿中萃取出青蒿素
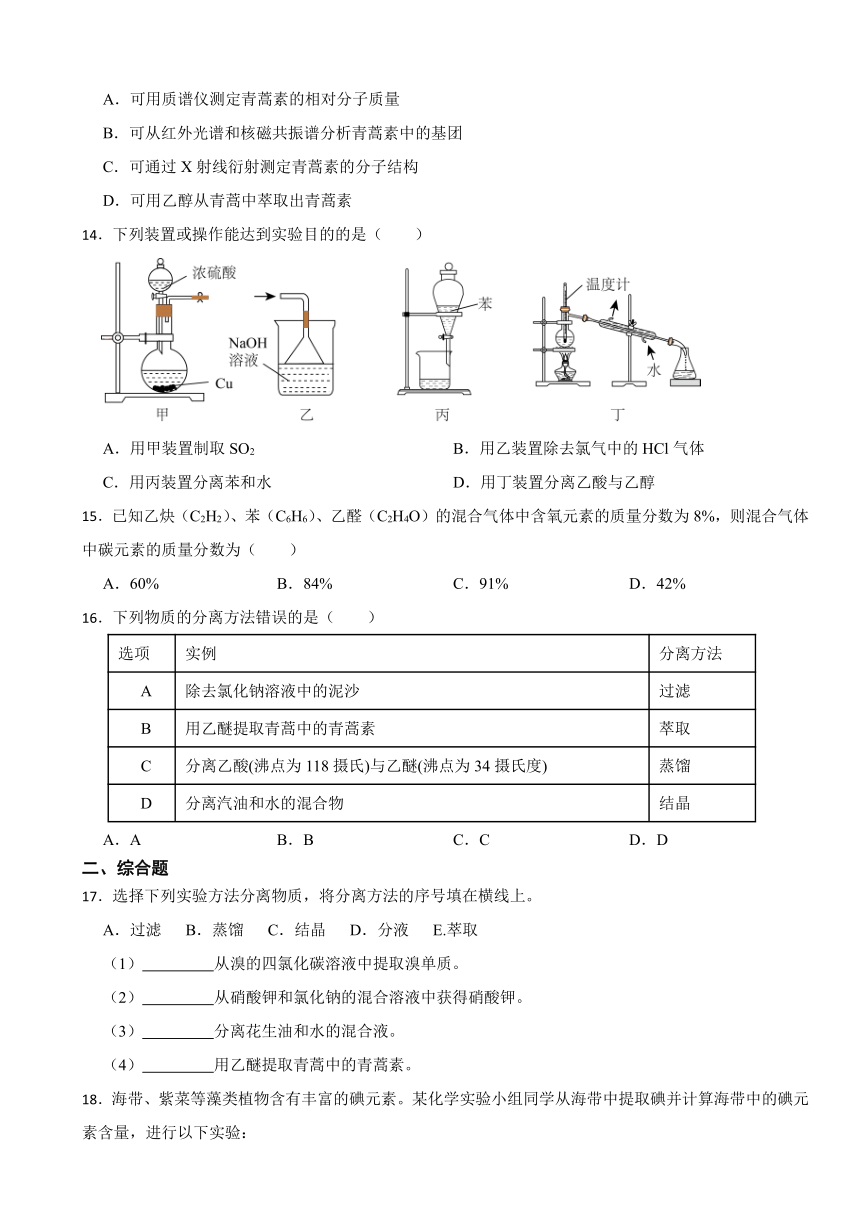
14.下列装置或操作能达到实验目的的是( )
A.用甲装置制取SO2 B.用乙装置除去氯气中的HCl气体
C.用丙装置分离苯和水 D.用丁装置分离乙酸与乙醇
15.已知乙炔(C2H2)、苯(C6H6)、乙醛(C2H4O)的混合气体中含氧元素的质量分数为8%,则混合气体中碳元素的质量分数为( )
A.60% B.84% C.91% D.42%
16.下列物质的分离方法错误的是( )
选项 实例 分离方法
A 除去氯化钠溶液中的泥沙 过滤
B 用乙醚提取青蒿中的青蒿素 萃取
C 分离乙酸(沸点为118摄氏)与乙醚(沸点为34摄氏度) 蒸馏
D 分离汽油和水的混合物 结晶
A.A B.B C.C D.D
二、综合题
17.选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.过滤 B.蒸馏 C.结晶 D.分液 E.萃取
(1) 从溴的四氯化碳溶液中提取溴单质。
(2) 从硝酸钾和氯化钠的混合溶液中获得硝酸钾。
(3) 分离花生油和水的混合液。
(4) 用乙醚提取青蒿中的青蒿素。
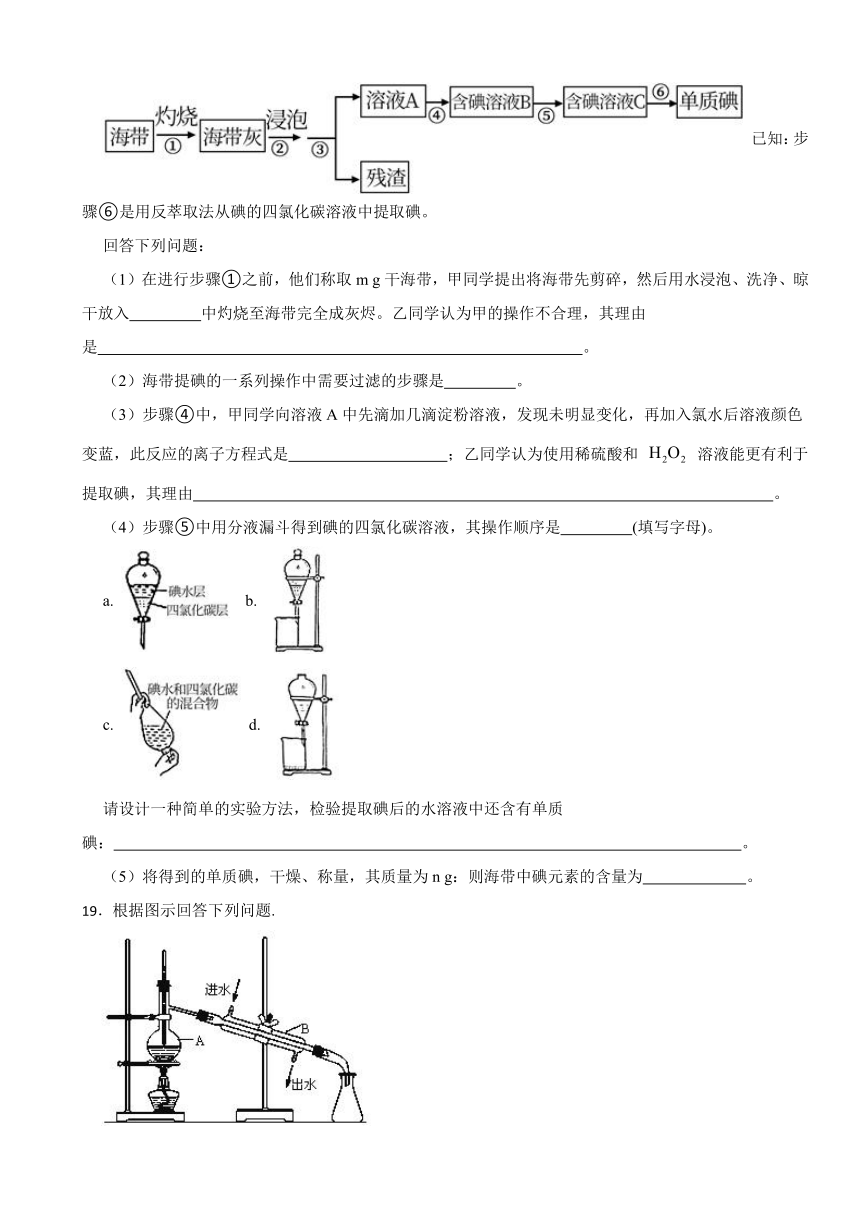
18.海带、紫菜等藻类植物含有丰富的碘元素。某化学实验小组同学从海带中提取碘并计算海带中的碘元素含量,进行以下实验:
已知:步骤⑥是用反萃取法从碘的四氯化碳溶液中提取碘。
回答下列问题:
(1)在进行步骤①之前,他们称取m g干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入 中灼烧至海带完全成灰烬。乙同学认为甲的操作不合理,其理由是 。
(2)海带提碘的一系列操作中需要过滤的步骤是 。
(3)步骤④中,甲同学向溶液A中先滴加几滴淀粉溶液,发现未明显变化,再加入氯水后溶液颜色变蓝,此反应的离子方程式是 ;乙同学认为使用稀硫酸和 溶液能更有利于提取碘,其理由 。
(4)步骤⑤中用分液漏斗得到碘的四氯化碳溶液,其操作顺序是 (填写字母)。
a. b.
c. d.
请设计一种简单的实验方法,检验提取碘后的水溶液中还含有单质碘: 。
(5)将得到的单质碘,干燥、称量,其质量为n g:则海带中碘元素的含量为 。
19.根据图示回答下列问题.
(1)A仪器的名称是 ,B仪器的名称是
(2)图中有两处明显的错误是:
(3)实验时A中除加入少量自来水外,还需要加入少量的 ,其作用是
20.下列物质的转化或分离是用哪种方法实现的 请将所选方法的字母代号填在横线上(每一项只填写一种最主要的方法)。
A.干馏 B.萃取 C.分液
(1)四氯化碳和水的混合物的分离 ;
(2)把煤转化为焦炉气、煤焦油和焦炭等 ;
(3)海水提溴获得的溴水中,用苯提取溴单质 。
21.某实验小组欲用CCl4萃取碘水中的碘,准备的实验用品有:带铁圈的铁架台,烧杯、碘水、CCl4、蒸馏水.
(1)要做“萃取碘水中的碘”实验,还缺少的仪器是
(2)萃取时CCl4层的颜色是 ,在 层(填“上”或“下”).
(3)已知碘在酒精中的溶解度比在水中大的多,能不能用酒精来萃取碘水中的碘 (填“能”或“不能”),其理由是
答案解析部分
1.【答案】B
【解析】【解答】A、C、D中均为互溶液体混合物,应选蒸馏法分离,只有B中水和四氯化碳分层,可选分液漏斗进行分液分离,
故答案为:B。
【分析】分液漏斗分离的是互不相溶、密度不同的液体混合物,据此解答即可。
2.【答案】D
【解析】【解答】
A.在蒸发操作的过程中,当加热到有少量液体剩余时停止加热,利用余热蒸发干,选项A不符合题意;
B.蒸馏操作时,温度计测的是要流出组分的温度,应使温度计水银球靠近蒸馏烧瓶支管口处,选项B不符合题意;
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出,一避免两种液体相互污染,选项C不符合题意;
D.萃取剂的选择与密度无关,选项D符合题意;
故答案为:D。
【分析】
A.蒸发要在大部分晶体析出就停止加热;
B.蒸馏中温度计测量的是蒸汽的温度;
C.分液要上从上出,下从下出;
D.萃取时选取萃取剂要不互溶,不反应,溶解度较大。
3.【答案】D
【解析】【解答】A.灼烧海带可在坩埚中进行,A项不符合题意;
B.操作①为加水浸泡、过滤、洗涤残渣,获得含I-的溶液,B项不符合题意;
C.反应②中,氯水将碘离子氧化成I2,主要反应的离子方程式为Cl2+2I-=I2+2Cl-,C项不符合题意;
D.乙醇和水互溶,不能选用乙醇作萃取剂从含I2的溶液中萃取出I2,即试剂③不能选用无水乙醇,可选用苯或四氯化碳等与水互不相溶的有机溶剂,D项符合题意;
故答案为:D。
【分析】海带灼烧后,溶解、过滤分离出残渣与含碘离子的溶液,②中发生的主要反应为Cl2+2I-=I2+2Cl-,且碘不易溶于水、易溶于有机溶剂,加有机溶剂萃取、分液分离出碘的有机层,还需蒸馏分离出碘。
4.【答案】B
【解析】【解答】1869年俄国化学家门捷列夫在前人的基础上进行研究,初步发现元素周期律并绘制了第一张元素周期表,
故答案为:B。
【分析】门捷列夫发现了元素周期律并根据相对原子质量的大小绘制元素周期表
5.【答案】C
【解析】【解答】解:A.盖斯提出了盖斯定律,故A错误;
B.阿伏加德罗提出了分子学说,故B错误;
C.俄国化学家门捷列夫发现了元素周期律,并编制出元素周期表,故C正确;
D.道尔顿提出了近代原子学说,故D错误.
故选C.
【分析】1869年,俄国化学家门捷列夫发现了元素周期律,并编制出元素周期表,使得化学学习和研究变得有规律可循.
6.【答案】D
【解析】【解答】A、破碎可增大接触面积,提高青蒿素的浸取率,A不符合题意。
B、操作Ⅰ后得到溶液和固体,因此操作Ⅰ为过滤,所需的玻璃仪器有烧杯、漏斗、玻璃棒,B不符合题意。
C、操作Ⅱ中通过蒸馏得到乙醚,乙醚的沸点为35℃,因此需采用水浴加热,C不符合题意。
D、操作Ⅲ从青蒿素粗品中得到较纯的青蒿素,若采用蒸发浓缩,则由于青蒿素的热稳定性较差,可能使青蒿素受热分解,D符合题意。
故答案为:D
【分析】A、破碎可增大接触面积,加快反应速率。
B、操作Ⅰ为过滤,据此确定所需的仪器。
C、乙醚的沸点为35℃,因此需采用水浴加热。
D、青蒿素的热稳定性较差,不能采用蒸发浓缩。
7.【答案】A
【解析】【解答】解:由图中第一个装置的仪器以及操作分离固液化合物,可知本实验操作名称过滤;
由图中第二个装置的仪器以及操作从溶液中分离溶质,可知本实验操作名称蒸发;
由图中第三个装置的仪器以及操作分离沸点不同的液体混合物,可知本实验操作名称蒸馏;
由图中第四个装置的仪器以及操作分离互不相溶的液体,可知本实验操作名称是萃取分液;
故四种实验操作名称从左到右依次是过滤、蒸发、蒸馏、萃取分液.
故选A.
【分析】根据物质分离的方法和化学实验的基本操知识及常见仪器漏斗、蒸发皿、蒸馏烧瓶、分液漏斗的用途来分析,由装置可知从左到右分别是过滤、蒸发、蒸馏、萃取分液,据此即可解答.
8.【答案】D
【解析】【解答】蒸馏操作所用的温度计的水银球的位置应在蒸馏烧瓶支管口处,所以B项错.
【分析】本题考查蒸馏操作需要的注意仪器和基本的实验操作步骤,题目难度不大,熟练掌握蒸馏操作是解题的关键 。
9.【答案】D
【解析】【解答】萃取适合于溶质在不同溶剂中的溶解性不同而分离的一种方法,选用的萃取剂的原则是:①和原溶液中的溶剂互不相溶更不能发生化学反应;②溶质在该溶剂中溶解度要远大于原溶剂。乙酸、乙醇和水是互溶的,不能作为从溴水中萃取溴的萃取剂。四氯化碳不溶于水,溴易溶在有机溶剂中,四氯化碳可以作为萃取剂,所以答案选C。
【分析】该题是常识性知识的考查,侧重对学生实验能力的培养,有利于培养学生的逻辑思维能力和规范严谨的实验设计能力。该题的关键是明确萃取剂选择的依据,然后结合题意灵活运用即可。
10.【答案】C
【解析】【解答】核磁共振氢谱中有几个峰,有机物中就有几种氢原子,在确定氢原子的种类时,要考虑分子的对称性,①有4种不同化学环境的氢原子,②有2种,③有5种,④和⑤有3种,
故答案为:C。
【分析】核磁共振氢谱中有几个峰,有机物中就有几种氢原子,在确定氢原子的种类时,要考虑分子的对称性。
11.【答案】A
【解析】【解答】A.道尔顿提出了原子学说,而元素周期律是俄国化学家门捷列夫根据元素之间的关系发现的规律,A符合题意;
B.侯德榜在前人研究的基础上,进行改进发明联合制碱法,B不符合题意;
C.我国科学家屠呦呦从菁蒿中提取菁蒿素,可以用来治疗疟疾,C不符合题意;
D.卢瑟福根据金箔实验,发现在原子中有相对较大的空间,提出原子核式模型,D不符合题意;
故答案为:A。
【分析】门捷列夫发现了元素周期律并编排了元素周期表。
12.【答案】B
【解析】【解答】解:水与苯互不相溶,混合后会分层,互不相溶的两层液体分开要采用分液法,
故选B.
【分析】互不相溶的两种物质的分离用分液法.
13.【答案】D
【解析】【解答】A、用质谱法可测定有机物的相对分子质量,因此可用质谱仪测定青蒿素的相对分子质量,故A正确;
B、红外光谱可检测化学键及官能团,核磁共振氢谱可以测定不同环境的氢原子,因此可从红外光谱和核磁共振谱分析青蒿素中的基团,故B正确;
C、X射线衍射可以观测微观结构,测定晶体的晶胞参数,因此可通过X射线衍射测定青蒿素的分子结构,故C正确;
D、青蒿素易溶于酒精、水等溶剂,乙醇与水互溶,不能用乙醇从青蒿浸取液中萃取出青蒿素,故D错误;
故答案为:D。
【分析】A、一般用质谱法测定有机物的相对分子质量;
B、红外光谱可检测化学键及官能团,核磁共振氢谱可以测定不同环境的氢原子;
C、X射线衍射可以观测微观结构,测定晶体的晶胞参数;
D、乙醇和水互溶。
14.【答案】C
【解析】【解答】A、Cu与浓硫酸反应制取SO2的化学方程式为:Cu+2H2SO4(浓)CuSO4+2H2O+SO2↑,该反应需要加热,A不符合题意。
B、Cl2、HCl都能与NaOH反应,因此不能用NaOH溶液除去Cl2中混有的HCl,应用饱和食盐水除去Cl2中混有的HCl,B不符合题意。
C、苯和水不互溶,可用分液操作进行分离,C符合题意。
D、蒸馏装置中,温度计测量的是蒸汽的温度,因此温度计的水银球应位于蒸馏烧瓶的支管口处,不能伸入溶液内,D不符合题意。
故答案为:C
【分析】A、Cu与浓硫酸的反应需要加热。
B、Cl2、HCl都能与NaOH溶液反应。
C、苯和水不互溶,可用分液进行分离。
D、蒸馏时温度计应位于蒸馏烧瓶支管口处,不能伸入溶液中。
15.【答案】B
【解析】【解答】这三种物质的化学式可改写为乙炔(CH)2、苯(CH)6、乙醛(CH)2·H2O,分析可知除去水的质量分数后,C和H的质量之比都是12:1,已知O的质量分数为8%,则H2O的质量分数为8%× =9%,所以混合气体中除水之外的C、H元素的质量分数之和为91%,根据C和H的质量之比为12:1可得,混合气体中碳元素的质量分数为91%× =84%,
故答案为:B。
【分析】分析各种有机物分子中元素质量比关系,然后计算碳元素的质量分数。
16.【答案】D
【解析】【解答】A.泥沙难溶于氯化钠溶液,可以过滤分离,A不符合题意;
B.青蒿素更易溶液乙醚,可以用乙醚萃取青蒿中的青蒿素,B不符合题意;
C.乙酸和乙醚的沸点差异较大,可以蒸馏分离,C不符合题意;
D.汽油和水不互溶,分液分离即可,D符合题意;
故答案为:D。
【分析】A.固液混合物的分离用过滤;
B.乙醚可用作萃取剂;
C.互溶但沸点不同的液体的分离用蒸馏;
D.不互溶液体的分离用分液;
17.【答案】(1)B
(2)C
(3)D
(4)E
【解析】【解答】(1)溴与四氯化碳互溶,但沸点不同,可蒸馏分离,故答案为:B;
(2)二者溶解度受温度影响不同,降温结晶可以获取纯净的硝酸钾,故答案为:C;
(3)花生油和水不互溶,会分层,可分液分离,故答案为:D;
(4)青蒿素更易溶于乙醚,乙醚可萃取青蒿素,为萃取法分离,故答案为:E。
【分析】A、过滤用于分离固液混合物;B、蒸馏是用于分离互溶但沸点不同的液体;C、结晶是从溶液中获得可溶性溶质的操作;D、分液是用于分离不互溶的两种液体;E、萃取是利用溶质在不同溶剂中的溶解度差异进行分离的操作。
18.【答案】(1)甘埚;水浸泡、洗净时,碘化物会溶解在水中,使得碘元素的含量减少
(2)③⑥
(3)Cl2+2I-=2Cl-+I2;在酸性条件下,H2O2能氧化I-为单质碘,且萃取时它们溶于水中,易与I2分离
(4)acbd;取萃取分液后的水溶液于试管中,滴入几滴淀粉溶液,溶液变蓝,说明含有碘单质。
(5)
【解析】【解答】(1)灼烧操作应在坩埚中进行;水浸泡、洗净时,碘化物会溶解在水中,使得碘元素的含量减少,所以甲的操作不合理;
(2)步骤③需要将含有I-的溶液和残渣分离,需要过滤,反萃取过程中会得到碘的悬浊液,需过滤得到碘单质,故答案为③⑥;
(3)根据实验现象可知溶液中含有I-,加入氯水后将I-氧化为碘单质,离子方程式为Cl2+2I-=2Cl-+I2;在酸性条件下,H2O2能氧化I-为单质碘,且萃取时它们溶于水中,易与I2分离,而使用氯水是,Cl2也会被萃取;
(4)萃取分液时,先将混合物置于分液漏斗中,然后将分液漏斗下口朝上震荡,充分萃取,之后静置分层,然后先将下层液体从下口放出,所以顺序为acbd;
碘单质遇淀粉变蓝,所以检验碘单质可以:取萃取分液后的水溶液于试管中,滴入几滴淀粉溶液,溶液变蓝,说明含有碘单质;
(5)海带质量为m g,得到n g碘单质,即海带中含有n g碘单质,所以海带中碘元素的含量为 。
【分析】海带经灼烧除去有机杂质后得到海带灰,加入浸泡溶解,过滤得到含有I-的溶液A,加入氧化剂将I-氧化为碘单质,得到含碘溶液B,加入四氯化碳萃取分液得到含碘溶液C,经反萃取得到碘单质。
19.【答案】(1)蒸馏烧瓶;冷凝管
(2)冷凝管从上口进水,下口出水;温度计液泡靠近液体的上方;
(3)加沸石(或碎瓷片);防止暴沸
【解析】【解答】(1)蒸馏时用到的仪器蒸馏烧瓶、酒精灯、冷凝管、牛角管、锥形瓶等,由仪器的结构可知,A为蒸馏烧瓶,B为冷凝管,
故答案为:蒸馏烧瓶;冷凝管;
(2)温度计水银球应处在蒸馏烧瓶的支管口附近,冷凝管应从下口进水,上口出水,以保证水充满冷凝管,起到充分冷凝的作用,所以图中有两处明显的错误是:冷凝管从上口进水,下口出水,温度计液泡靠近液体的上方,
故答案为:冷凝管从上口进水,下口出水;温度计液泡靠近液体的上方;
(3)蒸馏原理为液体变为气体,由气体变为液体,为防止液体暴沸,应加碎瓷片,
故答案为:加沸石(或碎瓷片);防止暴沸.
【分析】(1)根据蒸馏时用到的仪器以及常用仪器的名称作用分析解答;
(2)根据蒸馏时需注意的事项解答;注意冷凝水方向;温度计位置;
(3)为防止液体暴沸,常加入碎瓷片.
20.【答案】(1)C
(2)A
(3)B
【解析】【解答】(1)CCl4和水不互溶,属于两种不互溶液体的分离,应采用分液操作,故答案为:C;
(2)把煤转化为焦炉气、煤焦油和焦炭,应采用隔绝空气加强热的方法,为干馏,故答案为:A;
(3)溴在苯中的溶解度大于在水中的溶解度,因此用苯提取溴单质为萃取操作,故答案为:B;
【分析】此题是对干馏、萃取和分液的考查,结合相关操作的概念和应用范围进行分析;干馏是指隔绝空气加强热,使物质分解;萃取是利用物质在不同溶剂中溶解度的差异进行分析;分液是将两种不互溶液体进行分离。据此结合题干设问进行分析作答。
21.【答案】(1)分液漏斗;
(2)紫色;下
(3)不能;酒精和水可以互溶
【解析】【解答】(1)萃取需要使用分液漏斗、烧杯、铁架台,还缺少分液漏斗,故答案为:分液漏斗;
(2)碘的CCl4溶液为紫红色,四氯化碳密度比水大,位于下层,故答案为:紫色;下;
(3)酒精能与水互溶,不分层,不能做萃取剂,故答案为:不能;酒精和水可以互溶.
【分析】(1)萃取需要使用分液漏斗、烧杯、铁架台;
(2)碘的CCl4溶液为紫红色;
(3)萃取剂必须具备下列条件:两种溶剂互不相溶;溶质在萃取剂中的溶解度大于在原溶剂中的溶解度;溶质与萃取剂不反应.
一、单选题
1.下列各组混合物,能用分液漏斗进行分离的是( )
A.汽油和植物油 B.水和四氯化碳
C.酒精和水 D.溴和四氯化碳
2.下列实验操作中错误的是( )
A.蒸发操作时,应使混合物中的水分少量剩余时,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
3.从海带中提取碘的一种实验流程如图所示,下列说法错误的是( )
A.灼烧海带可在坩埚中进行
B.操作①为加水浸泡、过滤、洗涤残渣
C.反应②中发生的主要反应为
D.试剂③可以选用无水乙醇
4.十九世纪,初步发现元素周期律并发明元素周期表的科学家是( )
A.道尔顿 B.门捷列夫 C.舍勒 D.拉瓦锡
5.提出元素周期律并绘制了第一个元素周期表的科学家是( )
A.盖斯 B.阿伏加德罗 C.门捷列夫 D.道尔顿
6.青蒿素是高效的抗疟疾药,为无色针状晶体,易溶于有机溶剂,在水中几乎不溶,熔点为156℃~157℃,热稳定性差。提取青蒿素的主要工艺如下。(已知: 乙醚的沸点为35℃)
下列说法不正确的是( )
A.破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素浸取率
B.操作I需要用到玻璃仪器有漏斗、玻璃棒、烧杯
C.操作II蒸馏时最好选用水浴加热
D.操作III的主要过程为加水溶解、蒸发浓缩、冷却结晶、过滤
7.下列图示的四种实验操作名称从左到右依次是( )
A.过滤、蒸发、蒸馏、分液 B.过滤、蒸馏、蒸发、分液
C.蒸发、蒸馏、过滤、分液 D.分液、蒸馏、蒸发、过滤
8.下列关于蒸馏操作的有关叙述不正确的是 ( )
A.蒸馏操作的主要仪器是:蒸馏烧瓶、酒精灯、铁架台、冷凝管、锥形瓶、牛角管、温度计等
B.蒸馏操作使用的温度计的水银球应插入到液体内
C.在蒸馏烧瓶内放入少量碎瓷片,目的是防止暴沸
D.冷凝管进出水的方向是下口进、上口出
9.从溴水中萃取溴,下列试剂中能用做萃取剂的是()
A.乙酸 B.水 C.四氯化碳 D.酒精
10.核磁共振氢谱中根据分子中不同化学环境的氢原子在谱图中给出的信号峰不同来确定分子中氢原子种类的。在下列5种有机分子中,核磁共振氢谱中给出的信号峰数目相同的一组是( )
A.①② B.②④ C.④⑤ D.③⑤
11.化学发展史是科学史重要组成部分,下列科学家与主要成就不匹配的是( )
A.道尔顿——发现元素周期律
B.侯德榜——发明联合制碱法
C.屠呦呦——从菁蒿中提取菁蒿素
D.卢瑟福——提出原子核式模型
12.苯是一种不溶于水的无色液体,有特殊气味,密度比水小,沸点为80.1℃.现有苯和水的混合物,能将苯从该混合物中提取出来的最合理的方法是( )
A.过滤 B.分液 C.萃取 D.蒸馏
13.我国屠呦呦等科学家用乙醚从青蒿中提取出抗疟疾有效成分青蒿素,下列有关研究青蒿素方法不正确的是( )
A.可用质谱仪测定青蒿素的相对分子质量
B.可从红外光谱和核磁共振谱分析青蒿素中的基团
C.可通过X射线衍射测定青蒿素的分子结构
D.可用乙醇从青蒿中萃取出青蒿素
14.下列装置或操作能达到实验目的的是( )
A.用甲装置制取SO2 B.用乙装置除去氯气中的HCl气体
C.用丙装置分离苯和水 D.用丁装置分离乙酸与乙醇
15.已知乙炔(C2H2)、苯(C6H6)、乙醛(C2H4O)的混合气体中含氧元素的质量分数为8%,则混合气体中碳元素的质量分数为( )
A.60% B.84% C.91% D.42%
16.下列物质的分离方法错误的是( )
选项 实例 分离方法
A 除去氯化钠溶液中的泥沙 过滤
B 用乙醚提取青蒿中的青蒿素 萃取
C 分离乙酸(沸点为118摄氏)与乙醚(沸点为34摄氏度) 蒸馏
D 分离汽油和水的混合物 结晶
A.A B.B C.C D.D
二、综合题
17.选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.过滤 B.蒸馏 C.结晶 D.分液 E.萃取
(1) 从溴的四氯化碳溶液中提取溴单质。
(2) 从硝酸钾和氯化钠的混合溶液中获得硝酸钾。
(3) 分离花生油和水的混合液。
(4) 用乙醚提取青蒿中的青蒿素。
18.海带、紫菜等藻类植物含有丰富的碘元素。某化学实验小组同学从海带中提取碘并计算海带中的碘元素含量,进行以下实验:
已知:步骤⑥是用反萃取法从碘的四氯化碳溶液中提取碘。
回答下列问题:
(1)在进行步骤①之前,他们称取m g干海带,甲同学提出将海带先剪碎,然后用水浸泡、洗净、晾干放入 中灼烧至海带完全成灰烬。乙同学认为甲的操作不合理,其理由是 。
(2)海带提碘的一系列操作中需要过滤的步骤是 。
(3)步骤④中,甲同学向溶液A中先滴加几滴淀粉溶液,发现未明显变化,再加入氯水后溶液颜色变蓝,此反应的离子方程式是 ;乙同学认为使用稀硫酸和 溶液能更有利于提取碘,其理由 。
(4)步骤⑤中用分液漏斗得到碘的四氯化碳溶液,其操作顺序是 (填写字母)。
a. b.
c. d.
请设计一种简单的实验方法,检验提取碘后的水溶液中还含有单质碘: 。
(5)将得到的单质碘,干燥、称量,其质量为n g:则海带中碘元素的含量为 。
19.根据图示回答下列问题.
(1)A仪器的名称是 ,B仪器的名称是
(2)图中有两处明显的错误是:
(3)实验时A中除加入少量自来水外,还需要加入少量的 ,其作用是
20.下列物质的转化或分离是用哪种方法实现的 请将所选方法的字母代号填在横线上(每一项只填写一种最主要的方法)。
A.干馏 B.萃取 C.分液
(1)四氯化碳和水的混合物的分离 ;
(2)把煤转化为焦炉气、煤焦油和焦炭等 ;
(3)海水提溴获得的溴水中,用苯提取溴单质 。
21.某实验小组欲用CCl4萃取碘水中的碘,准备的实验用品有:带铁圈的铁架台,烧杯、碘水、CCl4、蒸馏水.
(1)要做“萃取碘水中的碘”实验,还缺少的仪器是
(2)萃取时CCl4层的颜色是 ,在 层(填“上”或“下”).
(3)已知碘在酒精中的溶解度比在水中大的多,能不能用酒精来萃取碘水中的碘 (填“能”或“不能”),其理由是
答案解析部分
1.【答案】B
【解析】【解答】A、C、D中均为互溶液体混合物,应选蒸馏法分离,只有B中水和四氯化碳分层,可选分液漏斗进行分液分离,
故答案为:B。
【分析】分液漏斗分离的是互不相溶、密度不同的液体混合物,据此解答即可。
2.【答案】D
【解析】【解答】
A.在蒸发操作的过程中,当加热到有少量液体剩余时停止加热,利用余热蒸发干,选项A不符合题意;
B.蒸馏操作时,温度计测的是要流出组分的温度,应使温度计水银球靠近蒸馏烧瓶支管口处,选项B不符合题意;
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出,一避免两种液体相互污染,选项C不符合题意;
D.萃取剂的选择与密度无关,选项D符合题意;
故答案为:D。
【分析】
A.蒸发要在大部分晶体析出就停止加热;
B.蒸馏中温度计测量的是蒸汽的温度;
C.分液要上从上出,下从下出;
D.萃取时选取萃取剂要不互溶,不反应,溶解度较大。
3.【答案】D
【解析】【解答】A.灼烧海带可在坩埚中进行,A项不符合题意;
B.操作①为加水浸泡、过滤、洗涤残渣,获得含I-的溶液,B项不符合题意;
C.反应②中,氯水将碘离子氧化成I2,主要反应的离子方程式为Cl2+2I-=I2+2Cl-,C项不符合题意;
D.乙醇和水互溶,不能选用乙醇作萃取剂从含I2的溶液中萃取出I2,即试剂③不能选用无水乙醇,可选用苯或四氯化碳等与水互不相溶的有机溶剂,D项符合题意;
故答案为:D。
【分析】海带灼烧后,溶解、过滤分离出残渣与含碘离子的溶液,②中发生的主要反应为Cl2+2I-=I2+2Cl-,且碘不易溶于水、易溶于有机溶剂,加有机溶剂萃取、分液分离出碘的有机层,还需蒸馏分离出碘。
4.【答案】B
【解析】【解答】1869年俄国化学家门捷列夫在前人的基础上进行研究,初步发现元素周期律并绘制了第一张元素周期表,
故答案为:B。
【分析】门捷列夫发现了元素周期律并根据相对原子质量的大小绘制元素周期表
5.【答案】C
【解析】【解答】解:A.盖斯提出了盖斯定律,故A错误;
B.阿伏加德罗提出了分子学说,故B错误;
C.俄国化学家门捷列夫发现了元素周期律,并编制出元素周期表,故C正确;
D.道尔顿提出了近代原子学说,故D错误.
故选C.
【分析】1869年,俄国化学家门捷列夫发现了元素周期律,并编制出元素周期表,使得化学学习和研究变得有规律可循.
6.【答案】D
【解析】【解答】A、破碎可增大接触面积,提高青蒿素的浸取率,A不符合题意。
B、操作Ⅰ后得到溶液和固体,因此操作Ⅰ为过滤,所需的玻璃仪器有烧杯、漏斗、玻璃棒,B不符合题意。
C、操作Ⅱ中通过蒸馏得到乙醚,乙醚的沸点为35℃,因此需采用水浴加热,C不符合题意。
D、操作Ⅲ从青蒿素粗品中得到较纯的青蒿素,若采用蒸发浓缩,则由于青蒿素的热稳定性较差,可能使青蒿素受热分解,D符合题意。
故答案为:D
【分析】A、破碎可增大接触面积,加快反应速率。
B、操作Ⅰ为过滤,据此确定所需的仪器。
C、乙醚的沸点为35℃,因此需采用水浴加热。
D、青蒿素的热稳定性较差,不能采用蒸发浓缩。
7.【答案】A
【解析】【解答】解:由图中第一个装置的仪器以及操作分离固液化合物,可知本实验操作名称过滤;
由图中第二个装置的仪器以及操作从溶液中分离溶质,可知本实验操作名称蒸发;
由图中第三个装置的仪器以及操作分离沸点不同的液体混合物,可知本实验操作名称蒸馏;
由图中第四个装置的仪器以及操作分离互不相溶的液体,可知本实验操作名称是萃取分液;
故四种实验操作名称从左到右依次是过滤、蒸发、蒸馏、萃取分液.
故选A.
【分析】根据物质分离的方法和化学实验的基本操知识及常见仪器漏斗、蒸发皿、蒸馏烧瓶、分液漏斗的用途来分析,由装置可知从左到右分别是过滤、蒸发、蒸馏、萃取分液,据此即可解答.
8.【答案】D
【解析】【解答】蒸馏操作所用的温度计的水银球的位置应在蒸馏烧瓶支管口处,所以B项错.
【分析】本题考查蒸馏操作需要的注意仪器和基本的实验操作步骤,题目难度不大,熟练掌握蒸馏操作是解题的关键 。
9.【答案】D
【解析】【解答】萃取适合于溶质在不同溶剂中的溶解性不同而分离的一种方法,选用的萃取剂的原则是:①和原溶液中的溶剂互不相溶更不能发生化学反应;②溶质在该溶剂中溶解度要远大于原溶剂。乙酸、乙醇和水是互溶的,不能作为从溴水中萃取溴的萃取剂。四氯化碳不溶于水,溴易溶在有机溶剂中,四氯化碳可以作为萃取剂,所以答案选C。
【分析】该题是常识性知识的考查,侧重对学生实验能力的培养,有利于培养学生的逻辑思维能力和规范严谨的实验设计能力。该题的关键是明确萃取剂选择的依据,然后结合题意灵活运用即可。
10.【答案】C
【解析】【解答】核磁共振氢谱中有几个峰,有机物中就有几种氢原子,在确定氢原子的种类时,要考虑分子的对称性,①有4种不同化学环境的氢原子,②有2种,③有5种,④和⑤有3种,
故答案为:C。
【分析】核磁共振氢谱中有几个峰,有机物中就有几种氢原子,在确定氢原子的种类时,要考虑分子的对称性。
11.【答案】A
【解析】【解答】A.道尔顿提出了原子学说,而元素周期律是俄国化学家门捷列夫根据元素之间的关系发现的规律,A符合题意;
B.侯德榜在前人研究的基础上,进行改进发明联合制碱法,B不符合题意;
C.我国科学家屠呦呦从菁蒿中提取菁蒿素,可以用来治疗疟疾,C不符合题意;
D.卢瑟福根据金箔实验,发现在原子中有相对较大的空间,提出原子核式模型,D不符合题意;
故答案为:A。
【分析】门捷列夫发现了元素周期律并编排了元素周期表。
12.【答案】B
【解析】【解答】解:水与苯互不相溶,混合后会分层,互不相溶的两层液体分开要采用分液法,
故选B.
【分析】互不相溶的两种物质的分离用分液法.
13.【答案】D
【解析】【解答】A、用质谱法可测定有机物的相对分子质量,因此可用质谱仪测定青蒿素的相对分子质量,故A正确;
B、红外光谱可检测化学键及官能团,核磁共振氢谱可以测定不同环境的氢原子,因此可从红外光谱和核磁共振谱分析青蒿素中的基团,故B正确;
C、X射线衍射可以观测微观结构,测定晶体的晶胞参数,因此可通过X射线衍射测定青蒿素的分子结构,故C正确;
D、青蒿素易溶于酒精、水等溶剂,乙醇与水互溶,不能用乙醇从青蒿浸取液中萃取出青蒿素,故D错误;
故答案为:D。
【分析】A、一般用质谱法测定有机物的相对分子质量;
B、红外光谱可检测化学键及官能团,核磁共振氢谱可以测定不同环境的氢原子;
C、X射线衍射可以观测微观结构,测定晶体的晶胞参数;
D、乙醇和水互溶。
14.【答案】C
【解析】【解答】A、Cu与浓硫酸反应制取SO2的化学方程式为:Cu+2H2SO4(浓)CuSO4+2H2O+SO2↑,该反应需要加热,A不符合题意。
B、Cl2、HCl都能与NaOH反应,因此不能用NaOH溶液除去Cl2中混有的HCl,应用饱和食盐水除去Cl2中混有的HCl,B不符合题意。
C、苯和水不互溶,可用分液操作进行分离,C符合题意。
D、蒸馏装置中,温度计测量的是蒸汽的温度,因此温度计的水银球应位于蒸馏烧瓶的支管口处,不能伸入溶液内,D不符合题意。
故答案为:C
【分析】A、Cu与浓硫酸的反应需要加热。
B、Cl2、HCl都能与NaOH溶液反应。
C、苯和水不互溶,可用分液进行分离。
D、蒸馏时温度计应位于蒸馏烧瓶支管口处,不能伸入溶液中。
15.【答案】B
【解析】【解答】这三种物质的化学式可改写为乙炔(CH)2、苯(CH)6、乙醛(CH)2·H2O,分析可知除去水的质量分数后,C和H的质量之比都是12:1,已知O的质量分数为8%,则H2O的质量分数为8%× =9%,所以混合气体中除水之外的C、H元素的质量分数之和为91%,根据C和H的质量之比为12:1可得,混合气体中碳元素的质量分数为91%× =84%,
故答案为:B。
【分析】分析各种有机物分子中元素质量比关系,然后计算碳元素的质量分数。
16.【答案】D
【解析】【解答】A.泥沙难溶于氯化钠溶液,可以过滤分离,A不符合题意;
B.青蒿素更易溶液乙醚,可以用乙醚萃取青蒿中的青蒿素,B不符合题意;
C.乙酸和乙醚的沸点差异较大,可以蒸馏分离,C不符合题意;
D.汽油和水不互溶,分液分离即可,D符合题意;
故答案为:D。
【分析】A.固液混合物的分离用过滤;
B.乙醚可用作萃取剂;
C.互溶但沸点不同的液体的分离用蒸馏;
D.不互溶液体的分离用分液;
17.【答案】(1)B
(2)C
(3)D
(4)E
【解析】【解答】(1)溴与四氯化碳互溶,但沸点不同,可蒸馏分离,故答案为:B;
(2)二者溶解度受温度影响不同,降温结晶可以获取纯净的硝酸钾,故答案为:C;
(3)花生油和水不互溶,会分层,可分液分离,故答案为:D;
(4)青蒿素更易溶于乙醚,乙醚可萃取青蒿素,为萃取法分离,故答案为:E。
【分析】A、过滤用于分离固液混合物;B、蒸馏是用于分离互溶但沸点不同的液体;C、结晶是从溶液中获得可溶性溶质的操作;D、分液是用于分离不互溶的两种液体;E、萃取是利用溶质在不同溶剂中的溶解度差异进行分离的操作。
18.【答案】(1)甘埚;水浸泡、洗净时,碘化物会溶解在水中,使得碘元素的含量减少
(2)③⑥
(3)Cl2+2I-=2Cl-+I2;在酸性条件下,H2O2能氧化I-为单质碘,且萃取时它们溶于水中,易与I2分离
(4)acbd;取萃取分液后的水溶液于试管中,滴入几滴淀粉溶液,溶液变蓝,说明含有碘单质。
(5)
【解析】【解答】(1)灼烧操作应在坩埚中进行;水浸泡、洗净时,碘化物会溶解在水中,使得碘元素的含量减少,所以甲的操作不合理;
(2)步骤③需要将含有I-的溶液和残渣分离,需要过滤,反萃取过程中会得到碘的悬浊液,需过滤得到碘单质,故答案为③⑥;
(3)根据实验现象可知溶液中含有I-,加入氯水后将I-氧化为碘单质,离子方程式为Cl2+2I-=2Cl-+I2;在酸性条件下,H2O2能氧化I-为单质碘,且萃取时它们溶于水中,易与I2分离,而使用氯水是,Cl2也会被萃取;
(4)萃取分液时,先将混合物置于分液漏斗中,然后将分液漏斗下口朝上震荡,充分萃取,之后静置分层,然后先将下层液体从下口放出,所以顺序为acbd;
碘单质遇淀粉变蓝,所以检验碘单质可以:取萃取分液后的水溶液于试管中,滴入几滴淀粉溶液,溶液变蓝,说明含有碘单质;
(5)海带质量为m g,得到n g碘单质,即海带中含有n g碘单质,所以海带中碘元素的含量为 。
【分析】海带经灼烧除去有机杂质后得到海带灰,加入浸泡溶解,过滤得到含有I-的溶液A,加入氧化剂将I-氧化为碘单质,得到含碘溶液B,加入四氯化碳萃取分液得到含碘溶液C,经反萃取得到碘单质。
19.【答案】(1)蒸馏烧瓶;冷凝管
(2)冷凝管从上口进水,下口出水;温度计液泡靠近液体的上方;
(3)加沸石(或碎瓷片);防止暴沸
【解析】【解答】(1)蒸馏时用到的仪器蒸馏烧瓶、酒精灯、冷凝管、牛角管、锥形瓶等,由仪器的结构可知,A为蒸馏烧瓶,B为冷凝管,
故答案为:蒸馏烧瓶;冷凝管;
(2)温度计水银球应处在蒸馏烧瓶的支管口附近,冷凝管应从下口进水,上口出水,以保证水充满冷凝管,起到充分冷凝的作用,所以图中有两处明显的错误是:冷凝管从上口进水,下口出水,温度计液泡靠近液体的上方,
故答案为:冷凝管从上口进水,下口出水;温度计液泡靠近液体的上方;
(3)蒸馏原理为液体变为气体,由气体变为液体,为防止液体暴沸,应加碎瓷片,
故答案为:加沸石(或碎瓷片);防止暴沸.
【分析】(1)根据蒸馏时用到的仪器以及常用仪器的名称作用分析解答;
(2)根据蒸馏时需注意的事项解答;注意冷凝水方向;温度计位置;
(3)为防止液体暴沸,常加入碎瓷片.
20.【答案】(1)C
(2)A
(3)B
【解析】【解答】(1)CCl4和水不互溶,属于两种不互溶液体的分离,应采用分液操作,故答案为:C;
(2)把煤转化为焦炉气、煤焦油和焦炭,应采用隔绝空气加强热的方法,为干馏,故答案为:A;
(3)溴在苯中的溶解度大于在水中的溶解度,因此用苯提取溴单质为萃取操作,故答案为:B;
【分析】此题是对干馏、萃取和分液的考查,结合相关操作的概念和应用范围进行分析;干馏是指隔绝空气加强热,使物质分解;萃取是利用物质在不同溶剂中溶解度的差异进行分析;分液是将两种不互溶液体进行分离。据此结合题干设问进行分析作答。
21.【答案】(1)分液漏斗;
(2)紫色;下
(3)不能;酒精和水可以互溶
【解析】【解答】(1)萃取需要使用分液漏斗、烧杯、铁架台,还缺少分液漏斗,故答案为:分液漏斗;
(2)碘的CCl4溶液为紫红色,四氯化碳密度比水大,位于下层,故答案为:紫色;下;
(3)酒精能与水互溶,不分层,不能做萃取剂,故答案为:不能;酒精和水可以互溶.
【分析】(1)萃取需要使用分液漏斗、烧杯、铁架台;
(2)碘的CCl4溶液为紫红色;
(3)萃取剂必须具备下列条件:两种溶剂互不相溶;溶质在萃取剂中的溶解度大于在原溶剂中的溶解度;溶质与萃取剂不反应.
