3.1 铁及其化合物 课件(共31张PPT)
文档属性
| 名称 | 3.1 铁及其化合物 课件(共31张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-29 00:00:00 | ||
图片预览










文档简介
(共31张PPT)
铁及其化合物(第一课时)
高中化学
人类使用铁的历史
·公元前2500年人类已发现和使用铁
·约公元前2000年人类发明了用铁矿石冶炼铁的
方法
陨铁
高中化学
甘肃灵台山出土的春秋初年秦国的铜柄铁剑
高中化学
我国目前发现最早的人工冶铁制品
战国时期最大的铁器——长方形铁炉
高中化学
我国古代冶铁技术
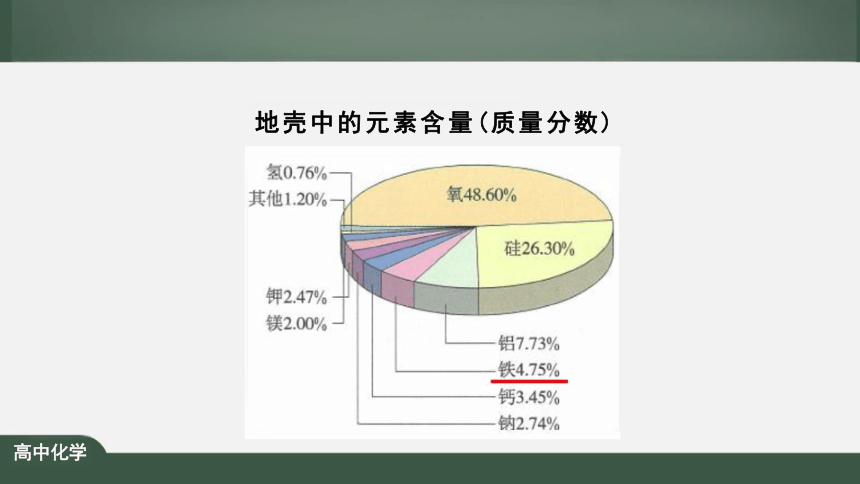
地壳中的元素含量(质量分数)
高中化学
常见的铁矿石
赤铁矿 (Fe O )
菱铁矿 (FeCO )
磁铁矿 (Fe O )
黄铁矿
(FeS )
高中化学
丹霞地貌的岩石
高中化学
作颜料、催化剂、医药领域等。
高中化学
Fe O 粉末用途
任务 用化学方法制备Fe O
活动1 哪些途径可以制备氧化铁
碱性氧化物 F8o
Fe+O - → Fe O
3Fe+20 点燃 Fe O
金属
l+0
金属氧化物
高中化学
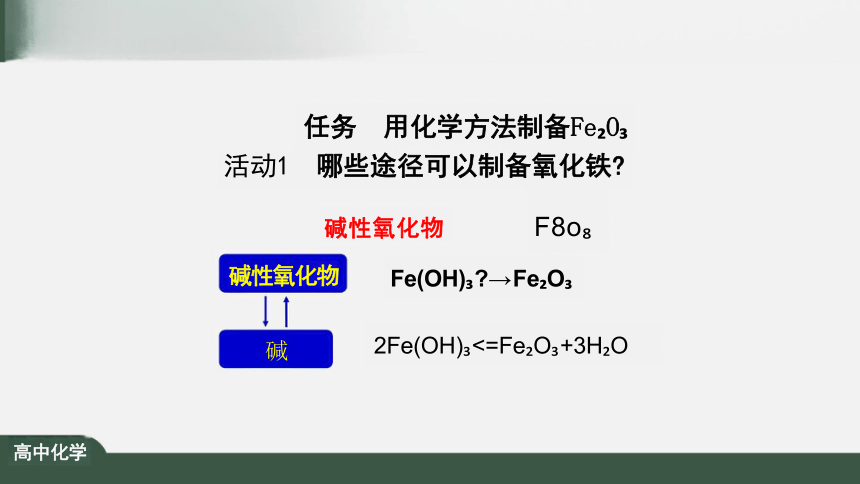
任务 用化学方法制备Fe O
活动1 哪些途径可以制备氧化铁
碱性氧化物 F8o
Fe(OH) → Fe O
2Fe(OH) <=Fe O +3H O
碱性氧化物
碱
高中化学
任务 用化学方法制备Fe O
活动1 哪些途径可以制备Fe O
F 0
Fe+O +H O → Fe O ·xH O
3Fe+20 点燃 Fe O
Fe+H O- >Fe O
高中化学
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu ……
高中化学
还原 铁粉 FeO Fe O Fe O Fe(OH)
Fe(OH) 3
黑色 黑色 红棕色 黑色 白色
红褐色
受热 不分解 受热 不分解 受热 不分解 受热 不分解 不稳定
Fe+H 0(g)△>Fe(OH) +H
Fe+H 0(g) 高温 Fe O +H
活动2 预测铁与水蒸气反应的产物,说出依据
预测
相关物质的性质
500 ℃
分解为Fe O
高中化学
2
活动2 预测铁与水蒸气反应的产物,说出依据
预测 Fe+H O(g)△>Fe(OH) +H
Fe+H 0(g) 高温 Fe O +H
活动3 如何检验气体产物
活动4 实验装置应有几部分构成
高中化学
水蒸气发生器 主反应装置 除杂装置 收集检验装置
方 案
高中化学
铁粉与水蒸气反应
实验现象:加热时玻璃管内铁粉红热,点燃产物 气体能安静地燃烧。
反应原理:3Fe+4H O(g) 高温 Fe O +4H,
实验结论:铁能与水蒸气发生反应,生成Fe O 与氢气
高中化学
肥皂液 除杂收集
检验装置
燃着的火柴
铁粉与水蒸气反应
还原铁粉一
湿棉花一
水蒸气 发生器
主反应装置
方案评价
高中化学
方 案 二
金属
碱性氧化物
Fe
Fe O
△
e (0H)
任务 用化学方法制备Fe O
+O /H O(g)
Fe O
碱 盐
高中化学
3
一、铁的化学性质总结
1.与非金属单质(氯气、氧气等)反应
2.与非氧化性酸(稀盐酸、稀硫酸等)反应
3.与某些盐溶液 (CuSO 溶液等)反应
Fe与Cl Fe与稀盐酸 Fe 与 CuSO 溶 液
高中化学
一 、铁的化学性质总结
铁的化学性质: 还原性
铁与氯气反应
铁与盐酸反应 Fe+2H =F62+H T
铁与硫酸铜溶液反应 Fe+cuz=Fe+cu
高中化学
+3
Fe FeCl 等
Fe O
+2
Fe FeCl 、FeSO 等
+强氧化剂
+O 或H O(g)
+弱氧化剂
还原剂+氧化剂— → 氧化还原反应产物
一、铁的化学性质总结
还 原
化学性质
Fe
性
高中化学
一、铁的化学性质总结
4.与水的反应
2Na+2H O=2NaOH+H ↑
Mg+2H O( 热 ) = Mg(OH) +H ↑
2Al+6H O ( 沸 ) = 2Al(OH) +3H 个
3Fe+4H 0(g) 高温 Fe O +4H
高中化学
小结:金属与水的反应
高中化学
物质 FeO Fe O
Fe O
来源、俗名 赤铁矿、铁红
磁铁矿、磁性氧
化铁
色态 黑色粉末 红棕色粉末
黑色晶体
水溶性 不溶 不溶
不溶
二、 铁的氧化物性质总结
活动5 请预测Fe O 的化学性质,说出依据
高中化学
物质类别和元素价态,是学习元素及其化合物性
质的重要认识视角。
基于物质类别和元素价态,可以预测物质的性质。
例如,对于Fe O , 从物质类别来看,它属于金属氧化 物,据此可以预测它可能与酸发生反应;从元素价态 来看, Fe O 中铁元素的化合价是+3价,为铁元素的 高价态,据此可以预测它具有氧化性,可能与具有还 原性的物质发生反应。
高中化学
方法导引
认识元素及其化合物性质的视角
二 、铁的氧化物性质总结
物质类别:碱性氧化物
+3 Fe O +6H+=-2Fe ++3H O
Fe O { 2Fe(0H) -Fe O +3H O
(元素价态: 氧化性
Fe O +3C0 高温2Fe +3CO
高中化学
二 、铁的氧化物性质总结
物质类别:碱性氧化物
+2 FeO+2H+=—Fe ++H O
FeO
氧化性
《元素价态: Fe0 +CO: Fe +CO
( 还原性
6FeO+O =<=2Fe O
高中化学
高温
二 、铁的氧化物性质总结
物质类别:特殊氧化物
Fe O +8H+=—Fe ++2Fe ++4H O
Fe 0 X
(元素价态: 氧化性
Fe O +4C0 3Fe +4CO
高中化学
课堂小结:铁及其化合物(1)
单质 氧化物 碱 盐
Fe O — Fe(OH) Fe +
Fe .Fe O
Fe0 Fe +
性质 转化
高中化学
价 态
类别
某同学从食品袋里取出一包脱氧剂(主要 成分是还原铁粉),想要探究其是否还有脱氧 能力,请你利用本节课所学知识和方法,设计 实验方案,并与同学讨论。
课后作业
高中化学
谢谢!
高中化学
铁及其化合物(第一课时)
高中化学
人类使用铁的历史
·公元前2500年人类已发现和使用铁
·约公元前2000年人类发明了用铁矿石冶炼铁的
方法
陨铁
高中化学
甘肃灵台山出土的春秋初年秦国的铜柄铁剑
高中化学
我国目前发现最早的人工冶铁制品
战国时期最大的铁器——长方形铁炉
高中化学
我国古代冶铁技术
地壳中的元素含量(质量分数)
高中化学
常见的铁矿石
赤铁矿 (Fe O )
菱铁矿 (FeCO )
磁铁矿 (Fe O )
黄铁矿
(FeS )
高中化学
丹霞地貌的岩石
高中化学
作颜料、催化剂、医药领域等。
高中化学
Fe O 粉末用途
任务 用化学方法制备Fe O
活动1 哪些途径可以制备氧化铁
碱性氧化物 F8o
Fe+O - → Fe O
3Fe+20 点燃 Fe O
金属
l+0
金属氧化物
高中化学
任务 用化学方法制备Fe O
活动1 哪些途径可以制备氧化铁
碱性氧化物 F8o
Fe(OH) → Fe O
2Fe(OH) <=Fe O +3H O
碱性氧化物
碱
高中化学
任务 用化学方法制备Fe O
活动1 哪些途径可以制备Fe O
F 0
Fe+O +H O → Fe O ·xH O
3Fe+20 点燃 Fe O
Fe+H O- >Fe O
高中化学
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu ……
高中化学
还原 铁粉 FeO Fe O Fe O Fe(OH)
Fe(OH) 3
黑色 黑色 红棕色 黑色 白色
红褐色
受热 不分解 受热 不分解 受热 不分解 受热 不分解 不稳定
Fe+H 0(g)△>Fe(OH) +H
Fe+H 0(g) 高温 Fe O +H
活动2 预测铁与水蒸气反应的产物,说出依据
预测
相关物质的性质
500 ℃
分解为Fe O
高中化学
2
活动2 预测铁与水蒸气反应的产物,说出依据
预测 Fe+H O(g)△>Fe(OH) +H
Fe+H 0(g) 高温 Fe O +H
活动3 如何检验气体产物
活动4 实验装置应有几部分构成
高中化学
水蒸气发生器 主反应装置 除杂装置 收集检验装置
方 案
高中化学
铁粉与水蒸气反应
实验现象:加热时玻璃管内铁粉红热,点燃产物 气体能安静地燃烧。
反应原理:3Fe+4H O(g) 高温 Fe O +4H,
实验结论:铁能与水蒸气发生反应,生成Fe O 与氢气
高中化学
肥皂液 除杂收集
检验装置
燃着的火柴
铁粉与水蒸气反应
还原铁粉一
湿棉花一
水蒸气 发生器
主反应装置
方案评价
高中化学
方 案 二
金属
碱性氧化物
Fe
Fe O
△
e (0H)
任务 用化学方法制备Fe O
+O /H O(g)
Fe O
碱 盐
高中化学
3
一、铁的化学性质总结
1.与非金属单质(氯气、氧气等)反应
2.与非氧化性酸(稀盐酸、稀硫酸等)反应
3.与某些盐溶液 (CuSO 溶液等)反应
Fe与Cl Fe与稀盐酸 Fe 与 CuSO 溶 液
高中化学
一 、铁的化学性质总结
铁的化学性质: 还原性
铁与氯气反应
铁与盐酸反应 Fe+2H =F62+H T
铁与硫酸铜溶液反应 Fe+cuz=Fe+cu
高中化学
+3
Fe FeCl 等
Fe O
+2
Fe FeCl 、FeSO 等
+强氧化剂
+O 或H O(g)
+弱氧化剂
还原剂+氧化剂— → 氧化还原反应产物
一、铁的化学性质总结
还 原
化学性质
Fe
性
高中化学
一、铁的化学性质总结
4.与水的反应
2Na+2H O=2NaOH+H ↑
Mg+2H O( 热 ) = Mg(OH) +H ↑
2Al+6H O ( 沸 ) = 2Al(OH) +3H 个
3Fe+4H 0(g) 高温 Fe O +4H
高中化学
小结:金属与水的反应
高中化学
物质 FeO Fe O
Fe O
来源、俗名 赤铁矿、铁红
磁铁矿、磁性氧
化铁
色态 黑色粉末 红棕色粉末
黑色晶体
水溶性 不溶 不溶
不溶
二、 铁的氧化物性质总结
活动5 请预测Fe O 的化学性质,说出依据
高中化学
物质类别和元素价态,是学习元素及其化合物性
质的重要认识视角。
基于物质类别和元素价态,可以预测物质的性质。
例如,对于Fe O , 从物质类别来看,它属于金属氧化 物,据此可以预测它可能与酸发生反应;从元素价态 来看, Fe O 中铁元素的化合价是+3价,为铁元素的 高价态,据此可以预测它具有氧化性,可能与具有还 原性的物质发生反应。
高中化学
方法导引
认识元素及其化合物性质的视角
二 、铁的氧化物性质总结
物质类别:碱性氧化物
+3 Fe O +6H+=-2Fe ++3H O
Fe O { 2Fe(0H) -Fe O +3H O
(元素价态: 氧化性
Fe O +3C0 高温2Fe +3CO
高中化学
二 、铁的氧化物性质总结
物质类别:碱性氧化物
+2 FeO+2H+=—Fe ++H O
FeO
氧化性
《元素价态: Fe0 +CO: Fe +CO
( 还原性
6FeO+O =<=2Fe O
高中化学
高温
二 、铁的氧化物性质总结
物质类别:特殊氧化物
Fe O +8H+=—Fe ++2Fe ++4H O
Fe 0 X
(元素价态: 氧化性
Fe O +4C0 3Fe +4CO
高中化学
课堂小结:铁及其化合物(1)
单质 氧化物 碱 盐
Fe O — Fe(OH) Fe +
Fe .Fe O
Fe0 Fe +
性质 转化
高中化学
价 态
类别
某同学从食品袋里取出一包脱氧剂(主要 成分是还原铁粉),想要探究其是否还有脱氧 能力,请你利用本节课所学知识和方法,设计 实验方案,并与同学讨论。
课后作业
高中化学
谢谢!
高中化学
