8.2 金属的化学性质练习(含答案)-2023-2024学年九年级化学人教版下册
文档属性
| 名称 | 8.2 金属的化学性质练习(含答案)-2023-2024学年九年级化学人教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 71.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-30 00:00:00 | ||
图片预览


文档简介
8.2 金属的化学性质-2023-2024学年九年级化学人教版下册
一、单选题
1.现有甲、乙、丙三种颗粒大小相同的金属,分别投入相同的稀硫酸中,只有甲表面有气泡产生,再把乙和丙投入相同的硝酸银溶液中,过一会儿后,丙的表面有银析出,而乙没变化。则三种金属的活动性由强到弱顺序是()
A.甲 丙 乙 B.乙 丙 甲
C.丙 乙 甲 D.乙 甲 丙
2.下列化学反应属于置换反应的是()
A.CO+CuO Cu+CO2 B.Cl2+H2O=HCl+HClO
C.Na2O+2HCl=2NaCl+H2O D.Fe+CuSO4=FeSO4+Cu
3.北斗系统的全面建成彰显了中国航天的力量。在航天科技中运用了大量金属材料,下列有关金属材料的说法正确的是( )
A.常温下所有的金属都是固体
B.钢是纯净物,生铁是混合物
C.铁与硫酸铜溶液的反应属于复分解反应
D.为防止钢铁制品生锈,可在其表面刷漆
4.下列金属中,活动性最强的是( )
A.铝 B.银 C.镁 D.汞
5.甲、乙、丙、丁四种金属,只有丙在自然界中主要以单质形式存在,用甲制的容器可以盛放丁盐的水溶液,乙制的容器不可以盛放丁盐的水溶液。由此可以推断四种金属的活动性由强到弱的顺序为()
A.丙>乙>甲>丁 B.甲>丁>乙>丙
C.乙>丁>甲>丙 D.甲>乙>丁>丙
6.比较铜和银的金属活动性强弱,可选用的药品是( )
A.稀盐酸 B.稀硫酸 C.硫酸锌溶液 D.硝酸汞溶液
7.一定质量的镁条在氧气中完全燃烧后生成氧化镁。固体质量随时间的变化关系如下图所示。其中M2与M1的差表示的是 ( )
A.生成MgO的质量 B.参加反应的Mg的质量
C.参加反应的O2的质量 D.剩余的O2的质量
8.为延长食品保质期,在月饼、蛋糕等食品包装袋内常放有一小包食品抗氧化剂,下列物质可以用作食品抗氧化剂的是 ( )
A.炭粉 B.铁粉 C.氯化钙 D.生石灰
9.对反应: ,下列说法正确的是( )
A.该化学反应属于置换反应
B.反应中CO与CO2之间的质量比为1:1
C.反应后,固体物质的质量减少
D.该反应方程式读作:高温条件下,氧化铁加一氧化碳等于铁加二氧化碳
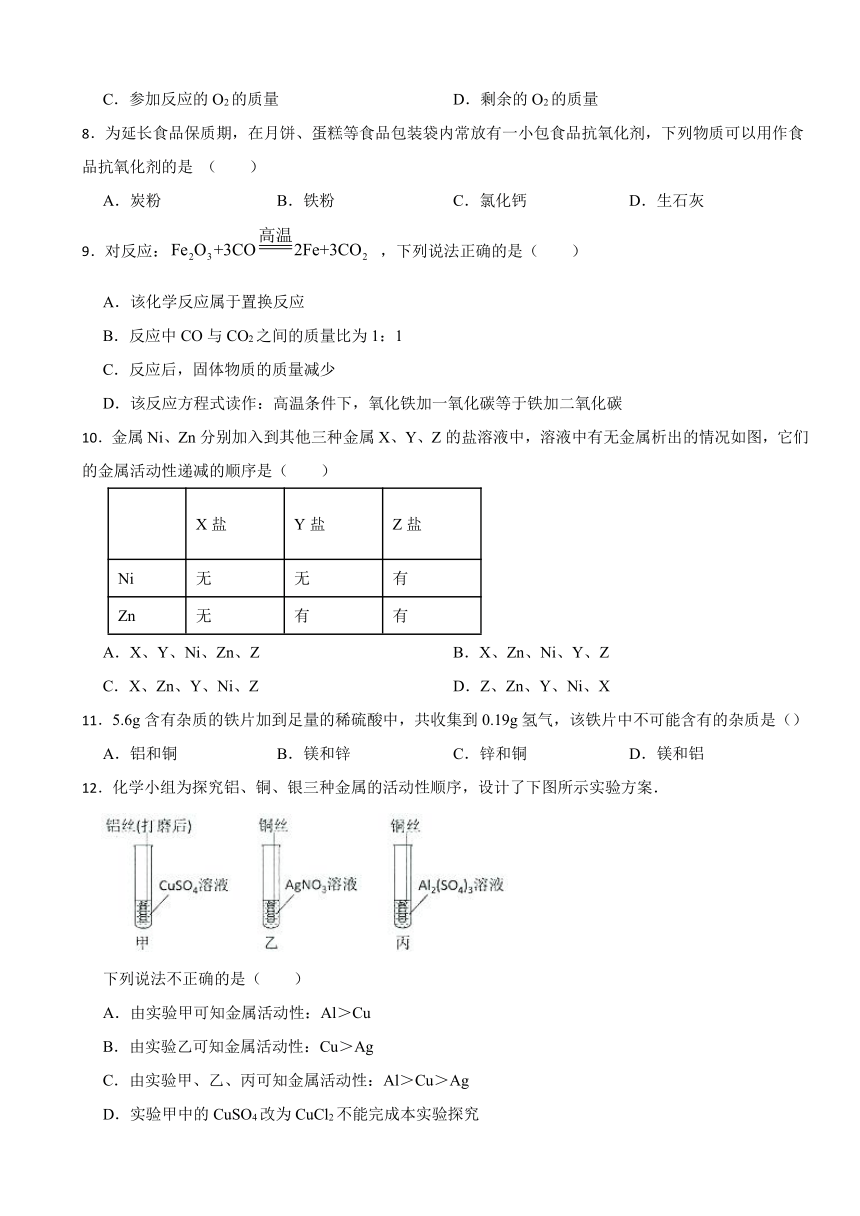
10.金属Ni、Zn分别加入到其他三种金属X、Y、Z的盐溶液中,溶液中有无金属析出的情况如图,它们的金属活动性递减的顺序是( )
X盐 Y盐 Z盐
Ni 无 无 有
Zn 无 有 有
A.X、Y、Ni、Zn、Z B.X、Zn、Ni、Y、Z
C.X、Zn、Y、Ni、Z D.Z、Zn、Y、Ni、X
11.5.6g含有杂质的铁片加到足量的稀硫酸中,共收集到0.19g氢气,该铁片中不可能含有的杂质是()
A.铝和铜 B.镁和锌 C.锌和铜 D.镁和铝
12.化学小组为探究铝、铜、银三种金属的活动性顺序,设计了下图所示实验方案.
下列说法不正确的是( )
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.由实验甲、乙、丙可知金属活动性:Al>Cu>Ag
D.实验甲中的CuSO4改为CuCl2不能完成本实验探究
二、填空题
13.相同质量的M、N两种活泼金属,分别与足量的稀盐酸在室温下发生反应(M、N在生成物中的化合价为均为+2价),生成H2的质量m和反应时间t的关系如图所示.
金属活动顺序是M比N (填“强”或“弱”);相对原的相对原子质量是M比N的 (填“大”或“小”).
14.金属材料与人类的生产和生活密切相关,请回答.
(1)下列用品中,主要利用金属导电性的是 (填字母).
A.金箔饰品 B.铁锅 C.铝导线
(2)为验证锌、铜、银的活动性顺序,设计了下列方案,其中可行的是 (填序号)
①将锌、银分别浸入到硫酸铜溶液中;
②将银分别浸入到硫酸锌、硫酸铜溶液中;
③将铜、银分别浸入到硫酸铝溶液中;
④将铜分别浸入到硫酸铝、硝酸银溶液中
(3)在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液.向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是 (填化学式).
三、计算题
15.欲测定某锌 铜合金中铜的质量分数,进行如下实验:取合金样品10克放入烧杯中,将60克稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
实验次数 第一次 第二次 第三次
加入稀硫酸质量 20 20 20
生成气体质量 m
请回答下列问题并计算:
(1)第二次实验时生成气体质量 克;
(2)计算该合金样品中铜的质量分数 .
四、实验探究题
16.一般情况下,金属越活泼,与酸反应的速度越快。为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下的实验。
(实验步骤)
①取ABC三支试管,分别加入2mL浓度相同的盐酸溶液,
②分别加入足量的、大小相等的Mg、Zn、Fe,立即把三个相同的气球分别套在各试管口上。
(实验预测与分析)
(1)写出铁与盐酸反应的化学方程式: .
(2)气球膨胀速度最快的是 (填试管编号),根据实验现象,你能得出这三种金属的活动性顺序为 。
(3)若用金属与化合物(盐)溶液的反应来比较Mg、Zn、Fe三种金属的活动性顺序,现已有Mg和Fe,还需用到的一种化合物(盐)溶液为 溶液。
17.某合金粉末中含有铜、银、铬(Cr),为了从中回收贵金属银和一种盐晶体,某化学兴趣小组的同学们将这三种金属随意编号为:A、B、C,设计了如下实验流程:
(1)A、B、C三种金属的活动性顺序由大到小为(用化学式作答) .
(2)操作a中除烧杯、玻璃棒外还需用到的玻璃仪器是 ,操作b的名称是 .
(3)已知A的硫酸盐中A元素是+2价,请写出步骤①的化学反应方程式 .
(4)已知D易溶于水,溶液D中的溶质是(写化学式) ,写出步骤②的化学反应方程式 .
(5)溶液D的质量(填“大于”、“小于”或“等于”) 溶液E的质量.
五、综合题
18.工业上处理黄铜渣(含有Cu、Zn、ZnO、CuO和杂质)废料时,通常将其转化为硫酸锌和铜等回收再利用。其主要流程如图所示(已知:杂质中不含铜,且不溶于水也不参与反应)。
(1)过程Ⅰ中,分离操作名称是 。
(2)写出加入B或试剂D反应的化学方程式为 。
答案解析部分
1.【答案】A
2.【答案】D
3.【答案】D
4.【答案】C
5.【答案】C
6.【答案】D
7.【答案】C
8.【答案】B
9.【答案】C
10.【答案】C
11.【答案】D
12.【答案】D
13.【答案】强;小
14.【答案】C;①④;Fe、Cu
15.【答案】(1)0.08g
(2)解:设锌的质量为x
Zn+H2SO4=ZnSO4+ H2↑
65 2
x 0.2g
x=6.5g 合金样品中铜的质量分数= ×100%=35%
16.【答案】(1)Fe + 2HCl = FeCl2 + H2↑
(2)A;Mg、Zn、Fe
(3)硫酸锌
17.【答案】(1)Cr>Cu>Ag
(2)漏斗;蒸发
(3)Cr+H2SO4═CrSO4+H2↑
(4)AgNO3;Cu+2AgNO3═Cu(NO3)2+2Ag
(5)大于
18.【答案】(1)过滤
(2)或
一、单选题
1.现有甲、乙、丙三种颗粒大小相同的金属,分别投入相同的稀硫酸中,只有甲表面有气泡产生,再把乙和丙投入相同的硝酸银溶液中,过一会儿后,丙的表面有银析出,而乙没变化。则三种金属的活动性由强到弱顺序是()
A.甲 丙 乙 B.乙 丙 甲
C.丙 乙 甲 D.乙 甲 丙
2.下列化学反应属于置换反应的是()
A.CO+CuO Cu+CO2 B.Cl2+H2O=HCl+HClO
C.Na2O+2HCl=2NaCl+H2O D.Fe+CuSO4=FeSO4+Cu
3.北斗系统的全面建成彰显了中国航天的力量。在航天科技中运用了大量金属材料,下列有关金属材料的说法正确的是( )
A.常温下所有的金属都是固体
B.钢是纯净物,生铁是混合物
C.铁与硫酸铜溶液的反应属于复分解反应
D.为防止钢铁制品生锈,可在其表面刷漆
4.下列金属中,活动性最强的是( )
A.铝 B.银 C.镁 D.汞
5.甲、乙、丙、丁四种金属,只有丙在自然界中主要以单质形式存在,用甲制的容器可以盛放丁盐的水溶液,乙制的容器不可以盛放丁盐的水溶液。由此可以推断四种金属的活动性由强到弱的顺序为()
A.丙>乙>甲>丁 B.甲>丁>乙>丙
C.乙>丁>甲>丙 D.甲>乙>丁>丙
6.比较铜和银的金属活动性强弱,可选用的药品是( )
A.稀盐酸 B.稀硫酸 C.硫酸锌溶液 D.硝酸汞溶液
7.一定质量的镁条在氧气中完全燃烧后生成氧化镁。固体质量随时间的变化关系如下图所示。其中M2与M1的差表示的是 ( )
A.生成MgO的质量 B.参加反应的Mg的质量
C.参加反应的O2的质量 D.剩余的O2的质量
8.为延长食品保质期,在月饼、蛋糕等食品包装袋内常放有一小包食品抗氧化剂,下列物质可以用作食品抗氧化剂的是 ( )
A.炭粉 B.铁粉 C.氯化钙 D.生石灰
9.对反应: ,下列说法正确的是( )
A.该化学反应属于置换反应
B.反应中CO与CO2之间的质量比为1:1
C.反应后,固体物质的质量减少
D.该反应方程式读作:高温条件下,氧化铁加一氧化碳等于铁加二氧化碳
10.金属Ni、Zn分别加入到其他三种金属X、Y、Z的盐溶液中,溶液中有无金属析出的情况如图,它们的金属活动性递减的顺序是( )
X盐 Y盐 Z盐
Ni 无 无 有
Zn 无 有 有
A.X、Y、Ni、Zn、Z B.X、Zn、Ni、Y、Z
C.X、Zn、Y、Ni、Z D.Z、Zn、Y、Ni、X
11.5.6g含有杂质的铁片加到足量的稀硫酸中,共收集到0.19g氢气,该铁片中不可能含有的杂质是()
A.铝和铜 B.镁和锌 C.锌和铜 D.镁和铝
12.化学小组为探究铝、铜、银三种金属的活动性顺序,设计了下图所示实验方案.
下列说法不正确的是( )
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.由实验甲、乙、丙可知金属活动性:Al>Cu>Ag
D.实验甲中的CuSO4改为CuCl2不能完成本实验探究
二、填空题
13.相同质量的M、N两种活泼金属,分别与足量的稀盐酸在室温下发生反应(M、N在生成物中的化合价为均为+2价),生成H2的质量m和反应时间t的关系如图所示.
金属活动顺序是M比N (填“强”或“弱”);相对原的相对原子质量是M比N的 (填“大”或“小”).
14.金属材料与人类的生产和生活密切相关,请回答.
(1)下列用品中,主要利用金属导电性的是 (填字母).
A.金箔饰品 B.铁锅 C.铝导线
(2)为验证锌、铜、银的活动性顺序,设计了下列方案,其中可行的是 (填序号)
①将锌、银分别浸入到硫酸铜溶液中;
②将银分别浸入到硫酸锌、硫酸铜溶液中;
③将铜、银分别浸入到硫酸铝溶液中;
④将铜分别浸入到硫酸铝、硝酸银溶液中
(3)在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液.向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是 (填化学式).
三、计算题
15.欲测定某锌 铜合金中铜的质量分数,进行如下实验:取合金样品10克放入烧杯中,将60克稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
实验次数 第一次 第二次 第三次
加入稀硫酸质量 20 20 20
生成气体质量 m
请回答下列问题并计算:
(1)第二次实验时生成气体质量 克;
(2)计算该合金样品中铜的质量分数 .
四、实验探究题
16.一般情况下,金属越活泼,与酸反应的速度越快。为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下的实验。
(实验步骤)
①取ABC三支试管,分别加入2mL浓度相同的盐酸溶液,
②分别加入足量的、大小相等的Mg、Zn、Fe,立即把三个相同的气球分别套在各试管口上。
(实验预测与分析)
(1)写出铁与盐酸反应的化学方程式: .
(2)气球膨胀速度最快的是 (填试管编号),根据实验现象,你能得出这三种金属的活动性顺序为 。
(3)若用金属与化合物(盐)溶液的反应来比较Mg、Zn、Fe三种金属的活动性顺序,现已有Mg和Fe,还需用到的一种化合物(盐)溶液为 溶液。
17.某合金粉末中含有铜、银、铬(Cr),为了从中回收贵金属银和一种盐晶体,某化学兴趣小组的同学们将这三种金属随意编号为:A、B、C,设计了如下实验流程:
(1)A、B、C三种金属的活动性顺序由大到小为(用化学式作答) .
(2)操作a中除烧杯、玻璃棒外还需用到的玻璃仪器是 ,操作b的名称是 .
(3)已知A的硫酸盐中A元素是+2价,请写出步骤①的化学反应方程式 .
(4)已知D易溶于水,溶液D中的溶质是(写化学式) ,写出步骤②的化学反应方程式 .
(5)溶液D的质量(填“大于”、“小于”或“等于”) 溶液E的质量.
五、综合题
18.工业上处理黄铜渣(含有Cu、Zn、ZnO、CuO和杂质)废料时,通常将其转化为硫酸锌和铜等回收再利用。其主要流程如图所示(已知:杂质中不含铜,且不溶于水也不参与反应)。
(1)过程Ⅰ中,分离操作名称是 。
(2)写出加入B或试剂D反应的化学方程式为 。
答案解析部分
1.【答案】A
2.【答案】D
3.【答案】D
4.【答案】C
5.【答案】C
6.【答案】D
7.【答案】C
8.【答案】B
9.【答案】C
10.【答案】C
11.【答案】D
12.【答案】D
13.【答案】强;小
14.【答案】C;①④;Fe、Cu
15.【答案】(1)0.08g
(2)解:设锌的质量为x
Zn+H2SO4=ZnSO4+ H2↑
65 2
x 0.2g
x=6.5g 合金样品中铜的质量分数= ×100%=35%
16.【答案】(1)Fe + 2HCl = FeCl2 + H2↑
(2)A;Mg、Zn、Fe
(3)硫酸锌
17.【答案】(1)Cr>Cu>Ag
(2)漏斗;蒸发
(3)Cr+H2SO4═CrSO4+H2↑
(4)AgNO3;Cu+2AgNO3═Cu(NO3)2+2Ag
(5)大于
18.【答案】(1)过滤
(2)或
同课章节目录
