化学人教版(2019)选择性必修2 2.1.1共价键(共25张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修2 2.1.1共价键(共25张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 13.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-30 00:00:00 | ||
图片预览








文档简介
(共25张PPT)
第一节 共价键
2.1.1 共价键
人教版高中化学选必二
课程导入
诺贝尔物理学奖得主理查德·费曼曾说过,假如发生了大灾难,人类全部的科学知识只能概括为一句话传诸后世,那么这句话应该是“万物皆由原子构成”。
原子是如何构成物质的?
目录
σ键和π键的判断
03
04
共价键的概念与特征
01
共价键的形成
02
PART 01
·共价键的概念与特征·
SAFE USE EDUCATION
共价键的概念
概念:共价键是原子间通过共用电子对所形成的强烈相互作用。
成键的粒子:一般为 原子 (相同或不相同)之间或少部分金属原子与非金属原子之间(如AlCl3、BeCl2等化合物)
非金属
本质:原子之间通过共用电子对(即原子轨道的重叠)产生的强烈作用,且自旋方向相反的未成对电子形成共用电子对。
共价键的特征
饱和性:一个原子有几个 ,便可和几个 电子配对成键。如只能有H2、HCl、Cl2等,不可能有H3、H2Cl、Cl3等。
未成对电子
自旋状态相反的
方向性:除s轨道球对称外,其他原子轨道在空间都具有一定的分布特点。在形成共价键时,原子轨道重叠的越多,电子出现在核间的概率越大,共价键就越牢固。因此共价键将尽可能
沿着电子出现概率最大的方向形成,即共价键
具有方向性。
PART 02
·共价键的形成·
SAFE USE EDUCATION
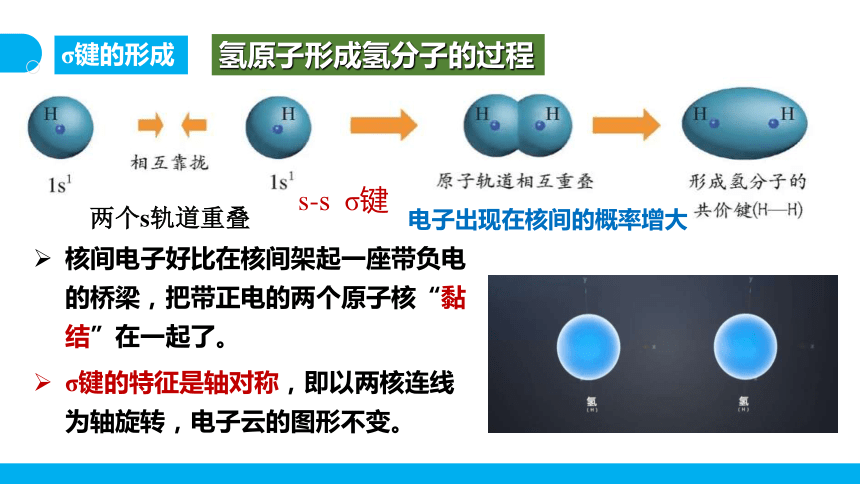
σ键的形成
氢原子形成氢分子的过程
s-s σ键
两个s轨道重叠
电子出现在核间的概率增大
核间电子好比在核间架起一座带负电的桥梁,把带正电的两个原子核“黏结”在一起了。
σ键的特征是轴对称,即以两核连线为轴旋转,电子云的图形不变。
σ键的形成
H-Cl的s-p σ键形成
↑
1s1
↑↓
↑↓
↑↓
↑
3s2
3p5
s-p轨道以 “头碰头”
的方式重叠
s-p σ键
特征:轴对称
σ键的形成
Cl-Cl的p-p σ键形成
↑↓
↑↓
↑↓
↑
3s2
3p5
↑↓
↑↓
↑↓
↑
3s2
3p5
p-p σ键
特征:轴对称
p-p 轨道以 “头碰头”
的方式重叠
π键的形成
p轨道与p轨道除了能形成σ键外,还能形成π键。
p-p π键
电子云由两块组成,互为镜像
特征:镜面对称
p-p 轨道以 “肩并肩”
的方式重叠
π键的形成
N2中1个p-p σ键和2个p-p π键的形成过程
↑ ↑ ↑
2P3轨道
π键的形成
O2 中 p-p σ键和 p-p π键的形成过程
p-p σ键
p-p π键
两对孤对电子对电子云
↑↓ ↑ ↑
2P4轨道
σ键和π键的强度不同。
乙烯、乙炔分子中π键不如σ键牢固,容易断裂,所以含有π键的乙烯、乙炔与只有σ键的乙烷化学性质不同;
N2分子中的π键比σ键稳定。
σ键和π键的强度
PART 03
·σ键和π键的判断·
SAFE USE EDUCATION
判断σ键、π键的一般规律
数目角度:
共价单键为 键;
共价双键中有一个 键、一个 键;
共价三键由一个 键和两个 键构成。
σ
σ
π
σ
π
原子轨道角度:
s-s电子、s-p电子只形成σ键;
p-p电子可形成σ键,也可形成π键,且先形成σ键, 后形成π键。
探究共价键——问题和预测
观察乙烷、乙烯和乙炔的分子的结构,它们的分子中的共价键分别由几个σ键和几个π键构成?
乙烷分子中由7个σ键组成;乙烯分子中由5个σ键和1个π键组成;乙炔分子中由3个σ键和2个π键组成。
乙烷
乙烯
乙炔
探究共价键——问题与讨论
钠和氯通过得失电子同样是形成电子对,为什么这对电子不被钠原子和氯原子共用形成共价键而是离子键呢?你能从元素的电负性差别来理解吗?
原子 Na Cl H Cl C O
电负性 0.9 3.0 2.1 3.0 2.5 3.5
电负性之差 (绝对值) 2.1 0.9 1.0 当成键原子的电负性相差很大时,形成的电子对不会被共用,形成的将是离子键;而共价键是电负性相差不大的原子之间形成的化学键。
课堂小结
本质:原子之间通过共用电子对(或原子轨道重叠)形成共价键
特征:具有方向性和饱和性
成键方式
σ键
原子轨道“头碰头”重叠,电子云呈轴对称
π键
原子轨道“肩并肩”重叠,电子云呈镜面对称
共价三键——1个σ键、2个π键
共价单键——1个σ键
共价双键——1个σ键、1个π键
一般规律
本质和特征
课堂练习
√
1.下列不属于共价键成键因素的是
A.共用电子对在两原子核之间高概率出现
B.共用的电子必须配对
C.成键后体系能量降低,趋于稳定
D.两原子体积大小要适中
课堂练习
√
2.下列说法正确的是
A.Cl2是双原子分子,H2S是三原子分子,这是由共价键的方向性决定的
B.H2O与H2S的空间结构一样是由共价键的饱和性决定的
C.并非所有的共价键都有方向性
D.两原子轨道发生重叠后,电子在两核间出现的概率减小
课堂练习
√
3.下列说法对σ键和π键的认识不正确的是
A.分子中只要含有共价键,则至少含有一个σ键
B.s-s σ键、p-p σ键与s-p σ键都是轴对称的
C.p-p σ键和p-p π键的重叠方式是相同的
D.含有π键的分子在反应时,π键是化学反应的积极参与者
课堂练习
√
4.丁烯二酸(HOOCCH==CHCOOH)分子结构中含有σ键、π键的个数分别是
A.4个σ键,1个π键 B.11个σ键,3个π键
C.4个σ键,3个π键 D.9个σ键,5个π键
课堂练习
5.(1) 分子中σ键和π键的比例为________。
9∶1
(2)已知反应N2O4(l)+2N2H4(l)===3N2(g)+4H2O(l),若该反应中有4 mol N—H断裂,则形成的π键的数目为_____。
3NA
课 程 结 束
人教版高中化学选必二
第一节 共价键
2.1.1 共价键
人教版高中化学选必二
课程导入
诺贝尔物理学奖得主理查德·费曼曾说过,假如发生了大灾难,人类全部的科学知识只能概括为一句话传诸后世,那么这句话应该是“万物皆由原子构成”。
原子是如何构成物质的?
目录
σ键和π键的判断
03
04
共价键的概念与特征
01
共价键的形成
02
PART 01
·共价键的概念与特征·
SAFE USE EDUCATION
共价键的概念
概念:共价键是原子间通过共用电子对所形成的强烈相互作用。
成键的粒子:一般为 原子 (相同或不相同)之间或少部分金属原子与非金属原子之间(如AlCl3、BeCl2等化合物)
非金属
本质:原子之间通过共用电子对(即原子轨道的重叠)产生的强烈作用,且自旋方向相反的未成对电子形成共用电子对。
共价键的特征
饱和性:一个原子有几个 ,便可和几个 电子配对成键。如只能有H2、HCl、Cl2等,不可能有H3、H2Cl、Cl3等。
未成对电子
自旋状态相反的
方向性:除s轨道球对称外,其他原子轨道在空间都具有一定的分布特点。在形成共价键时,原子轨道重叠的越多,电子出现在核间的概率越大,共价键就越牢固。因此共价键将尽可能
沿着电子出现概率最大的方向形成,即共价键
具有方向性。
PART 02
·共价键的形成·
SAFE USE EDUCATION
σ键的形成
氢原子形成氢分子的过程
s-s σ键
两个s轨道重叠
电子出现在核间的概率增大
核间电子好比在核间架起一座带负电的桥梁,把带正电的两个原子核“黏结”在一起了。
σ键的特征是轴对称,即以两核连线为轴旋转,电子云的图形不变。
σ键的形成
H-Cl的s-p σ键形成
↑
1s1
↑↓
↑↓
↑↓
↑
3s2
3p5
s-p轨道以 “头碰头”
的方式重叠
s-p σ键
特征:轴对称
σ键的形成
Cl-Cl的p-p σ键形成
↑↓
↑↓
↑↓
↑
3s2
3p5
↑↓
↑↓
↑↓
↑
3s2
3p5
p-p σ键
特征:轴对称
p-p 轨道以 “头碰头”
的方式重叠
π键的形成
p轨道与p轨道除了能形成σ键外,还能形成π键。
p-p π键
电子云由两块组成,互为镜像
特征:镜面对称
p-p 轨道以 “肩并肩”
的方式重叠
π键的形成
N2中1个p-p σ键和2个p-p π键的形成过程
↑ ↑ ↑
2P3轨道
π键的形成
O2 中 p-p σ键和 p-p π键的形成过程
p-p σ键
p-p π键
两对孤对电子对电子云
↑↓ ↑ ↑
2P4轨道
σ键和π键的强度不同。
乙烯、乙炔分子中π键不如σ键牢固,容易断裂,所以含有π键的乙烯、乙炔与只有σ键的乙烷化学性质不同;
N2分子中的π键比σ键稳定。
σ键和π键的强度
PART 03
·σ键和π键的判断·
SAFE USE EDUCATION
判断σ键、π键的一般规律
数目角度:
共价单键为 键;
共价双键中有一个 键、一个 键;
共价三键由一个 键和两个 键构成。
σ
σ
π
σ
π
原子轨道角度:
s-s电子、s-p电子只形成σ键;
p-p电子可形成σ键,也可形成π键,且先形成σ键, 后形成π键。
探究共价键——问题和预测
观察乙烷、乙烯和乙炔的分子的结构,它们的分子中的共价键分别由几个σ键和几个π键构成?
乙烷分子中由7个σ键组成;乙烯分子中由5个σ键和1个π键组成;乙炔分子中由3个σ键和2个π键组成。
乙烷
乙烯
乙炔
探究共价键——问题与讨论
钠和氯通过得失电子同样是形成电子对,为什么这对电子不被钠原子和氯原子共用形成共价键而是离子键呢?你能从元素的电负性差别来理解吗?
原子 Na Cl H Cl C O
电负性 0.9 3.0 2.1 3.0 2.5 3.5
电负性之差 (绝对值) 2.1 0.9 1.0 当成键原子的电负性相差很大时,形成的电子对不会被共用,形成的将是离子键;而共价键是电负性相差不大的原子之间形成的化学键。
课堂小结
本质:原子之间通过共用电子对(或原子轨道重叠)形成共价键
特征:具有方向性和饱和性
成键方式
σ键
原子轨道“头碰头”重叠,电子云呈轴对称
π键
原子轨道“肩并肩”重叠,电子云呈镜面对称
共价三键——1个σ键、2个π键
共价单键——1个σ键
共价双键——1个σ键、1个π键
一般规律
本质和特征
课堂练习
√
1.下列不属于共价键成键因素的是
A.共用电子对在两原子核之间高概率出现
B.共用的电子必须配对
C.成键后体系能量降低,趋于稳定
D.两原子体积大小要适中
课堂练习
√
2.下列说法正确的是
A.Cl2是双原子分子,H2S是三原子分子,这是由共价键的方向性决定的
B.H2O与H2S的空间结构一样是由共价键的饱和性决定的
C.并非所有的共价键都有方向性
D.两原子轨道发生重叠后,电子在两核间出现的概率减小
课堂练习
√
3.下列说法对σ键和π键的认识不正确的是
A.分子中只要含有共价键,则至少含有一个σ键
B.s-s σ键、p-p σ键与s-p σ键都是轴对称的
C.p-p σ键和p-p π键的重叠方式是相同的
D.含有π键的分子在反应时,π键是化学反应的积极参与者
课堂练习
√
4.丁烯二酸(HOOCCH==CHCOOH)分子结构中含有σ键、π键的个数分别是
A.4个σ键,1个π键 B.11个σ键,3个π键
C.4个σ键,3个π键 D.9个σ键,5个π键
课堂练习
5.(1) 分子中σ键和π键的比例为________。
9∶1
(2)已知反应N2O4(l)+2N2H4(l)===3N2(g)+4H2O(l),若该反应中有4 mol N—H断裂,则形成的π键的数目为_____。
3NA
课 程 结 束
人教版高中化学选必二
