9.3 溶液的浓度 练习(含答案)-2023-2024学年九年级化学人教版下册
文档属性
| 名称 | 9.3 溶液的浓度 练习(含答案)-2023-2024学年九年级化学人教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 111.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-30 00:00:00 | ||
图片预览


文档简介
9.3 溶液的浓度-2023-2024学年九年级化学人教版下册
一、单选题
1.甲、乙两种固体的溶解度曲线如图所示。下列说法错误的是( )
A.20℃时,甲和乙两种物质的溶解度均为30 g
B.40℃时,甲物质的溶解度比乙物质的溶解度大10 g
C.将20℃时乙的饱和溶液升温至40℃,溶质质量分数不变
D.将40℃时甲的不饱和溶液降温至20℃,溶液会变为饱和溶液
2.对“溶质质量分数为15%的氯化钠溶液”的含义理解错误的是( )
A.100g氯化钠溶液中溶解了15g氯化钠
B.将氯化钠与水按15:85的质量比配成的溶液
C.将30g氯化钠溶解于170g水中所得到的溶液
D.100g水中溶解了15g氯化钠
3.如图为a、b、c三种不含结晶水的固体物质的溶解度曲线,下列叙述中正确的是( )
A.t1℃时,a、b、c饱和溶液的溶质质量分数为20%
B.P点表示时,t2℃时,a、b的溶液是饱和状态,c的溶液是不饱和状态
C.t2℃时,a、b、c三种物质溶液的溶质质量分数a>b>c
D.70ga的饱和溶液从t2℃降温到t1℃时,析出晶体15g
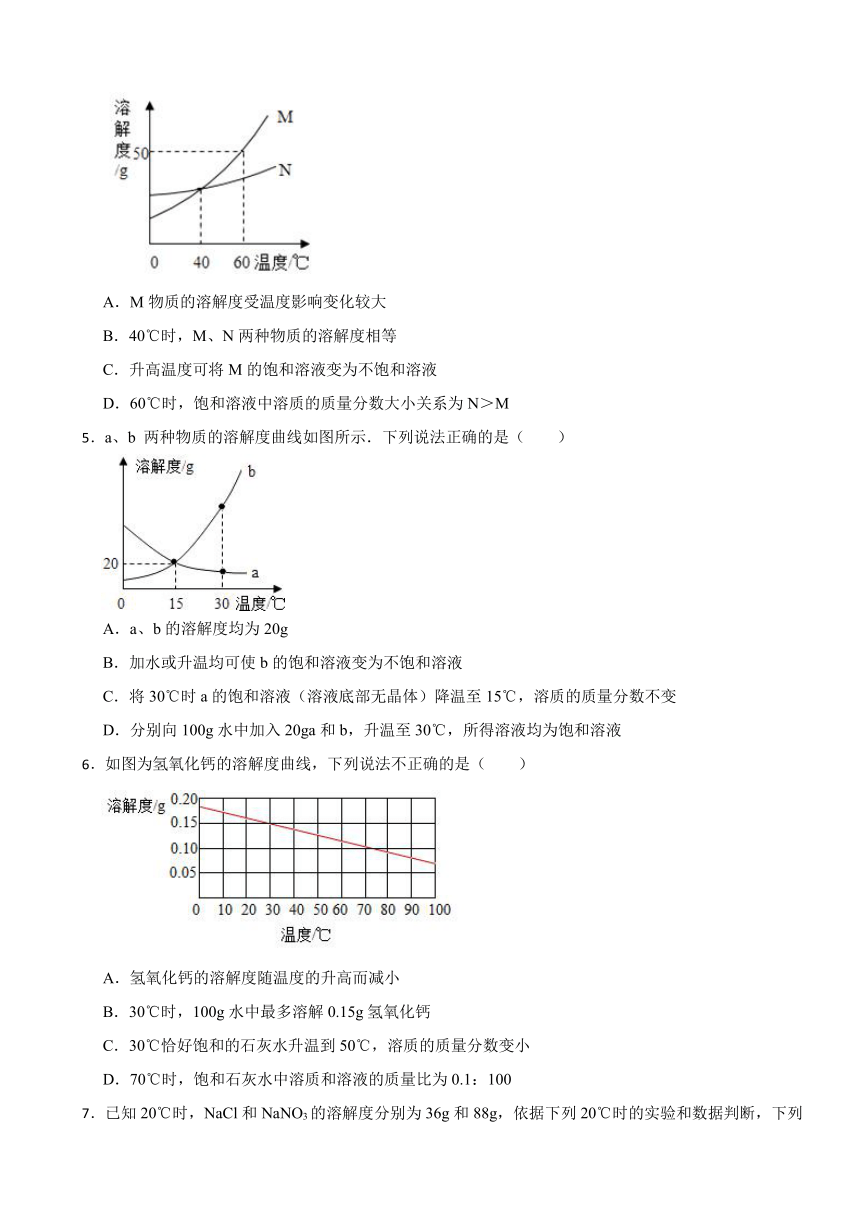
4.右图是M、N两种固体物质的溶解度曲线,下列说法错误的是( )
A.M物质的溶解度受温度影响变化较大
B.40℃时,M、N两种物质的溶解度相等
C.升高温度可将M的饱和溶液变为不饱和溶液
D.60℃时,饱和溶液中溶质的质量分数大小关系为N>M
5.a、b 两种物质的溶解度曲线如图所示.下列说法正确的是( )
A.a、b的溶解度均为20g
B.加水或升温均可使b的饱和溶液变为不饱和溶液
C.将30℃时a的饱和溶液(溶液底部无晶体)降温至15℃,溶质的质量分数不变
D.分别向100g水中加入20ga和b,升温至30℃,所得溶液均为饱和溶液
6.如图为氢氧化钙的溶解度曲线,下列说法不正确的是( )
A.氢氧化钙的溶解度随温度的升高而减小
B.30℃时,100g水中最多溶解0.15g氢氧化钙
C.30℃恰好饱和的石灰水升温到50℃,溶质的质量分数变小
D.70℃时,饱和石灰水中溶质和溶液的质量比为0.1:100
7.已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g,依据下列20℃时的实验和数据判断,下列说法不正确的是( )
序号 ① ② ③ ④ ⑤.
固体种类 NaCl NaCl NaNO3 NaNO3 NaNO3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
A.②⑤属于饱和溶液:
B.溶液质量:②<④
C.溶质质量分数:①=③
D.⑤中溶质与溶剂的质量比为9:10
8.下列有关溶液的说法中,正确的是()
A.常温下将10mL饱和Ca(OH)2溶液加热到50℃,会使溶液由饱和溶液变为不饱和溶液
B.将95gCaCl2溶液蒸干得到15g固体,则原溶液中CaCl2的质分数为15%
C.从质量分数为10%的H2SO4溶液中取出10mL,则取出的10mLH2SO4溶液的质分数仍为10%
D.20℃时,50g水中溶解了18gNaCl,则20℃时NaCl的溶解度为36g
9.现有氢氧化钠和氢氧化钙的固体混合物7.7克,与100克7.3%的稀盐酸恰好完全反应,则所得溶液中两种溶质的总质量为( )
A.13.2克 B.13.5克
C.11.7克 D.11.4克
10.如图是A,B,C三种固体物质的溶解度曲线,下列分析正确的是( )
A.20℃时等质量的A和C两种物质的溶液中溶质的质量相等
B.50℃时把50gA放入100g水中能得到A的饱和溶液,其溶质质量分数为50%
C.将50℃时A,B,C三种物质的饱和溶液都降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=C
D.将C的饱和溶液变为不饱和溶液,可采用降温的方法
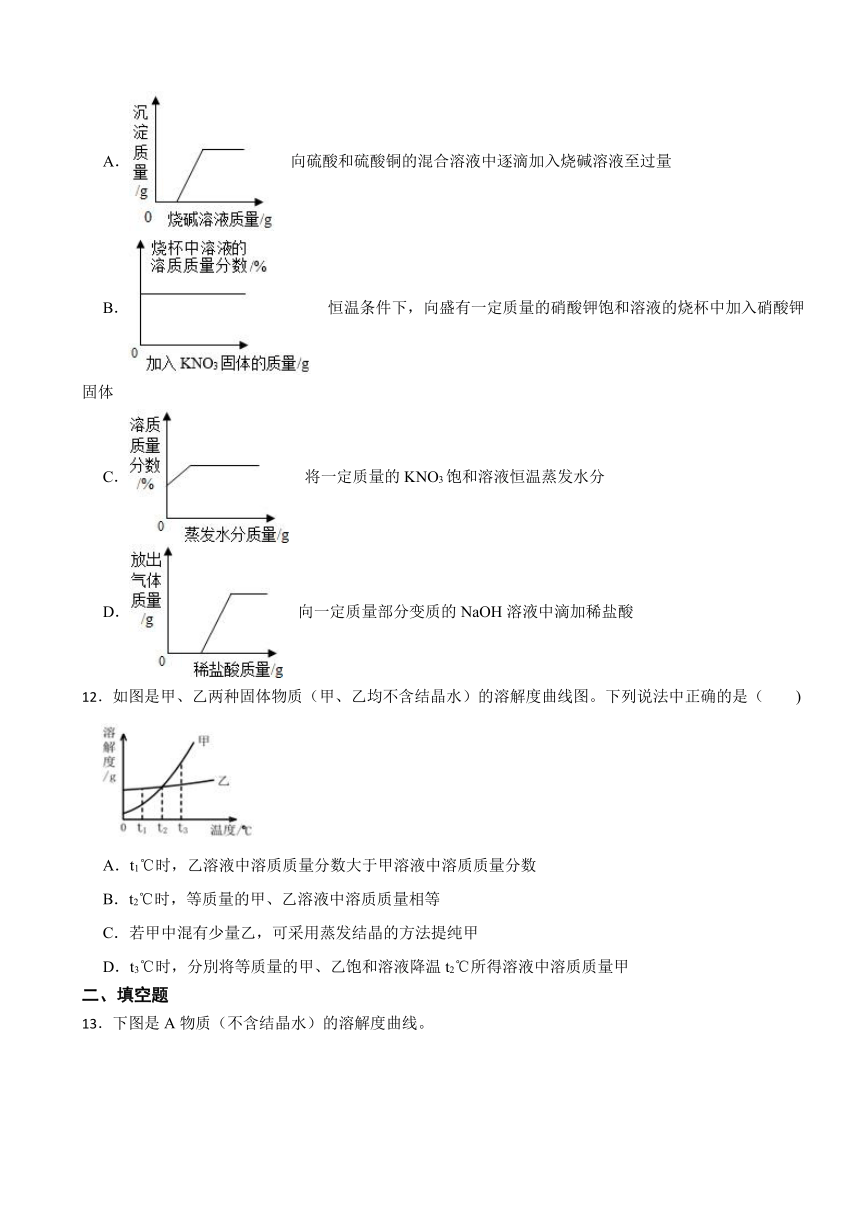
11.下列图像不能正确反映其对应操作中各量变化关系的是( )
A. 向硫酸和硫酸铜的混合溶液中逐滴加入烧碱溶液至过量
B. 恒温条件下,向盛有一定质量的硝酸钾饱和溶液的烧杯中加入硝酸钾固体
C. 将一定质量的KNO3饱和溶液恒温蒸发水分
D. 向一定质量部分变质的NaOH溶液中滴加稀盐酸
12.如图是甲、乙两种固体物质(甲、乙均不含结晶水)的溶解度曲线图。下列说法中正确的是( )
A.t1℃时,乙溶液中溶质质量分数大于甲溶液中溶质质量分数
B.t2℃时,等质量的甲、乙溶液中溶质质量相等
C.若甲中混有少量乙,可采用蒸发结晶的方法提纯甲
D.t3℃时,分別将等质量的甲、乙饱和溶液降温t2℃所得溶液中溶质质量甲
二、填空题
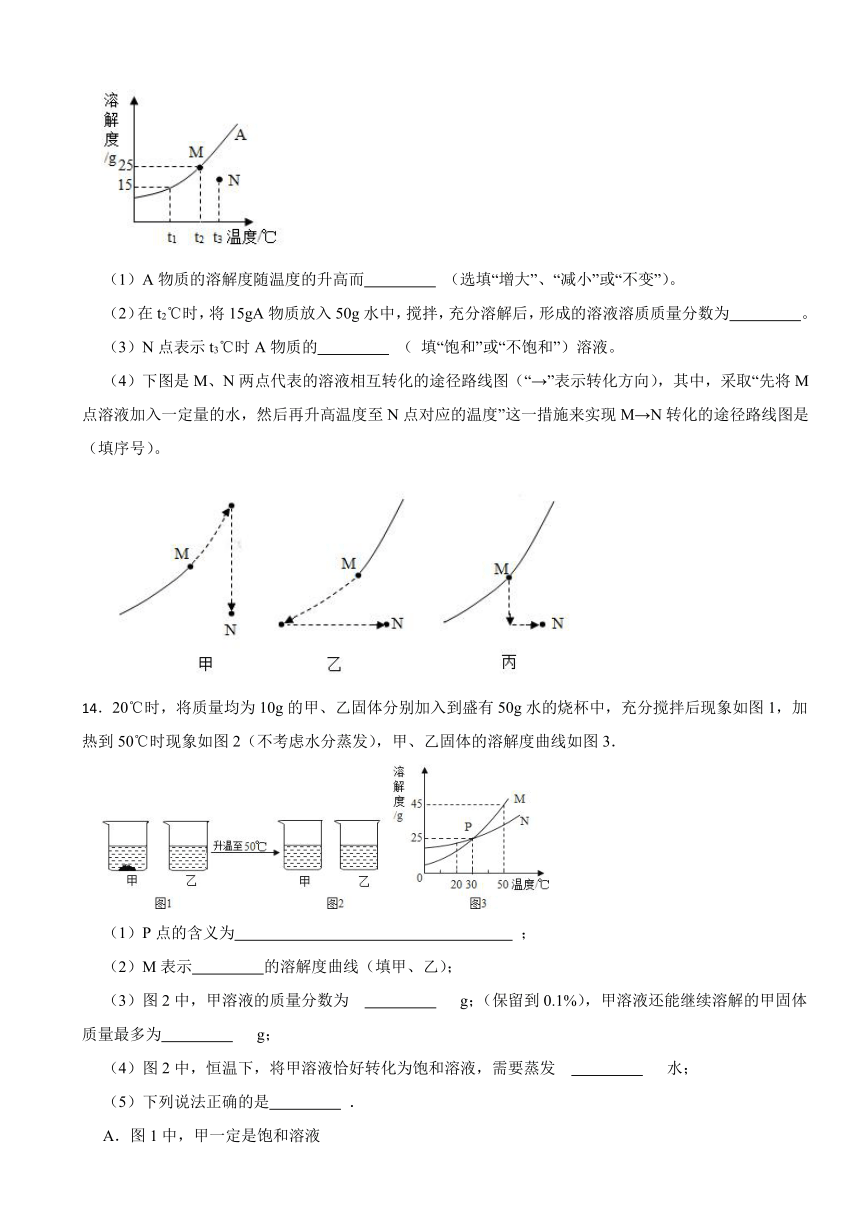
13.下图是A物质(不含结晶水)的溶解度曲线。
(1)A物质的溶解度随温度的升高而 (选填“增大”、“减小”或“不变”)。
(2)在t2℃时,将15gA物质放入50g水中,搅拌,充分溶解后,形成的溶液溶质质量分数为 。
(3)N点表示t3℃时A物质的 ( 填“饱和”或“不饱和”)溶液。
(4)下图是M、N两点代表的溶液相互转化的途径路线图(“→”表示转化方向),其中,采取“先将M点溶液加入一定量的水,然后再升高温度至N点对应的温度”这一措施来实现M→N转化的途径路线图是 (填序号)。
14.20℃时,将质量均为10g的甲、乙固体分别加入到盛有50g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解度曲线如图3.
(1)P点的含义为 ;
(2)M表示 的溶解度曲线(填甲、乙);
(3)图2中,甲溶液的质量分数为 g;(保留到0.1%),甲溶液还能继续溶解的甲固体质量最多为 g;
(4)图2中,恒温下,将甲溶液恰好转化为饱和溶液,需要蒸发 水;
(5)下列说法正确的是 .
A.图1中,甲一定是饱和溶液
B.图2中,两溶液中溶质的质量分数一定相等
C.图2中,两溶液降温至30℃一定都不会析出晶体.
三、计算题
15.现有一瓶久置的过氧化氢溶液(标签如图所示)。已知过氧化氢溶液在存放过程中会缓慢分解。取该溶液 34g 于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是 33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣 3g.请计算:
(1)完全反应后生成氧气的质量 。
(2)求该瓶溶液中溶质的质量分数 。
(3)用该瓶溶液配制 100g 溶质质量分数为 3%的过氧化氢溶液需要加入水的质量 。
四、实验探究题
16.如图为A、B两种固体物质的溶解度曲线,请根据图示信息回答:
(1)t1℃时,A物质的溶解度是 g。
(2)A,B两种物质中, 的溶解度受温度的影响较小。
(3)t2℃时,将35gA物质加入到50g水中,充分溶解后,得到该温度下A物质的 (填“饱和”或“不饱和”)溶液。此时溶液的溶质质量分数为 。
17.实验小组同学在一定温度下进行硝酸钾的固体的溶解实验。
(1)(定性研究)同学们进行如下实验,发现1号试管中硝酸钾全部溶解,2号试管中固体没有完全溶解。要使2号试管中的固体全部溶解,可采取的方法有 。(列举一条即可)。
(2)(定量研究)实验小组同学在一定温度下进行硝酸钾的固体溶液实验。实验数据如下:
实验序号 实验1 实验2 实验3 实验4
水的质量(g) 100 100 100 100
加入硝酸钾的质量(g) 80 100 120 140
溶液质量(g) 180 200 210 M
请根据数据进行分析:
请计算实验2所得溶液中硝酸钾的质量分数是 。
(3)现将实验2中的溶液稀释成10%的硝酸钾溶液,需要加水的质量为 g。
(4)请判断实验2中硝酸钾溶液是 溶液。(选填“饱和”或“不饱和”)
(5)实验4中M的数值是 。
18.溶解度可表示物质溶解性的大小.
(1)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.
①20℃时,甲的溶解度 (填“>”、“<”或“=”)乙的溶解度.
②40℃时,乙和丙 (填“能”或“不能”)形成溶质质量分数相同的饱和溶液.
③20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃.请填写下表.
烧杯中的溶质 烧杯中固体的变化
甲 固体逐渐
乙 固体逐渐
丙 固体逐渐
(2)气体的溶解度也有一定的变化规律:
打开可乐瓶,逸出大量气泡.由此可见,压强越小,CO2的溶解度越 .为增大CO2的溶解度,可采用的一种方法是 .
五、综合题
19.水是人类宝贵的自然资源.
(1)硬水给人们生活和生产带来很多麻烦,区分硬水和软水生活中常用的物质是 .
(2)在厨房用水洗涤餐具时,通常在水里加些洗涤剂,这样就可以很容易的除去餐具上的油污,这是因为洗涤剂具有 (填“溶解”或“乳化”)作用.
(3)电影《火星救援》中马特 达蒙采用①液态的火箭燃料联氨(N2H4)在密闭容器中高温分解生成氮气、氢气和氨气(NH3),②分解出的氢气燃烧制取水的方法,解决了火星上缺少液态水的问题,写出①的化学方程式
(4)如图是A、B、C三种固体物质的溶解度曲线,据图回答:
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 .
②t2℃时,C物质的饱和溶液转化为不饱和溶液的方法是 .
③t1℃时,30gA物质加入到50g水中不断搅拌形成的溶液质量是 g.
④t2℃时,将A、B、C三种物质饱和溶液分别降温至t1℃时,所得溶液中的溶质质量分数由大到小顺序为 .
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】A
4.【答案】D
5.【答案】C
6.【答案】D
7.【答案】D
8.【答案】C
9.【答案】D
10.【答案】D
11.【答案】C
12.【答案】D
13.【答案】(1)增大
(2)20%
(3)不饱和
(4)丙
14.【答案】30℃,M、N两种物质的溶解度相等;甲;16.7%;12.5;27.8;ABC
15.【答案】(1)解:生成氧气的质量为:34g+3g-33.8g=3.2g,
(2)解:设:取出的34g过氧化氢溶液中含H2O2的质量为x,
2H2O2 2H2O+ O2↑
68 32
x 3.2g
x=6.8g, 所以该过氧化氢溶液中溶质质量分数为: 答:该过氧化氢溶液中溶质质量分数为20%.
(3)解:设配制100g溶质质量分数为3%的过氧化氢溶液需该溶液质量为y, 100g×3%=20%×y, y=15g, 则需加水的质量为:100g-15g=85g, 答:需加水的质量为85g.
16.【答案】(1)20
(2)B
(3)饱和;37.5%
17.【答案】(1)加水或升温
(2)50%
(3)800
(4)不饱和
(5)210
18.【答案】(1)<;能;全部溶解;部分溶解;固体不溶解,反而增多
(2)小;增大压强或降低温度
19.【答案】(1)肥皂水
(2)乳化
(3)2N2H4 N2↑+H2↑+2NH3↑
(4)BCA;降低温度(或加入水);65;BAC
一、单选题
1.甲、乙两种固体的溶解度曲线如图所示。下列说法错误的是( )
A.20℃时,甲和乙两种物质的溶解度均为30 g
B.40℃时,甲物质的溶解度比乙物质的溶解度大10 g
C.将20℃时乙的饱和溶液升温至40℃,溶质质量分数不变
D.将40℃时甲的不饱和溶液降温至20℃,溶液会变为饱和溶液
2.对“溶质质量分数为15%的氯化钠溶液”的含义理解错误的是( )
A.100g氯化钠溶液中溶解了15g氯化钠
B.将氯化钠与水按15:85的质量比配成的溶液
C.将30g氯化钠溶解于170g水中所得到的溶液
D.100g水中溶解了15g氯化钠
3.如图为a、b、c三种不含结晶水的固体物质的溶解度曲线,下列叙述中正确的是( )
A.t1℃时,a、b、c饱和溶液的溶质质量分数为20%
B.P点表示时,t2℃时,a、b的溶液是饱和状态,c的溶液是不饱和状态
C.t2℃时,a、b、c三种物质溶液的溶质质量分数a>b>c
D.70ga的饱和溶液从t2℃降温到t1℃时,析出晶体15g
4.右图是M、N两种固体物质的溶解度曲线,下列说法错误的是( )
A.M物质的溶解度受温度影响变化较大
B.40℃时,M、N两种物质的溶解度相等
C.升高温度可将M的饱和溶液变为不饱和溶液
D.60℃时,饱和溶液中溶质的质量分数大小关系为N>M
5.a、b 两种物质的溶解度曲线如图所示.下列说法正确的是( )
A.a、b的溶解度均为20g
B.加水或升温均可使b的饱和溶液变为不饱和溶液
C.将30℃时a的饱和溶液(溶液底部无晶体)降温至15℃,溶质的质量分数不变
D.分别向100g水中加入20ga和b,升温至30℃,所得溶液均为饱和溶液
6.如图为氢氧化钙的溶解度曲线,下列说法不正确的是( )
A.氢氧化钙的溶解度随温度的升高而减小
B.30℃时,100g水中最多溶解0.15g氢氧化钙
C.30℃恰好饱和的石灰水升温到50℃,溶质的质量分数变小
D.70℃时,饱和石灰水中溶质和溶液的质量比为0.1:100
7.已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g,依据下列20℃时的实验和数据判断,下列说法不正确的是( )
序号 ① ② ③ ④ ⑤.
固体种类 NaCl NaCl NaNO3 NaNO3 NaNO3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
A.②⑤属于饱和溶液:
B.溶液质量:②<④
C.溶质质量分数:①=③
D.⑤中溶质与溶剂的质量比为9:10
8.下列有关溶液的说法中,正确的是()
A.常温下将10mL饱和Ca(OH)2溶液加热到50℃,会使溶液由饱和溶液变为不饱和溶液
B.将95gCaCl2溶液蒸干得到15g固体,则原溶液中CaCl2的质分数为15%
C.从质量分数为10%的H2SO4溶液中取出10mL,则取出的10mLH2SO4溶液的质分数仍为10%
D.20℃时,50g水中溶解了18gNaCl,则20℃时NaCl的溶解度为36g
9.现有氢氧化钠和氢氧化钙的固体混合物7.7克,与100克7.3%的稀盐酸恰好完全反应,则所得溶液中两种溶质的总质量为( )
A.13.2克 B.13.5克
C.11.7克 D.11.4克
10.如图是A,B,C三种固体物质的溶解度曲线,下列分析正确的是( )
A.20℃时等质量的A和C两种物质的溶液中溶质的质量相等
B.50℃时把50gA放入100g水中能得到A的饱和溶液,其溶质质量分数为50%
C.将50℃时A,B,C三种物质的饱和溶液都降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=C
D.将C的饱和溶液变为不饱和溶液,可采用降温的方法
11.下列图像不能正确反映其对应操作中各量变化关系的是( )
A. 向硫酸和硫酸铜的混合溶液中逐滴加入烧碱溶液至过量
B. 恒温条件下,向盛有一定质量的硝酸钾饱和溶液的烧杯中加入硝酸钾固体
C. 将一定质量的KNO3饱和溶液恒温蒸发水分
D. 向一定质量部分变质的NaOH溶液中滴加稀盐酸
12.如图是甲、乙两种固体物质(甲、乙均不含结晶水)的溶解度曲线图。下列说法中正确的是( )
A.t1℃时,乙溶液中溶质质量分数大于甲溶液中溶质质量分数
B.t2℃时,等质量的甲、乙溶液中溶质质量相等
C.若甲中混有少量乙,可采用蒸发结晶的方法提纯甲
D.t3℃时,分別将等质量的甲、乙饱和溶液降温t2℃所得溶液中溶质质量甲
二、填空题
13.下图是A物质(不含结晶水)的溶解度曲线。
(1)A物质的溶解度随温度的升高而 (选填“增大”、“减小”或“不变”)。
(2)在t2℃时,将15gA物质放入50g水中,搅拌,充分溶解后,形成的溶液溶质质量分数为 。
(3)N点表示t3℃时A物质的 ( 填“饱和”或“不饱和”)溶液。
(4)下图是M、N两点代表的溶液相互转化的途径路线图(“→”表示转化方向),其中,采取“先将M点溶液加入一定量的水,然后再升高温度至N点对应的温度”这一措施来实现M→N转化的途径路线图是 (填序号)。
14.20℃时,将质量均为10g的甲、乙固体分别加入到盛有50g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解度曲线如图3.
(1)P点的含义为 ;
(2)M表示 的溶解度曲线(填甲、乙);
(3)图2中,甲溶液的质量分数为 g;(保留到0.1%),甲溶液还能继续溶解的甲固体质量最多为 g;
(4)图2中,恒温下,将甲溶液恰好转化为饱和溶液,需要蒸发 水;
(5)下列说法正确的是 .
A.图1中,甲一定是饱和溶液
B.图2中,两溶液中溶质的质量分数一定相等
C.图2中,两溶液降温至30℃一定都不会析出晶体.
三、计算题
15.现有一瓶久置的过氧化氢溶液(标签如图所示)。已知过氧化氢溶液在存放过程中会缓慢分解。取该溶液 34g 于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是 33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣 3g.请计算:
(1)完全反应后生成氧气的质量 。
(2)求该瓶溶液中溶质的质量分数 。
(3)用该瓶溶液配制 100g 溶质质量分数为 3%的过氧化氢溶液需要加入水的质量 。
四、实验探究题
16.如图为A、B两种固体物质的溶解度曲线,请根据图示信息回答:
(1)t1℃时,A物质的溶解度是 g。
(2)A,B两种物质中, 的溶解度受温度的影响较小。
(3)t2℃时,将35gA物质加入到50g水中,充分溶解后,得到该温度下A物质的 (填“饱和”或“不饱和”)溶液。此时溶液的溶质质量分数为 。
17.实验小组同学在一定温度下进行硝酸钾的固体的溶解实验。
(1)(定性研究)同学们进行如下实验,发现1号试管中硝酸钾全部溶解,2号试管中固体没有完全溶解。要使2号试管中的固体全部溶解,可采取的方法有 。(列举一条即可)。
(2)(定量研究)实验小组同学在一定温度下进行硝酸钾的固体溶液实验。实验数据如下:
实验序号 实验1 实验2 实验3 实验4
水的质量(g) 100 100 100 100
加入硝酸钾的质量(g) 80 100 120 140
溶液质量(g) 180 200 210 M
请根据数据进行分析:
请计算实验2所得溶液中硝酸钾的质量分数是 。
(3)现将实验2中的溶液稀释成10%的硝酸钾溶液,需要加水的质量为 g。
(4)请判断实验2中硝酸钾溶液是 溶液。(选填“饱和”或“不饱和”)
(5)实验4中M的数值是 。
18.溶解度可表示物质溶解性的大小.
(1)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线.
①20℃时,甲的溶解度 (填“>”、“<”或“=”)乙的溶解度.
②40℃时,乙和丙 (填“能”或“不能”)形成溶质质量分数相同的饱和溶液.
③20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃.请填写下表.
烧杯中的溶质 烧杯中固体的变化
甲 固体逐渐
乙 固体逐渐
丙 固体逐渐
(2)气体的溶解度也有一定的变化规律:
打开可乐瓶,逸出大量气泡.由此可见,压强越小,CO2的溶解度越 .为增大CO2的溶解度,可采用的一种方法是 .
五、综合题
19.水是人类宝贵的自然资源.
(1)硬水给人们生活和生产带来很多麻烦,区分硬水和软水生活中常用的物质是 .
(2)在厨房用水洗涤餐具时,通常在水里加些洗涤剂,这样就可以很容易的除去餐具上的油污,这是因为洗涤剂具有 (填“溶解”或“乳化”)作用.
(3)电影《火星救援》中马特 达蒙采用①液态的火箭燃料联氨(N2H4)在密闭容器中高温分解生成氮气、氢气和氨气(NH3),②分解出的氢气燃烧制取水的方法,解决了火星上缺少液态水的问题,写出①的化学方程式
(4)如图是A、B、C三种固体物质的溶解度曲线,据图回答:
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 .
②t2℃时,C物质的饱和溶液转化为不饱和溶液的方法是 .
③t1℃时,30gA物质加入到50g水中不断搅拌形成的溶液质量是 g.
④t2℃时,将A、B、C三种物质饱和溶液分别降温至t1℃时,所得溶液中的溶质质量分数由大到小顺序为 .
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】A
4.【答案】D
5.【答案】C
6.【答案】D
7.【答案】D
8.【答案】C
9.【答案】D
10.【答案】D
11.【答案】C
12.【答案】D
13.【答案】(1)增大
(2)20%
(3)不饱和
(4)丙
14.【答案】30℃,M、N两种物质的溶解度相等;甲;16.7%;12.5;27.8;ABC
15.【答案】(1)解:生成氧气的质量为:34g+3g-33.8g=3.2g,
(2)解:设:取出的34g过氧化氢溶液中含H2O2的质量为x,
2H2O2 2H2O+ O2↑
68 32
x 3.2g
x=6.8g, 所以该过氧化氢溶液中溶质质量分数为: 答:该过氧化氢溶液中溶质质量分数为20%.
(3)解:设配制100g溶质质量分数为3%的过氧化氢溶液需该溶液质量为y, 100g×3%=20%×y, y=15g, 则需加水的质量为:100g-15g=85g, 答:需加水的质量为85g.
16.【答案】(1)20
(2)B
(3)饱和;37.5%
17.【答案】(1)加水或升温
(2)50%
(3)800
(4)不饱和
(5)210
18.【答案】(1)<;能;全部溶解;部分溶解;固体不溶解,反而增多
(2)小;增大压强或降低温度
19.【答案】(1)肥皂水
(2)乳化
(3)2N2H4 N2↑+H2↑+2NH3↑
(4)BCA;降低温度(或加入水);65;BAC
同课章节目录
